2.1.3元素与物质的分类 课件(共29张PPT)2023-2024学年鲁科版高中化学必修一
文档属性
| 名称 | 2.1.3元素与物质的分类 课件(共29张PPT)2023-2024学年鲁科版高中化学必修一 |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-02 00:00:00 | ||
图片预览








文档简介
(共29张PPT)
第一节 元素与物质分类(第3课时)
第二章 元素与物质世界
学习目标
1、宏观辨识与微观探究
通过观察、辨识3种分散系的形态及宏观现象,形成“结构决定性质,性质决定应用”的观念。
2、证据推理与模型认知
能初步学会收集各种科学史证据和实验证据.基于证据进行分析推理,证实或证伪假设:能解释证据与结论之间的关系。
3、实验探究与创新意识
从生活中的胶体豆浆入手,设计探究豆浆中分散系,能对观察记录的实验信息迸行加工并获得结论。
4、科学精神与社会责任
通过胶体科学史的学习,培养自己终身学习的意识和严谨求实的科学态度:深刻理解化学、技术、社会和环境之间的相互关系,赞赏化学对社会发展的重大贡献。
什么是分散系?
课前自主学习
课前自主学习
一、分散系
1.定义:把一种(或多种)物质分散到另一种物质中得到的混合体系
2.组成
分散质:被分散的物质
分散剂:容纳分散质的物质
3.分类
分散系可以分为溶液、胶体、浊液(悬浊液、乳浊液)。
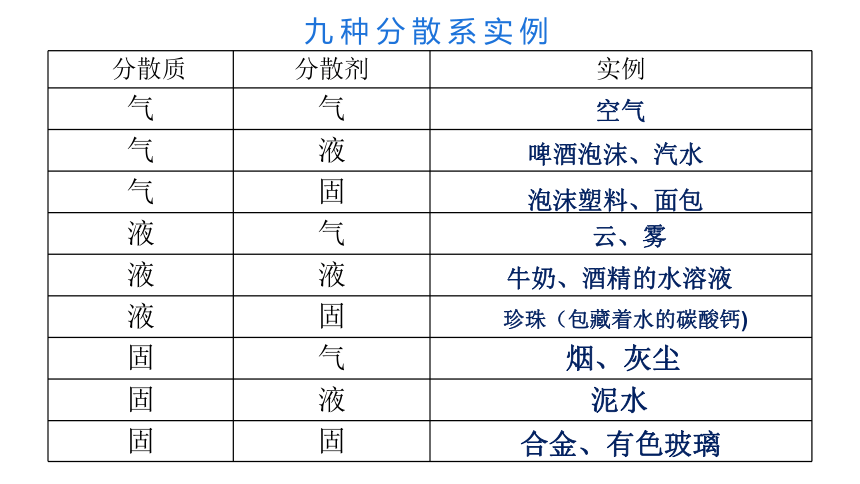
九种分散系实例
分散质 分散剂 实例
气 气
气 液
气 固
液 气
液 液
液 固
固 气
固 液
固 固
空气
啤酒泡沫、汽水
泡沫塑料、面包
云、雾
牛奶、酒精的水溶液
珍珠(包藏着水的碳酸钙)
烟、灰尘
泥水
合金、有色玻璃
课前自主学习
一、分散系
宏观特征:
溶液:透明、均一、稳定
浊液:浑浊、不稳定
胶体有什么特征?
二、胶体
【科学史话】胶体的发现史
1663年卡修斯偶尔制得金溶胶,只是将其视为普通溶液
1845~1850年间,意大利科学家塞尔米在实验中曾制得一些“溶液”,他发现这些溶液中的分散质点比通常的分子要大得多,他把这些奇怪的“溶液”称为“假溶液”。
1861年,英国化学家格雷厄姆对“假溶液”进行了更系统的研究,他发 现将真溶液溶剂蒸发后易于析出晶体,而假溶液溶剂蒸发后大多形成无定形胶状物质,格雷厄姆将它称为“胶体”。
1857年,英国科学家法拉第做实验,使一束光通过玫瑰红色的金溶胶出现了奇特的现象。
英国科学家丁达尔对奇特现象进行了深入的研究,发现光照在胶体上时形成光路,这种现象被称为“丁达尔现象”。
寻找胶体
思考1:你能辨别出胶体吗?动手试一试。
思考2:生活中你见过与上述现象一样的美景吗?
可用丁达尔现象确定胶体
任务一
丁达尔现象
定义:当可见光束通过胶体时,从入射
光侧面可观察到光亮的通路,这种现象
就叫做丁达尔现象或丁达尔效应。
生活中的丁达尔现象
胶体
液溶胶
气溶胶
固溶胶
任务二
走进胶体内部
资料1 豆浆分离示意图
资料2 滤纸和半透膜孔径大小
滤纸孔径大于100nm(纳米)
半透膜孔径1nm左右(1nm = 10-9m)
资料3 可见光照射到不同大小颗粒的情况
当可见光照射到不同大小的颗粒时,会产生3种情况:反射、散射、透过。
反射:可见光照到很大颗粒时,会反射,使光线无法透过
散射:可见光照到与其波长相近的颗粒时,光线会偏离原来的方向往
四面八方照射,原来入射方向的光减弱,即使不迎着入射光从
侧面也可以看到光
透过:可见光照到小颗粒时,会透过
任务二
走进胶体内部
交流研讨1:结合上述资料,尝试分析浊液分散质粒子、胶体分散质粒子(简称胶粒)、溶液分散质粒子(简称溶质)直径的大小范围。
交流研讨2:结合资料3和分散质粒子的大小,从微观结构的角度分析,为什么只有胶体产生了丁达尔现象?丁达尔现象的光学实质是什么?
浊液分散质粒子直径:大于100nm
胶粒直径:处于1-100nm之间
溶质直径:小于1nm
半透膜外液体
(溶液)
半透膜内液体
(胶体)
透过半透膜
透过滤纸
滤液
滤渣
现磨豆浆
小资料
滤纸孔径:大于100nm
半透膜孔径:1nm左右
过滤
渗析
任务二
走进胶体内部
资料1 豆浆分离示意图
资料2 滤纸和半透膜孔径大小
资料3 可见光照射到不同大小颗粒的情况
交流研讨1:结合上述资料,尝试分析浊液分散质粒子、胶体分散质粒子(简称胶粒)、溶液分散质粒子(简称溶质)直径的大小范围。
交流研讨2:结合资料3和分散质粒子的大小,从微观结构的角度分析,为什么只有胶体产生了丁达尔现象?丁达尔现象的光学实质是什么?
浊液分散质粒子直径:大于100nm
胶粒直径:处于1-100nm之间
溶质直径:小于1nm
丁达尔现象是胶粒对光的散射现象
任务三
感受胶体的应用
交流研讨3:将适量石膏固体加入到热豆浆中并搅拌,你能观察到什么现象?
胶体发生聚沉现象
什么是胶体的聚沉?
1、聚沉
定义:把酸、碱、盐等物质加入到胶体中
时,它们溶解产生的阳离子或阴离子所带
电荷与胶体的分散质微粒所带电荷中和,
会使胶体的分散质微粒聚集成较大的微粒,
再重力的作用下沉淀析出,这种胶体形成沉
淀析出的现象称为聚沉
为什么加热或搅拌也可能引起胶体的聚沉?
拓展思考
加热或搅拌会使胶粒运动加剧,使其碰撞机会增多,使胶核对离子的吸附作用减弱,导致胶体聚沉。
胶体还有哪些性质呢?
拓展思考
2.电泳
3.吸附性
1.定义:胶体中的分散质微粒在直流电的作用下产生定向移动的现象叫做电泳。电泳现象说明胶体中的分散质微粒带有电荷。
2.应用:①电镀②静电除尘
在水的净化过程中,由于胶体分散质具有巨大的比表面积(单位质量的微粒具有的表面积),形成较强的吸附能力,吸附水中的色素、悬浮固体等以达到净水的目的。
如何制备氢氧化铁胶体?
拓展思考
氢氧化铁胶体的制备
拓展思考
方法:向沸水中逐滴加1mol/L FeCI3溶液,至溶液呈透明的红褐色
原理为
FeCI3+3H2O = Fe(OH)3(胶体)+3HCI
△
结构
性质
用途
决定
决定
胶粒处于
1-100nm
胶体比较稳定
有丁达尔现象
胶体有广泛的应用(例如:制豆腐,形成三角洲等等)
概括提升
巩固目标
1.溶液、胶体和浊液这三种分散系的根本区别是( )
A.是否为大量分子或离子的集合体
B.分散质微粒直径的大小
C.能否透过滤纸
D.是否均一、稳定、透明
B
2.下列分散系属于胶体的是( )
①血液②豆浆③食盐水④蔗糖水⑤泥水⑥淀粉溶液
A.只有② B.①②⑥ C.①②③ D.①②③④⑥
B
巩固目标
3.下列事实与胶体知识无关的( )
A.医院里通过渗析,除去肾炎病人血液中毒素,称为透析。
B.向饱和氯化铁溶液中加入NaOH溶液,会出现红褐色沉淀。
C.一束平行光线照射蛋白质溶液时,从侧面可看到光亮的通路
D.一支钢笔使用两种不同牌号的墨水,易出现堵塞。
B
(聚沉)
(胶粒直径在1~100nm之间,不能通过半透膜)
(丁达尔效应)
(FeCl3+3NaOH==Fe(OH)3 +3NaCl)
二、胶体
【科学史话】胶体的发现史
1663年卡修斯偶尔制得金溶胶,只是将其视为普通溶液
1845~1850年间,意大利科学家塞尔米在实验中曾制得一些“溶液”,他发现这些溶液中的分散质点比通常的分子要大得多,他把这些奇怪的“溶液”称为“假溶液”。
1861年,英国化学家格雷厄姆对“假溶液”进行了更系统的研究,他发 现将真溶液溶剂蒸发后易于析出晶体,而假溶液溶剂蒸发后大多形成无定形胶状物质,格雷厄姆将它称为“胶体”。
1857年,英国科学家法拉第做实验,使一束光通过玫瑰红色的金溶胶出现了奇特的现象。
英国科学家丁达尔对奇特现象进行了深入的研究,发现光照在胶体上时形成光路,这种现象被称为“丁达尔现象”。
学习胶体后,请你根据性质决定用途的观点,分析下列图示中胶体的用途与哪些性质有关,并做出相关注解。
胶体的用途
肥皂的
制取和分离
水泥的硬化
FeCl3溶液
用于伤口止血
土壤胶体
中离子的
吸附与交换
制豆腐
冶金厂大
量的烟尘
用高压电除除尘
手电筒在
晚上产生光柱
明矾的净水
课后作业
谢谢大家观看
第一节 元素与物质分类(第3课时)
第二章 元素与物质世界
学习目标
1、宏观辨识与微观探究
通过观察、辨识3种分散系的形态及宏观现象,形成“结构决定性质,性质决定应用”的观念。
2、证据推理与模型认知
能初步学会收集各种科学史证据和实验证据.基于证据进行分析推理,证实或证伪假设:能解释证据与结论之间的关系。
3、实验探究与创新意识
从生活中的胶体豆浆入手,设计探究豆浆中分散系,能对观察记录的实验信息迸行加工并获得结论。
4、科学精神与社会责任
通过胶体科学史的学习,培养自己终身学习的意识和严谨求实的科学态度:深刻理解化学、技术、社会和环境之间的相互关系,赞赏化学对社会发展的重大贡献。
什么是分散系?
课前自主学习
课前自主学习
一、分散系
1.定义:把一种(或多种)物质分散到另一种物质中得到的混合体系
2.组成
分散质:被分散的物质
分散剂:容纳分散质的物质
3.分类
分散系可以分为溶液、胶体、浊液(悬浊液、乳浊液)。
九种分散系实例
分散质 分散剂 实例
气 气
气 液
气 固
液 气
液 液
液 固
固 气
固 液
固 固
空气
啤酒泡沫、汽水
泡沫塑料、面包
云、雾
牛奶、酒精的水溶液
珍珠(包藏着水的碳酸钙)
烟、灰尘
泥水
合金、有色玻璃
课前自主学习
一、分散系
宏观特征:
溶液:透明、均一、稳定
浊液:浑浊、不稳定
胶体有什么特征?
二、胶体
【科学史话】胶体的发现史
1663年卡修斯偶尔制得金溶胶,只是将其视为普通溶液
1845~1850年间,意大利科学家塞尔米在实验中曾制得一些“溶液”,他发现这些溶液中的分散质点比通常的分子要大得多,他把这些奇怪的“溶液”称为“假溶液”。
1861年,英国化学家格雷厄姆对“假溶液”进行了更系统的研究,他发 现将真溶液溶剂蒸发后易于析出晶体,而假溶液溶剂蒸发后大多形成无定形胶状物质,格雷厄姆将它称为“胶体”。
1857年,英国科学家法拉第做实验,使一束光通过玫瑰红色的金溶胶出现了奇特的现象。
英国科学家丁达尔对奇特现象进行了深入的研究,发现光照在胶体上时形成光路,这种现象被称为“丁达尔现象”。
寻找胶体
思考1:你能辨别出胶体吗?动手试一试。
思考2:生活中你见过与上述现象一样的美景吗?
可用丁达尔现象确定胶体
任务一
丁达尔现象
定义:当可见光束通过胶体时,从入射
光侧面可观察到光亮的通路,这种现象
就叫做丁达尔现象或丁达尔效应。
生活中的丁达尔现象
胶体
液溶胶
气溶胶
固溶胶
任务二
走进胶体内部
资料1 豆浆分离示意图
资料2 滤纸和半透膜孔径大小
滤纸孔径大于100nm(纳米)
半透膜孔径1nm左右(1nm = 10-9m)
资料3 可见光照射到不同大小颗粒的情况
当可见光照射到不同大小的颗粒时,会产生3种情况:反射、散射、透过。
反射:可见光照到很大颗粒时,会反射,使光线无法透过
散射:可见光照到与其波长相近的颗粒时,光线会偏离原来的方向往
四面八方照射,原来入射方向的光减弱,即使不迎着入射光从
侧面也可以看到光
透过:可见光照到小颗粒时,会透过
任务二
走进胶体内部
交流研讨1:结合上述资料,尝试分析浊液分散质粒子、胶体分散质粒子(简称胶粒)、溶液分散质粒子(简称溶质)直径的大小范围。
交流研讨2:结合资料3和分散质粒子的大小,从微观结构的角度分析,为什么只有胶体产生了丁达尔现象?丁达尔现象的光学实质是什么?
浊液分散质粒子直径:大于100nm
胶粒直径:处于1-100nm之间
溶质直径:小于1nm
半透膜外液体
(溶液)
半透膜内液体
(胶体)
透过半透膜
透过滤纸
滤液
滤渣
现磨豆浆
小资料
滤纸孔径:大于100nm
半透膜孔径:1nm左右
过滤
渗析
任务二
走进胶体内部
资料1 豆浆分离示意图
资料2 滤纸和半透膜孔径大小
资料3 可见光照射到不同大小颗粒的情况
交流研讨1:结合上述资料,尝试分析浊液分散质粒子、胶体分散质粒子(简称胶粒)、溶液分散质粒子(简称溶质)直径的大小范围。
交流研讨2:结合资料3和分散质粒子的大小,从微观结构的角度分析,为什么只有胶体产生了丁达尔现象?丁达尔现象的光学实质是什么?
浊液分散质粒子直径:大于100nm
胶粒直径:处于1-100nm之间
溶质直径:小于1nm
丁达尔现象是胶粒对光的散射现象
任务三
感受胶体的应用
交流研讨3:将适量石膏固体加入到热豆浆中并搅拌,你能观察到什么现象?
胶体发生聚沉现象
什么是胶体的聚沉?
1、聚沉
定义:把酸、碱、盐等物质加入到胶体中
时,它们溶解产生的阳离子或阴离子所带
电荷与胶体的分散质微粒所带电荷中和,
会使胶体的分散质微粒聚集成较大的微粒,
再重力的作用下沉淀析出,这种胶体形成沉
淀析出的现象称为聚沉
为什么加热或搅拌也可能引起胶体的聚沉?
拓展思考
加热或搅拌会使胶粒运动加剧,使其碰撞机会增多,使胶核对离子的吸附作用减弱,导致胶体聚沉。
胶体还有哪些性质呢?
拓展思考
2.电泳
3.吸附性
1.定义:胶体中的分散质微粒在直流电的作用下产生定向移动的现象叫做电泳。电泳现象说明胶体中的分散质微粒带有电荷。
2.应用:①电镀②静电除尘
在水的净化过程中,由于胶体分散质具有巨大的比表面积(单位质量的微粒具有的表面积),形成较强的吸附能力,吸附水中的色素、悬浮固体等以达到净水的目的。
如何制备氢氧化铁胶体?
拓展思考
氢氧化铁胶体的制备
拓展思考
方法:向沸水中逐滴加1mol/L FeCI3溶液,至溶液呈透明的红褐色
原理为
FeCI3+3H2O = Fe(OH)3(胶体)+3HCI
△
结构
性质
用途
决定
决定
胶粒处于
1-100nm
胶体比较稳定
有丁达尔现象
胶体有广泛的应用(例如:制豆腐,形成三角洲等等)
概括提升
巩固目标
1.溶液、胶体和浊液这三种分散系的根本区别是( )
A.是否为大量分子或离子的集合体
B.分散质微粒直径的大小
C.能否透过滤纸
D.是否均一、稳定、透明
B
2.下列分散系属于胶体的是( )
①血液②豆浆③食盐水④蔗糖水⑤泥水⑥淀粉溶液
A.只有② B.①②⑥ C.①②③ D.①②③④⑥
B
巩固目标
3.下列事实与胶体知识无关的( )
A.医院里通过渗析,除去肾炎病人血液中毒素,称为透析。
B.向饱和氯化铁溶液中加入NaOH溶液,会出现红褐色沉淀。
C.一束平行光线照射蛋白质溶液时,从侧面可看到光亮的通路
D.一支钢笔使用两种不同牌号的墨水,易出现堵塞。
B
(聚沉)
(胶粒直径在1~100nm之间,不能通过半透膜)
(丁达尔效应)
(FeCl3+3NaOH==Fe(OH)3 +3NaCl)
二、胶体
【科学史话】胶体的发现史
1663年卡修斯偶尔制得金溶胶,只是将其视为普通溶液
1845~1850年间,意大利科学家塞尔米在实验中曾制得一些“溶液”,他发现这些溶液中的分散质点比通常的分子要大得多,他把这些奇怪的“溶液”称为“假溶液”。
1861年,英国化学家格雷厄姆对“假溶液”进行了更系统的研究,他发 现将真溶液溶剂蒸发后易于析出晶体,而假溶液溶剂蒸发后大多形成无定形胶状物质,格雷厄姆将它称为“胶体”。
1857年,英国科学家法拉第做实验,使一束光通过玫瑰红色的金溶胶出现了奇特的现象。
英国科学家丁达尔对奇特现象进行了深入的研究,发现光照在胶体上时形成光路,这种现象被称为“丁达尔现象”。
学习胶体后,请你根据性质决定用途的观点,分析下列图示中胶体的用途与哪些性质有关,并做出相关注解。
胶体的用途
肥皂的
制取和分离
水泥的硬化
FeCl3溶液
用于伤口止血
土壤胶体
中离子的
吸附与交换
制豆腐
冶金厂大
量的烟尘
用高压电除除尘
手电筒在
晚上产生光柱
明矾的净水
课后作业
谢谢大家观看
