化学人教版(2019)必修第一册1.1.2物质的转化(共49张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第一册1.1.2物质的转化(共49张ppt) |  | |
| 格式 | pptx | ||
| 文件大小 | 3.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-02 17:48:33 | ||
图片预览










文档简介
(共49张PPT)
青年时种下什么,老年时就收获什么。
——易卜生
原料:石灰石、水、纯碱
要求:画出生产流程图
请判断以上转化的反应类型。
问题解决
土法制碱
转化
物质的
Transformation of matter
酸、碱、盐的性质
物质的转化
A
B
分类
化学性质——通性
物质的转化链
物质的转化网
物质的转化条件:金属转换及复分解反应
物质的转化应用
学
习
目
标
酸、碱、盐的性质
01
将HCl、H2SO4、HNO3进行分类。
HCl、H2SO4、HNO3
小试身手
1.1 酸
1.1.1 分类
酸、碱、盐的性质
1
酸
组成中是否含氧
含氧酸
无氧酸
H2SO4、HNO3
HCl、H2S
HCl、H2SO4、HNO3
将HCl、H2SO4、HNO3进行分类。
小试身手
1.1 酸
1.1.1 分类
酸、碱、盐的性质
1
酸
组成中是否含氧
含氧酸
无氧酸
H2SO4、HNO3
HCl、H2S
电离出的H+数目
一元酸
二元酸
三元酸
HCl、HNO3
H2SO4
H3PO4
有无挥发性
挥发酸
难挥发酸
HCl、HNO3
H2SO4
电离能力
强酸
弱酸
HCl、H2SO4、HNO3
H2CO3
CH3COOH
HClO
回顾练习
以硫酸为例,写出它可能与哪些物质发生反应。
主要化学性质 反应实例(写化学方程式)
与活泼金属反应
与碱性氧化物反应
与碱反应
与某些盐反应
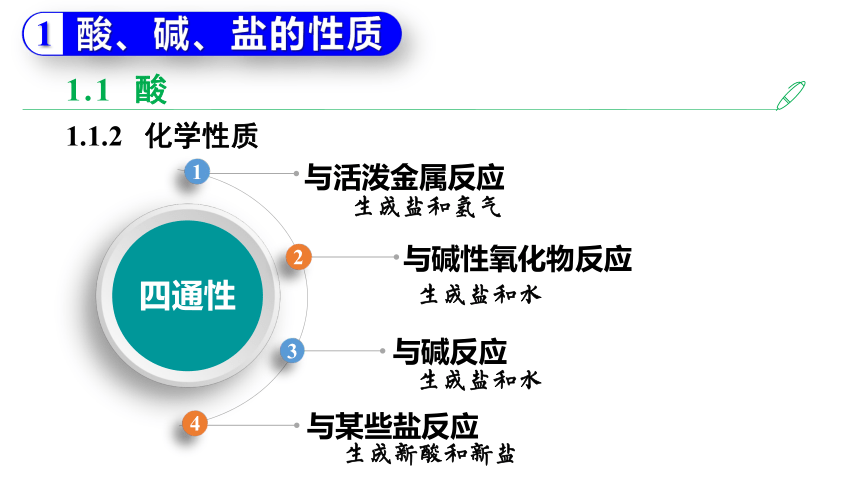
1.1 酸
1.1.2 化学性质
酸、碱、盐的性质
1
1
四通性
与活泼金属反应
生成盐和氢气
2
与碱性氧化物反应
生成盐和水
3
与碱反应
生成盐和水
4
与某些盐反应
生成新酸和新盐
感受﹒ 理解
酸具有相似化学性质的原因是什么呢?
从微观角度来看
同的酸溶液中都含有____。
H+
1.2 碱
1.2.1 分类
酸、碱、盐的性质
1
碱
溶解性
易溶
NaOH KOH Ba(OH)2
Mg(OH)2 Fe(OH)2 Fe(OH)3
微溶
Ca(OH)2
难溶
电离OH-数目
一元碱
NaOH KOH
二元碱
Ca(OH)2 Ba(OH)2 Fe(OH)2
电离能力
强碱
弱碱
NaOH KOH Ba(OH)2
Mg(OH)2 Fe(OH)2 Fe(OH)3
回顾练习
以烧碱为例,写出可能与哪些物质发生反应。
主要化学性质 反应实例(写化学方程式)
与酸性氧化物反应
与酸反应
与某些盐反应
1.2 碱
1.2.2 化学性质
酸、碱、盐的性质
1
与酸性氧化物反应
1
三通性
生成盐和水
2
与酸反应
生成盐和水
3
与某些盐反应
生成新盐和新盐
OH-
碱具有相似化学性质的原因:从微观角度来看,不同的碱溶液中都含有______。
问题探究
为什么酸、碱之间具有相似的化学性质呢?
微粒观
HCl H2SO4 HNO3
H+
NaOH KOH Ba(OH)2
OH-
回顾练习
以Na2CO3、K2CO3为例,写出可能与哪些物质发生反应。
主要化学性质 反应实例(写化学方程式)
与某些酸反应
与某些碱反应
与某些盐反应
为什么两种碳酸盐具有相似的化学性质呢?
CO32-
1.3.1 化学通性
酸、碱、盐的性质
1
1.3 盐
与金属反应
1
生成新盐和新金属
2
与碱反应
生成新盐和新碱
3
与某些盐反应
生成新盐和新盐
三通性
盐具有相似化学性质的原因:从微观角度来看,组成上含有相同阴离子或阳离子。
将Na2CO3、NaHCO3、CaCO3、Cu2(OH)2CO3进行分类。
思考﹒ 讨论
1.3 盐
酸、碱、盐的性质
1
1.3.2 分类
盐
溶解性
可溶盐
难溶盐
微溶盐
Na2CO3
CaCO3、Cu2(OH)2CO3
CaSO4
将Na2CO3、NaHCO3、CaCO3、Cu2(OH)2CO3进行分类。
思考﹒ 讨论
1.3 盐
1.3.1 分类
酸、碱、盐的性质
1
盐
溶解性
可溶盐
难溶盐
微溶盐
Na2CO3
CaCO3、Cu2(OH)2CO3
CaSO4
组成
正盐
酸式盐
碱式盐
Na2CO3、CaCO3
物质分类的依据不同,其结果不同,试对NaHSO4按照不同的标准进行分类。
钠盐
硫酸盐
酸式盐
可溶性盐
含氧酸盐
考考你自己
思考﹒ 讨论
下列物质的转化,不能一步实现的是
A.K2SO4―→KOH
B.Zn―→ZnCl2
C.Fe2O3―→Fe(OH)3
D.MgCl2―→Mg(OH)2
牛刀小试
下列物质可直接与其他物质反应生成盐的有
①金属 ②碱性氧化物 ③碱 ④酸性氧化物 ⑤酸
A.仅①②
B.仅①④⑤
C.仅②④⑤
D.全部
牛刀小试
交流讨论
酸、碱、盐发生的反应中,涉及了哪些反应类型?
酸、碱、盐的性质
1
1.4 反应类型
反应类型 反应模型
A+B=AB
AB=A+B
AB+C=A+CB
AB+CD=AD+CB
化合反应
分解反应
置换反应
复分解反应
置换反应
金属与酸、盐
复分解反应
酸与碱、盐;盐与碱、盐
某同学要在奥运五连环中填入物质,使相连物质间能发生反应,不相连物质间不能发生反应。你认为“五连环”中有空缺的一环应填入的物质是
考考你自己
A.稀硫酸 B.氧气
C.二氧化碳 D.氧化铜
物质的转化
02
思考﹒ 讨论
写出下列物质之间转化的化学方程式,体会由金属单质、非金属单质到盐的转化关系。
Ca → CaO → Ca(OH)2 → CaSO4
C → CO2 → H2CO3 → CaCO3
对于上述转化关系,从物质分类的角度看,你发现了什么规律?将你的想法与同学交流。
2.1 转化链
物质的转化
2
金属单质
碱性氧化物
碱
盐
酸或酸性氧化物
H2O
O2
非金属单质
酸性氧化物
酸
盐
碱或碱性氧化物
H2O
O2
如FeO Fe2O3 CuO等不与水反应
只有SiO2不与水反应
金属活动顺序表Al及以后金属的碱性氧化物与水不反应
各物质间还有没有其他什么转化?
2.2 转化网
物质的转化
2
金属单质
碱性氧化物
碱
盐
酸或酸性氧化物
H2O
O2
非金属单质
酸性氧化物
酸
盐
碱或碱性氧化物
H2O
O2
盐
判断以下反应能否发生。
1.锌与氯化铜
2.银与硫酸铜溶
3.碳酸钾与稀盐酸
4.硝酸银与氯化钡溶液
5.稀硫酸与氢氧化钠溶液
6.稀硝酸与硫酸钠
看谁做得既准又快
2.3 转化条件
物质的转化
2
置换反应
1
两反应
活泼性强的金属置换活泼性弱的金属
(K、Na、Ca、Ba先与水反应!)
2
复分解反应
气体、沉淀、水
有三条件中之一即可
无机物能否生成有机物?
6H2O+6CO2
C6H12O6+6O2
首次由无机物制备的有机物
化学史话
时间:19世纪
理论: 活力论
认为无机物与有机物有根本性差异
所以无机物无法变成有机物
有机化合物只能由生物的细胞
在一种特殊的力量
——生命力的作用下产生
人工合成是不可能的
尿素
哺乳动物、两栖动物和一些鱼的尿中含有尿素
1828年,他在合成氰酸铵时,却得到了尿素
1824年开始研究氰酸铵
化学史话
什么物质间反应可氢氧化钠?请写出化学方程式。
氧化钠与水反应
碳酸钠与氢氧化钙反应
上述过程的成本都较高,现在的工业生产中,一般选择电解饱和食盐水的方法来生产氢氧化钠。
考考你自己
已知在通电条件下,氯化钠和水反应生成氢氧化钠、氢气和氯气,请写出反应的化学方程式。
2NaCl+2H2O 2NaOH+H2↑+Cl2↑
2NaCl+2H2O 2NaOH+H2↑+Cl2↑
通电
电解槽
这节课我学到了什么?
(用一句话表示)
还有什么疑问?
课堂小结
课堂小结
酸、碱、盐的性质
1
酸有共同的性质:
酸溶液中,都含有H+
2
碱有共同的性质:
碱溶液中,都含有OH-
盐溶液中,都含有相同酸根或阳离子
3
某类盐有共同的性质:
思考﹒ 运用
氯化镁用于制金属镁、氧化镁、冷冻盐水、陶瓷,并用于填充织物、造纸等方面。
请写出制备氯化镁的途径,看谁写得最多。
盐
金属
碱性氧化物
酸
盐
非金属单质
盐
酸性氧化物
酸
金属
碱性氧化物
碱
酸
碱
盐
物质的转化
课堂小结
金属
单质
碱
盐
酸
盐
盐
盐和水
碱性
氧化物
酸性
氧化物
非金属
单质
碱和盐
酸和盐
另两种盐
金属和盐
氢气和盐
下列变化不能通过一步化学反应实现的是
A.BaCl2→BaSO4
B.CuO→Cu(OH)2
C.NaOH→Na2SO3
D.MgSO4→Mg(OH)2
考考你自己
铁、稀盐酸、澄清石灰水、氯化铜溶液是初中化学中常见的物质,四种物质间的反应关系如图所示。图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应四个反应类型的说法正确的是
牛刀小试
A.复分解反应、复分解反应、化合反应、置换反应
B.中和反应、置换反应、复分解反应、置换反应
C.复分解反应、复分解反应、置换反应、置换反应
D.分解反应、复分解反应、置换反应、置换反应
下表所列各组物质中,物质之间按箭头方向不能通过一步反应实现如图所示转化的是
A.甲为CuO、乙为CO2、丙为CO
B.甲为C、乙为CO、丙为CO2
C.甲为CaCO3、乙为CaO、丙为Ca(OH)2
D.甲为H2SO4、乙为H2O、丙为H2
请你试一试
甲
乙
丙
图中,“——”表示相连的物质间在一定条件下可以反应,“―→”表示丁在一定条件下通过置换反应可以转化为乙。下面四组选项中,符合图示要求的是
选项 甲 乙 丙 丁
A H2SO4 Na2SO4 NaOH NaCl
B BaCl2 K2CO3 HCl KOH
C O2 CO CuO C
D Fe CuCl2 Zn HCl
甲
乙
丙
丁
看我七十二变
X、Y、Z、W各代表一种物质,若X+Y==Z+W,则X和Y之间不可能是
A.盐和盐的反应
B.碱性氧化物和水的反应
C.酸与碱的反应
D.酸性氧化物和碱的反应
成功体验
抓住微粒认识性质
重视物质的转化条件
青年时种下什么,老年时就收获什么。
——易卜生
原料:石灰石、水、纯碱
要求:画出生产流程图
请判断以上转化的反应类型。
问题解决
土法制碱
转化
物质的
Transformation of matter
酸、碱、盐的性质
物质的转化
A
B
分类
化学性质——通性
物质的转化链
物质的转化网
物质的转化条件:金属转换及复分解反应
物质的转化应用
学
习
目
标
酸、碱、盐的性质
01
将HCl、H2SO4、HNO3进行分类。
HCl、H2SO4、HNO3
小试身手
1.1 酸
1.1.1 分类
酸、碱、盐的性质
1
酸
组成中是否含氧
含氧酸
无氧酸
H2SO4、HNO3
HCl、H2S
HCl、H2SO4、HNO3
将HCl、H2SO4、HNO3进行分类。
小试身手
1.1 酸
1.1.1 分类
酸、碱、盐的性质
1
酸
组成中是否含氧
含氧酸
无氧酸
H2SO4、HNO3
HCl、H2S
电离出的H+数目
一元酸
二元酸
三元酸
HCl、HNO3
H2SO4
H3PO4
有无挥发性
挥发酸
难挥发酸
HCl、HNO3
H2SO4
电离能力
强酸
弱酸
HCl、H2SO4、HNO3
H2CO3
CH3COOH
HClO
回顾练习
以硫酸为例,写出它可能与哪些物质发生反应。
主要化学性质 反应实例(写化学方程式)
与活泼金属反应
与碱性氧化物反应
与碱反应
与某些盐反应
1.1 酸
1.1.2 化学性质
酸、碱、盐的性质
1
1
四通性
与活泼金属反应
生成盐和氢气
2
与碱性氧化物反应
生成盐和水
3
与碱反应
生成盐和水
4
与某些盐反应
生成新酸和新盐
感受﹒ 理解
酸具有相似化学性质的原因是什么呢?
从微观角度来看
同的酸溶液中都含有____。
H+
1.2 碱
1.2.1 分类
酸、碱、盐的性质
1
碱
溶解性
易溶
NaOH KOH Ba(OH)2
Mg(OH)2 Fe(OH)2 Fe(OH)3
微溶
Ca(OH)2
难溶
电离OH-数目
一元碱
NaOH KOH
二元碱
Ca(OH)2 Ba(OH)2 Fe(OH)2
电离能力
强碱
弱碱
NaOH KOH Ba(OH)2
Mg(OH)2 Fe(OH)2 Fe(OH)3
回顾练习
以烧碱为例,写出可能与哪些物质发生反应。
主要化学性质 反应实例(写化学方程式)
与酸性氧化物反应
与酸反应
与某些盐反应
1.2 碱
1.2.2 化学性质
酸、碱、盐的性质
1
与酸性氧化物反应
1
三通性
生成盐和水
2
与酸反应
生成盐和水
3
与某些盐反应
生成新盐和新盐
OH-
碱具有相似化学性质的原因:从微观角度来看,不同的碱溶液中都含有______。
问题探究
为什么酸、碱之间具有相似的化学性质呢?
微粒观
HCl H2SO4 HNO3
H+
NaOH KOH Ba(OH)2
OH-
回顾练习
以Na2CO3、K2CO3为例,写出可能与哪些物质发生反应。
主要化学性质 反应实例(写化学方程式)
与某些酸反应
与某些碱反应
与某些盐反应
为什么两种碳酸盐具有相似的化学性质呢?
CO32-
1.3.1 化学通性
酸、碱、盐的性质
1
1.3 盐
与金属反应
1
生成新盐和新金属
2
与碱反应
生成新盐和新碱
3
与某些盐反应
生成新盐和新盐
三通性
盐具有相似化学性质的原因:从微观角度来看,组成上含有相同阴离子或阳离子。
将Na2CO3、NaHCO3、CaCO3、Cu2(OH)2CO3进行分类。
思考﹒ 讨论
1.3 盐
酸、碱、盐的性质
1
1.3.2 分类
盐
溶解性
可溶盐
难溶盐
微溶盐
Na2CO3
CaCO3、Cu2(OH)2CO3
CaSO4
将Na2CO3、NaHCO3、CaCO3、Cu2(OH)2CO3进行分类。
思考﹒ 讨论
1.3 盐
1.3.1 分类
酸、碱、盐的性质
1
盐
溶解性
可溶盐
难溶盐
微溶盐
Na2CO3
CaCO3、Cu2(OH)2CO3
CaSO4
组成
正盐
酸式盐
碱式盐
Na2CO3、CaCO3
物质分类的依据不同,其结果不同,试对NaHSO4按照不同的标准进行分类。
钠盐
硫酸盐
酸式盐
可溶性盐
含氧酸盐
考考你自己
思考﹒ 讨论
下列物质的转化,不能一步实现的是
A.K2SO4―→KOH
B.Zn―→ZnCl2
C.Fe2O3―→Fe(OH)3
D.MgCl2―→Mg(OH)2
牛刀小试
下列物质可直接与其他物质反应生成盐的有
①金属 ②碱性氧化物 ③碱 ④酸性氧化物 ⑤酸
A.仅①②
B.仅①④⑤
C.仅②④⑤
D.全部
牛刀小试
交流讨论
酸、碱、盐发生的反应中,涉及了哪些反应类型?
酸、碱、盐的性质
1
1.4 反应类型
反应类型 反应模型
A+B=AB
AB=A+B
AB+C=A+CB
AB+CD=AD+CB
化合反应
分解反应
置换反应
复分解反应
置换反应
金属与酸、盐
复分解反应
酸与碱、盐;盐与碱、盐
某同学要在奥运五连环中填入物质,使相连物质间能发生反应,不相连物质间不能发生反应。你认为“五连环”中有空缺的一环应填入的物质是
考考你自己
A.稀硫酸 B.氧气
C.二氧化碳 D.氧化铜
物质的转化
02
思考﹒ 讨论
写出下列物质之间转化的化学方程式,体会由金属单质、非金属单质到盐的转化关系。
Ca → CaO → Ca(OH)2 → CaSO4
C → CO2 → H2CO3 → CaCO3
对于上述转化关系,从物质分类的角度看,你发现了什么规律?将你的想法与同学交流。
2.1 转化链
物质的转化
2
金属单质
碱性氧化物
碱
盐
酸或酸性氧化物
H2O
O2
非金属单质
酸性氧化物
酸
盐
碱或碱性氧化物
H2O
O2
如FeO Fe2O3 CuO等不与水反应
只有SiO2不与水反应
金属活动顺序表Al及以后金属的碱性氧化物与水不反应
各物质间还有没有其他什么转化?
2.2 转化网
物质的转化
2
金属单质
碱性氧化物
碱
盐
酸或酸性氧化物
H2O
O2
非金属单质
酸性氧化物
酸
盐
碱或碱性氧化物
H2O
O2
盐
判断以下反应能否发生。
1.锌与氯化铜
2.银与硫酸铜溶
3.碳酸钾与稀盐酸
4.硝酸银与氯化钡溶液
5.稀硫酸与氢氧化钠溶液
6.稀硝酸与硫酸钠
看谁做得既准又快
2.3 转化条件
物质的转化
2
置换反应
1
两反应
活泼性强的金属置换活泼性弱的金属
(K、Na、Ca、Ba先与水反应!)
2
复分解反应
气体、沉淀、水
有三条件中之一即可
无机物能否生成有机物?
6H2O+6CO2
C6H12O6+6O2
首次由无机物制备的有机物
化学史话
时间:19世纪
理论: 活力论
认为无机物与有机物有根本性差异
所以无机物无法变成有机物
有机化合物只能由生物的细胞
在一种特殊的力量
——生命力的作用下产生
人工合成是不可能的
尿素
哺乳动物、两栖动物和一些鱼的尿中含有尿素
1828年,他在合成氰酸铵时,却得到了尿素
1824年开始研究氰酸铵
化学史话
什么物质间反应可氢氧化钠?请写出化学方程式。
氧化钠与水反应
碳酸钠与氢氧化钙反应
上述过程的成本都较高,现在的工业生产中,一般选择电解饱和食盐水的方法来生产氢氧化钠。
考考你自己
已知在通电条件下,氯化钠和水反应生成氢氧化钠、氢气和氯气,请写出反应的化学方程式。
2NaCl+2H2O 2NaOH+H2↑+Cl2↑
2NaCl+2H2O 2NaOH+H2↑+Cl2↑
通电
电解槽
这节课我学到了什么?
(用一句话表示)
还有什么疑问?
课堂小结
课堂小结
酸、碱、盐的性质
1
酸有共同的性质:
酸溶液中,都含有H+
2
碱有共同的性质:
碱溶液中,都含有OH-
盐溶液中,都含有相同酸根或阳离子
3
某类盐有共同的性质:
思考﹒ 运用
氯化镁用于制金属镁、氧化镁、冷冻盐水、陶瓷,并用于填充织物、造纸等方面。
请写出制备氯化镁的途径,看谁写得最多。
盐
金属
碱性氧化物
酸
盐
非金属单质
盐
酸性氧化物
酸
金属
碱性氧化物
碱
酸
碱
盐
物质的转化
课堂小结
金属
单质
碱
盐
酸
盐
盐
盐和水
碱性
氧化物
酸性
氧化物
非金属
单质
碱和盐
酸和盐
另两种盐
金属和盐
氢气和盐
下列变化不能通过一步化学反应实现的是
A.BaCl2→BaSO4
B.CuO→Cu(OH)2
C.NaOH→Na2SO3
D.MgSO4→Mg(OH)2
考考你自己
铁、稀盐酸、澄清石灰水、氯化铜溶液是初中化学中常见的物质,四种物质间的反应关系如图所示。图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应四个反应类型的说法正确的是
牛刀小试
A.复分解反应、复分解反应、化合反应、置换反应
B.中和反应、置换反应、复分解反应、置换反应
C.复分解反应、复分解反应、置换反应、置换反应
D.分解反应、复分解反应、置换反应、置换反应
下表所列各组物质中,物质之间按箭头方向不能通过一步反应实现如图所示转化的是
A.甲为CuO、乙为CO2、丙为CO
B.甲为C、乙为CO、丙为CO2
C.甲为CaCO3、乙为CaO、丙为Ca(OH)2
D.甲为H2SO4、乙为H2O、丙为H2
请你试一试
甲
乙
丙
图中,“——”表示相连的物质间在一定条件下可以反应,“―→”表示丁在一定条件下通过置换反应可以转化为乙。下面四组选项中,符合图示要求的是
选项 甲 乙 丙 丁
A H2SO4 Na2SO4 NaOH NaCl
B BaCl2 K2CO3 HCl KOH
C O2 CO CuO C
D Fe CuCl2 Zn HCl
甲
乙
丙
丁
看我七十二变
X、Y、Z、W各代表一种物质,若X+Y==Z+W,则X和Y之间不可能是
A.盐和盐的反应
B.碱性氧化物和水的反应
C.酸与碱的反应
D.酸性氧化物和碱的反应
成功体验
抓住微粒认识性质
重视物质的转化条件
