1.1.2 有机化合物中的共价键和有机化合物的同分异构现象 课件(共52张PPT)高中化学选修三有机化学基础课件(人教版)
文档属性
| 名称 | 1.1.2 有机化合物中的共价键和有机化合物的同分异构现象 课件(共52张PPT)高中化学选修三有机化学基础课件(人教版) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-04 00:00:00 | ||
图片预览









文档简介
(共52张PPT)
第一节 有机化合物的结构特点
学习目标
1.认识有机化合物分子中共价键的类型、极性及其与有机反应的关系。
2.认识有机化合物的分子结构决定于原子间的连接顺序、成键方式和空间排布,认识有机化合物存在构造异构和立体异构等同分异构现象。
3.通过有机化合物分子的结构模型,建立对有机化合物分子的直观认识。
4.建立有机化合物同分异构体书写的基本思维模型,能正确书写和判断常见有机化合物的同分异构体。
核心素养
宏观辨识与微观探析:
能从宏观和微观的角度理解有机化合物分子的组成、性质与变化,能从不同角度认识有机化合物种类繁多的原因,从微观角度认识“同分异构现象”。
证据推理与模型认知:
建立书写和判断同分异构体的思维模型,并运用模型正确书写和判断有机化合物的同分异构体。
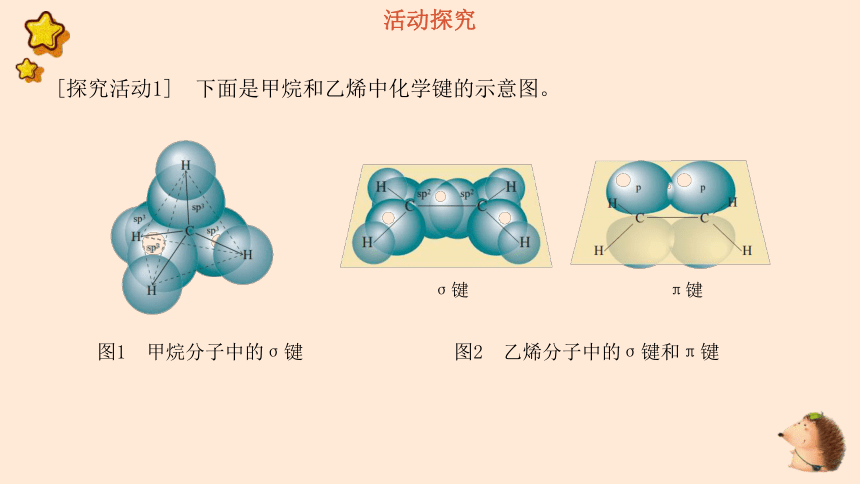
[探究活动1] 下面是甲烷和乙烯中化学键的示意图。
活动探究
图1 甲烷分子中的σ键
图2 乙烯分子中的σ键和π键
σ键
π键
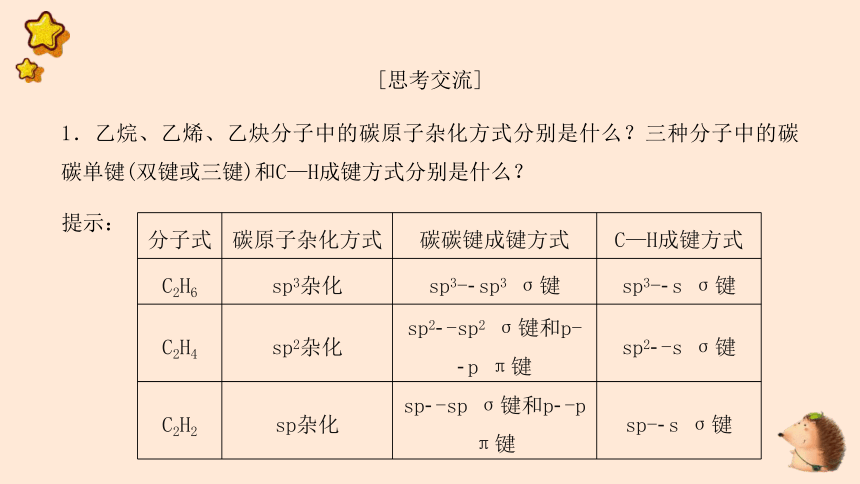
1.乙烷、乙烯、乙炔分子中的碳原子杂化方式分别是什么?三种分子中的碳碳单键(双键或三键)和C—H成键方式分别是什么?
提示:
分子式 碳原子杂化方式 碳碳键成键方式 C—H成键方式
C2H6 sp3杂化 sp3- sp3 σ键 sp3- s σ键
C2H4 sp2杂化 sp2 -sp2 σ键和p- p π键 sp2 -s σ键
C2H2 sp杂化 sp -sp σ键和p -p π键 sp- s σ键
[思考交流]
[思考交流]
2.乙醇与钠反应时分子中 (填字母代号,下同)键断裂,化学方程式为
。
3.乙醇与HBr发生取代反应时 键断裂,化学方程式为
。
[探究活动2] 共价键极性越强,在反应中越容易发生断裂,因此有机化合物的官能团及其邻近的化学键往往是发生化学反应的活性部位。根据乙醇的分子结构预测乙醇发生反应时的断键位置。
a
2CH3CH2OH+2Na―→2CH3CH2ONa+H2↑
b
4.写出乙酸与乙醇反应的化学方程式,根据乙酸与乙醇酯化反应的原理,说明乙酸分子结构中哪些共价键的极性较强?
提示:CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O;乙酸分子中的C—O的极性较强,容易发生断裂。
1.杂化方式的判断方法
(1)根据杂化轨道的空间结构判断
①若杂化轨道在空间的分布为四面体形或三角锥形,则中心原子发生sp3杂化。②若杂化轨道在空间的分布呈平面三角形,则中心原子发生sp2杂化。③若杂化轨道在空间的分布呈直线形,则中心原子发生sp杂化。
(2)根据中心原子价层电子对数判断:若中心原子的价层电子对数是4,则为sp3杂化;若中心原子的价层电子对数是3,则为sp2杂化;若中心原子的价层电子对数是2,则为sp杂化。
一、有机化合物中的共价键
知识梳理
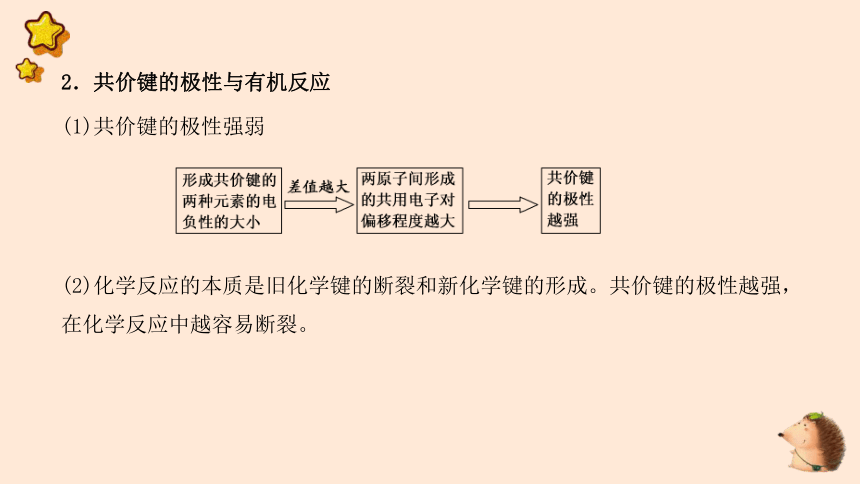
2.共价键的极性与有机反应
(1)共价键的极性强弱
(2)化学反应的本质是旧化学键的断裂和新化学键的形成。共价键的极性越强,在化学反应中越容易断裂。
1.下列关于丙烯(CH3—CH==CH2)的说法正确的是( )
A.丙烯分子中3个碳原子在同一直线上
B.丙烯分子中3个碳原子都是sp3杂化
C.丙烯分子中不存在非极性键
D.丙烯分子中有8个σ键、1个π键
巩固练习
D
【解析】乙烯分子中所有原子共平面,甲基为四面体结构,所以该分子中3个C原子不在同一直线上,但是位于同一平面上,故A错误;甲基上C原子价层电子对数是4、碳碳双键两端的C原子价层电子对数都是3,根据价层电子对互斥模型判断C原子杂化类型,甲基上C原子采用sp3杂化、其余两个C原子采用sp2杂化,故B错误;同种非金属元素之间易形成非极性键,不同非金属元素之间易形成极性键,该分子中存在C—C非极性键、C—H极性键,故C错误;共价单键为σ键,共价双键中一个是σ键、一个是π键,所以该分子中含有8个σ键、1个π键,故D正确。
2.图中1、2、3号碳原子的杂化类型分别是( )
A.sp3、sp、sp2
B.sp2、sp、sp2
C.sp2、sp2、sp3
D.sp2、sp2、sp2
【解析】双键含有1个π键,1个σ键,CH2==CH—COOH分子中存在碳碳双键,双键C原子价层电子对数=σ键数+孤电子对数=3+0=3,不含孤电子对,所以图中1、2号C原子采用sp2杂化;—COOH中,C原子价层电子对数=3+0=3,形成3个σ键,无孤电子对,所以图中3号C原子采用sp2杂化。
D
3.相同条件下金属钠和水反应与金属钠和无水乙醇反应相比前者较为剧烈的原因是( )
A.水是无机物,而乙醇是有机物
B.水的相对分子质量小,乙醇的相对分子质量大
C.乙醇分子中羟基与乙基相连,受乙基影响不如水分子中的羟基活泼
D.水是电解质,乙醇是非电解质
【解析】水分子及乙醇分子均可认为含有羟基,其中水分子中羟基与H原子相连,乙醇分子中羟基与乙基相连,乙醇分子中羟基由于受乙基影响不如水分子中的羟基活泼。
C
4.氰气的化学式为(CN)2,结构式为N≡C—C≡N,性质与卤素相似,下列叙述正确的是( )
A.不和氢氧化钠溶液发生反应
B.分子中N≡C的键长大于C≡C的键长
C.分子中既有极性键,又有非极性键
D.分子中含有2个σ键和4个π键
C
【解析】氰气性质与卤素相似,能和氢氧化钠溶液发生反应,A错误;同一周期中,元素原子半径随着原子序数的增大而减小,原子半径越大其键长越长,碳原子半径大于氮原子,所以氰分子中C≡N键长小于C≡C键长,B错误;同种原子间形成非极性键,不同原子间形成极性键,该分子的结构式为N≡C—C≡N,分子中既有极性键,又有非极性键,C正确;该分子的结构式为N≡C—C≡N,该分子中含有3个σ键和4个π键,D错误。
同一种分子式出现不同的结构的现象,李比希和维勒在19世纪时就已发现,当时两人各自得到的两种的物质——氰酸和雷酸,但经测定这两种分子组成完全相同性质完全不同,随后由贝采尼乌斯提出了“同分异性”,后改为“同分异构”。分析下表中有机化合物产生异构的原因。
有机化合物 异构类别 形成原因
CH3CH2CH2CH3与
CH2==CH—CH2—CH3与 CH3—CH==CH—CH3
CH3CH2OH与CH3—O—CH3
活动探究
碳架异构
位置异构
官能团异构
碳骨架不同而产生的异构
官能团的位置不同而产生的异构
官能团不同而产生的异构
1. 是否为同分异构体?说明理由。
提示:不是同分异构体,由于二者均为四面体结构,为同一种物质。
2.CH3—CH==CH2与 互为同分异构体吗?同分异构体的化学性质一定相同吗?
提示:二者分子式相同,碳原子与碳原子间的连接方式不同,结构不同,是同分异构体;同分异构体可能是不同类的物质,如题干所述两种物质,它们的化学性质不同。
[思考交流]
3.分子式为C4H8且属于烯烃的同分异构体有几种?试写出其结构简式。
提示:C4H8属于烯烃的结构有3种,其结构简式分别为CH2==CH—CH2—CH3、CH3—CH==CH—CH3、 。
1.同分异构体的书写规律
(1)烷烃:烷烃只存在碳架异构,书写时要注意全面而不重复,具体规则如下:
二、同分异构现象与同分异构体
知识梳理
下面以己烷(C6H14)为例说明(用碳骨架表示)。
①将分子中全部碳原子连成直链作为母链。
C—C—C—C—C—C
②从母链的一端取下1个碳原子,依次连接在母链中心对称线一侧的各个碳原子上,即得到多个带有甲基、主链比母链少1个碳原子的异构体的碳骨架。
故己烷(C6H14)共有5种同分异构体。
③从母链上一端取下两个C原子,使这两个C原子相连(整连)或分开(散连),依次连接在母链所剩下的各个碳原子上,得多个带1个乙基或两个甲基、主链比母链少两个碳原子的异构体的碳骨架。
②位置异构:用箭头表示双键的位置,即 、 。C4H8属于烯烃的同分异构体共有3种。
(2)单烯烃同分异构体的书写
书写方法:先链后位,即先写出可能的碳链方式,再加上含有的官能团位置。下面以C4H8为例说明。
①碳架异构:C—C—C—C、 。
(3)苯的同系物的同分异构体的判断方法:从单取代到多取代,二取代时取代基有邻、间、对三种情况。例如分子式为C8H10的芳香族化合物,苯环外有两个饱和碳,单取代结构为 ,若为二取代,有邻( )、间
( )、对( )三种情况。
2.烃的衍生物同分异构体的书写
(1)卤代烃的同分异构体的书写
①一卤代烃的同分异构体判断方法:等效氢法
A.同一碳原子上的氢原子等效,如—CH3上的3个氢原子等效。
B.同一碳原子上所连甲基氢原子都是等效的。如新戊烷中四个甲基上的氢原子都是等效的。
C.同一分子中处于轴对称位置或镜面对称位置上的氢原子是等效的。如
分子中,在苯环所在的平面内有两条互相垂直的对称轴,故有两类等效氢。
②二卤代烃的同分异构体判断方法:定一动一。“定一”时,有几种氢就有几种情况;“动一”时,在“定一”确定的每一条碳骨架上寻找第二个取代基的位置。如乙烷的二氯代物共有2种。
③多卤代烃的同分异构体判断方法:换元法。即一种烃若有m个H可被取代,则它的n元取代物与(m-n)元取代物种类相等。如乙烷的二氯代物有2种,则四氯代物也有2种。
(2)烃的含氧衍生物的同分异构体
①官能团异构:官能团种类不同而产生的异构。
②碳架异构:碳骨架不同产生的异构。书写时应遵循“主链由长到短,支链由整到散,位置由心到边,排布由邻到间”的规律。
③位置异构:官能团在碳链中位置不同产生的异构。书写时在每一条碳链上移动官能团位置。需注意取代“等效氢”后所得结构为同一种。
④补氢:用氢原子补足碳原子的四个价键。
⑤检查:看是否有书写重复或书写遗漏,根据“碳四价”原则检验是否有书写错误。
例如:寻找符合分子式C4H10O的同分异构体有多少种。
四个碳原子构成的链状烷烃共有两条碳骨架,分别为C—C—C—C和 ,
若为醇,羟基连在碳原子上,位置有 共4种;若为醚,
醚键可用插入法放于两个碳原子之间,位置有 和 共3种。因此符合C4H10O分子式的共有7种同分异构体。
1.科学家发现铂的两种化合物(如图)有不同的特性,a具有抗癌作用,而b没有。则a和b属于( )
A.同分异构体 B.同素异形体
C.同位素 D.同一种物质
【解析】a和b的分子式相同,a具有抗癌作用而b没有,即性质不同,所以结构不同,则属于同分异构体。
巩固练习
A
C
【解析】A项,二者互为同系物,错误;B项,二者结构相同,分子式相同,属于同种物质,错误;C项,二者分子式相同,结构不同,互为同分异构体,正确;D项,二者互为同系物,错误。
3.如图均是由4个碳原子结合成的6种有机化合物(氢原子没有画出)。
(1)有机化合物a有一种同分异构体,试写出其结构简式________________。
(2)上述有机化合物中与c互为同分异构体的是______(填字母)。
(3)任写一种与e互为同系物的有机化合物的结构简式__________。
CH3CH2CH2CH3
bf
CH≡CH
【解析】a~f 6种有机化合物的结构简式分别为 、 、
CH3—CH==CH—CH3、CH2==CH—CH==CH2、HC≡C—CH2—CH3、 ,
再根据相关知识得出相应的答案。
立方烷(C8H8)为人工合成的烷烃,又称为五环辛烷,外观为有光泽的晶体。八个碳原子对称地排列在立方体的八个角上。人们曾一度认为其不可合成,因为碳碳键的键角均为90°,张力过大而不稳定。不过当此物质被合成出以后,人们发现它在动力学上很稳定。立方烷生成热、密度等均很大,因而备受瞩目。
情境探究
1.立方烷的一氯代物有几种?
提示:1种。立方烷只有一种氢原子。
2.立方烷的二氯代物有几种?
提示:3种。二氯代物的同分异构体分别是一条棱、面对角线、体对角线上的两个氢原子被氯原子代替,所以二氯代物的同分异构体有三种。
3.立方烷的三氯代物有几种?
提示:3种。立方烷有8个氢原子,依据(2)得知其中2个氢原子被氯原子取代形成立方烷的二氯代物有3种,那么在此基础上,剩余的氢原子的环境分别也只有一种,故得到三氯代物也有3种同分异构体。
[思考交流]
1.等效氢法
单官能团有机物分子可以看作烃分子中一个氢原子被其他的原子或官能团取代的产物,确定其同分异构体数目时,实质上是看处于不同位置的氢原子的数目,可用“等效氢法”判断。判断“等效氢”的三原则是:
(1)同一碳原子上的氢原子是等效的,如CH4中的4个氢原子等效。
(2)同一碳原子上所连的甲基上的氢原子是等效的,如C(CH3)4中的4个甲基上的12个氢原子等效。
三、同分异构体种数的判断
知识梳理
2.烃基取代法
(1)记住常见烃基的结构:丙基有2种结构,丁基有4种结构,戊基有8种结构。
(2)将有机物分子拆分为烃基和官能团两部分,根据烃基同分异构体的数目,确定目标分子的数目,如C4H10O属于醇的可改写为C4H9—OH,共有4种结构,C5H10O属于醛的可改写为C4H9—CHO,共有4种结构。
(3)处于对称位置上的氢原子是等效的,如CH3CH3中的6个氢原子等效,乙烯分子中的4个氢原子等效,苯分子中的6个氢原子等效,CH3C(CH3)2C(CH3)2CH3上的18个氢原子等效。
3.定一移一法
对于二元代物的同分异构体的判断,可固定一个取代基的位置,再移动另一个取代基,以确定同分异构体的数目。如CH3CH2CH3的二氯代物数目:第1步固
定1个氯原子有2种: 。第2步固定第2个氯原子:①有3
种,②有2种,其中①b和②d重复,故CH3CH2CH3的二氯代物有4种。
4.换元法
如:二氯苯C6H4Cl2有3种同分异构体: 、 。
用H代替Cl,用Cl代替H,则四氯苯也有3种同分异构体。
1.分子式为C4H9Cl的有机物同分异构体的数目有( )
A.1种 B.2种
C.3种 D.4种
【解析】
巩固练习
D
2.分子式为C7H8O的同分异构体中含有苯环且属于醇类的有几种( )
A.1种 B.2种
C.5种 D.3种
【解析】分子式为C7H8O的同分异构体中属于醇类的为 ,只有一种。
A
3.在欧洲一些国家曾发现饲料被污染,导致畜禽类制品及乳制品不能食用,经测定饲料中含有剧毒物质二噁英,其结构为 ,已知它的二氯代物有10种,则其六氯代物有( )
A.15种 B.11种 C.10种 D.5种
【解析】解答本题可用替代法:二噁英的分子式为C12H8O2,其二氯代物有10种,将氯原子代替氢原子,氢原子代替氯原子,可知其六氯代物也有10种同分异构体。
C
4.(1)三联苯 的一氯代物有________种同分异构体。
(2)与 互为同分异构体的芳香族化合物有________种。
(3)水杨酸的结构简式为 。
①水杨酸的同分异构体中,属于酚类同时还属于酯类的化合物有________种。
②水杨酸的同分异构体中,属于酚类,但不属于酯类也不属于羧酸的化合物必定含有__________(除了羟基之外的官能团名称)。
4
5
3
醛基
(3)①同时属于酯类和酚类的同分异构体分别是
共3种。②依题意,水杨酸的同分异构体中,属于酚类则含有 ,剩余残基为—COOH,因不属于酯类也不属于羧酸类,故只能将其再拆分为—OH和—
CHO连接在苯环上,形成 (羟基与醛基的位置可以改变)。
1.下列关于有机化合物中化学键的说法正确的是( )
A.烷烃中的化学键均为σ键
B.CH3NH2中C—H的极性比N—H的极性强
C.乙烯分子中只含有极性键不含有非极性键
D.丙炔分子中含有5个σ键和3个π键
【解析】有机化合物中单键均为σ键,A正确;N的电负性强于C,则N—H的极性强于C—H的极性,B错误;乙烯分子既含极性键又含有非极性键,C错误;丙炔中单键都是σ键,三键中有1个σ键和2个π键,所以丙炔含有6个σ键,2个π键,D错误。
当堂检测
A
2.互为同分异构体的物质不可能( )
A.具有相同的相对分子质量
B.具有相同的熔、沸点和密度
C.具有相同的分子式
D.组成元素相同
【解析】互为同分异构体的物质,其分子式相同(相对分子质量也相同),但结构不同,因此,其物理性质不同。
B
3.下列选项属于碳架异构的是( )
A.CH3—C≡C—CH3和CH3—CH2—C≡CH
B. 和CH3—CH2—CH2—CH2—CH3
C. 和
D.CH3—CH2—CH2Br和CH3—CHBr—CH3
【解析】碳架异构是碳骨架不同产生的异构现象。A、D选项属于位置异构,C选项是官能团异构,选项B是碳架异构。
B
4.分子式为C5H10O2并能与饱和NaHCO3溶液反应放出气体的有机化合物(不含立体异构)有( )
A.3种 B.4种
C.5种 D.6种
B
5.已知下列有机化合物:
②CH2===CH—CH2—CH3和CH3—CH===CH—CH3
③ CH3—CH2—OH和CH3—O—CH3
⑥CH3—CH2—CH===CH—CH3和 (环戊烷)
⑦CH2===CH—CH===CH2和CH3—CH2—C≡CH
⑧CH3—CH2—NO2和H2N—CH2—COOH
(1)其中互为同分异构体的是____________________。
(2)其中属于碳架异构的是____________________。
(3)其中属于位置异构的是____________________。
(4)其中属于官能团异构的是____________________。
(5)其中属于同一种物质的是____________________。
①②③④⑥⑦⑧
①
②
③④⑥⑦⑧
⑤
第一节 有机化合物的结构特点
学习目标
1.认识有机化合物分子中共价键的类型、极性及其与有机反应的关系。
2.认识有机化合物的分子结构决定于原子间的连接顺序、成键方式和空间排布,认识有机化合物存在构造异构和立体异构等同分异构现象。
3.通过有机化合物分子的结构模型,建立对有机化合物分子的直观认识。
4.建立有机化合物同分异构体书写的基本思维模型,能正确书写和判断常见有机化合物的同分异构体。
核心素养
宏观辨识与微观探析:
能从宏观和微观的角度理解有机化合物分子的组成、性质与变化,能从不同角度认识有机化合物种类繁多的原因,从微观角度认识“同分异构现象”。
证据推理与模型认知:
建立书写和判断同分异构体的思维模型,并运用模型正确书写和判断有机化合物的同分异构体。
[探究活动1] 下面是甲烷和乙烯中化学键的示意图。
活动探究
图1 甲烷分子中的σ键
图2 乙烯分子中的σ键和π键
σ键
π键
1.乙烷、乙烯、乙炔分子中的碳原子杂化方式分别是什么?三种分子中的碳碳单键(双键或三键)和C—H成键方式分别是什么?
提示:
分子式 碳原子杂化方式 碳碳键成键方式 C—H成键方式
C2H6 sp3杂化 sp3- sp3 σ键 sp3- s σ键
C2H4 sp2杂化 sp2 -sp2 σ键和p- p π键 sp2 -s σ键
C2H2 sp杂化 sp -sp σ键和p -p π键 sp- s σ键
[思考交流]
[思考交流]
2.乙醇与钠反应时分子中 (填字母代号,下同)键断裂,化学方程式为
。
3.乙醇与HBr发生取代反应时 键断裂,化学方程式为
。
[探究活动2] 共价键极性越强,在反应中越容易发生断裂,因此有机化合物的官能团及其邻近的化学键往往是发生化学反应的活性部位。根据乙醇的分子结构预测乙醇发生反应时的断键位置。
a
2CH3CH2OH+2Na―→2CH3CH2ONa+H2↑
b
4.写出乙酸与乙醇反应的化学方程式,根据乙酸与乙醇酯化反应的原理,说明乙酸分子结构中哪些共价键的极性较强?
提示:CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O;乙酸分子中的C—O的极性较强,容易发生断裂。
1.杂化方式的判断方法
(1)根据杂化轨道的空间结构判断
①若杂化轨道在空间的分布为四面体形或三角锥形,则中心原子发生sp3杂化。②若杂化轨道在空间的分布呈平面三角形,则中心原子发生sp2杂化。③若杂化轨道在空间的分布呈直线形,则中心原子发生sp杂化。
(2)根据中心原子价层电子对数判断:若中心原子的价层电子对数是4,则为sp3杂化;若中心原子的价层电子对数是3,则为sp2杂化;若中心原子的价层电子对数是2,则为sp杂化。
一、有机化合物中的共价键
知识梳理
2.共价键的极性与有机反应
(1)共价键的极性强弱
(2)化学反应的本质是旧化学键的断裂和新化学键的形成。共价键的极性越强,在化学反应中越容易断裂。
1.下列关于丙烯(CH3—CH==CH2)的说法正确的是( )
A.丙烯分子中3个碳原子在同一直线上
B.丙烯分子中3个碳原子都是sp3杂化
C.丙烯分子中不存在非极性键
D.丙烯分子中有8个σ键、1个π键
巩固练习
D
【解析】乙烯分子中所有原子共平面,甲基为四面体结构,所以该分子中3个C原子不在同一直线上,但是位于同一平面上,故A错误;甲基上C原子价层电子对数是4、碳碳双键两端的C原子价层电子对数都是3,根据价层电子对互斥模型判断C原子杂化类型,甲基上C原子采用sp3杂化、其余两个C原子采用sp2杂化,故B错误;同种非金属元素之间易形成非极性键,不同非金属元素之间易形成极性键,该分子中存在C—C非极性键、C—H极性键,故C错误;共价单键为σ键,共价双键中一个是σ键、一个是π键,所以该分子中含有8个σ键、1个π键,故D正确。
2.图中1、2、3号碳原子的杂化类型分别是( )
A.sp3、sp、sp2
B.sp2、sp、sp2
C.sp2、sp2、sp3
D.sp2、sp2、sp2
【解析】双键含有1个π键,1个σ键,CH2==CH—COOH分子中存在碳碳双键,双键C原子价层电子对数=σ键数+孤电子对数=3+0=3,不含孤电子对,所以图中1、2号C原子采用sp2杂化;—COOH中,C原子价层电子对数=3+0=3,形成3个σ键,无孤电子对,所以图中3号C原子采用sp2杂化。
D
3.相同条件下金属钠和水反应与金属钠和无水乙醇反应相比前者较为剧烈的原因是( )
A.水是无机物,而乙醇是有机物
B.水的相对分子质量小,乙醇的相对分子质量大
C.乙醇分子中羟基与乙基相连,受乙基影响不如水分子中的羟基活泼
D.水是电解质,乙醇是非电解质
【解析】水分子及乙醇分子均可认为含有羟基,其中水分子中羟基与H原子相连,乙醇分子中羟基与乙基相连,乙醇分子中羟基由于受乙基影响不如水分子中的羟基活泼。
C
4.氰气的化学式为(CN)2,结构式为N≡C—C≡N,性质与卤素相似,下列叙述正确的是( )
A.不和氢氧化钠溶液发生反应
B.分子中N≡C的键长大于C≡C的键长
C.分子中既有极性键,又有非极性键
D.分子中含有2个σ键和4个π键
C
【解析】氰气性质与卤素相似,能和氢氧化钠溶液发生反应,A错误;同一周期中,元素原子半径随着原子序数的增大而减小,原子半径越大其键长越长,碳原子半径大于氮原子,所以氰分子中C≡N键长小于C≡C键长,B错误;同种原子间形成非极性键,不同原子间形成极性键,该分子的结构式为N≡C—C≡N,分子中既有极性键,又有非极性键,C正确;该分子的结构式为N≡C—C≡N,该分子中含有3个σ键和4个π键,D错误。
同一种分子式出现不同的结构的现象,李比希和维勒在19世纪时就已发现,当时两人各自得到的两种的物质——氰酸和雷酸,但经测定这两种分子组成完全相同性质完全不同,随后由贝采尼乌斯提出了“同分异性”,后改为“同分异构”。分析下表中有机化合物产生异构的原因。
有机化合物 异构类别 形成原因
CH3CH2CH2CH3与
CH2==CH—CH2—CH3与 CH3—CH==CH—CH3
CH3CH2OH与CH3—O—CH3
活动探究
碳架异构
位置异构
官能团异构
碳骨架不同而产生的异构
官能团的位置不同而产生的异构
官能团不同而产生的异构
1. 是否为同分异构体?说明理由。
提示:不是同分异构体,由于二者均为四面体结构,为同一种物质。
2.CH3—CH==CH2与 互为同分异构体吗?同分异构体的化学性质一定相同吗?
提示:二者分子式相同,碳原子与碳原子间的连接方式不同,结构不同,是同分异构体;同分异构体可能是不同类的物质,如题干所述两种物质,它们的化学性质不同。
[思考交流]
3.分子式为C4H8且属于烯烃的同分异构体有几种?试写出其结构简式。
提示:C4H8属于烯烃的结构有3种,其结构简式分别为CH2==CH—CH2—CH3、CH3—CH==CH—CH3、 。
1.同分异构体的书写规律
(1)烷烃:烷烃只存在碳架异构,书写时要注意全面而不重复,具体规则如下:
二、同分异构现象与同分异构体
知识梳理
下面以己烷(C6H14)为例说明(用碳骨架表示)。
①将分子中全部碳原子连成直链作为母链。
C—C—C—C—C—C
②从母链的一端取下1个碳原子,依次连接在母链中心对称线一侧的各个碳原子上,即得到多个带有甲基、主链比母链少1个碳原子的异构体的碳骨架。
故己烷(C6H14)共有5种同分异构体。
③从母链上一端取下两个C原子,使这两个C原子相连(整连)或分开(散连),依次连接在母链所剩下的各个碳原子上,得多个带1个乙基或两个甲基、主链比母链少两个碳原子的异构体的碳骨架。
②位置异构:用箭头表示双键的位置,即 、 。C4H8属于烯烃的同分异构体共有3种。
(2)单烯烃同分异构体的书写
书写方法:先链后位,即先写出可能的碳链方式,再加上含有的官能团位置。下面以C4H8为例说明。
①碳架异构:C—C—C—C、 。
(3)苯的同系物的同分异构体的判断方法:从单取代到多取代,二取代时取代基有邻、间、对三种情况。例如分子式为C8H10的芳香族化合物,苯环外有两个饱和碳,单取代结构为 ,若为二取代,有邻( )、间
( )、对( )三种情况。
2.烃的衍生物同分异构体的书写
(1)卤代烃的同分异构体的书写
①一卤代烃的同分异构体判断方法:等效氢法
A.同一碳原子上的氢原子等效,如—CH3上的3个氢原子等效。
B.同一碳原子上所连甲基氢原子都是等效的。如新戊烷中四个甲基上的氢原子都是等效的。
C.同一分子中处于轴对称位置或镜面对称位置上的氢原子是等效的。如
分子中,在苯环所在的平面内有两条互相垂直的对称轴,故有两类等效氢。
②二卤代烃的同分异构体判断方法:定一动一。“定一”时,有几种氢就有几种情况;“动一”时,在“定一”确定的每一条碳骨架上寻找第二个取代基的位置。如乙烷的二氯代物共有2种。
③多卤代烃的同分异构体判断方法:换元法。即一种烃若有m个H可被取代,则它的n元取代物与(m-n)元取代物种类相等。如乙烷的二氯代物有2种,则四氯代物也有2种。
(2)烃的含氧衍生物的同分异构体
①官能团异构:官能团种类不同而产生的异构。
②碳架异构:碳骨架不同产生的异构。书写时应遵循“主链由长到短,支链由整到散,位置由心到边,排布由邻到间”的规律。
③位置异构:官能团在碳链中位置不同产生的异构。书写时在每一条碳链上移动官能团位置。需注意取代“等效氢”后所得结构为同一种。
④补氢:用氢原子补足碳原子的四个价键。
⑤检查:看是否有书写重复或书写遗漏,根据“碳四价”原则检验是否有书写错误。
例如:寻找符合分子式C4H10O的同分异构体有多少种。
四个碳原子构成的链状烷烃共有两条碳骨架,分别为C—C—C—C和 ,
若为醇,羟基连在碳原子上,位置有 共4种;若为醚,
醚键可用插入法放于两个碳原子之间,位置有 和 共3种。因此符合C4H10O分子式的共有7种同分异构体。
1.科学家发现铂的两种化合物(如图)有不同的特性,a具有抗癌作用,而b没有。则a和b属于( )
A.同分异构体 B.同素异形体
C.同位素 D.同一种物质
【解析】a和b的分子式相同,a具有抗癌作用而b没有,即性质不同,所以结构不同,则属于同分异构体。
巩固练习
A
C
【解析】A项,二者互为同系物,错误;B项,二者结构相同,分子式相同,属于同种物质,错误;C项,二者分子式相同,结构不同,互为同分异构体,正确;D项,二者互为同系物,错误。
3.如图均是由4个碳原子结合成的6种有机化合物(氢原子没有画出)。
(1)有机化合物a有一种同分异构体,试写出其结构简式________________。
(2)上述有机化合物中与c互为同分异构体的是______(填字母)。
(3)任写一种与e互为同系物的有机化合物的结构简式__________。
CH3CH2CH2CH3
bf
CH≡CH
【解析】a~f 6种有机化合物的结构简式分别为 、 、
CH3—CH==CH—CH3、CH2==CH—CH==CH2、HC≡C—CH2—CH3、 ,
再根据相关知识得出相应的答案。
立方烷(C8H8)为人工合成的烷烃,又称为五环辛烷,外观为有光泽的晶体。八个碳原子对称地排列在立方体的八个角上。人们曾一度认为其不可合成,因为碳碳键的键角均为90°,张力过大而不稳定。不过当此物质被合成出以后,人们发现它在动力学上很稳定。立方烷生成热、密度等均很大,因而备受瞩目。
情境探究
1.立方烷的一氯代物有几种?
提示:1种。立方烷只有一种氢原子。
2.立方烷的二氯代物有几种?
提示:3种。二氯代物的同分异构体分别是一条棱、面对角线、体对角线上的两个氢原子被氯原子代替,所以二氯代物的同分异构体有三种。
3.立方烷的三氯代物有几种?
提示:3种。立方烷有8个氢原子,依据(2)得知其中2个氢原子被氯原子取代形成立方烷的二氯代物有3种,那么在此基础上,剩余的氢原子的环境分别也只有一种,故得到三氯代物也有3种同分异构体。
[思考交流]
1.等效氢法
单官能团有机物分子可以看作烃分子中一个氢原子被其他的原子或官能团取代的产物,确定其同分异构体数目时,实质上是看处于不同位置的氢原子的数目,可用“等效氢法”判断。判断“等效氢”的三原则是:
(1)同一碳原子上的氢原子是等效的,如CH4中的4个氢原子等效。
(2)同一碳原子上所连的甲基上的氢原子是等效的,如C(CH3)4中的4个甲基上的12个氢原子等效。
三、同分异构体种数的判断
知识梳理
2.烃基取代法
(1)记住常见烃基的结构:丙基有2种结构,丁基有4种结构,戊基有8种结构。
(2)将有机物分子拆分为烃基和官能团两部分,根据烃基同分异构体的数目,确定目标分子的数目,如C4H10O属于醇的可改写为C4H9—OH,共有4种结构,C5H10O属于醛的可改写为C4H9—CHO,共有4种结构。
(3)处于对称位置上的氢原子是等效的,如CH3CH3中的6个氢原子等效,乙烯分子中的4个氢原子等效,苯分子中的6个氢原子等效,CH3C(CH3)2C(CH3)2CH3上的18个氢原子等效。
3.定一移一法
对于二元代物的同分异构体的判断,可固定一个取代基的位置,再移动另一个取代基,以确定同分异构体的数目。如CH3CH2CH3的二氯代物数目:第1步固
定1个氯原子有2种: 。第2步固定第2个氯原子:①有3
种,②有2种,其中①b和②d重复,故CH3CH2CH3的二氯代物有4种。
4.换元法
如:二氯苯C6H4Cl2有3种同分异构体: 、 。
用H代替Cl,用Cl代替H,则四氯苯也有3种同分异构体。
1.分子式为C4H9Cl的有机物同分异构体的数目有( )
A.1种 B.2种
C.3种 D.4种
【解析】
巩固练习
D
2.分子式为C7H8O的同分异构体中含有苯环且属于醇类的有几种( )
A.1种 B.2种
C.5种 D.3种
【解析】分子式为C7H8O的同分异构体中属于醇类的为 ,只有一种。
A
3.在欧洲一些国家曾发现饲料被污染,导致畜禽类制品及乳制品不能食用,经测定饲料中含有剧毒物质二噁英,其结构为 ,已知它的二氯代物有10种,则其六氯代物有( )
A.15种 B.11种 C.10种 D.5种
【解析】解答本题可用替代法:二噁英的分子式为C12H8O2,其二氯代物有10种,将氯原子代替氢原子,氢原子代替氯原子,可知其六氯代物也有10种同分异构体。
C
4.(1)三联苯 的一氯代物有________种同分异构体。
(2)与 互为同分异构体的芳香族化合物有________种。
(3)水杨酸的结构简式为 。
①水杨酸的同分异构体中,属于酚类同时还属于酯类的化合物有________种。
②水杨酸的同分异构体中,属于酚类,但不属于酯类也不属于羧酸的化合物必定含有__________(除了羟基之外的官能团名称)。
4
5
3
醛基
(3)①同时属于酯类和酚类的同分异构体分别是
共3种。②依题意,水杨酸的同分异构体中,属于酚类则含有 ,剩余残基为—COOH,因不属于酯类也不属于羧酸类,故只能将其再拆分为—OH和—
CHO连接在苯环上,形成 (羟基与醛基的位置可以改变)。
1.下列关于有机化合物中化学键的说法正确的是( )
A.烷烃中的化学键均为σ键
B.CH3NH2中C—H的极性比N—H的极性强
C.乙烯分子中只含有极性键不含有非极性键
D.丙炔分子中含有5个σ键和3个π键
【解析】有机化合物中单键均为σ键,A正确;N的电负性强于C,则N—H的极性强于C—H的极性,B错误;乙烯分子既含极性键又含有非极性键,C错误;丙炔中单键都是σ键,三键中有1个σ键和2个π键,所以丙炔含有6个σ键,2个π键,D错误。
当堂检测
A
2.互为同分异构体的物质不可能( )
A.具有相同的相对分子质量
B.具有相同的熔、沸点和密度
C.具有相同的分子式
D.组成元素相同
【解析】互为同分异构体的物质,其分子式相同(相对分子质量也相同),但结构不同,因此,其物理性质不同。
B
3.下列选项属于碳架异构的是( )
A.CH3—C≡C—CH3和CH3—CH2—C≡CH
B. 和CH3—CH2—CH2—CH2—CH3
C. 和
D.CH3—CH2—CH2Br和CH3—CHBr—CH3
【解析】碳架异构是碳骨架不同产生的异构现象。A、D选项属于位置异构,C选项是官能团异构,选项B是碳架异构。
B
4.分子式为C5H10O2并能与饱和NaHCO3溶液反应放出气体的有机化合物(不含立体异构)有( )
A.3种 B.4种
C.5种 D.6种
B
5.已知下列有机化合物:
②CH2===CH—CH2—CH3和CH3—CH===CH—CH3
③ CH3—CH2—OH和CH3—O—CH3
⑥CH3—CH2—CH===CH—CH3和 (环戊烷)
⑦CH2===CH—CH===CH2和CH3—CH2—C≡CH
⑧CH3—CH2—NO2和H2N—CH2—COOH
(1)其中互为同分异构体的是____________________。
(2)其中属于碳架异构的是____________________。
(3)其中属于位置异构的是____________________。
(4)其中属于官能团异构的是____________________。
(5)其中属于同一种物质的是____________________。
①②③④⑥⑦⑧
①
②
③④⑥⑦⑧
⑤
