2023-2024学年(人教版2019)高中化学必修1第二章 第三节 第1课时 物质的量 摩尔质量 学案 (含答案)
文档属性
| 名称 | 2023-2024学年(人教版2019)高中化学必修1第二章 第三节 第1课时 物质的量 摩尔质量 学案 (含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 465.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-06 00:00:00 | ||
图片预览


文档简介
第三节 物质的量
第1课时 物质的量 摩尔质量
[核心素养发展目标] 1.了解物质的量及其单位、阿伏加德罗常数、摩尔质量的含义与应用,利用物质的量将宏观物理量与微观粒子的个数联系起来,并能从宏观和微观结合的视角分析解决问题。2.能从物质的量的角度认识物质的组成及变化,建立物质的量、物质的质量和微观粒子数之间计算的思维模型。
一、物质的量的单位——摩尔
1.物质的量
(1)物质的量是表示含有____________________________的集合体的物理量,用符号n表示。
(2)物质的量的单位——摩尔
(3)表示方法及含义
明确物质的量的规范表示
如1 mol H指1 mol________,1 mol H2(氢气)指1 mol________,不能说1 mol氢,指代不明确。
2.阿伏加德罗常数(NA)
特别提醒 阿伏加德罗常数的单位为mol-1。
3.物质的量、阿伏加德罗常数与粒子数之间的关系
(1)关系式:n=________________。
思考1 通过下图可进一步认识水的组成,并理解物质的量与微粒数目的关系?
思考2 运用物质的量与微粒数目的关系,分析下列问题。
(1)1 mol CO2中有______ mol C和______ mol O,0.5 mol CO2中有__________ mol C和________ mol O。________ mol CO2含有0.5 mol氧原子。
(2)1 mol Na2SO4中含有Na+的数目是______,与________mol NaCl含有相同Na+数目。
(3)0.2 mol NH3与________ H2O中所含H原子数一样多。若用NA表示阿伏加德罗常数的值,0.3 mol H2O中含____个电子。
(2)结论:微粒之间的物质的量之比等于微粒的________之比。
1.判断正误
(1)物质的量可以理解为物质的数量( )
(2)1 mol任何粒子所含有的粒子数相等( )
(3)阿伏加德罗常数就是6.02×1023( )
(4)1 mol水中含有2 mol氢和1 mol氧( )
2.下列叙述正确的是( )
A.摩尔是表示物质所含微粒数量以及物质质量的具有双重意义的单位
B.摩尔是国际单位制中7个基本物理量之一
C.含有6.02×1023个氧原子的H3PO4的物质的量是0.25 mol
D.2H既可以表示2个氢原子又可以表示2 mol氢原子
二、摩尔质量
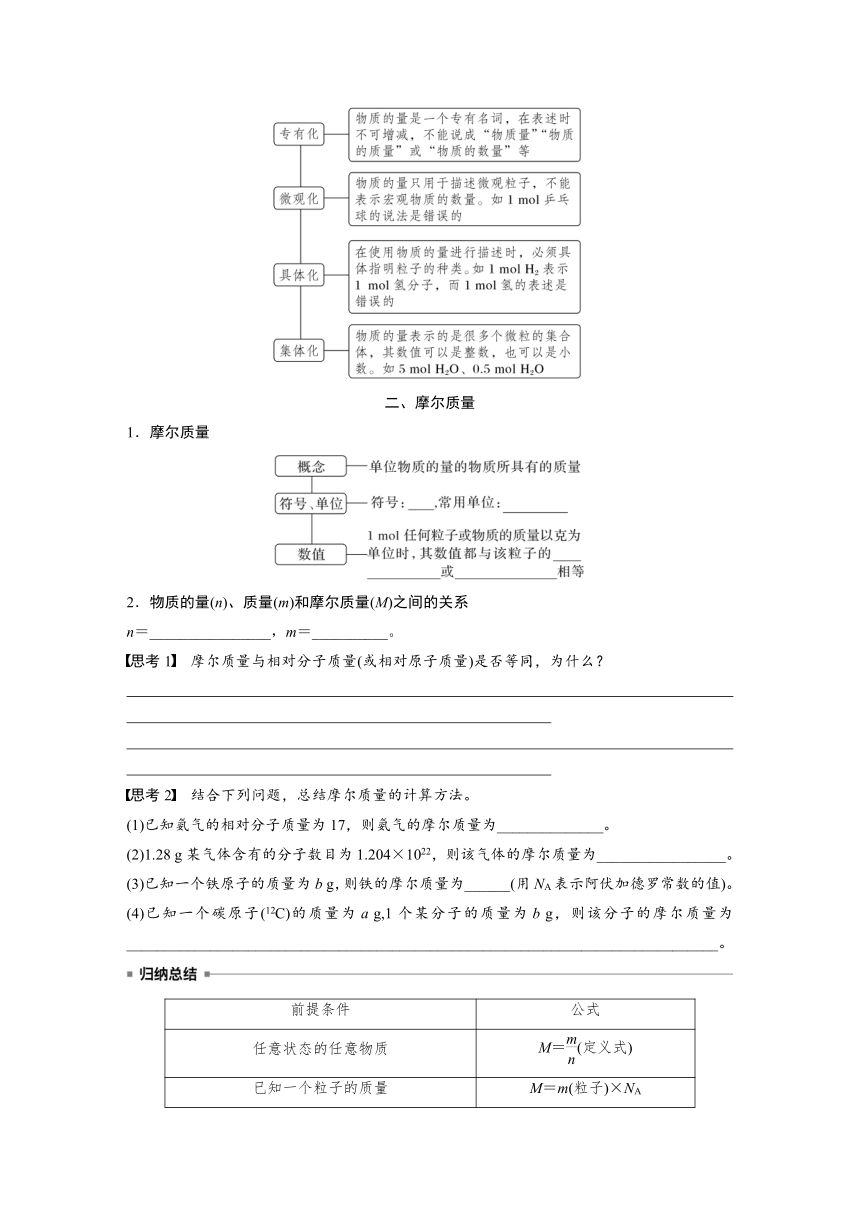
1.摩尔质量
2.物质的量(n)、质量(m)和摩尔质量(M)之间的关系
n=________________,m=__________。
思考1 摩尔质量与相对分子质量(或相对原子质量)是否等同,为什么?
思考2 结合下列问题,总结摩尔质量的计算方法。
(1)已知氨气的相对分子质量为17,则氨气的摩尔质量为______________。
(2)1.28 g某气体含有的分子数目为1.204×1022,则该气体的摩尔质量为_________________。
(3)已知一个铁原子的质量为b g,则铁的摩尔质量为______(用NA表示阿伏加德罗常数的值)。
(4)已知一个碳原子(12C)的质量为a g,1个某分子的质量为b g,则该分子的摩尔质量为______________________________________________________________________________。
前提条件 公式
任意状态的任意物质 M=(定义式)
已知一个粒子的质量 M=m(粒子)×NA
已知一个粒子的质量和一个12C原子的质量 M=
1.判断正误
(1)氯化氢的摩尔质量是36.5 g( )
(2)氮的摩尔质量是28 g·mol-1( )
(3)CH4的摩尔质量和NA个CH4分子的质量相等( )
(4)2NA个CO2的摩尔质量为88 g·mol-1( )
(5)Fe的摩尔质量为56 g·mol-1,则1个Fe原子质量为 g( )
2.我国科学家屠呦呦发现青蒿素,它是一种用于治疗疟疾的药物,2015年10月获得诺贝尔生理学或医学奖。下列有关青蒿素(化学式:C15H22O5)的叙述正确的是( )
A.青蒿素的摩尔质量为282
B.6.02×1023个青蒿素分子的质量约为282 g
C.1 mol青蒿素的质量为282 g·mol-1
D.282 g青蒿素中含有15个碳原子
1.(2023·重庆合川中学高一月考)下列有关说法中正确的是( )
A.原子、电子、质子、凳子等都可用物质的量来描述
B.1 mol任何物质都含有阿伏加德罗常数个原子
C.1 mol CO2中含1 mol碳和2 mol氧
D.“物质的量”表示含有一定数目粒子的集合体,是七个基本物理量之一
2.(2022·青岛校级月考)碳中和指控制一段时间内温室气体排放总量,实现CO2“零排放”。CO2的摩尔质量为( )
A.12 B.44 g·mol-1
C.12 g·mol-1 D.44
3.下雪时,常用融雪剂清理路面。醋酸钾(CH3COOK)是常用的融雪剂,但对道路、混凝土构件、桥梁设施等有害,对植物生长也有影响,目前正在研究环保高效的融雪剂。下列关于CH3COOK的叙述正确的是( )
A.CH3COOK的相对分子质量为98 g·mol-1
B.CH3COOK的摩尔质量为98 g
C.1 mol CH3COOK含有1.806×1024个H
D.1 mol CH3COOK含有2 mol氧
4.计算填空:
(1)2 mol NO2中含____ mol氮原子,____(用NA表示阿伏加德罗常数的值,下同)个氧原子,______个质子,质量是______ g。
(2)40.5 g某金属氯化物RCl2含有0.6 mol氯离子,则金属R的摩尔质量为____________________________________________________________________________。
(3)已知0.4 mol的CO和CO2的混合气体共14.4 g,则
①CO的质量为________。
②混合气体的平均摩尔质量为__________________________________________________。
第三节 物质的量
第1课时 物质的量 摩尔质量
一、
1.(1)一定数目粒子
(2)mol 6.02×1023 原子 分子 离子
(3)氢原子 氢分子
2.1 mol任何粒子的粒子数 NA 约6.2×1023 mol-1
3.(1)
思考1 1.204×1024 6.02×1023 2 mol 1 mol
微粒的物质的量之比等于微粒的粒子数目之比。
思考2 (1)1 2 0.5 1 0.25 (2)1.204×1024 2 (3)0.3 mol 3NA
(2)粒子数
应用体验
1.(1)× (2)√ (3)× (4)×
2.C
二、
1.M g·mol-1 相对原子质量 相对分子质量
2. n·M
思考1 不等同,摩尔质量与相对分子质量(或相对原子质量)是两个不同的概念。当摩尔质量以“g·mol-1”为单位时,两者在数值上相等,但前者单位是g·mol-1,后者单位是1,故两者不等同。
思考2 (1) 17 g·mol-1 (2)64 g·mol-1
(3)bNA g·mol-1 (4) g·mol-1
应用体验
1.(1)× (2)× (3)× (4)× (5)√
2.B
随堂演练 知识落实
1.D 2.B
3.C [CH3COOK的相对分子质量为98,故A错误;摩尔质量的单位为g·mol-1,在数值上等于该物质的相对分子质量,故B错误;CH3COOK中含3个H原子,故1 mol CH3COOK含有3 mol H原子即1.806×1024个H,故C正确;指代不明,没指明是氧原子还是氧气分子,故D错误。]
4.(1)2 4NA 46NA 92 (2)64 g·mol-1
(3)①5.6 g ②36 g·mol-1
第1课时 物质的量 摩尔质量
[核心素养发展目标] 1.了解物质的量及其单位、阿伏加德罗常数、摩尔质量的含义与应用,利用物质的量将宏观物理量与微观粒子的个数联系起来,并能从宏观和微观结合的视角分析解决问题。2.能从物质的量的角度认识物质的组成及变化,建立物质的量、物质的质量和微观粒子数之间计算的思维模型。
一、物质的量的单位——摩尔
1.物质的量
(1)物质的量是表示含有____________________________的集合体的物理量,用符号n表示。
(2)物质的量的单位——摩尔
(3)表示方法及含义
明确物质的量的规范表示
如1 mol H指1 mol________,1 mol H2(氢气)指1 mol________,不能说1 mol氢,指代不明确。
2.阿伏加德罗常数(NA)
特别提醒 阿伏加德罗常数的单位为mol-1。
3.物质的量、阿伏加德罗常数与粒子数之间的关系
(1)关系式:n=________________。
思考1 通过下图可进一步认识水的组成,并理解物质的量与微粒数目的关系?
思考2 运用物质的量与微粒数目的关系,分析下列问题。
(1)1 mol CO2中有______ mol C和______ mol O,0.5 mol CO2中有__________ mol C和________ mol O。________ mol CO2含有0.5 mol氧原子。
(2)1 mol Na2SO4中含有Na+的数目是______,与________mol NaCl含有相同Na+数目。
(3)0.2 mol NH3与________ H2O中所含H原子数一样多。若用NA表示阿伏加德罗常数的值,0.3 mol H2O中含____个电子。
(2)结论:微粒之间的物质的量之比等于微粒的________之比。
1.判断正误
(1)物质的量可以理解为物质的数量( )
(2)1 mol任何粒子所含有的粒子数相等( )
(3)阿伏加德罗常数就是6.02×1023( )
(4)1 mol水中含有2 mol氢和1 mol氧( )
2.下列叙述正确的是( )
A.摩尔是表示物质所含微粒数量以及物质质量的具有双重意义的单位
B.摩尔是国际单位制中7个基本物理量之一
C.含有6.02×1023个氧原子的H3PO4的物质的量是0.25 mol
D.2H既可以表示2个氢原子又可以表示2 mol氢原子
二、摩尔质量
1.摩尔质量
2.物质的量(n)、质量(m)和摩尔质量(M)之间的关系
n=________________,m=__________。
思考1 摩尔质量与相对分子质量(或相对原子质量)是否等同,为什么?
思考2 结合下列问题,总结摩尔质量的计算方法。
(1)已知氨气的相对分子质量为17,则氨气的摩尔质量为______________。
(2)1.28 g某气体含有的分子数目为1.204×1022,则该气体的摩尔质量为_________________。
(3)已知一个铁原子的质量为b g,则铁的摩尔质量为______(用NA表示阿伏加德罗常数的值)。
(4)已知一个碳原子(12C)的质量为a g,1个某分子的质量为b g,则该分子的摩尔质量为______________________________________________________________________________。
前提条件 公式
任意状态的任意物质 M=(定义式)
已知一个粒子的质量 M=m(粒子)×NA
已知一个粒子的质量和一个12C原子的质量 M=
1.判断正误
(1)氯化氢的摩尔质量是36.5 g( )
(2)氮的摩尔质量是28 g·mol-1( )
(3)CH4的摩尔质量和NA个CH4分子的质量相等( )
(4)2NA个CO2的摩尔质量为88 g·mol-1( )
(5)Fe的摩尔质量为56 g·mol-1,则1个Fe原子质量为 g( )
2.我国科学家屠呦呦发现青蒿素,它是一种用于治疗疟疾的药物,2015年10月获得诺贝尔生理学或医学奖。下列有关青蒿素(化学式:C15H22O5)的叙述正确的是( )
A.青蒿素的摩尔质量为282
B.6.02×1023个青蒿素分子的质量约为282 g
C.1 mol青蒿素的质量为282 g·mol-1
D.282 g青蒿素中含有15个碳原子
1.(2023·重庆合川中学高一月考)下列有关说法中正确的是( )
A.原子、电子、质子、凳子等都可用物质的量来描述
B.1 mol任何物质都含有阿伏加德罗常数个原子
C.1 mol CO2中含1 mol碳和2 mol氧
D.“物质的量”表示含有一定数目粒子的集合体,是七个基本物理量之一
2.(2022·青岛校级月考)碳中和指控制一段时间内温室气体排放总量,实现CO2“零排放”。CO2的摩尔质量为( )
A.12 B.44 g·mol-1
C.12 g·mol-1 D.44
3.下雪时,常用融雪剂清理路面。醋酸钾(CH3COOK)是常用的融雪剂,但对道路、混凝土构件、桥梁设施等有害,对植物生长也有影响,目前正在研究环保高效的融雪剂。下列关于CH3COOK的叙述正确的是( )
A.CH3COOK的相对分子质量为98 g·mol-1
B.CH3COOK的摩尔质量为98 g
C.1 mol CH3COOK含有1.806×1024个H
D.1 mol CH3COOK含有2 mol氧
4.计算填空:
(1)2 mol NO2中含____ mol氮原子,____(用NA表示阿伏加德罗常数的值,下同)个氧原子,______个质子,质量是______ g。
(2)40.5 g某金属氯化物RCl2含有0.6 mol氯离子,则金属R的摩尔质量为____________________________________________________________________________。
(3)已知0.4 mol的CO和CO2的混合气体共14.4 g,则
①CO的质量为________。
②混合气体的平均摩尔质量为__________________________________________________。
第三节 物质的量
第1课时 物质的量 摩尔质量
一、
1.(1)一定数目粒子
(2)mol 6.02×1023 原子 分子 离子
(3)氢原子 氢分子
2.1 mol任何粒子的粒子数 NA 约6.2×1023 mol-1
3.(1)
思考1 1.204×1024 6.02×1023 2 mol 1 mol
微粒的物质的量之比等于微粒的粒子数目之比。
思考2 (1)1 2 0.5 1 0.25 (2)1.204×1024 2 (3)0.3 mol 3NA
(2)粒子数
应用体验
1.(1)× (2)√ (3)× (4)×
2.C
二、
1.M g·mol-1 相对原子质量 相对分子质量
2. n·M
思考1 不等同,摩尔质量与相对分子质量(或相对原子质量)是两个不同的概念。当摩尔质量以“g·mol-1”为单位时,两者在数值上相等,但前者单位是g·mol-1,后者单位是1,故两者不等同。
思考2 (1) 17 g·mol-1 (2)64 g·mol-1
(3)bNA g·mol-1 (4) g·mol-1
应用体验
1.(1)× (2)× (3)× (4)× (5)√
2.B
随堂演练 知识落实
1.D 2.B
3.C [CH3COOK的相对分子质量为98,故A错误;摩尔质量的单位为g·mol-1,在数值上等于该物质的相对分子质量,故B错误;CH3COOK中含3个H原子,故1 mol CH3COOK含有3 mol H原子即1.806×1024个H,故C正确;指代不明,没指明是氧原子还是氧气分子,故D错误。]
4.(1)2 4NA 46NA 92 (2)64 g·mol-1
(3)①5.6 g ②36 g·mol-1
