化学人教版九上:4.4 化学式与化合价(第2课时)课件(共23张PPT)
文档属性
| 名称 | 化学人教版九上:4.4 化学式与化合价(第2课时)课件(共23张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 41.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-07 00:00:00 | ||
图片预览






文档简介
(共23张PPT)
课题4 化学式与化合价
第四单元 自然界的水
第2课时
化合价
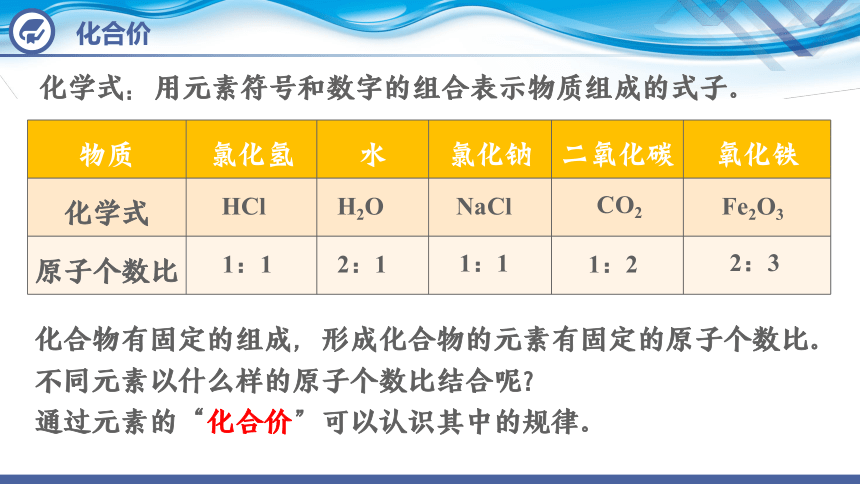
化学式:用元素符号和数字的组合表示物质组成的式子。
物质 氯化氢 水 氯化钠 二氧化碳 氧化铁
化学式
原子个数比
HCl
H2O
NaCl
Fe2O3
1:1
CO2
2:1
1:1
1:2
2:3
化合物有固定的组成,形成化合物的元素有固定的原子个数比。
不同元素以什么样的原子个数比结合呢?
通过元素的“化合价”可以认识其中的规律。
化合价的发展史
1799年,法国化学家普罗斯明确地阐述了定比定律:两种或两种以上元素相化合物成某一化合物,其重量的比例是一定的,不能或增或减。
1803年,英国化学家道尔顿分析了两种碳的氧化物CO和CO2,后又分析了沼气,明确地提出了倍比定律,并以此论证其原子学说。
化合价又叫原子价。原子价起源于倍比定律、定比定律,是为说明原子学说而提出的。
19世纪瑞典化学家阿仑尼乌斯提出电离理论以后,认为原子价有正负之分,
构成化合物的各原子的原子价的代数和为零。
化学价与原子结构的关系
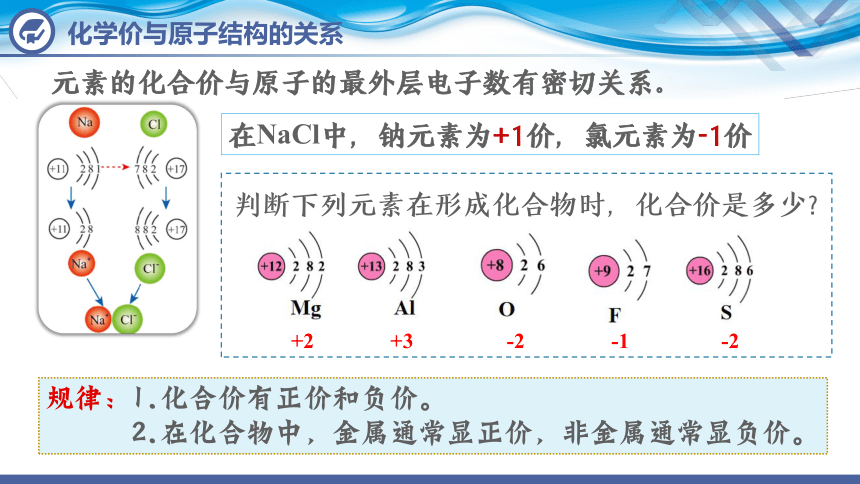
元素的化合价与原子的最外层电子数有密切关系。
在NaCl中,钠元素为+1价,氯元素为-1价
判断下列元素在形成化合物时,化合价是多少?
规律:1.化合价有正价和负价。
2.在化合物中,金属通常显正价,非金属通常显负价。
+2
+3
-2
-1
-2
化合价的表示方法
在元素符号的正上方依次标出“+”、“-”号和价数。
数字“1”不可以省略。
+1
-1
+2
-2
0
0
NaCl
MgO
O2
Fe
规律:单质化合价为0
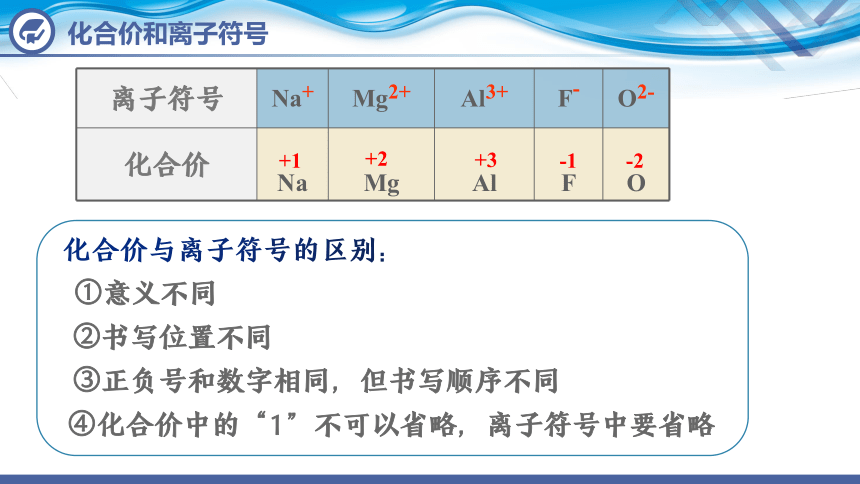
离子符号 Na+ Mg2+ Al3+ F- O2-
化合价 Na Mg Al F
O
化合价与离子符号的区别:
+1
+2
+3
-1
-2
化合价和离子符号
①意义不同
②书写位置不同
③正负号和数字相同,但书写顺序不同
④化合价中的“1”不可以省略,离子符号中要省略
小结:化合价的规律
(1)通常正价在左,负价在右
(2)在化合物中氧元素通常显-2价,氢元素显+1价,单质为0价
(3)在化合物中,正负化合价的代数和为0
(4)相同元素在不同的物质中可以显示不同的化合价
(5)相同元素在同一物质中可以显示不同的化合价
H2O
+1 -2
MgCl2
+2 +1
CO
+2 -2
CO2
+4 -2
O2
0
NH4NO3
-3 +1 +5 -2
化合价的意义
符号 意义
Cl
-1
H2O
+1
氯元素的化合价为-1价
水中的氢元素的化合价为+1价
P2O5
-2
五氧化二磷中的氧元素的化合价为-2价
原子团
它们可以分开计算每种元素的化合价,也可以合并计算总的化合价
这些原子常作为一个整体参加反应,
这样的原子团叫做根,原子团属于离子。
Ca(OH)2
CaCO3
氢氧根
碳酸根
OH-
氢氧根
SO42-
硫酸根
NO3-
硝酸根
CO32-
碳酸根
NH4+
铵根
常见的原子团及其化合价
-1
-2
-1
-2
+1
常见元素或原子团在化合物中的主要化合价
单击此处添加标题
元素 化合价 元素 化合价 元素 化合价 元素 化合价
氢(H ) +1 镁(Mg) +2 氧(O) -2 氢氧根 (OH - ) -1
钠(Na) +1 钙(Ca) +2 氯(Cl) -1 硝酸根(NO3-) -1
钾(K) +1 锌(Zn) +2 氮(N) -3 +5 硫酸根(SO42-) -2
银(Ag) +1 铁(Fe) +2 +3 硫(S) -2 +4 +6 碳酸根(CO32- ) -2
铜(Cu) +1 +2 铝(Al) +3 碳(C) +2 +4 铵根 (NH4+ ) +1
化合价之歌(童年版)
钾钠氢银正一价
钙镁钡锌正二价
氟氯负价负一价
通常氧是负二价
铜正一二铁二三
三铝四硅五价磷
单质元素价为零
负一硝酸、氢氧根
负二硫酸、碳酸根
负三记住磷酸根
正一价的是铵根
交流讨论
①从原子的结构示意图与元素化合价的关系角度去记忆。
②可以用顺口溜来记忆。
③听歌曲记忆
④分类记忆
⑤游戏记忆
⑥……
哪些方法可以帮助你快速记忆化合价
化合价的应用--根据元素的化合价写化学式
步骤
写出磷的氧化物的化学式
②求出两种元素的正、负化合价绝对值的最小公倍数
④把原子数写在元素符号的右下角,即得化学式
(如果原子数为1,则省略不写)
③求各元素的原子数
①写出组成化合物的元素,正价元素居左,
负价元素居右,标出元素的化合价
⑤检查化学式,计算正价和负价代数和是否为0
P O
5×2=10
P: 10÷5=2
O: 10÷2=5
P2O5
2×(+5)+5×(-2)=0
+5
-2
步骤
写出磷的氧化物的化学式
②将化合价的绝对值交叉并化简
①写出组成化合物的元素,正价元素居左,
负价元素居右,标出元素的化合价
③检查化学式,计算正价和负价代数和是否为0
P O
2×(+5)+5×(-2)=0
+5
-2
P O
+5
-2
P2O5
注意:化学式只能表示实际存在的物质的组成。
根据元素的化合价书写化学式,只有在该化学式表示的物质真实存在时才有意义。
化合价的应用--根据元素的化合价写化学式
化合价的应用--根据元素的化合价写化学式
P O
5×2=10
P: 10÷5=2
O: 10÷2=5
P2O5
+5
-2
P O
+5
-2
P O
+5
-2
P2O5
对比两种书写化学式的方法:
由分子构成的物质不能随意约分,如H2O2 ,要依据分子的构成
如实书写。
简便
根据物质名称和化合价书写化学式
氧化物 氯化物 硫化物
名称
化学式
名称
化学式
名称
化学式
水
氧化镁
氧化铝
氧化钠
氧化钙
氧化亚铁
氯化氢
氯化铜
氯化铁
硫化氢
硫化钾
硫化锌
Al2O3
MgO
H2O
Na2O
CaO
FeO
HCl
H2S
CuCl2
K2S
FeCl3
ZnS
步骤
写出氢氧化钙的化学式
②将化合价的绝对值交叉并化简
①写出组成化合物的元素,正价元素居左,
负价元素居右,标出元素的化合价
③检查化学式,计算正价和负价代数和是否为0
1×(+2)+2×(-1)=0
注意:当原子团右下角的数字大于1时,要先加括号,再在括号的右下角写数字。
化合价的应用--根据元素的化合价写化学式
Ca OH
+2
-1
Ca OH
+2
-1
Ca(OH)2
含原子团化学式的读法和写法
酸 碱 盐
名称
化学式
名称
化学式
名称
化学式
硫酸
硝酸
碳酸
氢氧化钠
氢氧化镁
氢氧化钙
硝酸钾
硫酸铜
碳酸钙
硝酸铵
硫酸铵
碳酸铵
H2CO3
HNO3
H2SO4
NaOH
Mg(OH)2
Ca(OH)2
KNO3
NH4NO3
CuSO4
(NH4)2SO4
CaCO3
(NH4)2CO3
化合价的应用--已知化学式,求某元素的化合价
已知氧化铁的化学式为Fe2O3,其中氧元素的化合价为-2价,
求氧化铁中铁元素的化合价。
解:设Fe2O3中铁元素的化合价为 x
2x + 3×(-2)= 0
x=3
答:在Fe2O3中,铁元素的化合价为+3价。
原则:化合物中各元素化合价代数和为0
课堂精练
1.下列物质中,碳元素化合价最低的是( )
A.CH4 B.CO
C. C D.CaCO3
A
2.①N2O5;②X;③N2O3;④N2;⑤NH3五种物质是按照氮元素的化合价由高到低的顺序排列的,则X可能是下列物质中的( )
A.NO2 B.NaNO2 C.NH4Cl D.N2O
A
课堂精练
3.某新冠病毒抗体检测试剂盒采用了胶体金法,该方法使用的原料为氯金酸(HAuCl4),已知HAuCl4中Cl为-1价,
则Au的化合价为( )
A.+4 B.+3
C.+2 D.+1
B
课堂小结
1.化合价的意义
2.常见元素和原子团(根)的化合价
3.化合价的一般规律
4.化合价与离子符号表示方法的区别
5.化合价的应用
①根据化学式确定某元素的化合价
②根据元素的化合价书写化学式
课题4 化学式与化合价
第四单元 自然界的水
第2课时
化合价
化学式:用元素符号和数字的组合表示物质组成的式子。
物质 氯化氢 水 氯化钠 二氧化碳 氧化铁
化学式
原子个数比
HCl
H2O
NaCl
Fe2O3
1:1
CO2
2:1
1:1
1:2
2:3
化合物有固定的组成,形成化合物的元素有固定的原子个数比。
不同元素以什么样的原子个数比结合呢?
通过元素的“化合价”可以认识其中的规律。
化合价的发展史
1799年,法国化学家普罗斯明确地阐述了定比定律:两种或两种以上元素相化合物成某一化合物,其重量的比例是一定的,不能或增或减。
1803年,英国化学家道尔顿分析了两种碳的氧化物CO和CO2,后又分析了沼气,明确地提出了倍比定律,并以此论证其原子学说。
化合价又叫原子价。原子价起源于倍比定律、定比定律,是为说明原子学说而提出的。
19世纪瑞典化学家阿仑尼乌斯提出电离理论以后,认为原子价有正负之分,
构成化合物的各原子的原子价的代数和为零。
化学价与原子结构的关系
元素的化合价与原子的最外层电子数有密切关系。
在NaCl中,钠元素为+1价,氯元素为-1价
判断下列元素在形成化合物时,化合价是多少?
规律:1.化合价有正价和负价。
2.在化合物中,金属通常显正价,非金属通常显负价。
+2
+3
-2
-1
-2
化合价的表示方法
在元素符号的正上方依次标出“+”、“-”号和价数。
数字“1”不可以省略。
+1
-1
+2
-2
0
0
NaCl
MgO
O2
Fe
规律:单质化合价为0
离子符号 Na+ Mg2+ Al3+ F- O2-
化合价 Na Mg Al F
O
化合价与离子符号的区别:
+1
+2
+3
-1
-2
化合价和离子符号
①意义不同
②书写位置不同
③正负号和数字相同,但书写顺序不同
④化合价中的“1”不可以省略,离子符号中要省略
小结:化合价的规律
(1)通常正价在左,负价在右
(2)在化合物中氧元素通常显-2价,氢元素显+1价,单质为0价
(3)在化合物中,正负化合价的代数和为0
(4)相同元素在不同的物质中可以显示不同的化合价
(5)相同元素在同一物质中可以显示不同的化合价
H2O
+1 -2
MgCl2
+2 +1
CO
+2 -2
CO2
+4 -2
O2
0
NH4NO3
-3 +1 +5 -2
化合价的意义
符号 意义
Cl
-1
H2O
+1
氯元素的化合价为-1价
水中的氢元素的化合价为+1价
P2O5
-2
五氧化二磷中的氧元素的化合价为-2价
原子团
它们可以分开计算每种元素的化合价,也可以合并计算总的化合价
这些原子常作为一个整体参加反应,
这样的原子团叫做根,原子团属于离子。
Ca(OH)2
CaCO3
氢氧根
碳酸根
OH-
氢氧根
SO42-
硫酸根
NO3-
硝酸根
CO32-
碳酸根
NH4+
铵根
常见的原子团及其化合价
-1
-2
-1
-2
+1
常见元素或原子团在化合物中的主要化合价
单击此处添加标题
元素 化合价 元素 化合价 元素 化合价 元素 化合价
氢(H ) +1 镁(Mg) +2 氧(O) -2 氢氧根 (OH - ) -1
钠(Na) +1 钙(Ca) +2 氯(Cl) -1 硝酸根(NO3-) -1
钾(K) +1 锌(Zn) +2 氮(N) -3 +5 硫酸根(SO42-) -2
银(Ag) +1 铁(Fe) +2 +3 硫(S) -2 +4 +6 碳酸根(CO32- ) -2
铜(Cu) +1 +2 铝(Al) +3 碳(C) +2 +4 铵根 (NH4+ ) +1
化合价之歌(童年版)
钾钠氢银正一价
钙镁钡锌正二价
氟氯负价负一价
通常氧是负二价
铜正一二铁二三
三铝四硅五价磷
单质元素价为零
负一硝酸、氢氧根
负二硫酸、碳酸根
负三记住磷酸根
正一价的是铵根
交流讨论
①从原子的结构示意图与元素化合价的关系角度去记忆。
②可以用顺口溜来记忆。
③听歌曲记忆
④分类记忆
⑤游戏记忆
⑥……
哪些方法可以帮助你快速记忆化合价
化合价的应用--根据元素的化合价写化学式
步骤
写出磷的氧化物的化学式
②求出两种元素的正、负化合价绝对值的最小公倍数
④把原子数写在元素符号的右下角,即得化学式
(如果原子数为1,则省略不写)
③求各元素的原子数
①写出组成化合物的元素,正价元素居左,
负价元素居右,标出元素的化合价
⑤检查化学式,计算正价和负价代数和是否为0
P O
5×2=10
P: 10÷5=2
O: 10÷2=5
P2O5
2×(+5)+5×(-2)=0
+5
-2
步骤
写出磷的氧化物的化学式
②将化合价的绝对值交叉并化简
①写出组成化合物的元素,正价元素居左,
负价元素居右,标出元素的化合价
③检查化学式,计算正价和负价代数和是否为0
P O
2×(+5)+5×(-2)=0
+5
-2
P O
+5
-2
P2O5
注意:化学式只能表示实际存在的物质的组成。
根据元素的化合价书写化学式,只有在该化学式表示的物质真实存在时才有意义。
化合价的应用--根据元素的化合价写化学式
化合价的应用--根据元素的化合价写化学式
P O
5×2=10
P: 10÷5=2
O: 10÷2=5
P2O5
+5
-2
P O
+5
-2
P O
+5
-2
P2O5
对比两种书写化学式的方法:
由分子构成的物质不能随意约分,如H2O2 ,要依据分子的构成
如实书写。
简便
根据物质名称和化合价书写化学式
氧化物 氯化物 硫化物
名称
化学式
名称
化学式
名称
化学式
水
氧化镁
氧化铝
氧化钠
氧化钙
氧化亚铁
氯化氢
氯化铜
氯化铁
硫化氢
硫化钾
硫化锌
Al2O3
MgO
H2O
Na2O
CaO
FeO
HCl
H2S
CuCl2
K2S
FeCl3
ZnS
步骤
写出氢氧化钙的化学式
②将化合价的绝对值交叉并化简
①写出组成化合物的元素,正价元素居左,
负价元素居右,标出元素的化合价
③检查化学式,计算正价和负价代数和是否为0
1×(+2)+2×(-1)=0
注意:当原子团右下角的数字大于1时,要先加括号,再在括号的右下角写数字。
化合价的应用--根据元素的化合价写化学式
Ca OH
+2
-1
Ca OH
+2
-1
Ca(OH)2
含原子团化学式的读法和写法
酸 碱 盐
名称
化学式
名称
化学式
名称
化学式
硫酸
硝酸
碳酸
氢氧化钠
氢氧化镁
氢氧化钙
硝酸钾
硫酸铜
碳酸钙
硝酸铵
硫酸铵
碳酸铵
H2CO3
HNO3
H2SO4
NaOH
Mg(OH)2
Ca(OH)2
KNO3
NH4NO3
CuSO4
(NH4)2SO4
CaCO3
(NH4)2CO3
化合价的应用--已知化学式,求某元素的化合价
已知氧化铁的化学式为Fe2O3,其中氧元素的化合价为-2价,
求氧化铁中铁元素的化合价。
解:设Fe2O3中铁元素的化合价为 x
2x + 3×(-2)= 0
x=3
答:在Fe2O3中,铁元素的化合价为+3价。
原则:化合物中各元素化合价代数和为0
课堂精练
1.下列物质中,碳元素化合价最低的是( )
A.CH4 B.CO
C. C D.CaCO3
A
2.①N2O5;②X;③N2O3;④N2;⑤NH3五种物质是按照氮元素的化合价由高到低的顺序排列的,则X可能是下列物质中的( )
A.NO2 B.NaNO2 C.NH4Cl D.N2O
A
课堂精练
3.某新冠病毒抗体检测试剂盒采用了胶体金法,该方法使用的原料为氯金酸(HAuCl4),已知HAuCl4中Cl为-1价,
则Au的化合价为( )
A.+4 B.+3
C.+2 D.+1
B
课堂小结
1.化合价的意义
2.常见元素和原子团(根)的化合价
3.化合价的一般规律
4.化合价与离子符号表示方法的区别
5.化合价的应用
①根据化学式确定某元素的化合价
②根据元素的化合价书写化学式
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
