2.1.1化学反应速率 课件(共31张ppt)化学人教版(2019)选择性必修1
文档属性
| 名称 | 2.1.1化学反应速率 课件(共31张ppt)化学人教版(2019)选择性必修1 |

|
|
| 格式 | pptx | ||
| 文件大小 | 62.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-11 00:00:00 | ||
图片预览









文档简介
(共31张PPT)
请你回忆!
这个图是合成氨的工厂,请你书写合成氨的方程式
空气变面包的反应
meiyangyang8602
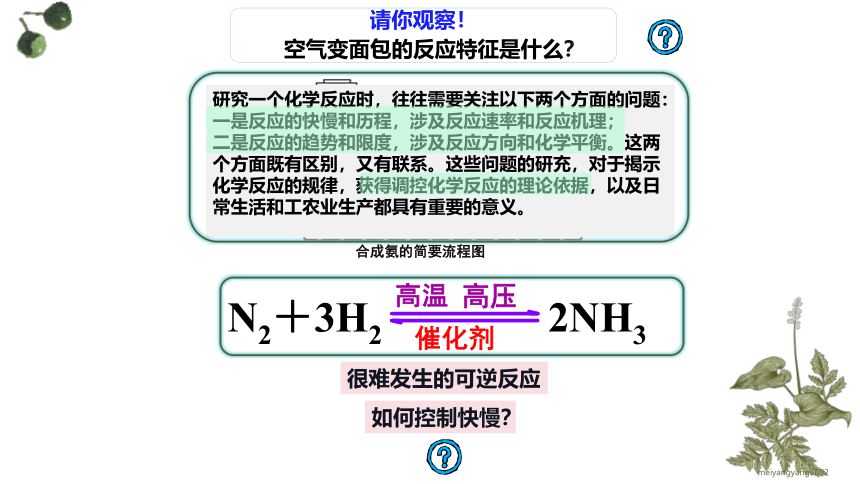
合成氨的简要流程图
很难发生的可逆反应
请你观察!
空气变面包的反应特征是什么?
如何控制快慢?
研究一个化学反应时,往往需要关注以下两个方面的问题:一是反应的快慢和历程,涉及反应速率和反应机理;
二是反应的趋势和限度,涉及反应方向和化学平衡。这两个方面既有区别,又有联系。这些问题的研充,对于揭示
化学反应的规律,获得调控化学反应的理论依据,以及日常生活和工农业生产都具有重要的意义。
meiyangyang8602
第二章 化学反应速率与化学平衡
meiyangyang8602
meiyangyang8602
请你回忆!
必修二学过的如何表示反应的快、慢呢?
化学反应有快有慢
赵健
如何表示快慢?
定性
定量
第一节
化学反应速率
第二章 化学反应速率与化学平衡
第1课时 化学反应速率
meiyangyang8602
meiy angy ang8602
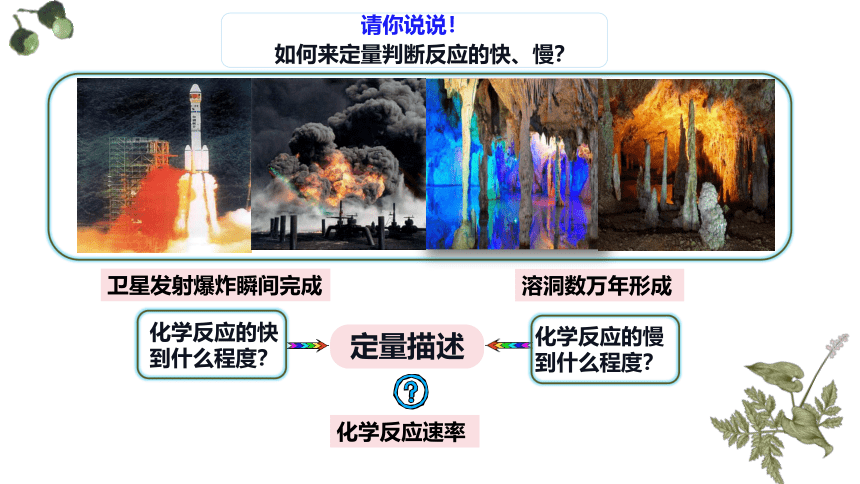
请你说说!
如何来定量判断反应的快、慢?
定量描述
溶洞数万年形成
卫星发射爆炸瞬间完成
meiyangyang8602
meiyangyang8602
化学反应的快到什么程度?
化学反应的慢到什么程度?
化学反应速率
01
化学反应速率
meiyangyang8602
化学反应速率
如果反应的体积是恒定的,化学反应速率通常用单位时间内反应物浓度的减小或生成物浓度的增大表示。
表达式
mol·L-1·s-1 或 mol/(L·s)
mol·L-1·min-1 或 mol/(L·min)
单位
1、通常用单位时间内反应物浓度的减小或生成物浓度的增加来表示,所以反应速率是正值。
2、中学阶段的化学反应速率是平均速率。
3、浓度仅指溶液或气体的,固体、纯液体无浓度可言。
固体和纯液体的浓度是不变的,是常数
注意
meiyangyang8602
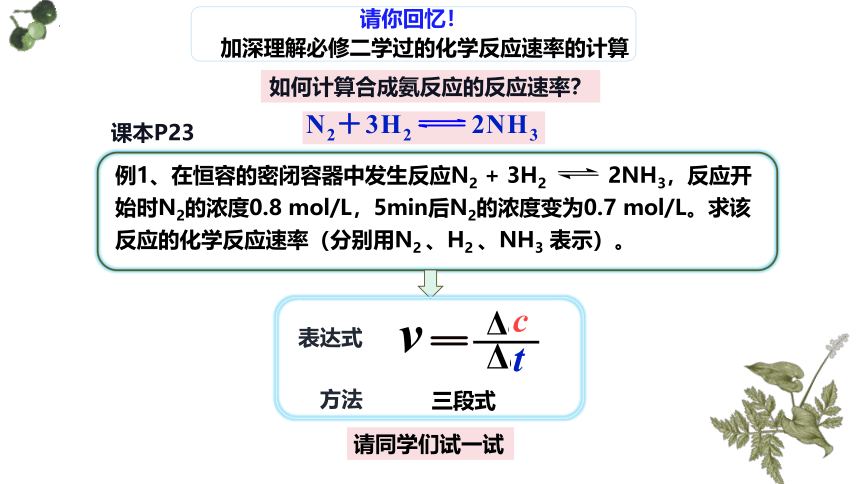
请你回忆!
加深理解必修二学过的化学反应速率的计算
如何计算合成氨反应的反应速率?
例1、在恒容的密闭容器中发生反应N2 + 3H2 2NH3,反应开始时N2的浓度0.8 mol/L,5min后N2的浓度变为0.7 mol/L。求该反应的化学反应速率(分别用N2 、H2 、NH3 表示)。
课本P23
表达式
方法
三段式
请同学们试一试
02
化学反应速率的计算
meiyangyang8602
meiyangyang8602
meiyangyang8602
meiyangyang8602
化学反应速率的计算
三段式
在恒容的密闭容器中发生反应N2 + 3H2 2NH3,反应开始时N2的浓度0.8 mol/L,5min后N2的浓度变为0.7 mol/L。
起始量/mol·L-1
变化量/mol·L-1
5min量/mol·L-1
0.8
0.7
0.1
0.3
0.2
0
υ(N2)
=
=
υ(H2)
=
Δc (H2)
Δt
=
0.1mol/L
5min
=
0.02 mol/(L min)
0.3mol/L
5min
=
0.06 mol/(L min)
υ(NH3)
=
Δc (NH3)
Δt
=
0.2mol/L
5min
=
0.04 mol/(L min)
Δc (N2)
Δt
meiyangyang8602
化学反应速率的计算
meiyangyang8602
同一反应中,各物质的速率之比等于他们在化学方程式中的化学计量数之比。
如在N2 + 3H2 = 2NH3 中, v(N2):v(H2):v(NH3)=1:3:2
也可表达为
同一化学反应 m A + n B p C + q D
υ(A)
m
υ(B)
n
υ(C)
p
υ(D)
q
=
=
=
υ(A)︰υ(B)︰υ(C)︰υ(D) = m︰n︰p︰q
不同物质表示的反应速率可能不相同,但表达的意义相同
meiyangyang8602
meiyangyang8602
[归纳提升] 三段式”法计算模板
例如:反应 mA + nB pC
起始浓度/(mol·L-1) a b c
转化浓度/(mol·L-1) x
t时刻浓度/(mol·L-1) a-x b- c+
计算中注意以下量的关系:
①对于反应物:c(起始)-c(转化)=c(某时刻);
②对于生成物:c(起始)+c(转化)=c(某时刻)。
meiyangyang8602
化学反应速率的计算
三段式
meiyangyang8602
meiyangyang8602
1,反应4NH3+5O2 == 4NO+6H2O(g) 在5升的密闭容器中进行,30秒后,NO 的物质的量增加了0.3mol,此反应的平均反应速率用NO来表示为多少?若用O2的浓度变化来表示此反应速率是多少?若用NH3 来表示呢 若用H2O(g)来表示呢
练习
v(NO)=0.002mol/(L·s)
v(O2)=0.0025mol/(L·s)
v(NH3)=0.002mol/(L·s)
v(H2O)=0.003mol/(L·s)
巩固:P28题3、4
meiyangyang8602
3,在2A(g)+B(g) 3C(g)+5D(g)反应中,表示该反应速率最快的是( )
A.v(A)=2mol·L-1·min-1 B.v(B)=0.3mol·L-1·s-1
C.v(C)=0.8mol·L-1·s-1 D.v(D)=1mol·L-1·s-1
B
统一单位
应化为同一物质表示的速率
不能单纯看数值大小
υ(A)
m
υ(B)
n
υ(C)
p
υ(D)
q
=
=
=
合成氨的简要流程图
请你回忆!
必修二学过的影响化学反应速率的因素有哪些?
meiyangyang8602
影响化学反应速率的本质因素是内因反应本身的性质或特点
浓度,压强,温度,催化剂等因素也会影响化学反应速率
定性
定量
探究
03
探究影响化学反应速率的因素
meiyangyang8602
影响化学反应速率的因素
相同条件下,不同的化学反应会有不同的速率
meiyangyang8602
meiyangyang8602
反应物或反应本身的性质或特点
内因
meiyangyang8602
meiyangyang8602
meiyangyang8602
影响化学反应速率的因素
meiyangyang8602
同一化学反应的速率,受到外界因素的影响
外因
浓度、压强、温度、催化剂、固体表面积等
实验探究课本P24
meiyangyang8602
meiyangyang8602
影响化学反应速率的因素
定性与定量研究影响化学反应速率的因素
定性
定量
探究
选择实验现象明显的化学反应。通过观察冒气泡快慢;颜色变化;固体量减少;浑浊程度;温度变化等。
选择合适实验装置准确测量时间、气体体积、压强、pH等的变化。
meiyangyang8602
meiyangyang8602
meiyangyang8602
影响化学反应速率的因素
定性与定量研究影响化学反应速率的因素
浓度、温度、催化剂等因素如何影响化学反应速率?如何测定化学反应速率?
选择实验用品,设计实验探究影响化学反应速率的因素。
0.1 mol/L Na2S2O3溶液、 0.1 mol/L H2SO4溶液、 0.5 mol/L H2SO4溶液、5% H2O2溶液、1 mol/L FeCl3溶液、蒸馏水、热水。
探究
课本P24
【提出问题】
【实验探究I】
实验用品:烧杯、试管、量筒、试管架、胶头滴管、温度计、秒表。
2H2O2 = 2H2O + O2
Na2S2O3+H2SO4 = Na2SO4+SO2 +S +H2O
meiyangyang8602meiyangyang8602定性探究影响化学反应速率的因素探究浓度对化学反应速率的影响Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O2mL0.1 mol/L Na2S2O3+2mL0.1 mol/L H2SO42mL0.1 mol/L Na2S2O3+2mL0.1 mol/L H2SO42mL0.1 mol/L Na2S2O3+2mL0.5 mol/L H2SO42mL0.1 mol/L Na2S2O3+2mL0.5 mol/L H2SO4影响因素实验步骤实验现象比较结论浓度2mL0.1 mol/L Na2S2O3溶液①+2mL0.1 mol/L H2SO4溶液② +2mL0.5 mol/L H2SO4溶液较快较慢均变浑浊增大反应物浓度,加快反应速率
meiyangyang8602
meiyangyang8602
定性探究影响化学反应速率的因素
探究温度对化学反应速率的影响
Na2S2O3+H2SO4 = Na2SO4+SO2 ↑+S↓+H2O
影响因素 实验步骤 实验现象比较 结论
温度
2mL0.1 mol/L Na2S2O3溶液
+ 2mL 0.5 mol/L H2SO4溶液
① 将 试管 放入 冷水 中
② 将 试管 放入 热水 中
较快
较慢
均变浑浊
升高温度,加快反应速率
meiyangyang8602
meiyangyang8602
定性探究影响化学反应速率的因素
探究催化剂对化学反应速率的影响
影响因素 实验步骤 实验现象比较 结论
催化剂
2 mL 5% H2O2溶液
① + 1mL 的 1 mol/L FeCl3溶液
② + 0mL 的 1 mol/L FeCl3溶液
较多气泡产生
几乎无气泡
其他条件相同时,催化剂可改变化学反应速率
2H2O2 = 2H2O + O2 ↑
meiyangyang8602
meiyangyang8602
恒温密闭容器
浓度增大
增大压强(减小容器容积)相当于增大反应物的浓度,化学反应速率增大;减小压强(增大容器容积)相当于减小反应物的浓度,化学反应速率减小。
探究压强对反应速率的影响
meiyangyang8602
定性探究影响化学反应速率的因素
meiyangyang8602
探究接触面积对反应速率的影响
meiyangyang8602
定性探究影响化学反应速率的因素
其他条件相同时,增大反应物的接触面积可以加快化学反应速率。
meiyangyang8602
meiyangyang8602
同一反应
外界条件对化学反应速率的影响
化学实验定性探究
影响化学反应速率的因素
浓度、压强、温度、催化剂、固体表面积等
定量探究
下节课
meiyangyang8602
meiyangyang8602
练习
例1 [2022·宁夏吴忠中学阶段考] 下列关于化学反应速率的说法中,正确的是 ( )
①用铁片与稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率
②SO2的催化氧化是一个放热反应,所以升高温度,反应速率减慢
③决定化学反应速率的主要因素是反应物的浓度
④汽车尾气中的NO与CO反应转化为无害的N2和CO2,减小压强,反应速率减慢
⑤增大压强,一定能加快化学反应速率
⑥用锌与稀硫酸反应制H2时,滴加几滴硫酸铜溶液能加快反应速率
⑦使用催化剂,会改变反应速率
⑧光是影响某些化学反应速率的外界条件之一
⑨增加反应物的用量,一定会增大化学反应速率
A.①②⑤⑨ B.④⑥⑦⑧ C.④⑥⑦⑨ D.③④⑥⑦
B
meiyangyang8602
meiyangyang8602
1、在下列影响化学反应速率的外界因素中,肯定能使化学反应速率加快的方法是( )
①升高温度 ②使用催化剂 ③增大反应物浓度 ④将块状固体反应物磨成粉末 ⑤增大压强
A.①②③⑤ B.①②④⑤ C.①②④ D.①②③④
D
练习
meiyangyang8602
meiyangyang8602
2,某同学探究影响硫代硫酸钠溶液与稀硫酸反应速率的因素时,设计如下系列实验:
实验序号 反应温度/℃ Na2S2O3溶液 稀H2SO4 H2O
V/mL c/(mol·L-1) V/mL c/(mol·L-1) V/mL
① 20 10.0 0.10 10.0 0.50 0
② 40 V1 0.10 V2 0.50 V3
③ 20 V4 0.10 4.0 0.50 V5
该实验①②可探究_________对反应速率的影响,因此V3=_______;实验①③可
探究____________________对反应速率的影响,因此V5=_________。
练习
温度
0
稀H2SO4的浓度
6.0
meiyangyang8602
meiyangyang8602
练习
3、下列各组反应(表中物质均为反应物)刚开始时,放出H2速率最快的是( )
选项 金属(粉末状) 酸的浓度及体积 反应温度
A Mg,2.4g 3.0 mol/L硫酸100mL 25℃
B Zn,6.5g 6.0 mol/L硝酸100mL 30℃
C Fe,5.6g 18.4 mol/L硫酸100mL 25℃
D Zn,6.5g 6.0 mol/L盐酸100mL 25℃
A
请你回忆!
这个图是合成氨的工厂,请你书写合成氨的方程式
空气变面包的反应
meiyangyang8602
合成氨的简要流程图
很难发生的可逆反应
请你观察!
空气变面包的反应特征是什么?
如何控制快慢?
研究一个化学反应时,往往需要关注以下两个方面的问题:一是反应的快慢和历程,涉及反应速率和反应机理;
二是反应的趋势和限度,涉及反应方向和化学平衡。这两个方面既有区别,又有联系。这些问题的研充,对于揭示
化学反应的规律,获得调控化学反应的理论依据,以及日常生活和工农业生产都具有重要的意义。
meiyangyang8602
第二章 化学反应速率与化学平衡
meiyangyang8602
meiyangyang8602
请你回忆!
必修二学过的如何表示反应的快、慢呢?
化学反应有快有慢
赵健
如何表示快慢?
定性
定量
第一节
化学反应速率
第二章 化学反应速率与化学平衡
第1课时 化学反应速率
meiyangyang8602
meiy angy ang8602
请你说说!
如何来定量判断反应的快、慢?
定量描述
溶洞数万年形成
卫星发射爆炸瞬间完成
meiyangyang8602
meiyangyang8602
化学反应的快到什么程度?
化学反应的慢到什么程度?
化学反应速率
01
化学反应速率
meiyangyang8602
化学反应速率
如果反应的体积是恒定的,化学反应速率通常用单位时间内反应物浓度的减小或生成物浓度的增大表示。
表达式
mol·L-1·s-1 或 mol/(L·s)
mol·L-1·min-1 或 mol/(L·min)
单位
1、通常用单位时间内反应物浓度的减小或生成物浓度的增加来表示,所以反应速率是正值。
2、中学阶段的化学反应速率是平均速率。
3、浓度仅指溶液或气体的,固体、纯液体无浓度可言。
固体和纯液体的浓度是不变的,是常数
注意
meiyangyang8602
请你回忆!
加深理解必修二学过的化学反应速率的计算
如何计算合成氨反应的反应速率?
例1、在恒容的密闭容器中发生反应N2 + 3H2 2NH3,反应开始时N2的浓度0.8 mol/L,5min后N2的浓度变为0.7 mol/L。求该反应的化学反应速率(分别用N2 、H2 、NH3 表示)。
课本P23
表达式
方法
三段式
请同学们试一试
02
化学反应速率的计算
meiyangyang8602
meiyangyang8602
meiyangyang8602
meiyangyang8602
化学反应速率的计算
三段式
在恒容的密闭容器中发生反应N2 + 3H2 2NH3,反应开始时N2的浓度0.8 mol/L,5min后N2的浓度变为0.7 mol/L。
起始量/mol·L-1
变化量/mol·L-1
5min量/mol·L-1
0.8
0.7
0.1
0.3
0.2
0
υ(N2)
=
=
υ(H2)
=
Δc (H2)
Δt
=
0.1mol/L
5min
=
0.02 mol/(L min)
0.3mol/L
5min
=
0.06 mol/(L min)
υ(NH3)
=
Δc (NH3)
Δt
=
0.2mol/L
5min
=
0.04 mol/(L min)
Δc (N2)
Δt
meiyangyang8602
化学反应速率的计算
meiyangyang8602
同一反应中,各物质的速率之比等于他们在化学方程式中的化学计量数之比。
如在N2 + 3H2 = 2NH3 中, v(N2):v(H2):v(NH3)=1:3:2
也可表达为
同一化学反应 m A + n B p C + q D
υ(A)
m
υ(B)
n
υ(C)
p
υ(D)
q
=
=
=
υ(A)︰υ(B)︰υ(C)︰υ(D) = m︰n︰p︰q
不同物质表示的反应速率可能不相同,但表达的意义相同
meiyangyang8602
meiyangyang8602
[归纳提升] 三段式”法计算模板
例如:反应 mA + nB pC
起始浓度/(mol·L-1) a b c
转化浓度/(mol·L-1) x
t时刻浓度/(mol·L-1) a-x b- c+
计算中注意以下量的关系:
①对于反应物:c(起始)-c(转化)=c(某时刻);
②对于生成物:c(起始)+c(转化)=c(某时刻)。
meiyangyang8602
化学反应速率的计算
三段式
meiyangyang8602
meiyangyang8602
1,反应4NH3+5O2 == 4NO+6H2O(g) 在5升的密闭容器中进行,30秒后,NO 的物质的量增加了0.3mol,此反应的平均反应速率用NO来表示为多少?若用O2的浓度变化来表示此反应速率是多少?若用NH3 来表示呢 若用H2O(g)来表示呢
练习
v(NO)=0.002mol/(L·s)
v(O2)=0.0025mol/(L·s)
v(NH3)=0.002mol/(L·s)
v(H2O)=0.003mol/(L·s)
巩固:P28题3、4
meiyangyang8602
3,在2A(g)+B(g) 3C(g)+5D(g)反应中,表示该反应速率最快的是( )
A.v(A)=2mol·L-1·min-1 B.v(B)=0.3mol·L-1·s-1
C.v(C)=0.8mol·L-1·s-1 D.v(D)=1mol·L-1·s-1
B
统一单位
应化为同一物质表示的速率
不能单纯看数值大小
υ(A)
m
υ(B)
n
υ(C)
p
υ(D)
q
=
=
=
合成氨的简要流程图
请你回忆!
必修二学过的影响化学反应速率的因素有哪些?
meiyangyang8602
影响化学反应速率的本质因素是内因反应本身的性质或特点
浓度,压强,温度,催化剂等因素也会影响化学反应速率
定性
定量
探究
03
探究影响化学反应速率的因素
meiyangyang8602
影响化学反应速率的因素
相同条件下,不同的化学反应会有不同的速率
meiyangyang8602
meiyangyang8602
反应物或反应本身的性质或特点
内因
meiyangyang8602
meiyangyang8602
meiyangyang8602
影响化学反应速率的因素
meiyangyang8602
同一化学反应的速率,受到外界因素的影响
外因
浓度、压强、温度、催化剂、固体表面积等
实验探究课本P24
meiyangyang8602
meiyangyang8602
影响化学反应速率的因素
定性与定量研究影响化学反应速率的因素
定性
定量
探究
选择实验现象明显的化学反应。通过观察冒气泡快慢;颜色变化;固体量减少;浑浊程度;温度变化等。
选择合适实验装置准确测量时间、气体体积、压强、pH等的变化。
meiyangyang8602
meiyangyang8602
meiyangyang8602
影响化学反应速率的因素
定性与定量研究影响化学反应速率的因素
浓度、温度、催化剂等因素如何影响化学反应速率?如何测定化学反应速率?
选择实验用品,设计实验探究影响化学反应速率的因素。
0.1 mol/L Na2S2O3溶液、 0.1 mol/L H2SO4溶液、 0.5 mol/L H2SO4溶液、5% H2O2溶液、1 mol/L FeCl3溶液、蒸馏水、热水。
探究
课本P24
【提出问题】
【实验探究I】
实验用品:烧杯、试管、量筒、试管架、胶头滴管、温度计、秒表。
2H2O2 = 2H2O + O2
Na2S2O3+H2SO4 = Na2SO4+SO2 +S +H2O
meiyangyang8602meiyangyang8602定性探究影响化学反应速率的因素探究浓度对化学反应速率的影响Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O2mL0.1 mol/L Na2S2O3+2mL0.1 mol/L H2SO42mL0.1 mol/L Na2S2O3+2mL0.1 mol/L H2SO42mL0.1 mol/L Na2S2O3+2mL0.5 mol/L H2SO42mL0.1 mol/L Na2S2O3+2mL0.5 mol/L H2SO4影响因素实验步骤实验现象比较结论浓度2mL0.1 mol/L Na2S2O3溶液①+2mL0.1 mol/L H2SO4溶液② +2mL0.5 mol/L H2SO4溶液较快较慢均变浑浊增大反应物浓度,加快反应速率
meiyangyang8602
meiyangyang8602
定性探究影响化学反应速率的因素
探究温度对化学反应速率的影响
Na2S2O3+H2SO4 = Na2SO4+SO2 ↑+S↓+H2O
影响因素 实验步骤 实验现象比较 结论
温度
2mL0.1 mol/L Na2S2O3溶液
+ 2mL 0.5 mol/L H2SO4溶液
① 将 试管 放入 冷水 中
② 将 试管 放入 热水 中
较快
较慢
均变浑浊
升高温度,加快反应速率
meiyangyang8602
meiyangyang8602
定性探究影响化学反应速率的因素
探究催化剂对化学反应速率的影响
影响因素 实验步骤 实验现象比较 结论
催化剂
2 mL 5% H2O2溶液
① + 1mL 的 1 mol/L FeCl3溶液
② + 0mL 的 1 mol/L FeCl3溶液
较多气泡产生
几乎无气泡
其他条件相同时,催化剂可改变化学反应速率
2H2O2 = 2H2O + O2 ↑
meiyangyang8602
meiyangyang8602
恒温密闭容器
浓度增大
增大压强(减小容器容积)相当于增大反应物的浓度,化学反应速率增大;减小压强(增大容器容积)相当于减小反应物的浓度,化学反应速率减小。
探究压强对反应速率的影响
meiyangyang8602
定性探究影响化学反应速率的因素
meiyangyang8602
探究接触面积对反应速率的影响
meiyangyang8602
定性探究影响化学反应速率的因素
其他条件相同时,增大反应物的接触面积可以加快化学反应速率。
meiyangyang8602
meiyangyang8602
同一反应
外界条件对化学反应速率的影响
化学实验定性探究
影响化学反应速率的因素
浓度、压强、温度、催化剂、固体表面积等
定量探究
下节课
meiyangyang8602
meiyangyang8602
练习
例1 [2022·宁夏吴忠中学阶段考] 下列关于化学反应速率的说法中,正确的是 ( )
①用铁片与稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率
②SO2的催化氧化是一个放热反应,所以升高温度,反应速率减慢
③决定化学反应速率的主要因素是反应物的浓度
④汽车尾气中的NO与CO反应转化为无害的N2和CO2,减小压强,反应速率减慢
⑤增大压强,一定能加快化学反应速率
⑥用锌与稀硫酸反应制H2时,滴加几滴硫酸铜溶液能加快反应速率
⑦使用催化剂,会改变反应速率
⑧光是影响某些化学反应速率的外界条件之一
⑨增加反应物的用量,一定会增大化学反应速率
A.①②⑤⑨ B.④⑥⑦⑧ C.④⑥⑦⑨ D.③④⑥⑦
B
meiyangyang8602
meiyangyang8602
1、在下列影响化学反应速率的外界因素中,肯定能使化学反应速率加快的方法是( )
①升高温度 ②使用催化剂 ③增大反应物浓度 ④将块状固体反应物磨成粉末 ⑤增大压强
A.①②③⑤ B.①②④⑤ C.①②④ D.①②③④
D
练习
meiyangyang8602
meiyangyang8602
2,某同学探究影响硫代硫酸钠溶液与稀硫酸反应速率的因素时,设计如下系列实验:
实验序号 反应温度/℃ Na2S2O3溶液 稀H2SO4 H2O
V/mL c/(mol·L-1) V/mL c/(mol·L-1) V/mL
① 20 10.0 0.10 10.0 0.50 0
② 40 V1 0.10 V2 0.50 V3
③ 20 V4 0.10 4.0 0.50 V5
该实验①②可探究_________对反应速率的影响,因此V3=_______;实验①③可
探究____________________对反应速率的影响,因此V5=_________。
练习
温度
0
稀H2SO4的浓度
6.0
meiyangyang8602
meiyangyang8602
练习
3、下列各组反应(表中物质均为反应物)刚开始时,放出H2速率最快的是( )
选项 金属(粉末状) 酸的浓度及体积 反应温度
A Mg,2.4g 3.0 mol/L硫酸100mL 25℃
B Zn,6.5g 6.0 mol/L硝酸100mL 30℃
C Fe,5.6g 18.4 mol/L硫酸100mL 25℃
D Zn,6.5g 6.0 mol/L盐酸100mL 25℃
A
