化学人教版(2019)必修第二册6.1.2原电池(共18张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第二册6.1.2原电池(共18张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 11.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-12 00:00:00 | ||
图片预览





文档简介
(共18张PPT)
原 电 池
原电池学习目标:
1.认识化学能转化为电能的实际意义及其重要应用。
2.能分析原电池的工作原理。(重点)
3.能辨识简单原电池的构成要素。
4.能表示电极反应式和电池反应方程式。
电池200年进化史
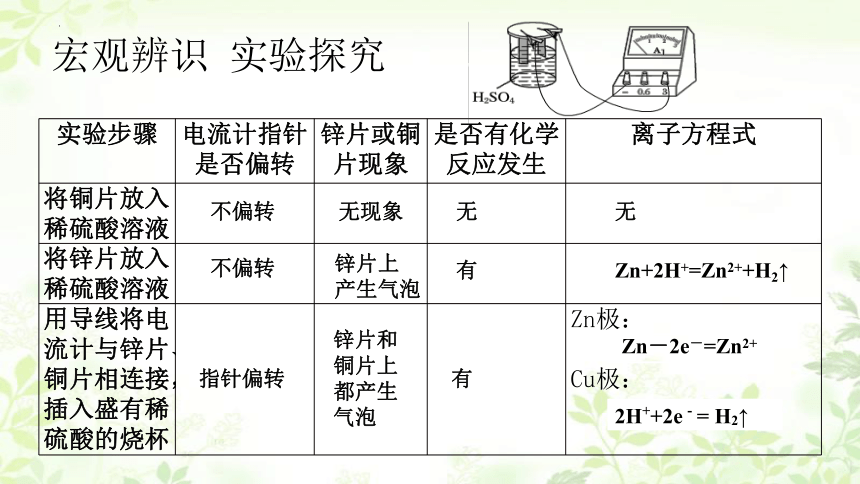
宏观辨识 实验探究
实验步骤 电流计指针是否偏转 锌片或铜片现象 是否有化学反应发生 离子方程式
将铜片放入稀硫酸溶液
将锌片放入稀硫酸溶液
用导线将电流计与锌片、铜片相连接,插入盛有稀硫酸的烧杯 Zn极:
Cu极:
不偏转
不偏转
指针偏转
无
锌片上
产生气泡
Zn+2H+=Zn2++H2↑
无现象
有
无
有
锌片和铜片上都产生气泡
Zn-2e-=Zn2+
2H++2e-= H2↑
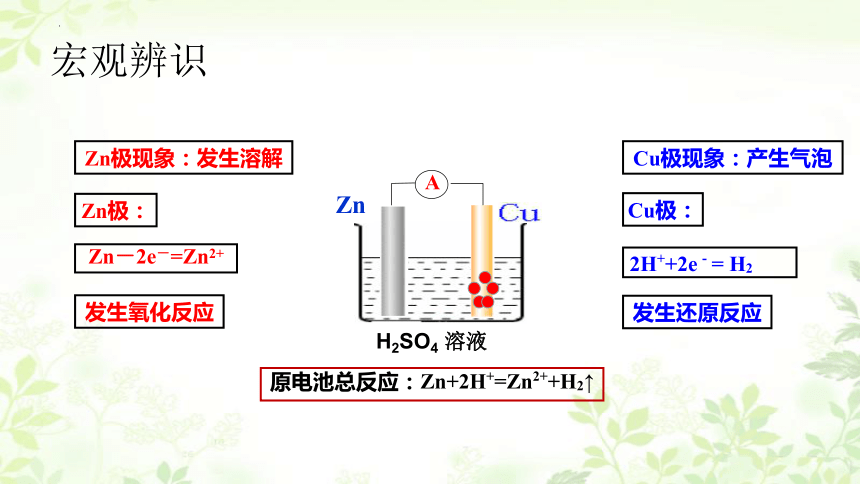
宏观辨识
H2SO4 溶液
A
Zn
Zn-2e-=Zn2+
发生氧化反应
Cu极:
Cu极现象:产生气泡
原电池总反应:Zn+2H+=Zn2++H2↑
2H++2e-= H2
发生还原反应
Zn极现象:发生溶解
Zn极:
微观探析 :
1.锌铜稀硫酸原电池中电子流向是怎样的?
电流方向呢?
2.锌片和铜片哪极是正极哪极是负极呢?
正负极分别发生了什么类型的反应?
3.稀硫酸溶液中有哪些离子?
原电池工作时溶液中的阴阳离子如何移动?
Cu
Zn
e -
e-
Zn2+
H+
H+
Zn-2e-=Zn2+
发生氧化反应
Zn极:
Cu极:
SO42-
Zn极现象:发生溶解
Cu极现象:产生气泡
原电池总反应:Zn+2H+=Zn2++H2↑
微观探析:工作原理
Zn极:
2H++2e-= H2
发生还原反应
Zn极:
Zn极:
Zn极:
Zn
下列装置能构成原电池的是
稀硫酸
(3)
Zn
Zn
A
Zn
H2SO4溶液
(2)
CuSO4 溶液
(9)
A
Zn
(1)(7)(9)
稀硫酸
(7)
需要哪些条件才能构成原电池呢?
H2SO4 溶液
(1)
A
Zn
(4)
(5)
(6)
稀硫酸
(8)
Ag
Cu
A
思考与讨论:如何改进该原电池装置?
盐桥中通常装有含KCl饱和溶液的琼脂
K+和Cl-在盐桥中能够自由移动
请根据下列仪器和试剂试着画出改进装置图。
实验用品:锌片、铜片、导线、电流表、烧杯、稀硫酸、盐桥 。(其他试剂任选)
SO42-
Zn2+
e-
e-
SO42-
H+
H+
K+
双液原电池工作示意图
H2
Zn
K+
Cl-
K+
Cl-
K+
Cl-
K+
Cl-
K+
Cl-
Cl-
K+
K+
Cl-
K+
K+
K+
Cl-
Cl-
K+
Cl-
Cl-
Cl-
KCl
想一想:
盐桥中K+和Cl-怎样移动?
2H++2e-= H2
发生还原反应
Zn-2e-=Zn2+
发生氧化反应
正极:
Cu极现象:产生气泡
负极:
Zn极现象:发生溶解
原电池总反应:Zn+2H+=Zn2++H2↑
H2SO4溶液
SO42-
Zn2+
e-
e-
SO42-
K+
双液原电池工作示意图
H2
Zn
K+
Cl-
K+
Cl-
K+
Cl-
K+
Cl-
K+
Cl-
Cl-
K+
K+
Cl-
K+
K+
K+
Cl-
Cl-
K+
Cl-
Cl-
Cl-
Cl-
K+
2H++2e-= H2
发生还原反应
Zn-2e-=Zn2+
发生氧化反应
正极:
Cu极现象:产生气泡
负极:
Zn极现象:发生溶解
原电池总反应:Zn+2H+=Zn2++H2↑
H2SO4溶液
H+
H+
【2020.全国Ⅰ.12】科学家近年发明了一种新型Zn CO2水介质电池。电池示意图如图,电极为金属锌和选择性催化材料,放电时,温室气体CO2被转化为储氢物质甲酸等,为解决环境和能源问题提供了一种新途径。
下列说法错误的是
A.放电时,负极反应为
B.放电时,1 mol CO2转化为
HCOOH,转移的电子数为2 mol
C.充电时,电池总反应为
D.充电时,正极溶液中OH 浓度升高
水介质电池
新型Zn CO2
【2018·全国II·6】我国科学家研发了一种室温下“可呼吸”的Na—CO2二次电池。将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO2+4Na=2Na2CO3+C。下列说法错误的是( )
A.放电时,ClO4-向负极移动
B.充电时释放CO2,放电时吸收CO2
C.放电时,正极反应为:
3CO2+4e =2CO32-+C
D.充电时,正极反应为:Na++e =Na
Na—CO2二次电池
【2016·全国II·11】Mg—AgCl电池是一种以海水为电解质溶液的水激活电池。下列叙述错误的是( )
A.负极反应式为Mg-2e-=Mg2+
B.正极反应式为Ag++e-=Ag
C.电池放电时Cl-由正极向负极迁移
D.负极会发生副反应Mg+2H2O=Mg(OH)2+H2↑
Mg—AgCl电池
【2020年新课标Ⅰ】科学家近年发明了一种新型Zn CO2水介质电池。电池示意图如图,电极为金属锌和选择性催化材料,放电时,温室气体CO2被转化为储氢物质甲酸等,为解决环境和能源问题提供了一种新途径。
下列说法错误的是
A.放电时,负极反应为
B.放电时,1 mol CO2转化为
HCOOH,转移的电子数为2 mol
C.充电时,电池总反应为
D.充电时,正极溶液中OH 浓度升高
A.放电时,负极反应为
新型Zn CO2
水介质电池
【2018·全国II·6】我国科学家研发了一种室温下“可呼吸”的Na—CO2二次电池。将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO2+4Na=2Na2CO3+C。下列说法错误的是( )
A.放电时,ClO4-向负极移动
B.充电时释放CO2,放电时吸收CO2
C.放电时,正极反应为:
3CO2+4e =2CO32-+C
D.充电时,正极反应为:Na++e =Na
A.放电时,ClO4-向负极移动
C.放电时,正极反应为:
3CO2+4e =2CO32-+C
Na—CO2二次电池
【2016·全国II·11】Mg—AgCl电池是一种以海水为电解质溶液的水激活电池。下列叙述错误的是( )
A.负极反应式为Mg-2e-=Mg2+
B.正极反应式为Ag++e-=Ag
C.电池放电时Cl-由正极向负极迁移
D.负极会发生副反应Mg+2H2O=Mg(OH)2+H2↑
A.负极反应式为Mg-2e-=Mg2+
B.正极反应式为Ag++e-=Ag
C.电池放电时Cl-由正极向负极迁移
Mg—AgCl电池
原 电 池
原电池学习目标:
1.认识化学能转化为电能的实际意义及其重要应用。
2.能分析原电池的工作原理。(重点)
3.能辨识简单原电池的构成要素。
4.能表示电极反应式和电池反应方程式。
电池200年进化史
宏观辨识 实验探究
实验步骤 电流计指针是否偏转 锌片或铜片现象 是否有化学反应发生 离子方程式
将铜片放入稀硫酸溶液
将锌片放入稀硫酸溶液
用导线将电流计与锌片、铜片相连接,插入盛有稀硫酸的烧杯 Zn极:
Cu极:
不偏转
不偏转
指针偏转
无
锌片上
产生气泡
Zn+2H+=Zn2++H2↑
无现象
有
无
有
锌片和铜片上都产生气泡
Zn-2e-=Zn2+
2H++2e-= H2↑
宏观辨识
H2SO4 溶液
A
Zn
Zn-2e-=Zn2+
发生氧化反应
Cu极:
Cu极现象:产生气泡
原电池总反应:Zn+2H+=Zn2++H2↑
2H++2e-= H2
发生还原反应
Zn极现象:发生溶解
Zn极:
微观探析 :
1.锌铜稀硫酸原电池中电子流向是怎样的?
电流方向呢?
2.锌片和铜片哪极是正极哪极是负极呢?
正负极分别发生了什么类型的反应?
3.稀硫酸溶液中有哪些离子?
原电池工作时溶液中的阴阳离子如何移动?
Cu
Zn
e -
e-
Zn2+
H+
H+
Zn-2e-=Zn2+
发生氧化反应
Zn极:
Cu极:
SO42-
Zn极现象:发生溶解
Cu极现象:产生气泡
原电池总反应:Zn+2H+=Zn2++H2↑
微观探析:工作原理
Zn极:
2H++2e-= H2
发生还原反应
Zn极:
Zn极:
Zn极:
Zn
下列装置能构成原电池的是
稀硫酸
(3)
Zn
Zn
A
Zn
H2SO4溶液
(2)
CuSO4 溶液
(9)
A
Zn
(1)(7)(9)
稀硫酸
(7)
需要哪些条件才能构成原电池呢?
H2SO4 溶液
(1)
A
Zn
(4)
(5)
(6)
稀硫酸
(8)
Ag
Cu
A
思考与讨论:如何改进该原电池装置?
盐桥中通常装有含KCl饱和溶液的琼脂
K+和Cl-在盐桥中能够自由移动
请根据下列仪器和试剂试着画出改进装置图。
实验用品:锌片、铜片、导线、电流表、烧杯、稀硫酸、盐桥 。(其他试剂任选)
SO42-
Zn2+
e-
e-
SO42-
H+
H+
K+
双液原电池工作示意图
H2
Zn
K+
Cl-
K+
Cl-
K+
Cl-
K+
Cl-
K+
Cl-
Cl-
K+
K+
Cl-
K+
K+
K+
Cl-
Cl-
K+
Cl-
Cl-
Cl-
KCl
想一想:
盐桥中K+和Cl-怎样移动?
2H++2e-= H2
发生还原反应
Zn-2e-=Zn2+
发生氧化反应
正极:
Cu极现象:产生气泡
负极:
Zn极现象:发生溶解
原电池总反应:Zn+2H+=Zn2++H2↑
H2SO4溶液
SO42-
Zn2+
e-
e-
SO42-
K+
双液原电池工作示意图
H2
Zn
K+
Cl-
K+
Cl-
K+
Cl-
K+
Cl-
K+
Cl-
Cl-
K+
K+
Cl-
K+
K+
K+
Cl-
Cl-
K+
Cl-
Cl-
Cl-
Cl-
K+
2H++2e-= H2
发生还原反应
Zn-2e-=Zn2+
发生氧化反应
正极:
Cu极现象:产生气泡
负极:
Zn极现象:发生溶解
原电池总反应:Zn+2H+=Zn2++H2↑
H2SO4溶液
H+
H+
【2020.全国Ⅰ.12】科学家近年发明了一种新型Zn CO2水介质电池。电池示意图如图,电极为金属锌和选择性催化材料,放电时,温室气体CO2被转化为储氢物质甲酸等,为解决环境和能源问题提供了一种新途径。
下列说法错误的是
A.放电时,负极反应为
B.放电时,1 mol CO2转化为
HCOOH,转移的电子数为2 mol
C.充电时,电池总反应为
D.充电时,正极溶液中OH 浓度升高
水介质电池
新型Zn CO2
【2018·全国II·6】我国科学家研发了一种室温下“可呼吸”的Na—CO2二次电池。将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO2+4Na=2Na2CO3+C。下列说法错误的是( )
A.放电时,ClO4-向负极移动
B.充电时释放CO2,放电时吸收CO2
C.放电时,正极反应为:
3CO2+4e =2CO32-+C
D.充电时,正极反应为:Na++e =Na
Na—CO2二次电池
【2016·全国II·11】Mg—AgCl电池是一种以海水为电解质溶液的水激活电池。下列叙述错误的是( )
A.负极反应式为Mg-2e-=Mg2+
B.正极反应式为Ag++e-=Ag
C.电池放电时Cl-由正极向负极迁移
D.负极会发生副反应Mg+2H2O=Mg(OH)2+H2↑
Mg—AgCl电池
【2020年新课标Ⅰ】科学家近年发明了一种新型Zn CO2水介质电池。电池示意图如图,电极为金属锌和选择性催化材料,放电时,温室气体CO2被转化为储氢物质甲酸等,为解决环境和能源问题提供了一种新途径。
下列说法错误的是
A.放电时,负极反应为
B.放电时,1 mol CO2转化为
HCOOH,转移的电子数为2 mol
C.充电时,电池总反应为
D.充电时,正极溶液中OH 浓度升高
A.放电时,负极反应为
新型Zn CO2
水介质电池
【2018·全国II·6】我国科学家研发了一种室温下“可呼吸”的Na—CO2二次电池。将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO2+4Na=2Na2CO3+C。下列说法错误的是( )
A.放电时,ClO4-向负极移动
B.充电时释放CO2,放电时吸收CO2
C.放电时,正极反应为:
3CO2+4e =2CO32-+C
D.充电时,正极反应为:Na++e =Na
A.放电时,ClO4-向负极移动
C.放电时,正极反应为:
3CO2+4e =2CO32-+C
Na—CO2二次电池
【2016·全国II·11】Mg—AgCl电池是一种以海水为电解质溶液的水激活电池。下列叙述错误的是( )
A.负极反应式为Mg-2e-=Mg2+
B.正极反应式为Ag++e-=Ag
C.电池放电时Cl-由正极向负极迁移
D.负极会发生副反应Mg+2H2O=Mg(OH)2+H2↑
A.负极反应式为Mg-2e-=Mg2+
B.正极反应式为Ag++e-=Ag
C.电池放电时Cl-由正极向负极迁移
Mg—AgCl电池
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
