2023-2024学年鲁科版高中化学选择性必修三 项目探究 乙醇的结构与性质 课件(共21张PPT)
文档属性
| 名称 | 2023-2024学年鲁科版高中化学选择性必修三 项目探究 乙醇的结构与性质 课件(共21张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-13 00:00:00 | ||
图片预览








文档简介
(共21张PPT)
项目探究 乙醇的结构与性质
何以解忧?唯有杜康。
酒逢知己千杯少。
已知乙醇由C、H、O三种元素组成,其中氧元素的质量分数约为34.8%。0.1mol乙醇完全燃烧生成8.8g CO2和0.3mol H2O。请你计算并求出乙醇的分子式。
确定分子式
项目一——项目背景
项目一 乙醇结构确定
C2H6O
搭建球棍模型
①
②
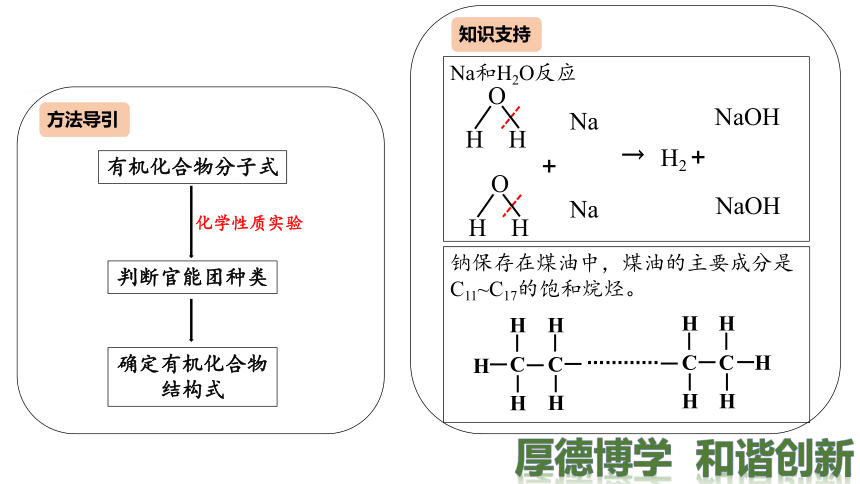
知识支持
钠保存在煤油中,煤油的主要成分是C11~C17的饱和烷烃。
Na和H2O反应
H
O
H
H
O
H
H2
Na
Na
NaOH
NaOH
方法导引
有机化合物分子式
判断官能团种类
确定有机化合物结构式
化学性质实验
+
+
→
C
H
H
C
H
H
H
············
C
H
H
C
H
H
H
任务 设计实验验证乙醇的结构
项目一——问题探究
①
②
乙醇和钠反应
现象
结论
密度:Na>CH3CH2OH
钠沉于底部,表面有气泡产生
乙醇和钠反应产生氢气
项目一——实验分析
结构确定
H—C—C—O—H
H
H
H
H
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
项目一——成果展示
项目二——项目背景
实验1
实验操作 实验现象 实验结论
向试管中滴入几滴酸性高锰酸钾溶液,加入无水乙醇,观察现象。
酸性高锰酸钾溶液褪色
羟基能被氧化
项目二 乙醇性质探究
——氧化反应中羟基结构变化
乙醇在人体内的代谢过程
【资料卡片】
乙醛是无色有刺激性气味的液体,是一种重要的化工原料。
项目二——项目背景
实验2
向试管中加入约2mL无水乙醇,取一根光洁的铜丝绕成螺旋状,置于酒精灯外焰上加热,然后伸入无水乙醇中,反复几次,观察铜丝的变化并闻一闻液体的气味。
项目二——实验探究
乙醛
H—C—C—O—H
H
H
H
H
乙醇
实验步骤 实验现象 原因或结论
将铜丝在酒精灯外焰上灼烧 铜丝颜色:
趁热将铜丝伸入乙醇中 铜丝颜色:
反复4次后闻试管中液体气味
红→黑
黑→红
有刺激性气味
Cu→CuO
CuO→Cu
乙醛
实验2-乙醇的催化氧化
活动1:通过搭建乙醇和乙醛的球棍模型,讨论分析乙醇反应生成乙醛的过程中断键和成键情况。
乙醛
H—C—C—O—H
H
H
H
H
乙醇
活动2:写出乙醇催化氧化过程中两步反应的化学方程式。
2Cu+O2 2CuO
CuO+ CH3CH2OH Cu+ CH3CHO+ H2O
铜在该反应中的作用是什么?
催化剂
催化剂是指参与化学反应中间历程的,又能选择性地改变化学反应速率,而其本身的数量和化学性质在反应前后基本保持不变的物质。
断同一个碳上的C—H和O—H
2CH3-CH-O + O2 2CH3-C-H+2H2O
Cu
H H
O
试推测该反应总的化学方程式
2CH3CH2OH+O2 2CH3CHO+2H2O
Cu
△
+ O2
请你写出丙醇催化氧化反应的化学方程式
2CH3-C-CH3 + O2 2CH3-C-CH3+2H2O
Cu/Ag
O
O
H
H
2CH3 - CH2-CH-O + O2 2CH3 - CH2-C-H+2H2O
Cu
H H
O
项目二——成果展示
羟基的化学性质
H—C—C—O—H
H
H
H
H
化学性质 断键位置
与钠反应
催化氧化
①
②
③
③
② ③
练习巩固
简述下列反应中,从反应物到生成物的官能团转化情况。
(1)CH2=CH2 + H2O → CH3CH2OH
(2)2CH3CH2OH+O2 2CH3CHO+2H2O
Cu
△
【课后作业】
完成课后练习
查阅相关资料,进一步了解乙醇的性质和用途
了解酒精检测仪的工作原理,思考其体现了乙醇的什么性质,并写出相关化学方程式
项目探究 乙醇的结构与性质
何以解忧?唯有杜康。
酒逢知己千杯少。
已知乙醇由C、H、O三种元素组成,其中氧元素的质量分数约为34.8%。0.1mol乙醇完全燃烧生成8.8g CO2和0.3mol H2O。请你计算并求出乙醇的分子式。
确定分子式
项目一——项目背景
项目一 乙醇结构确定
C2H6O
搭建球棍模型
①
②
知识支持
钠保存在煤油中,煤油的主要成分是C11~C17的饱和烷烃。
Na和H2O反应
H
O
H
H
O
H
H2
Na
Na
NaOH
NaOH
方法导引
有机化合物分子式
判断官能团种类
确定有机化合物结构式
化学性质实验
+
+
→
C
H
H
C
H
H
H
············
C
H
H
C
H
H
H
任务 设计实验验证乙醇的结构
项目一——问题探究
①
②
乙醇和钠反应
现象
结论
密度:Na>CH3CH2OH
钠沉于底部,表面有气泡产生
乙醇和钠反应产生氢气
项目一——实验分析
结构确定
H—C—C—O—H
H
H
H
H
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
项目一——成果展示
项目二——项目背景
实验1
实验操作 实验现象 实验结论
向试管中滴入几滴酸性高锰酸钾溶液,加入无水乙醇,观察现象。
酸性高锰酸钾溶液褪色
羟基能被氧化
项目二 乙醇性质探究
——氧化反应中羟基结构变化
乙醇在人体内的代谢过程
【资料卡片】
乙醛是无色有刺激性气味的液体,是一种重要的化工原料。
项目二——项目背景
实验2
向试管中加入约2mL无水乙醇,取一根光洁的铜丝绕成螺旋状,置于酒精灯外焰上加热,然后伸入无水乙醇中,反复几次,观察铜丝的变化并闻一闻液体的气味。
项目二——实验探究
乙醛
H—C—C—O—H
H
H
H
H
乙醇
实验步骤 实验现象 原因或结论
将铜丝在酒精灯外焰上灼烧 铜丝颜色:
趁热将铜丝伸入乙醇中 铜丝颜色:
反复4次后闻试管中液体气味
红→黑
黑→红
有刺激性气味
Cu→CuO
CuO→Cu
乙醛
实验2-乙醇的催化氧化
活动1:通过搭建乙醇和乙醛的球棍模型,讨论分析乙醇反应生成乙醛的过程中断键和成键情况。
乙醛
H—C—C—O—H
H
H
H
H
乙醇
活动2:写出乙醇催化氧化过程中两步反应的化学方程式。
2Cu+O2 2CuO
CuO+ CH3CH2OH Cu+ CH3CHO+ H2O
铜在该反应中的作用是什么?
催化剂
催化剂是指参与化学反应中间历程的,又能选择性地改变化学反应速率,而其本身的数量和化学性质在反应前后基本保持不变的物质。
断同一个碳上的C—H和O—H
2CH3-CH-O + O2 2CH3-C-H+2H2O
Cu
H H
O
试推测该反应总的化学方程式
2CH3CH2OH+O2 2CH3CHO+2H2O
Cu
△
+ O2
请你写出丙醇催化氧化反应的化学方程式
2CH3-C-CH3 + O2 2CH3-C-CH3+2H2O
Cu/Ag
O
O
H
H
2CH3 - CH2-CH-O + O2 2CH3 - CH2-C-H+2H2O
Cu
H H
O
项目二——成果展示
羟基的化学性质
H—C—C—O—H
H
H
H
H
化学性质 断键位置
与钠反应
催化氧化
①
②
③
③
② ③
练习巩固
简述下列反应中,从反应物到生成物的官能团转化情况。
(1)CH2=CH2 + H2O → CH3CH2OH
(2)2CH3CH2OH+O2 2CH3CHO+2H2O
Cu
△
【课后作业】
完成课后练习
查阅相关资料,进一步了解乙醇的性质和用途
了解酒精检测仪的工作原理,思考其体现了乙醇的什么性质,并写出相关化学方程式
