北京课改版化学九年级上册期末复习:07-专项素养综合全练(七) 科学探究
文档属性
| 名称 | 北京课改版化学九年级上册期末复习:07-专项素养综合全练(七) 科学探究 |  | |
| 格式 | docx | ||
| 文件大小 | 2.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-14 09:46:33 | ||
图片预览


文档简介
中小学教育资源及组卷应用平台
专项素养综合全练(七)
科学探究
类型一 数字化实验
1.【新题型·数字化实验】(2023湖北武汉汉阳期中)氯酸钾为白色固体,熔点为356 ℃,受热分解会释放氧气。李明同学利用图1所示装置(夹持装置略)探究氯酸钾的热分解温度,所得氧气的体积分数和温度随时间的变化关系如图2所示。下列说法不正确的是 ( )
图1
图2
A.因为加热后氯酸钾慢慢变成液态,故图1试管口略向上倾斜
B.该实验证明氯酸钾在没有催化剂的条件下也会分解产生氧气
C.由图2可知氯酸钾在356 ℃时就开始大量分解产生氧气
D.图2表示氧气体积分数的曲线为乙
2.(2022湖北黄石中考改编)某化学兴趣小组在学习O2制备时,对 MnO2做催化剂加快过氧化氢分解产生了兴趣,他们提出疑问:其他物质能否对过氧化氢分解速率产生影响
【查阅资料】影响化学反应速率的因素有很多,如:使用催化剂、改变温度、改变反应物的浓度等。
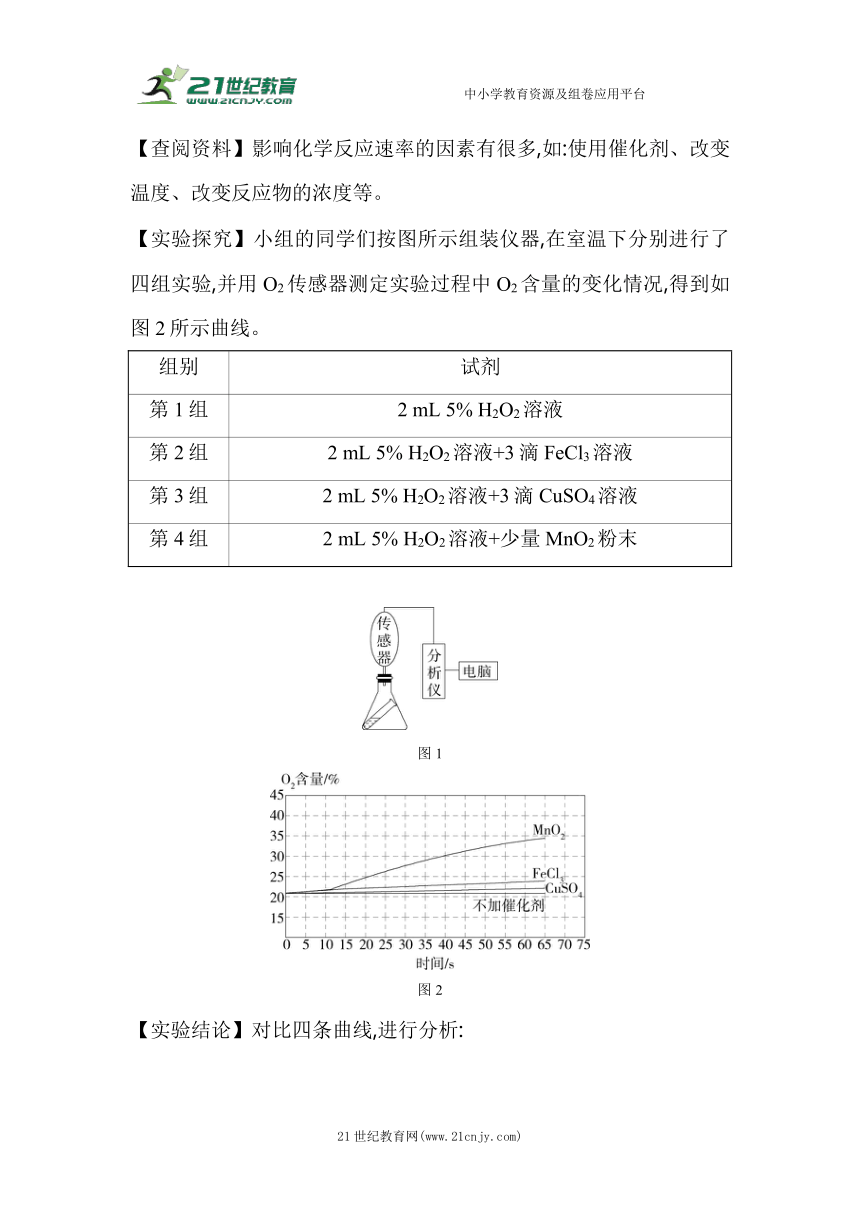
【实验探究】小组的同学们按图所示组装仪器,在室温下分别进行了四组实验,并用O2传感器测定实验过程中O2含量的变化情况,得到如图2所示曲线。
组别 试剂
第1组 2 mL 5% H2O2溶液
第2组 2 mL 5% H2O2溶液+3滴FeCl3溶液
第3组 2 mL 5% H2O2溶液+3滴CuSO4溶液
第4组 2 mL 5% H2O2溶液+少量MnO2粉末
图1
图2
【实验结论】对比四条曲线,进行分析:
(1)FeCl3溶液、CuSO4溶液对H2O2的分解 (填“有”或“无”)催化作用。
(2)写出实验中催化效果最优的使H2O2分解的化学方程式: 。
(3)第1组实验的目的是 。
(4)小组的同学们不加催化剂,在不同温度下,用不同浓度的H2O2溶液进行实验,记录实验现象如下表。据此可得出:升高温度或 (填“增大”或“减小”)反应物浓度可加快H2O2的分解。
温度 现象 H2O2溶液浓度 50 ℃ 60 ℃ 70 ℃
5% 无明显气泡 无明显气泡 极少量气泡
10% 无明显气泡 无明显气泡 少量气泡
15% 无明显气泡 少量气泡 较多气泡
类型二 项目式探究
3.(2021安徽中考)关于燃烧的研究是一项重要的课题。某小组以“探究燃烧的奥秘”为主题开展项目式学习。
【任务一】认识燃烧
(1)酒精、煤(含硫)、天然气是生活中常见的燃料,下列不属于三者燃烧共有的现象是 (填字母)。
A.发光
B.产生有刺激性气味的气体
C.放热
D.产生使澄清石灰水变浑浊的气体
(2)写出酒精(C2H5OH)完全燃烧的化学方程式: 。
【任务二】探究燃烧的条件及质量变化
(3)该小组同学按下列实验步骤开展探究。
步骤1:室温下,按如图组装装置,装入药品,称量装置总质量为m1 g。
步骤2:将锥形瓶浸入80 ℃的热水中,观察现象。
步骤3:取出装置,恢复至室温并擦干锥形瓶;打开止水夹K1和K2,从K1处缓慢通入约50 mL氧气,再关闭K1和K2,称量装置总质量为m2 g。
步骤4:将锥形瓶再次浸入80 ℃的热水中,观察现象。
步骤5:取出装置,恢复至室温并擦干锥形瓶,称量装置总质量为m3 g。
①通过上述实验,能证明燃烧需要氧气的实验现象是 。
②m1、m2、m3的大小关系是 。
【任务三】调控燃烧
(4)报道显示:国内外一些煤田因发生煤层自燃,带来了资源浪费和环境污染。一旦煤层自燃,请给出一条合理的灭火建议: 。
【任务四】再探铁的燃烧
(5)查阅文献:颗粒直径为20~30 nm的铁粉,在空气中会发生自燃生成氧化铁。结合已有知识,回答下列问题:
影响铁燃烧的因素有 (至少答出2点)。
答案全解全析
1.答案C 氯酸钾熔点为356 ℃,随着温度的慢慢升高,氯酸钾会变为液态,所以题图1试管口应略向上倾斜,A正确。该实验是氯酸钾直接加热生成氧气,可以证明氯酸钾在没有催化剂的条件下也会分解产生氧气,B正确。氧气约占空气体积的21%,与题图2中曲线乙起始的位置大致相同,所以曲线乙表示氧气的体积分数;由曲线乙可以看出,在150 s左右曲线变陡,说明开始大量分解产生氧气,C错误、D正确。
2.答案 (1)有 (2)2H2O2 2H2O+O2↑ (3)对比 (4)增大
解析 (1)分析题图2可知,FeCl3溶液、CuSO4溶液都可以加快过氧化氢的分解,都对过氧化氢分解有催化作用。(2)由题图2可知,二氧化锰的催化效果最好,过氧化氢在二氧化锰的催化作用下分解产生水和氧气,反应的化学方程式是2H2O22H2O+O2↑。(4)分析题表数据,浓度相同时,温度升高,H2O2分解加快;同一温度下,H2O2溶液浓度越大,分解越快,则升高温度或增大反应物浓度都可加快H2O2的分解。
3.答案 (1)B (2)C2H5OH+3O2 2CO2+3H2O (3)①步骤2中白磷未燃烧,步骤4中白磷燃烧 ②m1>m2=m3 (4)取土填埋,隔绝空气(合理即可) (5)铁的表面积;氧气的浓度;温度(合理即可)
解析 (1)燃烧是发光、放热的剧烈的氧化反应,所以燃烧都有发光、放热现象;含硫的煤燃烧会产生具有刺激性气味的气体,而酒精和天然气燃烧不会产生有刺激性气味的气体;酒精、煤和天然气燃烧都能产生使澄清石灰水变浑浊的气体,故选B。(3)①步骤2和步骤4中,温度都达到了白磷的着火点,但步骤2中白磷未与氧气接触,不发生燃烧现象;步骤4中白磷与氧气接触,发生燃烧现象,说明燃烧需要氧气。②通入50 mL O2的同时会排出相同体积的CO2,由于O2的密度小于CO2的密度,所以通入O2后装置的质量减小,故m1>m2;根据质量守恒定律可知,装置中物质总质量在燃烧前后不变,所以m2=m3,故m1、m2、m3的大小关系是m1>m2=m3。(4)煤田中的煤层自燃,可以用取土填埋,隔绝空气的方法灭火。(5)根据燃烧的条件和已知信息可知,影响铁燃烧的因素有温度、氧气的浓度、铁的表面积等。
21世纪教育网(www.21cnjy.com)
专项素养综合全练(七)
科学探究
类型一 数字化实验
1.【新题型·数字化实验】(2023湖北武汉汉阳期中)氯酸钾为白色固体,熔点为356 ℃,受热分解会释放氧气。李明同学利用图1所示装置(夹持装置略)探究氯酸钾的热分解温度,所得氧气的体积分数和温度随时间的变化关系如图2所示。下列说法不正确的是 ( )
图1
图2
A.因为加热后氯酸钾慢慢变成液态,故图1试管口略向上倾斜
B.该实验证明氯酸钾在没有催化剂的条件下也会分解产生氧气
C.由图2可知氯酸钾在356 ℃时就开始大量分解产生氧气
D.图2表示氧气体积分数的曲线为乙
2.(2022湖北黄石中考改编)某化学兴趣小组在学习O2制备时,对 MnO2做催化剂加快过氧化氢分解产生了兴趣,他们提出疑问:其他物质能否对过氧化氢分解速率产生影响
【查阅资料】影响化学反应速率的因素有很多,如:使用催化剂、改变温度、改变反应物的浓度等。
【实验探究】小组的同学们按图所示组装仪器,在室温下分别进行了四组实验,并用O2传感器测定实验过程中O2含量的变化情况,得到如图2所示曲线。
组别 试剂
第1组 2 mL 5% H2O2溶液
第2组 2 mL 5% H2O2溶液+3滴FeCl3溶液
第3组 2 mL 5% H2O2溶液+3滴CuSO4溶液
第4组 2 mL 5% H2O2溶液+少量MnO2粉末
图1
图2
【实验结论】对比四条曲线,进行分析:
(1)FeCl3溶液、CuSO4溶液对H2O2的分解 (填“有”或“无”)催化作用。
(2)写出实验中催化效果最优的使H2O2分解的化学方程式: 。
(3)第1组实验的目的是 。
(4)小组的同学们不加催化剂,在不同温度下,用不同浓度的H2O2溶液进行实验,记录实验现象如下表。据此可得出:升高温度或 (填“增大”或“减小”)反应物浓度可加快H2O2的分解。
温度 现象 H2O2溶液浓度 50 ℃ 60 ℃ 70 ℃
5% 无明显气泡 无明显气泡 极少量气泡
10% 无明显气泡 无明显气泡 少量气泡
15% 无明显气泡 少量气泡 较多气泡
类型二 项目式探究
3.(2021安徽中考)关于燃烧的研究是一项重要的课题。某小组以“探究燃烧的奥秘”为主题开展项目式学习。
【任务一】认识燃烧
(1)酒精、煤(含硫)、天然气是生活中常见的燃料,下列不属于三者燃烧共有的现象是 (填字母)。
A.发光
B.产生有刺激性气味的气体
C.放热
D.产生使澄清石灰水变浑浊的气体
(2)写出酒精(C2H5OH)完全燃烧的化学方程式: 。
【任务二】探究燃烧的条件及质量变化
(3)该小组同学按下列实验步骤开展探究。
步骤1:室温下,按如图组装装置,装入药品,称量装置总质量为m1 g。
步骤2:将锥形瓶浸入80 ℃的热水中,观察现象。
步骤3:取出装置,恢复至室温并擦干锥形瓶;打开止水夹K1和K2,从K1处缓慢通入约50 mL氧气,再关闭K1和K2,称量装置总质量为m2 g。
步骤4:将锥形瓶再次浸入80 ℃的热水中,观察现象。
步骤5:取出装置,恢复至室温并擦干锥形瓶,称量装置总质量为m3 g。
①通过上述实验,能证明燃烧需要氧气的实验现象是 。
②m1、m2、m3的大小关系是 。
【任务三】调控燃烧
(4)报道显示:国内外一些煤田因发生煤层自燃,带来了资源浪费和环境污染。一旦煤层自燃,请给出一条合理的灭火建议: 。
【任务四】再探铁的燃烧
(5)查阅文献:颗粒直径为20~30 nm的铁粉,在空气中会发生自燃生成氧化铁。结合已有知识,回答下列问题:
影响铁燃烧的因素有 (至少答出2点)。
答案全解全析
1.答案C 氯酸钾熔点为356 ℃,随着温度的慢慢升高,氯酸钾会变为液态,所以题图1试管口应略向上倾斜,A正确。该实验是氯酸钾直接加热生成氧气,可以证明氯酸钾在没有催化剂的条件下也会分解产生氧气,B正确。氧气约占空气体积的21%,与题图2中曲线乙起始的位置大致相同,所以曲线乙表示氧气的体积分数;由曲线乙可以看出,在150 s左右曲线变陡,说明开始大量分解产生氧气,C错误、D正确。
2.答案 (1)有 (2)2H2O2 2H2O+O2↑ (3)对比 (4)增大
解析 (1)分析题图2可知,FeCl3溶液、CuSO4溶液都可以加快过氧化氢的分解,都对过氧化氢分解有催化作用。(2)由题图2可知,二氧化锰的催化效果最好,过氧化氢在二氧化锰的催化作用下分解产生水和氧气,反应的化学方程式是2H2O22H2O+O2↑。(4)分析题表数据,浓度相同时,温度升高,H2O2分解加快;同一温度下,H2O2溶液浓度越大,分解越快,则升高温度或增大反应物浓度都可加快H2O2的分解。
3.答案 (1)B (2)C2H5OH+3O2 2CO2+3H2O (3)①步骤2中白磷未燃烧,步骤4中白磷燃烧 ②m1>m2=m3 (4)取土填埋,隔绝空气(合理即可) (5)铁的表面积;氧气的浓度;温度(合理即可)
解析 (1)燃烧是发光、放热的剧烈的氧化反应,所以燃烧都有发光、放热现象;含硫的煤燃烧会产生具有刺激性气味的气体,而酒精和天然气燃烧不会产生有刺激性气味的气体;酒精、煤和天然气燃烧都能产生使澄清石灰水变浑浊的气体,故选B。(3)①步骤2和步骤4中,温度都达到了白磷的着火点,但步骤2中白磷未与氧气接触,不发生燃烧现象;步骤4中白磷与氧气接触,发生燃烧现象,说明燃烧需要氧气。②通入50 mL O2的同时会排出相同体积的CO2,由于O2的密度小于CO2的密度,所以通入O2后装置的质量减小,故m1>m2;根据质量守恒定律可知,装置中物质总质量在燃烧前后不变,所以m2=m3,故m1、m2、m3的大小关系是m1>m2=m3。(4)煤田中的煤层自燃,可以用取土填埋,隔绝空气的方法灭火。(5)根据燃烧的条件和已知信息可知,影响铁燃烧的因素有温度、氧气的浓度、铁的表面积等。
21世纪教育网(www.21cnjy.com)
同课章节目录
