4.2物质组成的表示 同步练习 ---2023-2024学年九年级化学鲁教版上册
文档属性
| 名称 | 4.2物质组成的表示 同步练习 ---2023-2024学年九年级化学鲁教版上册 |

|
|
| 格式 | docx | ||
| 文件大小 | 582.1KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-15 00:00:00 | ||
图片预览




文档简介
4.2物质组成的表示
一、单选题
1.下列有关分子、原子的说法正确的是
A.分子能保持物质的化学性质,原子不能保持物质的化学性质
B.物质热胀冷缩是由于分子的大小随温度发生改变
C.汞由汞原子构成
D.在化学变化中分子和原子均不发生改变
2.下列有关化学用语表示正确的是
A.二氧化氯:ClO2 B.汞元素:Ag
C.2个碳酸分子:2CO3 D.3个氧原子:O3
3.下列化学用语与含义相符的是
A.Cu2+——铜元素的化合价为正二价 B.Fe(NO3)2——硝酸铁
C.2N——2个氮原子 D.KCO3——碳酸钾
4.下列物质的俗称与化学式不相符的是
A.水银 Ag B.干冰 CO2 C.烧碱 NaOH D.食盐 NaCl
5.碳纳米管和单晶硅在信息、材料等领域中应用广泛。碳原子和硅原子的结构示意图分别为和,下列关于碳元素和硅元素的说法错误的是
A.都是非金属元素 B.原子的最外层电子数相同
C.在化合物中都只显+4价 D.分别位于元素周期表第二、三周期
6.在常温下,臭氧是一种有特殊臭味的淡蓝色气体。对人类有利也有弊,结合图示判读下列叙述正确的是
A.臭氧是3个氧元素构成的
B.臭氧分子中质子数等于电子数
C.臭氧和氧气的化学性质相同
D.臭氧的符号表达式是3O
7.下列化学符号中数字“2”表示的意义,正确的是
A.2Hg:表示2个汞原子 B.CO2:1个氧分子中有2个氧原子
C.表示一个镁离子带2个单位正电荷 D.S2-:表示硫元素的化合价为﹣2价
8.N(NO2)3是科学家近年发现的一种新型火箭燃料。下列关于N(NO2)3说法正确的是
A.N(NO2)3中氮元素与氧元素的质量比是2:3
B.N(NO2)3的相对分子质量为152
C.N(NO2)3分子中总共有3个氮原子和6个氧原子
D.N(NO2)3中氮元素的质量分数为20%
9.下列数据关系的判断中正确的是( )
A.水中氧元素化合价为a,双氧水中氧元素化合价为b,则a=b
B.KMnO4中锰元素化合价为a, CaMnO4中锰元素化合价为b则a=b
C.NH4NO3中氮元素化合价为a,N2O中氮元素化合价为b,则a=b
D.FeSO4中铁元素化合价为a,FePO4铁元素化合价为b,则a10.科技创新奏响 2022 年北京冬奥会主火炬“冰与火”之歌。开幕式前夕首次实现奥运史上水下机器人之间的奥运火炬传递,奥运火炬使用绿色、环保的丙烷气体(C3H8)做燃料。下列有关丙烷的说法中,正确的是
A.由 C、H 两个元素组成
B.碳、氢元素间的质量比为 3∶8
C.1 个丙烷分子由 3 个碳原子和 8 个氢原子构成
D.含氢元素质量分数计算式
11.甲和乙在一定条件下反应生成丙和丁,微观示意图如下.有关说法正确的是
A.反应前后分子的种类不变
B.反应前后各元素的化合价均不变
C.四种物质中三种是化合物、一种单质
D.丙物质由2个氢原子和1个氧原子构成
12.瑞德西韦是一种核苷类似物,具有抗病毒活性。2020年2月用于少数2019-nCoV感染者的急症测试治疗。已知瑞德西韦的化学式为C27H35N6O8P。下列有关其说法正确的是( )
A.瑞德西韦的相对分子质量为60lg B.瑞德西韦中质量分数最小的为氢元素
C.瑞德西韦中氮氧元素质量比为21︰32 D.瑞德西韦属于氧化物
13.下列化学用语中表示的意义不正确的是
A.Ca:表示钙元素 B.4OH-:表示4个氢氧根离子
C.2N:表示2个氮分子 D.3K:表示3个钾原子
14.下列微粒符号中,对“2”含义的理解正确的是
A.2Cu中的“2”表示2个铜元素
B.中的“2”表示每个亚铁离子带有2个单位的正电荷
C.H2O中的“2”表示一个水分子中含有一个氢分子
D.中化学式上方的“2”表示硫元素为-2价
二、填空题
15.如图1是元素周期表的一部分,请回答:
(1)①处元素和②处元素形成常见化合物的化学式为Al2O3,该化合物中②处元素的化合价为 .
(2)图2表示如图1中 (填表中序号)的原子结构示意图,该原子易 (选填“得”或“失”)电子,形成的离子符号为 .
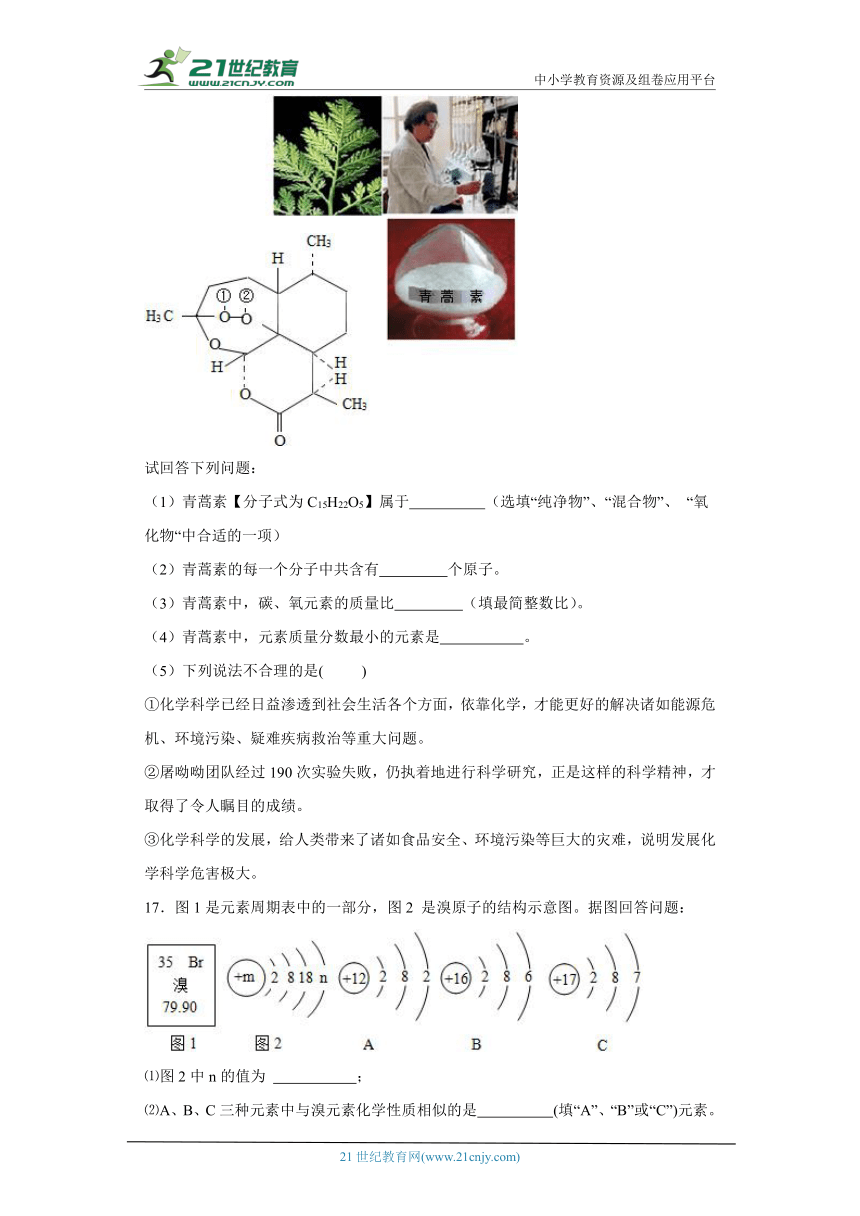
16.2015年10月,中国女药学家屠呦呦因创制新型抗疟药---青蒿素和双氢青蒿素的贡献,获得诺贝尔生理学或医学奖。青蒿素【分子式为C15H22O5】——一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命。
试回答下列问题:
(1)青蒿素【分子式为C15H22O5】属于 (选填“纯净物”、“混合物”、 “氧化物“中合适的一项)
(2)青蒿素的每一个分子中共含有 个原子。
(3)青蒿素中,碳、氧元素的质量比 (填最简整数比)。
(4)青蒿素中,元素质量分数最小的元素是 。
(5)下列说法不合理的是( )
①化学科学已经日益渗透到社会生活各个方面,依靠化学,才能更好的解决诸如能源危机、环境污染、疑难疾病救治等重大问题。
②屠呦呦团队经过190次实验失败,仍执着地进行科学研究,正是这样的科学精神,才取得了令人瞩目的成绩。
③化学科学的发展,给人类带来了诸如食品安全、环境污染等巨大的灾难,说明发展化学科学危害极大。
17.图1是元素周期表中的一部分,图2 是溴原子的结构示意图。据图回答问题:
⑴图2中n的值为 ;
⑵A、B、C三种元素中与溴元素化学性质相似的是 (填“A”、“B”或“C”)元素。
⑶若B原子得到2个电子形成离子,则其对应的化学符号为
⑷写出溴和A形成化合物的化学式
三、实验题
18.用浓氨水和浓盐酸做气体扩散速度的实验,如图所示,两种气体扩散相遇时形成白色烟环。
(1)已知气体的相对分子质量越小,扩散速度越快,由此判断物质甲是 。
(2)该实验利用了甲、乙的共同物理性质是 ;白色烟环的化学式是 。
(3)在形成白色烟环之前,乙会形成白雾,试从微观的角度解释这两种变化的本质区别。 。
四、计算题
19.蔗糖是食品中常用的甜味剂,其化学式为C12H22O11。请回答下列问题:
(1)蔗糖的相对分子质量为 。
(2)计算17.1g蔗糖中含氢元素的质量。
20.下图为某品牌巧克力的部分配料说明,查阅资料得知配料表中香兰素的化学式为C8H8O3,又名香草醛。是一种广泛使用的香料。食品厂商在生产时使用香兰素须遵守一定使用限量(mg/kg)。请计算:
(1)香兰素中碳、氢、氧元素的质量比为 。
(2)每个香兰素分子中共有 个原子。
(3)香兰素的相对分子质量是 。
(4)计算香兰素中碳元素的质量分数 。(精确到0.1%,写出计算过程,下同)
(5)304kg香兰素中含有的碳元素的质量为 ?
(6)若小明同学每天食用2块10g巧克力,根据配料表中数据分析计算,小明一天最多摄取的香兰素的质量为 ?
五、综合应用题
21.学好化学知识,助力个人防护,预防新冠病毒感染。
(1)出门要戴好口罩。制作口罩用的无纺布面料主要是聚丙烯,聚丙烯中碳、氢元素质量比为 (填写最简整数比)。
(2)预防期间,常用“84”消毒液和75%的酒精进行消毒。“84”消毒液的主要成分是次氯酸钠()和氯化钠(),两种物质中氯元素的化合价依次是 、 。酒精的学名为乙醇,其化学式是,酒精分子中碳、氢两种原子的个数比为 (填写最简整数比)
(3)为了增强体质,我们需要进行体育锻炼。锻炼后常出现肌肉酸痛,这是由于部分葡萄糖()无氧代谢产生乳酸()造成的,休息后即可缓解。
①乳酸的化学式量为 ;
②乳酸中碳元素的质量分数为 ;
③多少克乳酸中含有7.2g碳元素? (写出计算过程)
中小学教育资源及组卷应用平台
试卷第1页,共3页
21世纪教育网(www.21cnjy.com)
参考答案:
1.C
【详解】A、由分子构成的物质,分子保持物质的化学性质;由原子直接构成的物质,原子保持该物质的化学性质,不符合题意;
B、物质热胀冷缩是由于分子的间隔随温度发生改变,不符合题意;
C、汞是金属,汞由汞原子构成,符合题意;
D、在化学变化中分子可分,原子不发生改变,不符合题意。故选C。
2.A
【详解】A、根据化学式书写原则,正价在左负价在右,正负化合价代数和为零,化合价数值约到最简交叉写在元素右下角,二氧化氯中氯元素化合价为+4价,氧元素为-2价。化学式为,选项正确;
B、汞元素化学符号是,选项错误;
C、数字在分子式前表示分子个数,2个碳酸分子符号是,选项错误;
D、数字在元素符号前表示原子个数,3个氧原子表示为,选项错误;
故选:A。
3.C
【详解】A、Cu2+表示铜离子,铜元素的化合价为正二价,表示为,不符合题意;
B、硝酸铁中铁元素为+3价,硝酸根为-1价,化学式为Fe(NO3)3,不符合题意;
C、元素符号前面的数字表示原子个数,2N表示2个氮原子,符合题意;
D、碳酸钾中钾元素为+1价,碳酸根为-2价,化学式为K2CO3,不符合题意。
故选C。
4.A
【详解】A.水银是金属汞的俗称,其化学式为Hg,故A错误;
B.干冰是固态二氧化碳,其化学式为CO2,故B正确;
C.氢氧化钠的俗称是火碱、烧碱、苛性钠,其化学式为NaOH,故C正确;
D.氯化钠俗名食盐,其化学式为NaCl,故D正确;
故选A。
【点睛】熟练掌握常见物质的名称、俗称、化学式。
5.C
【详解】A、由碳、硅汉字结构可知,两者属于非金属元素,正确;
B、由图可知,两者原子的最外层电子数均为4,最外层电子数相同,正确;
C、在一氧化碳中碳元素化合价为+2,错误;
D、碳原子核外有2个电子层、硅原子核外有3个电子层,分别位于元素周期表第二、三周期,正确。
故选C。
6.B
【详解】A、元素是宏观概念,只讲种类、不讲个数,臭氧是由氧元素组成的,故A错误;
B、分子是由原子构成的,在原子中,质子数=电子数,所以臭氧分子中质子数等于电子数,故B正确;
C、臭氧的化学式为O3 ,氧气的化学式为O2 ,二者的分子结构不同,所以化学性质也不同,故C错误;
D、3O表示三个氧原子,由分子结构模型可知,臭氧的化学式为O3 ,故D错误。故选B。
7.A
【详解】A、元素符号前面的数字表示原子个数,故2Hg表示2个汞原子,符合题意;
B、位于化学式中元素符号(或原子团)的右下角,表示一个分子中所含的原子或原子团的个数。故CO2中的“2”表示1个二氧化碳分子中含2个氧原子,不符合题意;
C、位于元素或原子团的正上方,表示元素或原子团的化合价。故表示镁元素显+2价,不符合题意;
D、位于离子符号中元素或原子团的右上角,表示一个离子所带的电荷数。故S2-中的“2”表示1个硫离子带2个单位的负电荷,不符合题意。
故选A。
8.B
【详解】A、N(NO2)3中氮元素与氧元素的质量比是(14×4):(16×2×3)=7:12,故错误
B、N(NO2)3的相对分子质量=14×4+16×6=152,故正确;
C、每个N(NO2)3分子中总共有4个氮原子和6个氧原子,故错误;
D、N(NO2)3中氮元素的质量分数为≠20%,故错误。
故选:B。
9.D
【详解】A、双氧水中氧元素化合价为a,a=-1;水中氧元素化合价为b,b=-2,则b<a,故错误;
B、钾显+1价,氧显-2价,设化合物KMnO4中Mn元素化合价为a,依化合物中各元素化合价代数和为零的原则,有(+1)+a+(-2)×4=0,解得a=+7;设化合物CaMnO4中Mn元素化合价为b,依化合物中各元素化合价代数和为零的原则,有(+2)+b+(-2)×4=0,解得b=+6;则b<a,故错误;
C、NH4NO3中氮元素化合价分别为-3价、+5价,N2O中氮元素化合价为+1价,则a不等于b,故错误;
D、FeSO4中铁元素化合价为+2价,FePO4铁元素化合价为+3价,则a故选D。
10.C
【详解】A、元素只讲种类、不讲个数,故A选项说法错误;
B、丙烷C3H8中碳、氢元素的质量比=(12×3):(1×8)=9:2≠3:8,故B选项说法错误;
C、根据丙烷的化学式C3H8,1 个丙烷分子由 3 个碳原子和 8 个氢原子构成,故C 选项说法正确;
D、丙烷的化学式为C3H8,其中氢元素的质量分数为,故D选项说法错误。
故答案为:C。
11.C
【详解】由微观反应示意图可知,该反应是由氨气和氧气在一定条件下反应生成水和一氧化氮,化学方程式为:。
A.由化学方程式可知,反应前后分子的种类、数目均发生改变,选项说法错误;
B.该反应有单质参加反应,一定有元素化合价的变化,选项说法错误;
C.由物质的构成可知,四种物质中三种是化合物、一种单质,选项说法正确;
D.由物质的构成可知,丙物质的一个分子由2个氢原子和1个氧原子构成,选项说法错误。
故选:C。
12.C
【详解】A、相对分子质量单位是“1”,不是“克”,常常省略不写。瑞德西韦的相对分子质量为601,故选项说法错误。
B、瑞德西韦中碳、氢、氮、氧、磷5种元素的质量比为 ,瑞德西韦中质量分数最小的为磷元素,故选项说法错误。
C、瑞德西韦中氮、氧两种元素的质量比为 ,故选项说法正确。
D、瑞德西韦是由碳、氢、氮、氧、磷五种元素组成的化合物,不属于氧化物,故选项说法错误。.
故选: C。
13.C
【详解】A、元素符号第一个字母大写,第二个字母小写,钙元素的符号是:Ca,选项正确;
B、由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,数字在离子符号前表示离子的个数,4OH-表示4个氢氧根离子,选项正确;
C、数字在元素符号前表示原子个数,2N表示2个氮原子,选项错误;
D、数字在元素符号前表示原子个数,3K表示3个钾原子,选项正确;
故选:C。
14.B
【详解】A、元素符号前的数字表示原子个数,则2Cu中的“2”表示2个铜原子,且元素只有种类,没有个数,该选项理解不正确;
B、元素符号右上角的数字表示离子所带电荷数,Fe2+中的“2”表示每个亚铁离子带有2个单位的正电荷;,该选项理解正确;
C、元素符号右下角的数字表示分子中原子个数,则H2O中的“2”表示一个水分子中含有2个氢原子,该选项理解不正确;
D、元素符号正上方的数字表示元素化合价,但硫酸铝中,氧元素的化合价为-2价,硫酸根的化合价为-2价,设硫元素的化合价为x,则x+(-2)×4=-2,解得x=+6,即硫酸铝中硫元素的化合价为+6,该选项理解不正确。
故选B。
15. +3 ④ 得 Cl﹣
【详解】(1)根据元素周期表是按原子序数递增的顺序排列的,②处元素为铝元素,氧元素显-2价,设铝元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:2x+(-2)×3=0,则x=+3价;
(2)图2中原子的核内质子数为17,为氯元素,硅的原子序数为14,则表示如图1中④的原子结构示意图;最外层电子数是7,在化学反应中易得到1个电子而形成带1个单位负电荷的氯离子,形成的离子符号为Cl-。
16. 纯净物 42 9:4 H/氢元素 ③
【详解】(1)由青蒿素的【分子式为C15H22O5】可见它属于纯净物,故填纯净物
(2)元素符号右下角的数字表示该分子中原子的个数,可知青蒿素的每一个分子中含有15+22+5=42故填42
(3)青蒿素中碳氧元素的质量比为:碳原子的个数乘以碳原子的相对原子质量与氧原子的个数乘以氧原子的相对原子质量之比即(12×15):(16×5)=9:4故填9:4
(4)青蒿素中各种元素的质量分数为该元素的质量与青蒿素的相对分子质量之比故碳元素的质量分数为:氢元素的质量分数为:氧元素的质量分数为:故元素质量分数最小的元素为氢元素。
(5)由题中可知③不正确,化学是一把双刃剑合理利用化学可以为人类造福,故填③
17. 7 C S2- MgBr2
【详解】(1)在元素周期表中,元素名称左上角的数字表示原子序数,原子序数=质子数=m=35,在原子中,质子数=核外电子数,35=2+8+18+n,n=7;
(2)C与溴原子的最外层电子数相同,均是7,化学性质相似;
(3)质子数=原子序数,16号元素是硫元素,故B为硫原子,硫原子的最外层电子数为6,大于4,在化学反应中,容易得到2个电子,从而带上2个单位的负电荷,形成硫离子,表示为:S2-;
(4)A原子质子数为12,所以为镁原子,镁原子最外层电子数为2,在化学反应中,容易失去2个电子形成镁离子,显+2价,溴原子最外层电子数为7,在化学反应中,容易得到1个电子形成溴离子,显-1价,所以二者形成的化学式为:MgBr2。
18. 浓氨水 挥发性 形成白雾是物理变化,是挥发出的氯化氢分子溶于水蒸气形成的;形成白烟是化学变化,参加反应的氯化氢分子与氨气分子发生改变,重新组成了新的固态物质氯化铵
【详解】(1)已知气体的相对分子质量越小,扩散速度越快,氨气的相对分子质量小于氯化氢,由此判断物质甲是浓氨水;
(2)该实验利用了甲、乙的共同物理性质是挥发性;氨气与氯化氢反应生成氯化铵固体,白色烟环的化学式是;
(3)这两种变化的本质区别是形成白雾是物理变化,是挥发出的氯化氢分子溶于水蒸气形成的;形成白烟是化学变化,参加反应的氯化氢分子与氨气分子发生改变,重新组成了新的固态物质氯化铵。
19.(1)342
(2)1.1g
17.1g蔗糖中含氢元素的质量为17.1g××100%=1.1g;
答:17.1g蔗糖中含氢元素的质量为1.1g。
【解析】(1)
蔗糖的相对分子质量为12×12+1×22+16×11=342,故填:342;
(2)
见答案。
20.(1)12:1:6
(2)19
(3)152
(4)
(5)
(6)2×10×10-3kg×970mg/kg=19.4mg
【分析】(1)
香兰素中碳、氢、氧元素的质量比为:(12×8):8:(16×3)=12:1:6;
(2)
由化学式可知,每个香兰素分子中含有8个碳原子、8个氢原子、3个氧原子,共19个原子;
(3)
香兰素的相对分子质量是:12×8+8+16×3=152;
(4)
见答案;
(5)
见答案;
(6)
见答案。
21.(1)6:1
(2) +1 -1 1:3
(3) 90 40% 由于乳酸碳元素的质量分数为40%,故含有7.2g碳元素的乳酸质量为
【详解】(1)已知聚丙烯的化学式为,聚丙烯中碳、氢元素的质量比为。
(2)①、次氯酸钠中钠,元素化合价是+1,氧元素化合价是-2,根据化合物中元素化合价代数和为零可知,氯元素的化合价是+1;
②、氯化钠中,钠元素化合价是+1,根据化合物中元素化合价代数和为零可知,氯元素的化合价是-1;
③、酒精的学名是乙醇,化学式是,乙醇分子中共含有3种原子,一个酒精分子中含有2个碳原子,6个氢原子,故酒精分子中碳、氢两种原子的个数比为2:6=1:3。
(3)①、乳酸的化学式量为;
②、乳酸中碳元素的质量分数为;
③、由于乳酸碳元素的质量分数为40%,故含有7.2g碳元素的乳酸质量为。
一、单选题
1.下列有关分子、原子的说法正确的是
A.分子能保持物质的化学性质,原子不能保持物质的化学性质
B.物质热胀冷缩是由于分子的大小随温度发生改变
C.汞由汞原子构成
D.在化学变化中分子和原子均不发生改变
2.下列有关化学用语表示正确的是
A.二氧化氯:ClO2 B.汞元素:Ag
C.2个碳酸分子:2CO3 D.3个氧原子:O3
3.下列化学用语与含义相符的是
A.Cu2+——铜元素的化合价为正二价 B.Fe(NO3)2——硝酸铁
C.2N——2个氮原子 D.KCO3——碳酸钾
4.下列物质的俗称与化学式不相符的是
A.水银 Ag B.干冰 CO2 C.烧碱 NaOH D.食盐 NaCl
5.碳纳米管和单晶硅在信息、材料等领域中应用广泛。碳原子和硅原子的结构示意图分别为和,下列关于碳元素和硅元素的说法错误的是
A.都是非金属元素 B.原子的最外层电子数相同
C.在化合物中都只显+4价 D.分别位于元素周期表第二、三周期
6.在常温下,臭氧是一种有特殊臭味的淡蓝色气体。对人类有利也有弊,结合图示判读下列叙述正确的是
A.臭氧是3个氧元素构成的
B.臭氧分子中质子数等于电子数
C.臭氧和氧气的化学性质相同
D.臭氧的符号表达式是3O
7.下列化学符号中数字“2”表示的意义,正确的是
A.2Hg:表示2个汞原子 B.CO2:1个氧分子中有2个氧原子
C.表示一个镁离子带2个单位正电荷 D.S2-:表示硫元素的化合价为﹣2价
8.N(NO2)3是科学家近年发现的一种新型火箭燃料。下列关于N(NO2)3说法正确的是
A.N(NO2)3中氮元素与氧元素的质量比是2:3
B.N(NO2)3的相对分子质量为152
C.N(NO2)3分子中总共有3个氮原子和6个氧原子
D.N(NO2)3中氮元素的质量分数为20%
9.下列数据关系的判断中正确的是( )
A.水中氧元素化合价为a,双氧水中氧元素化合价为b,则a=b
B.KMnO4中锰元素化合价为a, CaMnO4中锰元素化合价为b则a=b
C.NH4NO3中氮元素化合价为a,N2O中氮元素化合价为b,则a=b
D.FeSO4中铁元素化合价为a,FePO4铁元素化合价为b,则a
A.由 C、H 两个元素组成
B.碳、氢元素间的质量比为 3∶8
C.1 个丙烷分子由 3 个碳原子和 8 个氢原子构成
D.含氢元素质量分数计算式
11.甲和乙在一定条件下反应生成丙和丁,微观示意图如下.有关说法正确的是
A.反应前后分子的种类不变
B.反应前后各元素的化合价均不变
C.四种物质中三种是化合物、一种单质
D.丙物质由2个氢原子和1个氧原子构成
12.瑞德西韦是一种核苷类似物,具有抗病毒活性。2020年2月用于少数2019-nCoV感染者的急症测试治疗。已知瑞德西韦的化学式为C27H35N6O8P。下列有关其说法正确的是( )
A.瑞德西韦的相对分子质量为60lg B.瑞德西韦中质量分数最小的为氢元素
C.瑞德西韦中氮氧元素质量比为21︰32 D.瑞德西韦属于氧化物
13.下列化学用语中表示的意义不正确的是
A.Ca:表示钙元素 B.4OH-:表示4个氢氧根离子
C.2N:表示2个氮分子 D.3K:表示3个钾原子
14.下列微粒符号中,对“2”含义的理解正确的是
A.2Cu中的“2”表示2个铜元素
B.中的“2”表示每个亚铁离子带有2个单位的正电荷
C.H2O中的“2”表示一个水分子中含有一个氢分子
D.中化学式上方的“2”表示硫元素为-2价
二、填空题
15.如图1是元素周期表的一部分,请回答:
(1)①处元素和②处元素形成常见化合物的化学式为Al2O3,该化合物中②处元素的化合价为 .
(2)图2表示如图1中 (填表中序号)的原子结构示意图,该原子易 (选填“得”或“失”)电子,形成的离子符号为 .
16.2015年10月,中国女药学家屠呦呦因创制新型抗疟药---青蒿素和双氢青蒿素的贡献,获得诺贝尔生理学或医学奖。青蒿素【分子式为C15H22O5】——一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命。
试回答下列问题:
(1)青蒿素【分子式为C15H22O5】属于 (选填“纯净物”、“混合物”、 “氧化物“中合适的一项)
(2)青蒿素的每一个分子中共含有 个原子。
(3)青蒿素中,碳、氧元素的质量比 (填最简整数比)。
(4)青蒿素中,元素质量分数最小的元素是 。
(5)下列说法不合理的是( )
①化学科学已经日益渗透到社会生活各个方面,依靠化学,才能更好的解决诸如能源危机、环境污染、疑难疾病救治等重大问题。
②屠呦呦团队经过190次实验失败,仍执着地进行科学研究,正是这样的科学精神,才取得了令人瞩目的成绩。
③化学科学的发展,给人类带来了诸如食品安全、环境污染等巨大的灾难,说明发展化学科学危害极大。
17.图1是元素周期表中的一部分,图2 是溴原子的结构示意图。据图回答问题:
⑴图2中n的值为 ;
⑵A、B、C三种元素中与溴元素化学性质相似的是 (填“A”、“B”或“C”)元素。
⑶若B原子得到2个电子形成离子,则其对应的化学符号为
⑷写出溴和A形成化合物的化学式
三、实验题
18.用浓氨水和浓盐酸做气体扩散速度的实验,如图所示,两种气体扩散相遇时形成白色烟环。
(1)已知气体的相对分子质量越小,扩散速度越快,由此判断物质甲是 。
(2)该实验利用了甲、乙的共同物理性质是 ;白色烟环的化学式是 。
(3)在形成白色烟环之前,乙会形成白雾,试从微观的角度解释这两种变化的本质区别。 。
四、计算题
19.蔗糖是食品中常用的甜味剂,其化学式为C12H22O11。请回答下列问题:
(1)蔗糖的相对分子质量为 。
(2)计算17.1g蔗糖中含氢元素的质量。
20.下图为某品牌巧克力的部分配料说明,查阅资料得知配料表中香兰素的化学式为C8H8O3,又名香草醛。是一种广泛使用的香料。食品厂商在生产时使用香兰素须遵守一定使用限量(mg/kg)。请计算:
(1)香兰素中碳、氢、氧元素的质量比为 。
(2)每个香兰素分子中共有 个原子。
(3)香兰素的相对分子质量是 。
(4)计算香兰素中碳元素的质量分数 。(精确到0.1%,写出计算过程,下同)
(5)304kg香兰素中含有的碳元素的质量为 ?
(6)若小明同学每天食用2块10g巧克力,根据配料表中数据分析计算,小明一天最多摄取的香兰素的质量为 ?
五、综合应用题
21.学好化学知识,助力个人防护,预防新冠病毒感染。
(1)出门要戴好口罩。制作口罩用的无纺布面料主要是聚丙烯,聚丙烯中碳、氢元素质量比为 (填写最简整数比)。
(2)预防期间,常用“84”消毒液和75%的酒精进行消毒。“84”消毒液的主要成分是次氯酸钠()和氯化钠(),两种物质中氯元素的化合价依次是 、 。酒精的学名为乙醇,其化学式是,酒精分子中碳、氢两种原子的个数比为 (填写最简整数比)
(3)为了增强体质,我们需要进行体育锻炼。锻炼后常出现肌肉酸痛,这是由于部分葡萄糖()无氧代谢产生乳酸()造成的,休息后即可缓解。
①乳酸的化学式量为 ;
②乳酸中碳元素的质量分数为 ;
③多少克乳酸中含有7.2g碳元素? (写出计算过程)
中小学教育资源及组卷应用平台
试卷第1页,共3页
21世纪教育网(www.21cnjy.com)
参考答案:
1.C
【详解】A、由分子构成的物质,分子保持物质的化学性质;由原子直接构成的物质,原子保持该物质的化学性质,不符合题意;
B、物质热胀冷缩是由于分子的间隔随温度发生改变,不符合题意;
C、汞是金属,汞由汞原子构成,符合题意;
D、在化学变化中分子可分,原子不发生改变,不符合题意。故选C。
2.A
【详解】A、根据化学式书写原则,正价在左负价在右,正负化合价代数和为零,化合价数值约到最简交叉写在元素右下角,二氧化氯中氯元素化合价为+4价,氧元素为-2价。化学式为,选项正确;
B、汞元素化学符号是,选项错误;
C、数字在分子式前表示分子个数,2个碳酸分子符号是,选项错误;
D、数字在元素符号前表示原子个数,3个氧原子表示为,选项错误;
故选:A。
3.C
【详解】A、Cu2+表示铜离子,铜元素的化合价为正二价,表示为,不符合题意;
B、硝酸铁中铁元素为+3价,硝酸根为-1价,化学式为Fe(NO3)3,不符合题意;
C、元素符号前面的数字表示原子个数,2N表示2个氮原子,符合题意;
D、碳酸钾中钾元素为+1价,碳酸根为-2价,化学式为K2CO3,不符合题意。
故选C。
4.A
【详解】A.水银是金属汞的俗称,其化学式为Hg,故A错误;
B.干冰是固态二氧化碳,其化学式为CO2,故B正确;
C.氢氧化钠的俗称是火碱、烧碱、苛性钠,其化学式为NaOH,故C正确;
D.氯化钠俗名食盐,其化学式为NaCl,故D正确;
故选A。
【点睛】熟练掌握常见物质的名称、俗称、化学式。
5.C
【详解】A、由碳、硅汉字结构可知,两者属于非金属元素,正确;
B、由图可知,两者原子的最外层电子数均为4,最外层电子数相同,正确;
C、在一氧化碳中碳元素化合价为+2,错误;
D、碳原子核外有2个电子层、硅原子核外有3个电子层,分别位于元素周期表第二、三周期,正确。
故选C。
6.B
【详解】A、元素是宏观概念,只讲种类、不讲个数,臭氧是由氧元素组成的,故A错误;
B、分子是由原子构成的,在原子中,质子数=电子数,所以臭氧分子中质子数等于电子数,故B正确;
C、臭氧的化学式为O3 ,氧气的化学式为O2 ,二者的分子结构不同,所以化学性质也不同,故C错误;
D、3O表示三个氧原子,由分子结构模型可知,臭氧的化学式为O3 ,故D错误。故选B。
7.A
【详解】A、元素符号前面的数字表示原子个数,故2Hg表示2个汞原子,符合题意;
B、位于化学式中元素符号(或原子团)的右下角,表示一个分子中所含的原子或原子团的个数。故CO2中的“2”表示1个二氧化碳分子中含2个氧原子,不符合题意;
C、位于元素或原子团的正上方,表示元素或原子团的化合价。故表示镁元素显+2价,不符合题意;
D、位于离子符号中元素或原子团的右上角,表示一个离子所带的电荷数。故S2-中的“2”表示1个硫离子带2个单位的负电荷,不符合题意。
故选A。
8.B
【详解】A、N(NO2)3中氮元素与氧元素的质量比是(14×4):(16×2×3)=7:12,故错误
B、N(NO2)3的相对分子质量=14×4+16×6=152,故正确;
C、每个N(NO2)3分子中总共有4个氮原子和6个氧原子,故错误;
D、N(NO2)3中氮元素的质量分数为≠20%,故错误。
故选:B。
9.D
【详解】A、双氧水中氧元素化合价为a,a=-1;水中氧元素化合价为b,b=-2,则b<a,故错误;
B、钾显+1价,氧显-2价,设化合物KMnO4中Mn元素化合价为a,依化合物中各元素化合价代数和为零的原则,有(+1)+a+(-2)×4=0,解得a=+7;设化合物CaMnO4中Mn元素化合价为b,依化合物中各元素化合价代数和为零的原则,有(+2)+b+(-2)×4=0,解得b=+6;则b<a,故错误;
C、NH4NO3中氮元素化合价分别为-3价、+5价,N2O中氮元素化合价为+1价,则a不等于b,故错误;
D、FeSO4中铁元素化合价为+2价,FePO4铁元素化合价为+3价,则a
10.C
【详解】A、元素只讲种类、不讲个数,故A选项说法错误;
B、丙烷C3H8中碳、氢元素的质量比=(12×3):(1×8)=9:2≠3:8,故B选项说法错误;
C、根据丙烷的化学式C3H8,1 个丙烷分子由 3 个碳原子和 8 个氢原子构成,故C 选项说法正确;
D、丙烷的化学式为C3H8,其中氢元素的质量分数为,故D选项说法错误。
故答案为:C。
11.C
【详解】由微观反应示意图可知,该反应是由氨气和氧气在一定条件下反应生成水和一氧化氮,化学方程式为:。
A.由化学方程式可知,反应前后分子的种类、数目均发生改变,选项说法错误;
B.该反应有单质参加反应,一定有元素化合价的变化,选项说法错误;
C.由物质的构成可知,四种物质中三种是化合物、一种单质,选项说法正确;
D.由物质的构成可知,丙物质的一个分子由2个氢原子和1个氧原子构成,选项说法错误。
故选:C。
12.C
【详解】A、相对分子质量单位是“1”,不是“克”,常常省略不写。瑞德西韦的相对分子质量为601,故选项说法错误。
B、瑞德西韦中碳、氢、氮、氧、磷5种元素的质量比为 ,瑞德西韦中质量分数最小的为磷元素,故选项说法错误。
C、瑞德西韦中氮、氧两种元素的质量比为 ,故选项说法正确。
D、瑞德西韦是由碳、氢、氮、氧、磷五种元素组成的化合物,不属于氧化物,故选项说法错误。.
故选: C。
13.C
【详解】A、元素符号第一个字母大写,第二个字母小写,钙元素的符号是:Ca,选项正确;
B、由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,数字在离子符号前表示离子的个数,4OH-表示4个氢氧根离子,选项正确;
C、数字在元素符号前表示原子个数,2N表示2个氮原子,选项错误;
D、数字在元素符号前表示原子个数,3K表示3个钾原子,选项正确;
故选:C。
14.B
【详解】A、元素符号前的数字表示原子个数,则2Cu中的“2”表示2个铜原子,且元素只有种类,没有个数,该选项理解不正确;
B、元素符号右上角的数字表示离子所带电荷数,Fe2+中的“2”表示每个亚铁离子带有2个单位的正电荷;,该选项理解正确;
C、元素符号右下角的数字表示分子中原子个数,则H2O中的“2”表示一个水分子中含有2个氢原子,该选项理解不正确;
D、元素符号正上方的数字表示元素化合价,但硫酸铝中,氧元素的化合价为-2价,硫酸根的化合价为-2价,设硫元素的化合价为x,则x+(-2)×4=-2,解得x=+6,即硫酸铝中硫元素的化合价为+6,该选项理解不正确。
故选B。
15. +3 ④ 得 Cl﹣
【详解】(1)根据元素周期表是按原子序数递增的顺序排列的,②处元素为铝元素,氧元素显-2价,设铝元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:2x+(-2)×3=0,则x=+3价;
(2)图2中原子的核内质子数为17,为氯元素,硅的原子序数为14,则表示如图1中④的原子结构示意图;最外层电子数是7,在化学反应中易得到1个电子而形成带1个单位负电荷的氯离子,形成的离子符号为Cl-。
16. 纯净物 42 9:4 H/氢元素 ③
【详解】(1)由青蒿素的【分子式为C15H22O5】可见它属于纯净物,故填纯净物
(2)元素符号右下角的数字表示该分子中原子的个数,可知青蒿素的每一个分子中含有15+22+5=42故填42
(3)青蒿素中碳氧元素的质量比为:碳原子的个数乘以碳原子的相对原子质量与氧原子的个数乘以氧原子的相对原子质量之比即(12×15):(16×5)=9:4故填9:4
(4)青蒿素中各种元素的质量分数为该元素的质量与青蒿素的相对分子质量之比故碳元素的质量分数为:氢元素的质量分数为:氧元素的质量分数为:故元素质量分数最小的元素为氢元素。
(5)由题中可知③不正确,化学是一把双刃剑合理利用化学可以为人类造福,故填③
17. 7 C S2- MgBr2
【详解】(1)在元素周期表中,元素名称左上角的数字表示原子序数,原子序数=质子数=m=35,在原子中,质子数=核外电子数,35=2+8+18+n,n=7;
(2)C与溴原子的最外层电子数相同,均是7,化学性质相似;
(3)质子数=原子序数,16号元素是硫元素,故B为硫原子,硫原子的最外层电子数为6,大于4,在化学反应中,容易得到2个电子,从而带上2个单位的负电荷,形成硫离子,表示为:S2-;
(4)A原子质子数为12,所以为镁原子,镁原子最外层电子数为2,在化学反应中,容易失去2个电子形成镁离子,显+2价,溴原子最外层电子数为7,在化学反应中,容易得到1个电子形成溴离子,显-1价,所以二者形成的化学式为:MgBr2。
18. 浓氨水 挥发性 形成白雾是物理变化,是挥发出的氯化氢分子溶于水蒸气形成的;形成白烟是化学变化,参加反应的氯化氢分子与氨气分子发生改变,重新组成了新的固态物质氯化铵
【详解】(1)已知气体的相对分子质量越小,扩散速度越快,氨气的相对分子质量小于氯化氢,由此判断物质甲是浓氨水;
(2)该实验利用了甲、乙的共同物理性质是挥发性;氨气与氯化氢反应生成氯化铵固体,白色烟环的化学式是;
(3)这两种变化的本质区别是形成白雾是物理变化,是挥发出的氯化氢分子溶于水蒸气形成的;形成白烟是化学变化,参加反应的氯化氢分子与氨气分子发生改变,重新组成了新的固态物质氯化铵。
19.(1)342
(2)1.1g
17.1g蔗糖中含氢元素的质量为17.1g××100%=1.1g;
答:17.1g蔗糖中含氢元素的质量为1.1g。
【解析】(1)
蔗糖的相对分子质量为12×12+1×22+16×11=342,故填:342;
(2)
见答案。
20.(1)12:1:6
(2)19
(3)152
(4)
(5)
(6)2×10×10-3kg×970mg/kg=19.4mg
【分析】(1)
香兰素中碳、氢、氧元素的质量比为:(12×8):8:(16×3)=12:1:6;
(2)
由化学式可知,每个香兰素分子中含有8个碳原子、8个氢原子、3个氧原子,共19个原子;
(3)
香兰素的相对分子质量是:12×8+8+16×3=152;
(4)
见答案;
(5)
见答案;
(6)
见答案。
21.(1)6:1
(2) +1 -1 1:3
(3) 90 40% 由于乳酸碳元素的质量分数为40%,故含有7.2g碳元素的乳酸质量为
【详解】(1)已知聚丙烯的化学式为,聚丙烯中碳、氢元素的质量比为。
(2)①、次氯酸钠中钠,元素化合价是+1,氧元素化合价是-2,根据化合物中元素化合价代数和为零可知,氯元素的化合价是+1;
②、氯化钠中,钠元素化合价是+1,根据化合物中元素化合价代数和为零可知,氯元素的化合价是-1;
③、酒精的学名是乙醇,化学式是,乙醇分子中共含有3种原子,一个酒精分子中含有2个碳原子,6个氢原子,故酒精分子中碳、氢两种原子的个数比为2:6=1:3。
(3)①、乳酸的化学式量为;
②、乳酸中碳元素的质量分数为;
③、由于乳酸碳元素的质量分数为40%,故含有7.2g碳元素的乳酸质量为。
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
