化学苏教版(2019)必修第一册 3.1.3氧化还原反应课件(20张)
文档属性
| 名称 | 化学苏教版(2019)必修第一册 3.1.3氧化还原反应课件(20张) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-19 00:00:00 | ||
图片预览






文档简介
(共20张PPT)
3.1.3 氧化还原反应
火箭产生的巨大推力来自
氧化还原反应
常见的氧化还原反应
金属腐蚀
节日焰火
生活、生产中常用的各种电池利用氧化还原反应
维C是一种抗氧化剂,其过程中发生的是氧化还原反应
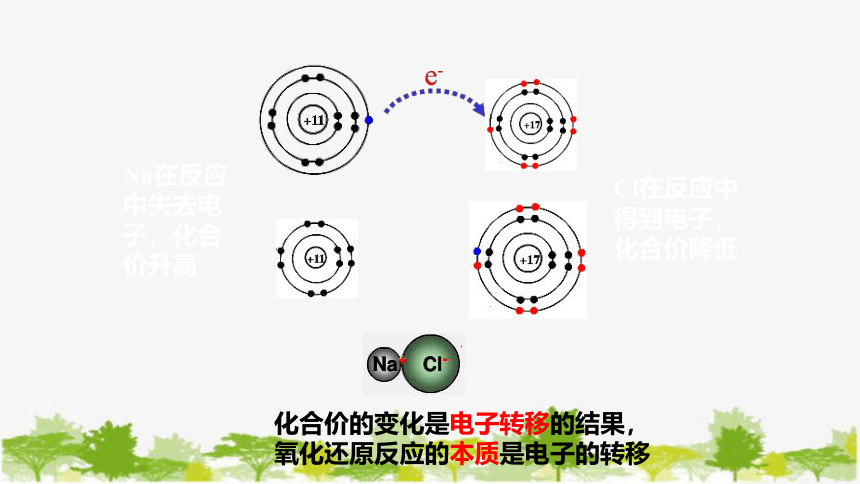
思考:钠和氯气反应生成氯化钠。请从元素的化合价是否发生变化的角度,对氯气和金属钠的化学反应进行分类,它属于何种反应类型?反应中化合价发生变化的原因是什么?
Cl在反应中得到电子,化合价降低
Na在反应中失去电子,化合价升高
化合价的变化是电子转移的结果,
氧化还原反应的本质是电子的转移
一、氧化还原反应的概念
1、定义:有电子转移的反应即氧化还原反应
没有电子转移的反应即非氧化还原反应
2、特点:元素化合价发生升降变化
3、实质:电子转移
4、氧化剂:得到电子的物质。
化合价降低,被还原,得到还原产物。
还原剂:失去电子的物质。
化合价升高,被氧化,得到氧化产物。
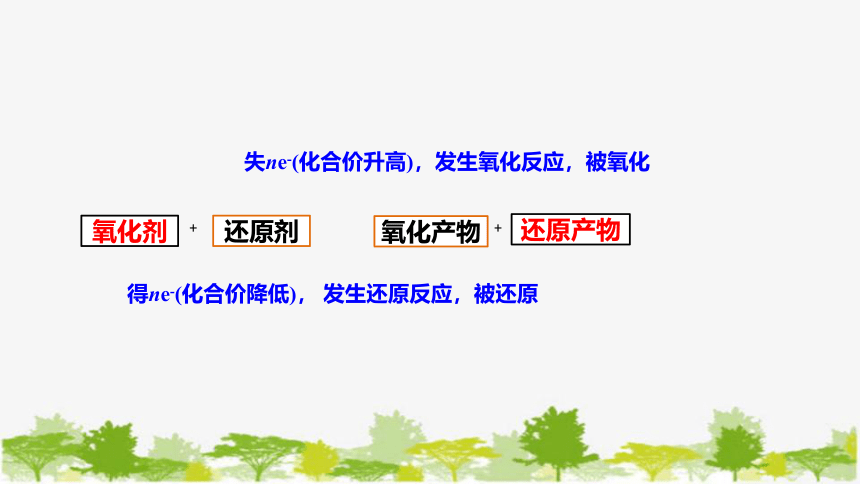
得ne-(化合价降低), 发生还原反应,被还原
失ne-(化合价升高),发生氧化反应,被氧化
氧化剂
还原剂
还原产物
氧化产物
+
+
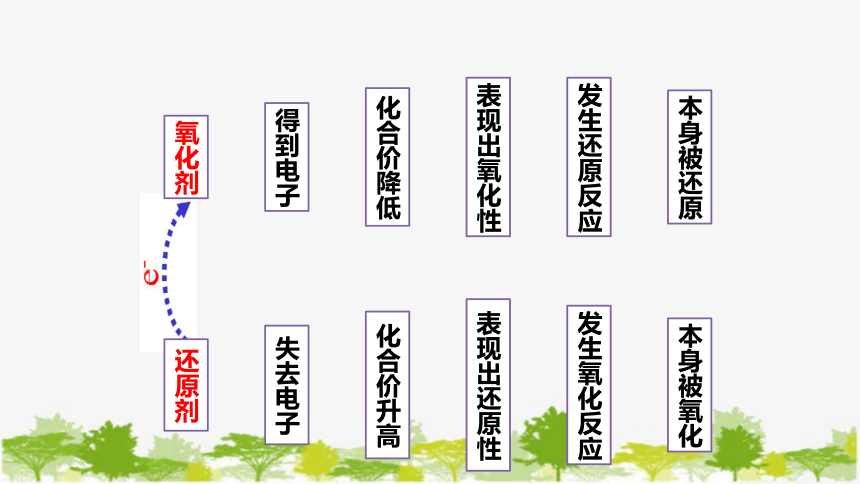
还原剂
失去电子
化合价升高
表现出还原性
发生氧化反应
本身被氧化
氧化剂
得到电子
化合价降低
表现出氧化性
发生还原反应
本身被还原
1.下列反应属于氧化还原反应的是( )
A.CuO+2HCl====CuCl2 +H2O
B.CaCO3+2HCl====2NaCl+CO2↑+H2O
C.2KMnO4====K2MnO4+MnO2+O2 ↑
D.Ca(OH)2+CO2====CaCO3↓ + H2O
C
2、下列叙述正确的是( )
A、在氧化还原反应中,失去电子的物质,所含元素化合价降低
B、凡是有元素化合价升降的化学反应都是氧化还原反应
C、在氧化还原反应中一定所有的元素化合价都发生变化
D、氧化还原反应的本质是电子的转移(得失或偏移)
B D
课堂练习
思考:钠原子与氯原子之间发生了电子转移,导致钠元素与氯元素的化合价发生了改变。那么怎样表示该化学反应中电子转移情况呢?
1、双线桥法:表示反应前后同一元素由反应物转化为生成物时电子转移的情况。
二、氧化还原反应中电子转移的表示方法
2Na+Cl2 == 2NaCl
失去2×e-,被氧化,做还原剂
得到2×e-,被还原,做氧化剂
书写步骤:
(1)标价态:正确标出反应前后各元素的化合价,明确变价元素 的化合价升降关系
(2)双箭头:一条线始于被还原的物质中的降价元素,止于还原产物中的相应元素;一条线始于被氧化的物质中的升价元素,终止于氧化产物中的相应元素
(3)注得失:标出“失去”或“得到”电子的总数
注意事项:
1、箭头、箭尾必须对应化合价变化的同种元素的原子;
2、必须注明“得到”或“失去”;
3、被还原的物质和被氧化的物质得、失电子数守恒。
学以致用:
高锰酸钾与浓盐酸在一定条件下可以反应生成氯气。2KMn04+16HCl(浓)==2KC1+2MnCl2+5Cl2↑+8H2O该反应是氧化还原反应吗?如果是,指出反应中化合价发生变化的元素,分析电子转移的方向和数目,并指出氧化剂和还原剂。如果不是,请给出理由。
2、单线桥法:表示反应过程中不同元素原子间的电子转移情况。
2Na + Cl2 == 2NaCl
2e-
还原剂
氧化剂
既是氧化产物,又是还原产物
书写步骤:
(1)标价态:正确标出反应前后各元素的化合价;明确变价元素的化合价升降关系
(2)单线桥:始于被氧化物质中化合价升高的元素,止于被还原物质中化合价降低的元素
(3)标数目:标出转移电子的总数
注意事项:
1、不需要标明“得到”或“失去”,只标明电子转移数目;
2、要用箭头标明电子转移的方向;
3、箭头由反应物中失电子元素原子指向得电子元素原子。
2KMn04+16HCl(浓)==2KC1+2MnCl2+5Cl2↑+8H2O
2KMn04+16HCl(浓)==2KC1+2MnCl2+5Cl2↑+8H2O
失去10e-,被氧化,做还原剂
得到10e-,被还原,做氧化剂
练习
10e-
思考:化学反应中遵循哪些守恒?
1、质量守恒:参加化学反应的各物质的总质量等于反应后生成的各物质的总质量。
2、化合价升降守恒:反应前后元素化合价升、降的总数相等。
3、电子守恒:反应中氧化剂得电子的数目等于还原剂失电子的数目。
课堂小结
概念
氧化还原反应
电子转移表示方式
三个守恒
双线桥法
单线桥法
氧化还原反应与非氧化还原反应
氧化还原反应的基本形式
相关概念
质量守恒
化合介升降守恒
电子转移守恒
当堂巩固
练习:火药是中国的“四大发明”之一,黑火药在发生爆炸时,发生如下的反应:
2KNO3+C+S=K2S+2NO2↑+CO2↑
(1)用双线桥法表示电子转移。
(2)反应中被还原的元素是 ,被氧化的元素是 ,
氧化剂是 ,还原剂是 ,
氧化产物是 ,还原产物是 。
N、S
C
KNO3、S
C
CO2
K2S、NO2
失4e-
得 2e-
得 2e-
3.1.3 氧化还原反应
火箭产生的巨大推力来自
氧化还原反应
常见的氧化还原反应
金属腐蚀
节日焰火
生活、生产中常用的各种电池利用氧化还原反应
维C是一种抗氧化剂,其过程中发生的是氧化还原反应
思考:钠和氯气反应生成氯化钠。请从元素的化合价是否发生变化的角度,对氯气和金属钠的化学反应进行分类,它属于何种反应类型?反应中化合价发生变化的原因是什么?
Cl在反应中得到电子,化合价降低
Na在反应中失去电子,化合价升高
化合价的变化是电子转移的结果,
氧化还原反应的本质是电子的转移
一、氧化还原反应的概念
1、定义:有电子转移的反应即氧化还原反应
没有电子转移的反应即非氧化还原反应
2、特点:元素化合价发生升降变化
3、实质:电子转移
4、氧化剂:得到电子的物质。
化合价降低,被还原,得到还原产物。
还原剂:失去电子的物质。
化合价升高,被氧化,得到氧化产物。
得ne-(化合价降低), 发生还原反应,被还原
失ne-(化合价升高),发生氧化反应,被氧化
氧化剂
还原剂
还原产物
氧化产物
+
+
还原剂
失去电子
化合价升高
表现出还原性
发生氧化反应
本身被氧化
氧化剂
得到电子
化合价降低
表现出氧化性
发生还原反应
本身被还原
1.下列反应属于氧化还原反应的是( )
A.CuO+2HCl====CuCl2 +H2O
B.CaCO3+2HCl====2NaCl+CO2↑+H2O
C.2KMnO4====K2MnO4+MnO2+O2 ↑
D.Ca(OH)2+CO2====CaCO3↓ + H2O
C
2、下列叙述正确的是( )
A、在氧化还原反应中,失去电子的物质,所含元素化合价降低
B、凡是有元素化合价升降的化学反应都是氧化还原反应
C、在氧化还原反应中一定所有的元素化合价都发生变化
D、氧化还原反应的本质是电子的转移(得失或偏移)
B D
课堂练习
思考:钠原子与氯原子之间发生了电子转移,导致钠元素与氯元素的化合价发生了改变。那么怎样表示该化学反应中电子转移情况呢?
1、双线桥法:表示反应前后同一元素由反应物转化为生成物时电子转移的情况。
二、氧化还原反应中电子转移的表示方法
2Na+Cl2 == 2NaCl
失去2×e-,被氧化,做还原剂
得到2×e-,被还原,做氧化剂
书写步骤:
(1)标价态:正确标出反应前后各元素的化合价,明确变价元素 的化合价升降关系
(2)双箭头:一条线始于被还原的物质中的降价元素,止于还原产物中的相应元素;一条线始于被氧化的物质中的升价元素,终止于氧化产物中的相应元素
(3)注得失:标出“失去”或“得到”电子的总数
注意事项:
1、箭头、箭尾必须对应化合价变化的同种元素的原子;
2、必须注明“得到”或“失去”;
3、被还原的物质和被氧化的物质得、失电子数守恒。
学以致用:
高锰酸钾与浓盐酸在一定条件下可以反应生成氯气。2KMn04+16HCl(浓)==2KC1+2MnCl2+5Cl2↑+8H2O该反应是氧化还原反应吗?如果是,指出反应中化合价发生变化的元素,分析电子转移的方向和数目,并指出氧化剂和还原剂。如果不是,请给出理由。
2、单线桥法:表示反应过程中不同元素原子间的电子转移情况。
2Na + Cl2 == 2NaCl
2e-
还原剂
氧化剂
既是氧化产物,又是还原产物
书写步骤:
(1)标价态:正确标出反应前后各元素的化合价;明确变价元素的化合价升降关系
(2)单线桥:始于被氧化物质中化合价升高的元素,止于被还原物质中化合价降低的元素
(3)标数目:标出转移电子的总数
注意事项:
1、不需要标明“得到”或“失去”,只标明电子转移数目;
2、要用箭头标明电子转移的方向;
3、箭头由反应物中失电子元素原子指向得电子元素原子。
2KMn04+16HCl(浓)==2KC1+2MnCl2+5Cl2↑+8H2O
2KMn04+16HCl(浓)==2KC1+2MnCl2+5Cl2↑+8H2O
失去10e-,被氧化,做还原剂
得到10e-,被还原,做氧化剂
练习
10e-
思考:化学反应中遵循哪些守恒?
1、质量守恒:参加化学反应的各物质的总质量等于反应后生成的各物质的总质量。
2、化合价升降守恒:反应前后元素化合价升、降的总数相等。
3、电子守恒:反应中氧化剂得电子的数目等于还原剂失电子的数目。
课堂小结
概念
氧化还原反应
电子转移表示方式
三个守恒
双线桥法
单线桥法
氧化还原反应与非氧化还原反应
氧化还原反应的基本形式
相关概念
质量守恒
化合介升降守恒
电子转移守恒
当堂巩固
练习:火药是中国的“四大发明”之一,黑火药在发生爆炸时,发生如下的反应:
2KNO3+C+S=K2S+2NO2↑+CO2↑
(1)用双线桥法表示电子转移。
(2)反应中被还原的元素是 ,被氧化的元素是 ,
氧化剂是 ,还原剂是 ,
氧化产物是 ,还原产物是 。
N、S
C
KNO3、S
C
CO2
K2S、NO2
失4e-
得 2e-
得 2e-
