第十单元 课题1 常见的酸和碱 课时1 什么是酸和碱 酸碱指示剂 常见的酸课件(共39张PPT)
文档属性
| 名称 | 第十单元 课题1 常见的酸和碱 课时1 什么是酸和碱 酸碱指示剂 常见的酸课件(共39张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 619.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-18 00:00:00 | ||
图片预览









文档简介
(共39张PPT)
第十单元 酸 和 碱
课题1 常见的酸和碱
课时1 什么是酸和碱 酸碱指示剂 常见的酸
目录
01
课程要求
02
03
04
知识点精讲
课堂检测
课前预习
1. 能依据物质的类别列举一些常见的酸和碱。
2. 能以盐酸、硫酸为例,通过实验探究认识酸的主要性质和用途。
3. 为会使用酸碱指示剂。
2. 在“分子运动”实验中,无色酚酞溶液遇氨水变 红 色。
红
紫
H2O+CO2↑
红
1. 酸是由 H+ 和 酸根离子 构成的。
(名称:一般读“某酸”)
常见 的酸 盐酸(HCl) 硫酸 (H2SO4) 硝酸(HNO3) 醋酸
(CH3COOH)
构成 H+和Cl- H+和
CH3COO-
H+
酸根离子
知识点1 什么是酸和碱
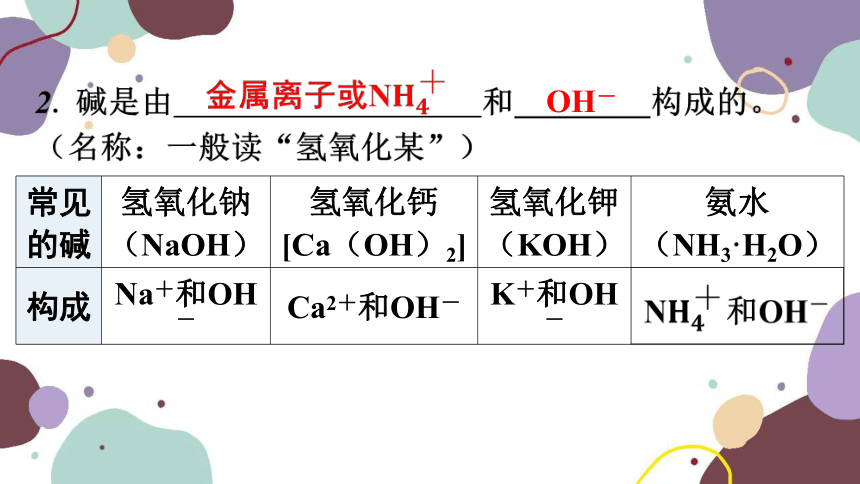
常见 的碱 氢氧化钠(NaOH) 氢氧化钙 [Ca(OH)2] 氢氧化钾 (KOH) 氨水
(NH3·H2O)
构成 Na+和OH- Ca2+和OH- K+和OH-
OH-
课堂练习
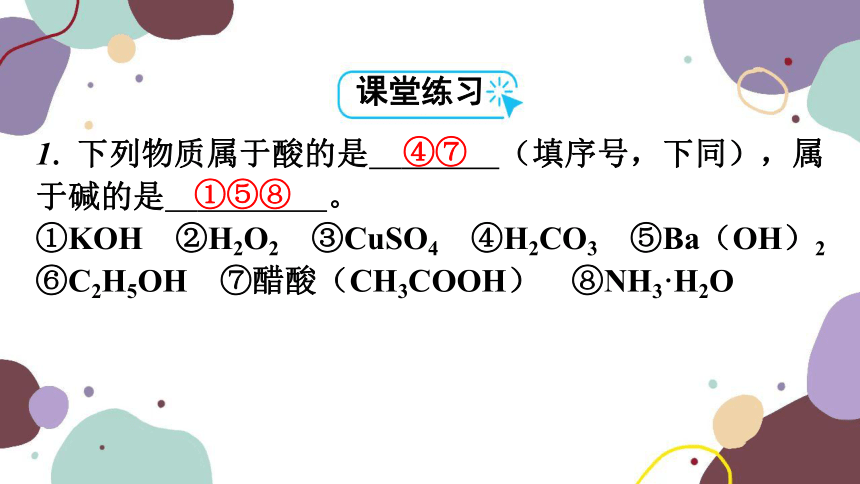
1. 下列物质属于酸的是 ④⑦ (填序号,下同),属于碱的是 ①⑤⑧ 。
①KOH ②H2O2 ③CuSO4 ④H2CO3 ⑤Ba(OH)2 ⑥C2H5OH ⑦醋酸(CH3COOH) ⑧NH3·H2O
④⑦
①⑤⑧
2. 下列关于酸和碱的说法错误的是( D )
A. 酸和碱中都含有氢元素
B. 碱中有都含有氢、氧元素
C. 酸中不一定含有氧元素
D. 碱中一定含有金属元素
D
知识点2 常见的酸碱指示剂及变色规律
3. 完成课本P50“实验10-1”,将下列物质加入紫色石蕊溶液或无色酚酞溶液反应后的颜色变化填入表中。
物 质 白醋 苹果汁 石灰水 氢氧化钠溶液
加入紫色石蕊溶液 变红色 变红色 变蓝色 变蓝色
变红色
变红色
变蓝色
变蓝色
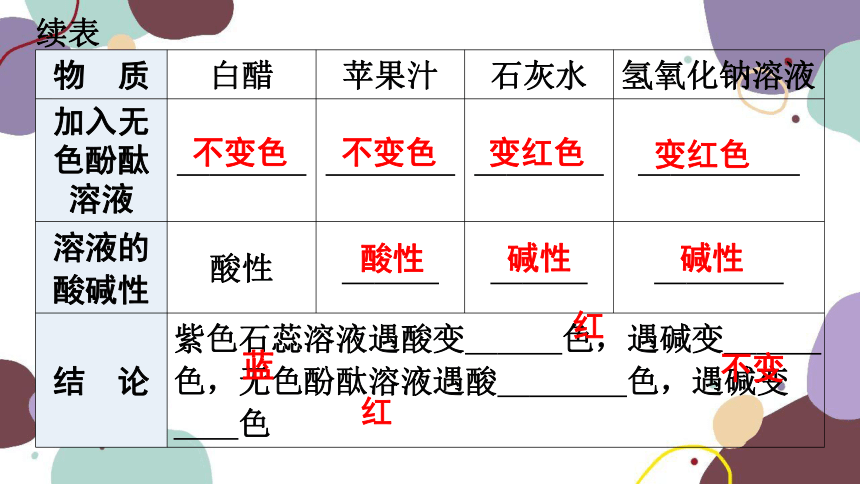
物 质 白醋 苹果汁 石灰水 氢氧化钠溶液
加入无色酚酞溶液 不变色 不变色 变红色 变红色
溶液的酸碱性 酸性 酸性 碱性 碱性
结 论 紫色石蕊溶液遇酸变 红 色,遇碱变 蓝 色,无色酚酞溶液遇酸 不变 色,遇碱变 红 色
酸性
碱性
碱性
红
蓝
不变
红
不变色
不变色
变红色
变红色
续表
【点拨】(1)变色的是酸碱指示剂,不是被测物质,指示剂变色过程属于 化学 变化。
化学
(3)水、氯化钠溶液为中性溶液,紫色石蕊溶液和无色酚酞溶液遇中性溶液均不变色(紫色石蕊溶液的显色口诀:酸红碱蓝中不变;无色酚酞溶液的显色口诀:酸无碱红中不变)。
(2)只有能溶于水的酸或碱才能使指示剂变色,氢氧化铝[Al(OH)3]、氢氧化镁[Mg(OH)2]等不溶性碱不能使指示剂变色。
课堂练习
3. 把氯化氢、氢氧化钠、食盐分别溶于水,往所得溶液中分别滴加紫色石蕊溶液,溶液呈现的颜色依次为( C )
A. 红、蓝、无 B. 蓝、红、无
C. 红、蓝、紫 D. 蓝、红、紫
C
思路点拨 紫色石蕊溶液遇酸性、中性、碱性溶液分别显示红色、紫色、蓝色。无色酚酞溶液遇酸性、中性、碱性溶液分别显示无色、无色、红色。相反地,可以根据这个规律判断溶液的酸碱性。
知识点3 浓盐酸和浓硫酸的性质及用途
4. 完成课本P52“实验10-2”,填写下表。
酸 盐酸 硫酸
溶质化学式 HCl H2SO4
颜色、状态、气味 无 色、有 刺激性 气味的 液 体 无 色无味的黏稠的 油状液体
HCl
H2SO4
无
刺
激性
液
无
油状液体
酸 盐酸 硫酸
打开试剂瓶后的现象 有 白雾 生成,说明浓盐酸具有 挥发 性(物理性质) 无明显现象
密 度 常用浓盐酸(37%~38%)1.19 g/cm3 常用浓硫酸(98%)
1.84 g/cm3
白雾
挥发
续表
酸 盐酸 硫酸
用 途 ①金属 除锈 、制造药物等; ②人体 胃液 中含有盐酸,可帮助消化 ①用于化肥、农药、火药、染料以及冶炼金属、精炼石油和金属除锈等;
②浓硫酸有 吸水 性(物理性质),在实验室常用它做 干燥剂
除锈
胃液
吸水
干燥剂
续表
注意:①浓盐酸挥发出的 氯化氢气体 遇到空气中的水蒸气形成盐酸小液滴;
②浓硫酸可干燥CO2、SO2、SO3、HCl等酸性气体和O2、H2、CO、N2、CH4等中性气体,但不能干燥NH3等碱性气体,常放入洗气瓶中使用;
③将分别盛放浓盐酸和浓硫酸的试剂瓶敞口放置一段时间,溶质、溶剂、溶液的变化情况如下表:
氯化氢气体
酸 性 质 溶质的质量 溶剂的质量 溶液的质量 溶质的质量分数
浓盐酸 挥发 减小 不变 减小 变小
浓硫酸 吸性 不变 增大 增大 变小
以上变化都属于 物理变化 ,浓盐酸、浓硫酸都需要 密封保存 。
挥发性
减小
不变
减小
变小
吸水性
不变
增大
增大
变小
物理变化
密封保存
课堂练习
4. 将浓盐酸、浓硫酸敞口放置一段时间,它们共同的变化是( D )
A. 颜色发生改变 B. 发生化学变化
C. 质量增大 D. 溶质的质量分数变小
D
思路点拨 (1)浓盐酸具有挥发性,挥发出的是HCl气体;浓硫酸具有吸水性,可吸收空气中的水蒸气。
(2)浓盐酸和浓硫酸敞口放置于空气中溶质质量分数都变小,但前者是因为溶质的质量减小,后者是因为溶剂的质量增加。
知识点4 浓硫酸的腐蚀性及稀释
5. 观察课本P53“实验10-3”,填写下表。
实验操作 放置一会儿 后的现象 实验结论
用玻璃棒蘸浓硫酸在纸上写字 字迹 变黑 浓硫酸有强烈的 腐蚀
性(脱水性)
变黑
腐蚀
实验操作 放置一会儿 后的现象 实验结论
用小木棍蘸少量浓硫酸 蘸浓硫酸的小木棍 变黑 浓硫酸有强烈的 腐蚀
性(脱水性)
将浓硫酸滴到一小块布上 滴浓硫酸的布 变黑甚至成
变黑
腐蚀
变黑甚至成洞
续表
【归纳】浓硫酸能夺取纸张、木材、布料、皮肤里的 水分 (脱水性),生成黑色的 炭 ,该过程属于 化学 (填“物理”或“化学”)变化。
水分
炭
化学
实验图示 操作步骤 现 象 实验结论
①将 浓硫酸 沿着器壁 缓慢 注入盛有水的烧杯中,并用 玻璃棒 (作用: 帮助散热 )不断搅拌;②用手触摸烧杯外壁 烧杯外壁 发 浓硫酸溶于水
放出大量
浓硫酸
缓慢
玻璃棒
帮助散热
发
热
放出大
量热
6. 观察课本P53“实验10-4”,填写下表。
注意:①稀释浓硫酸时,一定要把浓硫酸沿容器壁慢慢注入水里,并不断搅拌。切不可将水注入浓硫酸。如果将水注入浓硫酸中,由于 水的密度较小 ,会浮在浓硫酸上面,溶解时放出的 热 能使水立刻 沸腾 ,使浓硫酸液滴 向四周飞溅 ,这是非常危险的!(正确操作:酸入水,沿器壁,缓慢倒,不断搅)
水的密度较小
热
沸腾
向四周飞溅
②如果不慎将浓硫酸沾到皮肤或衣服上,应立即用大量 水 冲洗,然后再涂上 3%~5%的NaHCO3 溶液。
③如果不慎将稀硫酸沾到衣服上没有及时清洗,时间长了,水分不断蒸发,使稀硫酸逐渐变成浓硫酸,浓硫酸有腐蚀性,衣服上会出现小孔。
水
3%~5%的NaHCO3
课堂练习
5. 如图10-1-1是稀释浓硫酸实验的示意图。
图10-1-1
(1)b容器所盛的试剂是 浓硫酸 (填“水”或“浓硫酸”)。
浓硫酸
(2)稀释时,若两种试剂添加顺序颠倒,将会发生 液体飞溅 。
(3)【联系与拓展】据媒体报道,有一村民在家里误将装在酒瓶中的硫酸当成白酒喝下,造成食道和胃严重损伤,这是因为硫酸具有 腐蚀性 。这一事件警示我们,家中存放或使用药物时应注意 存放时要贴好标签,放在安全的地方 。
液体飞溅
腐蚀性
存放时要贴好标
签,放在安全的地方
思路点拨 浓硫酸的腐蚀性(脱水性):把有机物中的氢、氧元素按水的组成脱去,从而使有机物炭化,属于化学性质;浓硫酸的吸水性:把物质中的水分吸收,使物质变得干燥,属于物理性质,常用于干燥气体。
1. (创新实验)按图10-1-2所示的装置,玻璃棒末端固定一团喷有酚酞溶液的脱脂棉Y。先向集气瓶中加入物质X,再塞上带玻璃棒的橡胶塞。片刻后,能观察到喷有酚酞溶液的脱脂棉Y变红,则物质X可能是 ( B )
B
图10-1-2
A. 浓盐酸 B. 浓氨水
C. 浓醋酸 D. 浓氢氧化钠溶液
2. 在生产、运输、使用和贮存化学药品时,应注意安全。浓硫酸运输车须张贴的标志是( B )
B
3. 盐酸是一种主要的工业用酸,下列关于盐酸的叙述中,错误的是( D )
A. 盐酸是氯化氢的水溶液
B. 浓盐酸具有挥发性,在空气中会形成白雾
C. 人的胃液里含少量的盐酸,可以助消化
D. 浓盐酸敞口放置后溶质的质量分数变大
D
4. 如图10-1-3所示的装置可用来洗气。向其中装入足量浓硫酸,将氧气和水蒸气的混合气体由 a 端进, b 端出,出来的气体就只有 氧气 。这说明浓硫酸具有 吸水 性,这属于 物理 (填“物理”或“化学”)性质。
a
b
氧气
吸水
物理
图10-1-3
5. 许多植物中含有色素,现提取几种植物汁液,用稀酸、稀碱和蒸馏水逐一检验,
现象如下表。
植 物 溶液颜色
酸溶液 蒸馏水 碱溶液
牵牛花 红色 紫色 蓝色
万寿菊 黄色 黄色 黄色
胡萝卜 橙色 橙色 橙色
玫瑰 浅红色 浅红色 绿色
(1)上述植物的汁液不能用来区别稀硫酸和氢氧化钠溶液的是 万寿菊 、 胡萝卜 。
(2)用碱溶液浸泡一朵纸花后晾干,用所提取的玫瑰的汁液均匀地涂在纸花上,纸花变成 绿 色。
(3)四种植物中与紫色石蕊溶液的变色规律相似的是 牵牛花 。
万寿菊
胡萝卜
绿
牵牛花
6. 如图10-1-4是某科学小组所做的浓硫酸与水混合的两个实验装置。在两个相对密封的试管中各连着一个气球,实验一的试管壁上用蜡粘着一张小纸片,实验二的漏斗内的水中加有少量的红色有机染料。
图10-1-4
(1)在常规实验操作中,实验 一 (填“一”或“二”)的操作是正确的。
(2)当打开实验一中漏斗的活塞后,浓硫酸顺着试管壁缓缓流下。一段时间后发现,粘在试管上的小纸片会 掉落 ,其原因是 浓硫酸与水混合过程中放出热量,使蜡熔化 。
一
掉落
浓硫酸与水混合过程中放出热
量,使蜡熔化
(3)当打开实验二中漏斗的活塞后,加有红色有机染料的水顺着试管壁缓缓流下,并集中在浓硫酸的上层。一段时间后发现,液滴飞溅,红色液体逐渐变为黑色,这是因为浓硫酸使有机染料发生了炭化,说明浓硫酸具有 脱水 性。
脱水
谢 谢!
第十单元 酸 和 碱
课题1 常见的酸和碱
课时1 什么是酸和碱 酸碱指示剂 常见的酸
目录
01
课程要求
02
03
04
知识点精讲
课堂检测
课前预习
1. 能依据物质的类别列举一些常见的酸和碱。
2. 能以盐酸、硫酸为例,通过实验探究认识酸的主要性质和用途。
3. 为会使用酸碱指示剂。
2. 在“分子运动”实验中,无色酚酞溶液遇氨水变 红 色。
红
紫
H2O+CO2↑
红
1. 酸是由 H+ 和 酸根离子 构成的。
(名称:一般读“某酸”)
常见 的酸 盐酸(HCl) 硫酸 (H2SO4) 硝酸(HNO3) 醋酸
(CH3COOH)
构成 H+和Cl- H+和
CH3COO-
H+
酸根离子
知识点1 什么是酸和碱
常见 的碱 氢氧化钠(NaOH) 氢氧化钙 [Ca(OH)2] 氢氧化钾 (KOH) 氨水
(NH3·H2O)
构成 Na+和OH- Ca2+和OH- K+和OH-
OH-
课堂练习
1. 下列物质属于酸的是 ④⑦ (填序号,下同),属于碱的是 ①⑤⑧ 。
①KOH ②H2O2 ③CuSO4 ④H2CO3 ⑤Ba(OH)2 ⑥C2H5OH ⑦醋酸(CH3COOH) ⑧NH3·H2O
④⑦
①⑤⑧
2. 下列关于酸和碱的说法错误的是( D )
A. 酸和碱中都含有氢元素
B. 碱中有都含有氢、氧元素
C. 酸中不一定含有氧元素
D. 碱中一定含有金属元素
D
知识点2 常见的酸碱指示剂及变色规律
3. 完成课本P50“实验10-1”,将下列物质加入紫色石蕊溶液或无色酚酞溶液反应后的颜色变化填入表中。
物 质 白醋 苹果汁 石灰水 氢氧化钠溶液
加入紫色石蕊溶液 变红色 变红色 变蓝色 变蓝色
变红色
变红色
变蓝色
变蓝色
物 质 白醋 苹果汁 石灰水 氢氧化钠溶液
加入无色酚酞溶液 不变色 不变色 变红色 变红色
溶液的酸碱性 酸性 酸性 碱性 碱性
结 论 紫色石蕊溶液遇酸变 红 色,遇碱变 蓝 色,无色酚酞溶液遇酸 不变 色,遇碱变 红 色
酸性
碱性
碱性
红
蓝
不变
红
不变色
不变色
变红色
变红色
续表
【点拨】(1)变色的是酸碱指示剂,不是被测物质,指示剂变色过程属于 化学 变化。
化学
(3)水、氯化钠溶液为中性溶液,紫色石蕊溶液和无色酚酞溶液遇中性溶液均不变色(紫色石蕊溶液的显色口诀:酸红碱蓝中不变;无色酚酞溶液的显色口诀:酸无碱红中不变)。
(2)只有能溶于水的酸或碱才能使指示剂变色,氢氧化铝[Al(OH)3]、氢氧化镁[Mg(OH)2]等不溶性碱不能使指示剂变色。
课堂练习
3. 把氯化氢、氢氧化钠、食盐分别溶于水,往所得溶液中分别滴加紫色石蕊溶液,溶液呈现的颜色依次为( C )
A. 红、蓝、无 B. 蓝、红、无
C. 红、蓝、紫 D. 蓝、红、紫
C
思路点拨 紫色石蕊溶液遇酸性、中性、碱性溶液分别显示红色、紫色、蓝色。无色酚酞溶液遇酸性、中性、碱性溶液分别显示无色、无色、红色。相反地,可以根据这个规律判断溶液的酸碱性。
知识点3 浓盐酸和浓硫酸的性质及用途
4. 完成课本P52“实验10-2”,填写下表。
酸 盐酸 硫酸
溶质化学式 HCl H2SO4
颜色、状态、气味 无 色、有 刺激性 气味的 液 体 无 色无味的黏稠的 油状液体
HCl
H2SO4
无
刺
激性
液
无
油状液体
酸 盐酸 硫酸
打开试剂瓶后的现象 有 白雾 生成,说明浓盐酸具有 挥发 性(物理性质) 无明显现象
密 度 常用浓盐酸(37%~38%)1.19 g/cm3 常用浓硫酸(98%)
1.84 g/cm3
白雾
挥发
续表
酸 盐酸 硫酸
用 途 ①金属 除锈 、制造药物等; ②人体 胃液 中含有盐酸,可帮助消化 ①用于化肥、农药、火药、染料以及冶炼金属、精炼石油和金属除锈等;
②浓硫酸有 吸水 性(物理性质),在实验室常用它做 干燥剂
除锈
胃液
吸水
干燥剂
续表
注意:①浓盐酸挥发出的 氯化氢气体 遇到空气中的水蒸气形成盐酸小液滴;
②浓硫酸可干燥CO2、SO2、SO3、HCl等酸性气体和O2、H2、CO、N2、CH4等中性气体,但不能干燥NH3等碱性气体,常放入洗气瓶中使用;
③将分别盛放浓盐酸和浓硫酸的试剂瓶敞口放置一段时间,溶质、溶剂、溶液的变化情况如下表:
氯化氢气体
酸 性 质 溶质的质量 溶剂的质量 溶液的质量 溶质的质量分数
浓盐酸 挥发 减小 不变 减小 变小
浓硫酸 吸性 不变 增大 增大 变小
以上变化都属于 物理变化 ,浓盐酸、浓硫酸都需要 密封保存 。
挥发性
减小
不变
减小
变小
吸水性
不变
增大
增大
变小
物理变化
密封保存
课堂练习
4. 将浓盐酸、浓硫酸敞口放置一段时间,它们共同的变化是( D )
A. 颜色发生改变 B. 发生化学变化
C. 质量增大 D. 溶质的质量分数变小
D
思路点拨 (1)浓盐酸具有挥发性,挥发出的是HCl气体;浓硫酸具有吸水性,可吸收空气中的水蒸气。
(2)浓盐酸和浓硫酸敞口放置于空气中溶质质量分数都变小,但前者是因为溶质的质量减小,后者是因为溶剂的质量增加。
知识点4 浓硫酸的腐蚀性及稀释
5. 观察课本P53“实验10-3”,填写下表。
实验操作 放置一会儿 后的现象 实验结论
用玻璃棒蘸浓硫酸在纸上写字 字迹 变黑 浓硫酸有强烈的 腐蚀
性(脱水性)
变黑
腐蚀
实验操作 放置一会儿 后的现象 实验结论
用小木棍蘸少量浓硫酸 蘸浓硫酸的小木棍 变黑 浓硫酸有强烈的 腐蚀
性(脱水性)
将浓硫酸滴到一小块布上 滴浓硫酸的布 变黑甚至成
变黑
腐蚀
变黑甚至成洞
续表
【归纳】浓硫酸能夺取纸张、木材、布料、皮肤里的 水分 (脱水性),生成黑色的 炭 ,该过程属于 化学 (填“物理”或“化学”)变化。
水分
炭
化学
实验图示 操作步骤 现 象 实验结论
①将 浓硫酸 沿着器壁 缓慢 注入盛有水的烧杯中,并用 玻璃棒 (作用: 帮助散热 )不断搅拌;②用手触摸烧杯外壁 烧杯外壁 发 浓硫酸溶于水
放出大量
浓硫酸
缓慢
玻璃棒
帮助散热
发
热
放出大
量热
6. 观察课本P53“实验10-4”,填写下表。
注意:①稀释浓硫酸时,一定要把浓硫酸沿容器壁慢慢注入水里,并不断搅拌。切不可将水注入浓硫酸。如果将水注入浓硫酸中,由于 水的密度较小 ,会浮在浓硫酸上面,溶解时放出的 热 能使水立刻 沸腾 ,使浓硫酸液滴 向四周飞溅 ,这是非常危险的!(正确操作:酸入水,沿器壁,缓慢倒,不断搅)
水的密度较小
热
沸腾
向四周飞溅
②如果不慎将浓硫酸沾到皮肤或衣服上,应立即用大量 水 冲洗,然后再涂上 3%~5%的NaHCO3 溶液。
③如果不慎将稀硫酸沾到衣服上没有及时清洗,时间长了,水分不断蒸发,使稀硫酸逐渐变成浓硫酸,浓硫酸有腐蚀性,衣服上会出现小孔。
水
3%~5%的NaHCO3
课堂练习
5. 如图10-1-1是稀释浓硫酸实验的示意图。
图10-1-1
(1)b容器所盛的试剂是 浓硫酸 (填“水”或“浓硫酸”)。
浓硫酸
(2)稀释时,若两种试剂添加顺序颠倒,将会发生 液体飞溅 。
(3)【联系与拓展】据媒体报道,有一村民在家里误将装在酒瓶中的硫酸当成白酒喝下,造成食道和胃严重损伤,这是因为硫酸具有 腐蚀性 。这一事件警示我们,家中存放或使用药物时应注意 存放时要贴好标签,放在安全的地方 。
液体飞溅
腐蚀性
存放时要贴好标
签,放在安全的地方
思路点拨 浓硫酸的腐蚀性(脱水性):把有机物中的氢、氧元素按水的组成脱去,从而使有机物炭化,属于化学性质;浓硫酸的吸水性:把物质中的水分吸收,使物质变得干燥,属于物理性质,常用于干燥气体。
1. (创新实验)按图10-1-2所示的装置,玻璃棒末端固定一团喷有酚酞溶液的脱脂棉Y。先向集气瓶中加入物质X,再塞上带玻璃棒的橡胶塞。片刻后,能观察到喷有酚酞溶液的脱脂棉Y变红,则物质X可能是 ( B )
B
图10-1-2
A. 浓盐酸 B. 浓氨水
C. 浓醋酸 D. 浓氢氧化钠溶液
2. 在生产、运输、使用和贮存化学药品时,应注意安全。浓硫酸运输车须张贴的标志是( B )
B
3. 盐酸是一种主要的工业用酸,下列关于盐酸的叙述中,错误的是( D )
A. 盐酸是氯化氢的水溶液
B. 浓盐酸具有挥发性,在空气中会形成白雾
C. 人的胃液里含少量的盐酸,可以助消化
D. 浓盐酸敞口放置后溶质的质量分数变大
D
4. 如图10-1-3所示的装置可用来洗气。向其中装入足量浓硫酸,将氧气和水蒸气的混合气体由 a 端进, b 端出,出来的气体就只有 氧气 。这说明浓硫酸具有 吸水 性,这属于 物理 (填“物理”或“化学”)性质。
a
b
氧气
吸水
物理
图10-1-3
5. 许多植物中含有色素,现提取几种植物汁液,用稀酸、稀碱和蒸馏水逐一检验,
现象如下表。
植 物 溶液颜色
酸溶液 蒸馏水 碱溶液
牵牛花 红色 紫色 蓝色
万寿菊 黄色 黄色 黄色
胡萝卜 橙色 橙色 橙色
玫瑰 浅红色 浅红色 绿色
(1)上述植物的汁液不能用来区别稀硫酸和氢氧化钠溶液的是 万寿菊 、 胡萝卜 。
(2)用碱溶液浸泡一朵纸花后晾干,用所提取的玫瑰的汁液均匀地涂在纸花上,纸花变成 绿 色。
(3)四种植物中与紫色石蕊溶液的变色规律相似的是 牵牛花 。
万寿菊
胡萝卜
绿
牵牛花
6. 如图10-1-4是某科学小组所做的浓硫酸与水混合的两个实验装置。在两个相对密封的试管中各连着一个气球,实验一的试管壁上用蜡粘着一张小纸片,实验二的漏斗内的水中加有少量的红色有机染料。
图10-1-4
(1)在常规实验操作中,实验 一 (填“一”或“二”)的操作是正确的。
(2)当打开实验一中漏斗的活塞后,浓硫酸顺着试管壁缓缓流下。一段时间后发现,粘在试管上的小纸片会 掉落 ,其原因是 浓硫酸与水混合过程中放出热量,使蜡熔化 。
一
掉落
浓硫酸与水混合过程中放出热
量,使蜡熔化
(3)当打开实验二中漏斗的活塞后,加有红色有机染料的水顺着试管壁缓缓流下,并集中在浓硫酸的上层。一段时间后发现,液滴飞溅,红色液体逐渐变为黑色,这是因为浓硫酸使有机染料发生了炭化,说明浓硫酸具有 脱水 性。
脱水
谢 谢!
同课章节目录
