2023-2024学年鲁科版高中化学必修二 3.2.2煤的干馏 苯 课件(共33张PPT)
文档属性
| 名称 | 2023-2024学年鲁科版高中化学必修二 3.2.2煤的干馏 苯 课件(共33张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-21 00:00:00 | ||
图片预览










文档简介
(共33张PPT)
煤的干馏 苯
第3章 第2节 第2课时
如何消除苯污染?
1、知道从煤中获得有机化工原料的主要方法,认识化石燃料综合利用的意义。
2、通过实验能够描述苯的物理性质,并能通过实验探究的方式分析苯的结构。
3、能根据苯的结构预测苯的化学性质,通过苯的性质的实验探究,与甲烷、乙烯对比归纳描述苯的性质。
宏观辨识
微观探析
证据推理
微观探析
科学精神
社会责任
二、煤的干馏 苯
(一) 煤的干馏
1、 煤的干馏
将煤隔绝空气加强热使其分解的过程叫煤的干馏。
注意:煤的干馏是化学变化
目标1:知道从煤中获得有机化工原料的主要方法,认识化石燃料综合利用的意义。
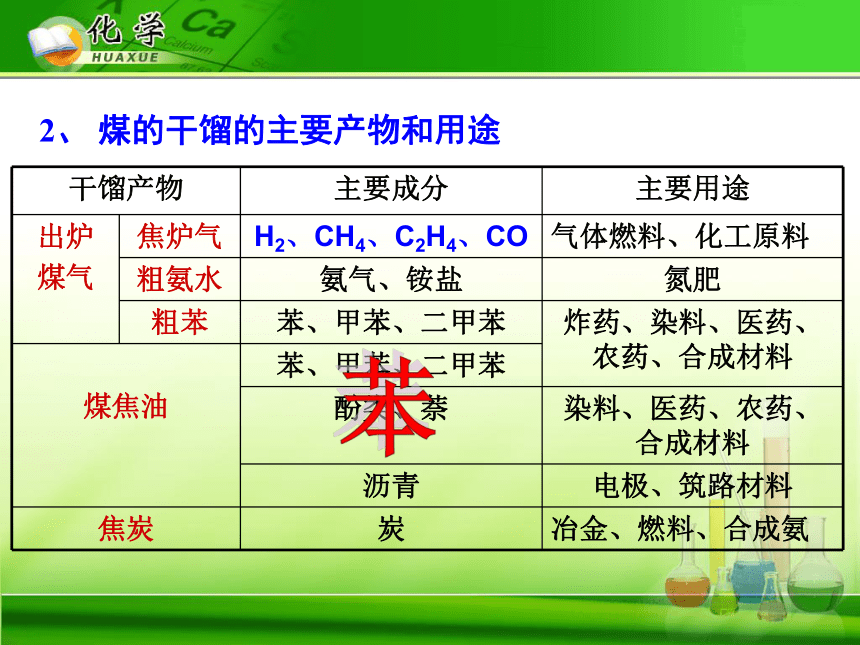
2、 煤的干馏的主要产物和用途
干馏产物 主要成分 主要用途
出炉 煤气 焦炉气 H2、CH4、C2H4、CO 气体燃料、化工原料
粗氨水 氨气、铵盐 氮肥
粗苯 苯、甲苯、二甲苯 炸药、染料、医药、农药、合成材料
煤焦油 苯、甲苯、二甲苯
酚类、萘 染料、医药、农药、合成材料
沥青 电极、筑路材料
焦炭 炭 冶金、燃料、合成氨
苯
炼制方法 原理 产物
气化 (化学变化) 把煤转化为可燃性气体,主要反应: 水煤气
(CO和H2)
液化 (化学变化) 把煤转化为液体燃料 液体燃料(甲醇、汽油等)
C + H2O= CO+H2
高温
3、 煤的气化和液化
煤的干馏产物用途:焦炭用于冶炼生铁,煤焦油用于制染料、医药、杀虫剂、消毒剂、合成材料,焦炉气可作气体燃料
以石油为原料所制成的部分产品:合成洗涤剂、合成纤维、塑料、油漆、医药、炸药、化肥、农药、合成橡胶等
天然气的用途:重要化工原料:制氢气,作燃料。
煤、石油、天然气在地球上的蕴藏量是有限的,且是重要的化工原料,仅仅作燃料,是对资源的一种浪费。
目标1:知道从煤中获得有机化工原料的主要方法,认识化石燃料综合利用的意义。
【目标1评价】下列说法正确的是( )
A、煤的干馏、气化、液化都是物理变化
B、由于煤中含有苯,所以可以从煤的干馏产品中分离得到苯
C、苯主要是以石油为原料而获得的一种重要化工原料
D、用煤的干馏产物粗氨水可以制氮肥
D
目 标 评 价
实验 目的 苯的物理性质
实验操作
实验现象
1、注意实验安全、小组分工合作
2、记录实验现象
①观察苯的颜色、状态;
闻苯的气味
【实验探究一】
实验与观察
②向试管中加入2mL水和1mL苯,振荡静置
③向试管中加入2mL酒精和1mL苯,振荡静置
目标2:通过实验能够描述苯的物理性质,并能通过实验探究的方式分析苯的结构。
1、物理性质
① ____色有_______气味的有毒液体
② 密度、溶解性:密度比水______,______溶于水,______溶于酒精等有机溶剂。
③ 熔、沸点:苯的沸点为80.5℃,易挥发;熔点5.5℃,当温度低于5.5℃时,苯就会凝结成无色的晶体。
特殊
无
小
易
(二)苯
难
目标2:通过实验能够描述苯的物理性质。
苯的发现史
1825年,英国科学家 法拉第 利用鱼油制煤气的过程中发现了一种无色有特殊气味的液体,当时称为“氢的重碳化合物”
1834年,德国科学家 米希尔里希 在实验中得到了与法拉第相同的液体,命名为苯。
李比希有机物燃烧分析法确定了苯的组成: C6H6
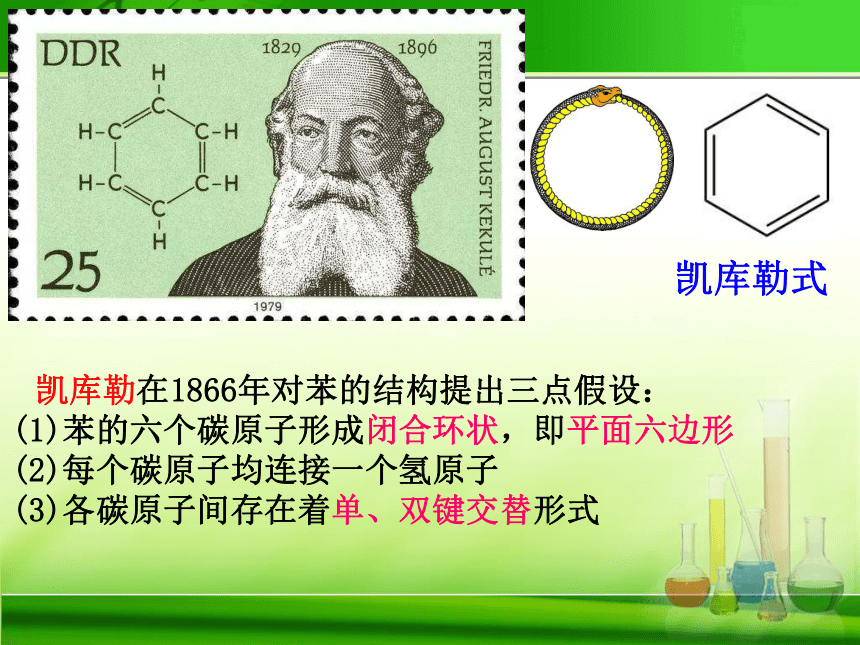
凯库勒式
凯库勒在1866年对苯的结构提出三点假设:
(1)苯的六个碳原子形成闭合环状,即平面六边形
(2)每个碳原子均连接一个氢原子
(3)各碳原子间存在着单、双键交替形式
穷且益坚,不坠青云之志
【思考】
如果苯分子具有凯库勒式的结构( )那么向苯中加入酸性KMnO4溶液和溴水会有什么现象?
【知识回顾】
将乙烯分别通入酸性的KMnO4溶液和溴水中有什么现象?
目标2:通过实验探究的方式分析苯的结构。
实验 目的 探究苯能否与酸性KMnO4溶液和溴水反应
实验操作
实验现象
1、注意实验安全、小组分工合作
2、记录实验现象:从是否褪色、各层的颜色角度描述
【实验探究二】
实验与观察
①向盛有2ml酸性KMnO4溶液的试管中滴入1ml苯,振荡试管,静置后观察现象
②向盛有2ml溴水的试管中滴入1ml苯,振荡试管,静置后观察现象
目标2:通过实验探究的方式分析苯的结构。
实验 目的 探究苯能否与酸性KMnO4溶液和溴水反应
实验操作
实验现象
【实验探究二】
苯不能使酸性KMnO4褪色,
上层无色,下层紫色
溶液分层,上层橙色,
下层无色。苯不能与溴水
发生反应而使其褪色,
只能发生萃取。
解释及结论
目标2:通过实验探究的方式分析苯的结构。
①向盛有2ml酸性KMnO4溶液的试管中滴入1ml苯,振荡试管,静置后观察现象
②向盛有2ml溴水的试管中滴入1ml苯,振荡试管,静置后观察现象
苯分子中的碳碳键是一种介于碳碳单键和碳碳双键之间的特殊的共价键,6条碳碳键完全相同。
空间填充模型
结构简式
苯分子中6个碳原子和6个氢原子都在同一个平面上,形成平面正六边形结构,4个原子共直线。
化学式
C6H6
最简式
CH
结构式
结构简式
2、苯的组成和结构
球棍模型
空间填充模型
(凯库勒式)
【目标2评价】
下列关于苯的叙述中,不正确的是( )
A.苯是无色有特殊气味的液体
B.常温下苯是一种不溶于水且密度小于水的液体
C.苯的分子式为C6H6
D.苯的结构式为
D
目 标 评 价
分析结构
预测性质
【小组合作探究】根据苯的结构及甲烷和乙烯的性质,
你能预测苯可以发生哪些类型的反应吗?
目标3:能根据苯的结构预测苯的化学性质,通过苯的性质的实验探究,与甲烷、乙烯对比归纳苯的性质。
特殊结构
决定
特殊性质
单键
双键
取代
加成
C、H元素
决定
可燃(氧化反应)
不与溴水和
KMnO4反应
反映
介于碳碳单键和碳碳双键之间的特殊的化学键
目标3:能根据苯的结构预测苯的化学性质。
(1)取代反应:
①与Br2的取代反应
3、苯的化学性质
Fe
+Br2
+HBr
溴苯:无色油状液体,
不溶于水,密度比水大。
液溴
【注意】苯不能与溴水或溴的CCl4溶液发生加成反应而使其褪色
② 取代反应——苯的硝化反应
硝基苯(苦杏仁味、无色油状液体 ,不溶于水,ρ>1 有毒)
浓硫酸
△
+ HNO3
+ H2O
易取代
(2)加成反应
环己烷
催化剂
△
+3H2
难加成
C6H6
C6H12
(3)氧化反应(燃烧)
现象:火焰明亮,伴有浓烈的黑烟。
苯分子中含碳量高,没有得到充分燃烧
点燃
2C6H6+15O2 12CO2+6H2O
【注意】苯不能被酸性高锰酸钾溶液氧化
难氧化
4.苯的用途
苯是一种重要的有机化工原料,广泛用于生产合成橡胶、合成纤维、塑料、农药、医药、染料、香料等;另外,苯也常用作有机溶剂。
目标3:与甲烷、乙烯对比归纳苯的性质。
甲烷 乙烯 苯
与Br2作用 Br2试剂
反应条件
反应类型
与酸性KMnO4溶液作用
点燃 现象
结论
溴蒸气
溴水
液溴
光照
取代反应
加成反应
Fe作催化剂
取代反应
现象
结论
不褪色
褪色
不褪色
甲烷不能被酸性KMnO4溶液氧化
乙烯易被酸性KMnO4溶液氧化
苯不能被酸性 KMnO4溶液氧化
淡蓝色火焰
火焰明亮,
伴有黑烟
火焰明亮,伴有浓烈的黑烟
含碳量低
含碳量较高
含碳量高
目 标 评 价
【目标3评价】下列物质中,既能因发生化学反应而使溴水褪色,又能使酸性KMnO4溶液褪色的是( )
①SO2 ② CH2=CH2 ③ 苯 ④ CH4
A.①②③④ B.③④ C.①②④ D.①②
D
如何消除苯污染?
苯易挥发
勤通风
课堂小结
化学学科核心素养
1
2
3
4
5
宏观辨识 微观探析
变化观念 平衡思想
证据推理 模型认知
科学精神 社会责任
科学探究 创新意识
青年一代,有理想,有本领,有担当,国家才有前途,民族才有希望!
练习册P89—P91
【课后作业】
煤的干馏 苯
第3章 第2节 第2课时
如何消除苯污染?
1、知道从煤中获得有机化工原料的主要方法,认识化石燃料综合利用的意义。
2、通过实验能够描述苯的物理性质,并能通过实验探究的方式分析苯的结构。
3、能根据苯的结构预测苯的化学性质,通过苯的性质的实验探究,与甲烷、乙烯对比归纳描述苯的性质。
宏观辨识
微观探析
证据推理
微观探析
科学精神
社会责任
二、煤的干馏 苯
(一) 煤的干馏
1、 煤的干馏
将煤隔绝空气加强热使其分解的过程叫煤的干馏。
注意:煤的干馏是化学变化
目标1:知道从煤中获得有机化工原料的主要方法,认识化石燃料综合利用的意义。
2、 煤的干馏的主要产物和用途
干馏产物 主要成分 主要用途
出炉 煤气 焦炉气 H2、CH4、C2H4、CO 气体燃料、化工原料
粗氨水 氨气、铵盐 氮肥
粗苯 苯、甲苯、二甲苯 炸药、染料、医药、农药、合成材料
煤焦油 苯、甲苯、二甲苯
酚类、萘 染料、医药、农药、合成材料
沥青 电极、筑路材料
焦炭 炭 冶金、燃料、合成氨
苯
炼制方法 原理 产物
气化 (化学变化) 把煤转化为可燃性气体,主要反应: 水煤气
(CO和H2)
液化 (化学变化) 把煤转化为液体燃料 液体燃料(甲醇、汽油等)
C + H2O= CO+H2
高温
3、 煤的气化和液化
煤的干馏产物用途:焦炭用于冶炼生铁,煤焦油用于制染料、医药、杀虫剂、消毒剂、合成材料,焦炉气可作气体燃料
以石油为原料所制成的部分产品:合成洗涤剂、合成纤维、塑料、油漆、医药、炸药、化肥、农药、合成橡胶等
天然气的用途:重要化工原料:制氢气,作燃料。
煤、石油、天然气在地球上的蕴藏量是有限的,且是重要的化工原料,仅仅作燃料,是对资源的一种浪费。
目标1:知道从煤中获得有机化工原料的主要方法,认识化石燃料综合利用的意义。
【目标1评价】下列说法正确的是( )
A、煤的干馏、气化、液化都是物理变化
B、由于煤中含有苯,所以可以从煤的干馏产品中分离得到苯
C、苯主要是以石油为原料而获得的一种重要化工原料
D、用煤的干馏产物粗氨水可以制氮肥
D
目 标 评 价
实验 目的 苯的物理性质
实验操作
实验现象
1、注意实验安全、小组分工合作
2、记录实验现象
①观察苯的颜色、状态;
闻苯的气味
【实验探究一】
实验与观察
②向试管中加入2mL水和1mL苯,振荡静置
③向试管中加入2mL酒精和1mL苯,振荡静置
目标2:通过实验能够描述苯的物理性质,并能通过实验探究的方式分析苯的结构。
1、物理性质
① ____色有_______气味的有毒液体
② 密度、溶解性:密度比水______,______溶于水,______溶于酒精等有机溶剂。
③ 熔、沸点:苯的沸点为80.5℃,易挥发;熔点5.5℃,当温度低于5.5℃时,苯就会凝结成无色的晶体。
特殊
无
小
易
(二)苯
难
目标2:通过实验能够描述苯的物理性质。
苯的发现史
1825年,英国科学家 法拉第 利用鱼油制煤气的过程中发现了一种无色有特殊气味的液体,当时称为“氢的重碳化合物”
1834年,德国科学家 米希尔里希 在实验中得到了与法拉第相同的液体,命名为苯。
李比希有机物燃烧分析法确定了苯的组成: C6H6
凯库勒式
凯库勒在1866年对苯的结构提出三点假设:
(1)苯的六个碳原子形成闭合环状,即平面六边形
(2)每个碳原子均连接一个氢原子
(3)各碳原子间存在着单、双键交替形式
穷且益坚,不坠青云之志
【思考】
如果苯分子具有凯库勒式的结构( )那么向苯中加入酸性KMnO4溶液和溴水会有什么现象?
【知识回顾】
将乙烯分别通入酸性的KMnO4溶液和溴水中有什么现象?
目标2:通过实验探究的方式分析苯的结构。
实验 目的 探究苯能否与酸性KMnO4溶液和溴水反应
实验操作
实验现象
1、注意实验安全、小组分工合作
2、记录实验现象:从是否褪色、各层的颜色角度描述
【实验探究二】
实验与观察
①向盛有2ml酸性KMnO4溶液的试管中滴入1ml苯,振荡试管,静置后观察现象
②向盛有2ml溴水的试管中滴入1ml苯,振荡试管,静置后观察现象
目标2:通过实验探究的方式分析苯的结构。
实验 目的 探究苯能否与酸性KMnO4溶液和溴水反应
实验操作
实验现象
【实验探究二】
苯不能使酸性KMnO4褪色,
上层无色,下层紫色
溶液分层,上层橙色,
下层无色。苯不能与溴水
发生反应而使其褪色,
只能发生萃取。
解释及结论
目标2:通过实验探究的方式分析苯的结构。
①向盛有2ml酸性KMnO4溶液的试管中滴入1ml苯,振荡试管,静置后观察现象
②向盛有2ml溴水的试管中滴入1ml苯,振荡试管,静置后观察现象
苯分子中的碳碳键是一种介于碳碳单键和碳碳双键之间的特殊的共价键,6条碳碳键完全相同。
空间填充模型
结构简式
苯分子中6个碳原子和6个氢原子都在同一个平面上,形成平面正六边形结构,4个原子共直线。
化学式
C6H6
最简式
CH
结构式
结构简式
2、苯的组成和结构
球棍模型
空间填充模型
(凯库勒式)
【目标2评价】
下列关于苯的叙述中,不正确的是( )
A.苯是无色有特殊气味的液体
B.常温下苯是一种不溶于水且密度小于水的液体
C.苯的分子式为C6H6
D.苯的结构式为
D
目 标 评 价
分析结构
预测性质
【小组合作探究】根据苯的结构及甲烷和乙烯的性质,
你能预测苯可以发生哪些类型的反应吗?
目标3:能根据苯的结构预测苯的化学性质,通过苯的性质的实验探究,与甲烷、乙烯对比归纳苯的性质。
特殊结构
决定
特殊性质
单键
双键
取代
加成
C、H元素
决定
可燃(氧化反应)
不与溴水和
KMnO4反应
反映
介于碳碳单键和碳碳双键之间的特殊的化学键
目标3:能根据苯的结构预测苯的化学性质。
(1)取代反应:
①与Br2的取代反应
3、苯的化学性质
Fe
+Br2
+HBr
溴苯:无色油状液体,
不溶于水,密度比水大。
液溴
【注意】苯不能与溴水或溴的CCl4溶液发生加成反应而使其褪色
② 取代反应——苯的硝化反应
硝基苯(苦杏仁味、无色油状液体 ,不溶于水,ρ>1 有毒)
浓硫酸
△
+ HNO3
+ H2O
易取代
(2)加成反应
环己烷
催化剂
△
+3H2
难加成
C6H6
C6H12
(3)氧化反应(燃烧)
现象:火焰明亮,伴有浓烈的黑烟。
苯分子中含碳量高,没有得到充分燃烧
点燃
2C6H6+15O2 12CO2+6H2O
【注意】苯不能被酸性高锰酸钾溶液氧化
难氧化
4.苯的用途
苯是一种重要的有机化工原料,广泛用于生产合成橡胶、合成纤维、塑料、农药、医药、染料、香料等;另外,苯也常用作有机溶剂。
目标3:与甲烷、乙烯对比归纳苯的性质。
甲烷 乙烯 苯
与Br2作用 Br2试剂
反应条件
反应类型
与酸性KMnO4溶液作用
点燃 现象
结论
溴蒸气
溴水
液溴
光照
取代反应
加成反应
Fe作催化剂
取代反应
现象
结论
不褪色
褪色
不褪色
甲烷不能被酸性KMnO4溶液氧化
乙烯易被酸性KMnO4溶液氧化
苯不能被酸性 KMnO4溶液氧化
淡蓝色火焰
火焰明亮,
伴有黑烟
火焰明亮,伴有浓烈的黑烟
含碳量低
含碳量较高
含碳量高
目 标 评 价
【目标3评价】下列物质中,既能因发生化学反应而使溴水褪色,又能使酸性KMnO4溶液褪色的是( )
①SO2 ② CH2=CH2 ③ 苯 ④ CH4
A.①②③④ B.③④ C.①②④ D.①②
D
如何消除苯污染?
苯易挥发
勤通风
课堂小结
化学学科核心素养
1
2
3
4
5
宏观辨识 微观探析
变化观念 平衡思想
证据推理 模型认知
科学精神 社会责任
科学探究 创新意识
青年一代,有理想,有本领,有担当,国家才有前途,民族才有希望!
练习册P89—P91
【课后作业】
