1.1 物质的分类及转化-高一化学人教版必修第一册同步课件(共29张PPT)
文档属性
| 名称 | 1.1 物质的分类及转化-高一化学人教版必修第一册同步课件(共29张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 22.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-21 00:00:00 | ||
图片预览







文档简介
(共29张PPT)
第一节 物质的分类及转化
第一节 物质的分类及转化
第1课时 物质的分类
小黄人分捡快递
垃圾分类
简单分类法及应用
菜谱分类
物以类聚
超市的商品、图书馆的书籍都是按照某些特征或属性分类摆放!
同素异形体
由同一元素形成的几种性质不同的单质。
C60
石墨
金刚石
(1)NaCl、KCl、NaSO4、BaCl2
(2)H2SO4、K2SO4、Cl2、Na2SO4
(3)空气、N2、HCl、CuSO4
思考:下列每组物质都有一种物质与其他物质在分类上不同,将这种不同类的物质找出来,并说明你的理由。
物质的分类
将大量事物按照事先设定的标准进行归类的方法
标准:分类依据
分类的好处:简便、快捷
分类是要有一定的标准;
标准不同,分类的结果也可能有所不同。
1
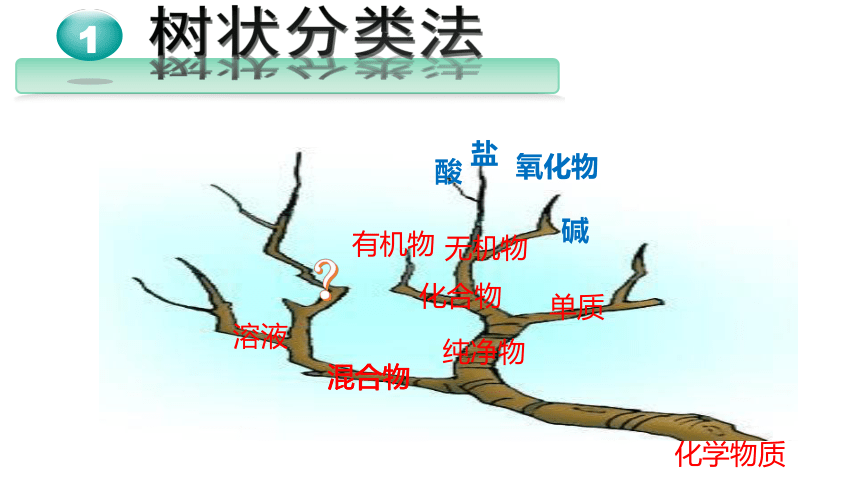
树状分类法
树状分类法
化学物质
单质
化合物
酸
碱
盐
氧化物
纯净物
混合物
混合物
混合物
溶液
无机物
有机物
?
树状分类法的分类原则
特点:同一层次的物质类别间一般是相互独立,没有交叉的。
单质
非金属
单
质
活泼金属
较活泼金属
不活泼金属
由分子构成
由原子构成
Ag 、Pt、 Au
金刚石、石墨、稀有气体(He、Ne)
H2、Cl2、N2、O2
K、Ca、Na等
Fe、Sn、Pb等
金属
酸
H2SO4、HNO3、H2CO3
HCl、H2S
按是否含氧
无氧酸
含氧酸
按性质
易挥发性酸
难挥发性酸
HCl、HNO3
H2SO4、 H3PO4
酸 = H+ + 酸根阴离子
碱
易溶碱
难溶碱
NaOH 、KOH、NH4Cl、Ba(OH)2
Cu(OH)2 、Fe(OH)3
碱 = 金属离子(铵根离子) + OH-
盐
按溶解性
按组成离子
无氧酸盐
钠盐
钾盐
铵盐
硫酸盐
碳酸盐
硝酸盐
按酸根是否含氧
含氧酸盐
可溶盐
难溶盐
NaCl、AgNO3、CuSO4、NH4Cl
CaCO3、 BaCO3 、BaSO4
KNO3、KMnO4、FeSO4
NaCl、CaCl2
……
盐 = 金属离子 (铵根离子) + 酸根离子
2
交叉分类法
交叉分类法
钠 盐
碳酸盐
Na2CO3
Na2CO3
物质类别之间有部分交叉。
特点:
交叉分类法:依据物质的不同属性从不同的角度对物质进行分类的方法。
试一试:将下列物质以不同标准分类
Na2CO3
K2SO4
钾 盐
硫酸盐
钠 盐
碳酸盐
Na2SO4
以所含阴离
子不同进行
分类
K2CO3
以所含阳离
子不同进行
分类
CuO、Fe2O3、Na2O
CO、P2O5、H2O
CO2、P2O5、SO3、Mn2O7
CaO、CuO、K2O
氧
化
物
组成元素
非金属氧化物
金属氧化物
酸性氧化物
碱性氧化物
性质
Na2O
SO2
CaO
CO2
非金属氧化物
酸 性 氧 化 物
金 属 氧 化 物
碱 性 氧 化 物
分类法
树状分类法
交叉分类法
下表中物质的分类组合完全正确的是( )
A B C D
氧化物 H2O H2O2 CuO K2O
酸 H2CO3 CH3COOH NaHCO3 HCl
碱 Mg(OH)Cl Na2CO3 Fe(OH)3 NaOH
盐 BaSO4 CuSO4·5H2O NaH2PO4 Na2S
D
1
跟 踪 训 练
(1)Fe、S、C、P _______________________________
(2)H2、O2、N2、S _____________________________
(3)Fe2O3、Na2CO3、CuO、H2O____________________
(4)AgCl、BaSO4、KNO3、CaCO3________________
下列五组物质,每组中有一种物质从某种角度分析与其他三种不同,请找出该物质,并说明理由。
Fe;Fe为金属
S;常温下S为固体
Na2CO3 ; Na2CO3为盐
a.溶解度:KNO3
b.酸根是否含氧:AgCl
2
交叉分类法
树状分类法
特点:物质类别间有相交叉的部分
特点:同层次中各类别间相互独立
分类角度多样
分类标准唯一
1.常用分类方法
2.分类一般步骤:
选择分类方法
得出正确的分类
分类的一般原则:行之有效,简单易行。
确定分类标准
课 堂 小 结
第一节 物质的分类及转化
第2课时 分散系及胶体的性质
一种物质或几种物质均匀分散到另一种物质中形成的均一、稳定的混合物叫溶液。
溶液
溶质
溶剂
CuSO4晶体
CuSO4溶液
温故知新
一、分散系
1.定义:
2.组成:
CuSO4溶液
分散质
CuSO4固体
分散剂
水
被分散成粒子的物质叫分散质,另一种物质叫分散剂。
把一种或多种物质以粒子形式分散到另一种(或多种)物质中所形成的混合物。
指导阅读
3.分类
(2)油状物质分散到水中可形成乳浊液;
不溶于水的固体分散到水中可形成悬浊液
(1)溶液是常见的一种分散系,溶质是分散质,溶剂是分散剂
指导阅读
按照分散质和分散剂所处的状态,它们之间的结合方式有哪些,并各举一两例
分散质 分散剂 举例
气体 气体
液体 气体
固体 气体
气体 液体
液体 液体
固体 液体
气体 固体
液体 固体
固体 固体
分散系具有多样性
空气
云、雾
烟、灰尘
泡沫
牛奶、酒精溶液
糖水、油漆
泡沫塑料
有色玻璃、合金
思考讨论
二、胶体
1.定义:
2.Fe(OH)3胶体的制备:
3.性质:
应用:
当光束通过胶体时,在胶体内部产生一条光亮的“通路”
分散质粒子直径在
1~100 nm的分散系
丁达尔效应
区分胶体和溶液
学习探究
胶体粒子能否透过滤纸?如何设计实验进行验证?
1.将上述得到的Fe(OH)3胶体进行过滤:
2.用激光笔照射Fe(OH)3胶体过滤后得到的液体:
过滤后得到的液体与原体系无明显差异
有丁达尔效应
实验探究
三种分散系比较
分散系 分散质粒子大小 主要特征 性质 举例
浊液
溶液
胶体
不均一、不稳定
均一、稳定
均一、介稳定
丁达尔效应
不能透过滤纸
能透过滤纸
泥水
盐酸、氯化
钠溶液
蛋清、牛奶
>100nm
<1nm
1~100 nm
总结反思
概念
分类
性质
制备
胶体
课堂小结
本节内容结束
第一节 物质的分类及转化
第一节 物质的分类及转化
第1课时 物质的分类
小黄人分捡快递
垃圾分类
简单分类法及应用
菜谱分类
物以类聚
超市的商品、图书馆的书籍都是按照某些特征或属性分类摆放!
同素异形体
由同一元素形成的几种性质不同的单质。
C60
石墨
金刚石
(1)NaCl、KCl、NaSO4、BaCl2
(2)H2SO4、K2SO4、Cl2、Na2SO4
(3)空气、N2、HCl、CuSO4
思考:下列每组物质都有一种物质与其他物质在分类上不同,将这种不同类的物质找出来,并说明你的理由。
物质的分类
将大量事物按照事先设定的标准进行归类的方法
标准:分类依据
分类的好处:简便、快捷
分类是要有一定的标准;
标准不同,分类的结果也可能有所不同。
1
树状分类法
树状分类法
化学物质
单质
化合物
酸
碱
盐
氧化物
纯净物
混合物
混合物
混合物
溶液
无机物
有机物
?
树状分类法的分类原则
特点:同一层次的物质类别间一般是相互独立,没有交叉的。
单质
非金属
单
质
活泼金属
较活泼金属
不活泼金属
由分子构成
由原子构成
Ag 、Pt、 Au
金刚石、石墨、稀有气体(He、Ne)
H2、Cl2、N2、O2
K、Ca、Na等
Fe、Sn、Pb等
金属
酸
H2SO4、HNO3、H2CO3
HCl、H2S
按是否含氧
无氧酸
含氧酸
按性质
易挥发性酸
难挥发性酸
HCl、HNO3
H2SO4、 H3PO4
酸 = H+ + 酸根阴离子
碱
易溶碱
难溶碱
NaOH 、KOH、NH4Cl、Ba(OH)2
Cu(OH)2 、Fe(OH)3
碱 = 金属离子(铵根离子) + OH-
盐
按溶解性
按组成离子
无氧酸盐
钠盐
钾盐
铵盐
硫酸盐
碳酸盐
硝酸盐
按酸根是否含氧
含氧酸盐
可溶盐
难溶盐
NaCl、AgNO3、CuSO4、NH4Cl
CaCO3、 BaCO3 、BaSO4
KNO3、KMnO4、FeSO4
NaCl、CaCl2
……
盐 = 金属离子 (铵根离子) + 酸根离子
2
交叉分类法
交叉分类法
钠 盐
碳酸盐
Na2CO3
Na2CO3
物质类别之间有部分交叉。
特点:
交叉分类法:依据物质的不同属性从不同的角度对物质进行分类的方法。
试一试:将下列物质以不同标准分类
Na2CO3
K2SO4
钾 盐
硫酸盐
钠 盐
碳酸盐
Na2SO4
以所含阴离
子不同进行
分类
K2CO3
以所含阳离
子不同进行
分类
CuO、Fe2O3、Na2O
CO、P2O5、H2O
CO2、P2O5、SO3、Mn2O7
CaO、CuO、K2O
氧
化
物
组成元素
非金属氧化物
金属氧化物
酸性氧化物
碱性氧化物
性质
Na2O
SO2
CaO
CO2
非金属氧化物
酸 性 氧 化 物
金 属 氧 化 物
碱 性 氧 化 物
分类法
树状分类法
交叉分类法
下表中物质的分类组合完全正确的是( )
A B C D
氧化物 H2O H2O2 CuO K2O
酸 H2CO3 CH3COOH NaHCO3 HCl
碱 Mg(OH)Cl Na2CO3 Fe(OH)3 NaOH
盐 BaSO4 CuSO4·5H2O NaH2PO4 Na2S
D
1
跟 踪 训 练
(1)Fe、S、C、P _______________________________
(2)H2、O2、N2、S _____________________________
(3)Fe2O3、Na2CO3、CuO、H2O____________________
(4)AgCl、BaSO4、KNO3、CaCO3________________
下列五组物质,每组中有一种物质从某种角度分析与其他三种不同,请找出该物质,并说明理由。
Fe;Fe为金属
S;常温下S为固体
Na2CO3 ; Na2CO3为盐
a.溶解度:KNO3
b.酸根是否含氧:AgCl
2
交叉分类法
树状分类法
特点:物质类别间有相交叉的部分
特点:同层次中各类别间相互独立
分类角度多样
分类标准唯一
1.常用分类方法
2.分类一般步骤:
选择分类方法
得出正确的分类
分类的一般原则:行之有效,简单易行。
确定分类标准
课 堂 小 结
第一节 物质的分类及转化
第2课时 分散系及胶体的性质
一种物质或几种物质均匀分散到另一种物质中形成的均一、稳定的混合物叫溶液。
溶液
溶质
溶剂
CuSO4晶体
CuSO4溶液
温故知新
一、分散系
1.定义:
2.组成:
CuSO4溶液
分散质
CuSO4固体
分散剂
水
被分散成粒子的物质叫分散质,另一种物质叫分散剂。
把一种或多种物质以粒子形式分散到另一种(或多种)物质中所形成的混合物。
指导阅读
3.分类
(2)油状物质分散到水中可形成乳浊液;
不溶于水的固体分散到水中可形成悬浊液
(1)溶液是常见的一种分散系,溶质是分散质,溶剂是分散剂
指导阅读
按照分散质和分散剂所处的状态,它们之间的结合方式有哪些,并各举一两例
分散质 分散剂 举例
气体 气体
液体 气体
固体 气体
气体 液体
液体 液体
固体 液体
气体 固体
液体 固体
固体 固体
分散系具有多样性
空气
云、雾
烟、灰尘
泡沫
牛奶、酒精溶液
糖水、油漆
泡沫塑料
有色玻璃、合金
思考讨论
二、胶体
1.定义:
2.Fe(OH)3胶体的制备:
3.性质:
应用:
当光束通过胶体时,在胶体内部产生一条光亮的“通路”
分散质粒子直径在
1~100 nm的分散系
丁达尔效应
区分胶体和溶液
学习探究
胶体粒子能否透过滤纸?如何设计实验进行验证?
1.将上述得到的Fe(OH)3胶体进行过滤:
2.用激光笔照射Fe(OH)3胶体过滤后得到的液体:
过滤后得到的液体与原体系无明显差异
有丁达尔效应
实验探究
三种分散系比较
分散系 分散质粒子大小 主要特征 性质 举例
浊液
溶液
胶体
不均一、不稳定
均一、稳定
均一、介稳定
丁达尔效应
不能透过滤纸
能透过滤纸
泥水
盐酸、氯化
钠溶液
蛋清、牛奶
>100nm
<1nm
1~100 nm
总结反思
概念
分类
性质
制备
胶体
课堂小结
本节内容结束
