2.2.2 氯气的实验室制法-高一化学人教版必修第一册同步课件(共15张PPT)
文档属性
| 名称 | 2.2.2 氯气的实验室制法-高一化学人教版必修第一册同步课件(共15张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 13.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-22 00:00:00 | ||
图片预览






文档简介
(共15张PPT)
第二章 海水中的重要元素----钠和氯
第二节 氯及其化合物
氯气的实验室制法
化学1 必修 人民教育出版社
化学2 必修 人民教育出版社
教 学 目 标
核 心 素 养
1 .掌握氯气的实验室制法。
2.掌握氯离子的检验方法。
1.通过小组分工合作完成氯气的实验室制备,理解实验室中气体的制备装置的选择原则,形成从问题出发,依据探究目的设计探究方案,并运用化学实验进行实验探究的化学核心素养。
2.通过对氯离子的检验掌握常见离子的检验方法,形成能基于物质组成提出可能假设,通过分析加以证实的论据推理和模型认知的化学核心素养。
舍勒 【瑞典】
资料卡片
18世纪,人们致力于采矿事业, 瑞典化学家舍勒也把精力放在了软锰矿(主要成分是MnO2)的研究上。
1774年的一天当他把软锰矿粉末和浓盐酸混合加热时,惊奇的看到一种黄绿色的气体冒出。这种呛人的气体不但能使染料褪色,还有许多奇特的性质。
直到1807年,英国化学家戴维对这种气体进行了细致的研究,并于1810年11月在英国皇家学会上正式定名确认上述黄绿色气体是由一种新元素组成,英文定名为“Chlorine”,希腊文的意思是“绿色的”。
戴维 【英国】
思考交流
1. 从氯气的发现到确认为一种新的元素,时间长达三十多年。你从这一史实中得到什么启示?
2. 舍勒发现氯气的方法至今还是实验室制取氯气的主要方法之一。请写出舍勒发现氯气的化学反应方程式。
启示3:科学研究需要有热爱科学的思想和奉献科学的精神。
启示1:科学研究需要有正确的理论作指导,错误的理论只能浪费时间和精力。
启示2:科学研究需要以大量事实为依据,只有大量事实才能推翻错误的理论,建立正确的理论或推动科学理论的发展。
MnO2+4HCl MnCl2+2H2O+Cl2↑
加热
(浓)
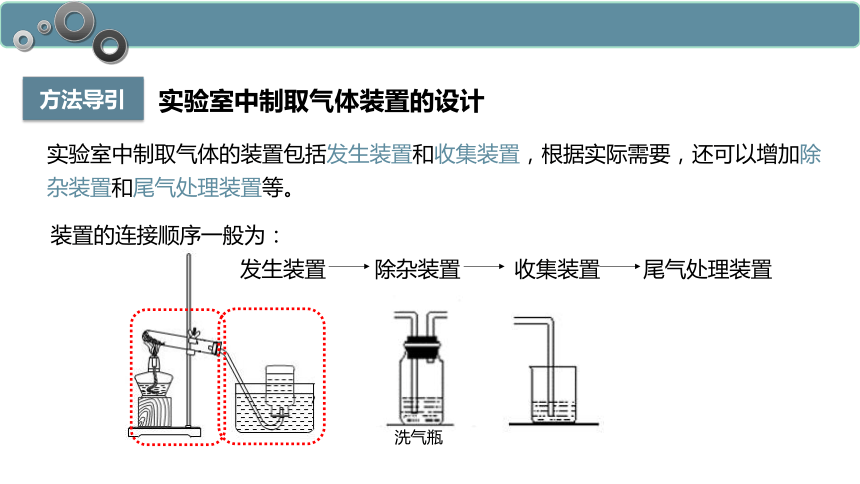
方法导引
实验室中制取气体的装置包括发生装置和收集装置,根据实际需要,还可以增加除杂装置和尾气处理装置等。
实验室中制取气体装置的设计
装置的连接顺序一般为:
发生装置 除杂装置 收集装置 尾气处理装置
洗气瓶
交流讨论
MnO2+4HCl MnCl2+2H2O+Cl2↑
加热
(浓)
1.二氧化锰和浓盐酸如何进行混合呢?
2.既可存放盐酸又可分次滴加的仪器是什么?
3.此反应可选择什么反应容器呢?
4.生成的氯气中可能含有哪些杂质呢?
6.饱和食盐水可吸收HCl且同时降低Cl2在水中的溶解,在干燥前还是干燥后?
5.除去气体中杂质的装置是什么?
7.要达到最佳洗涤或干燥效果,从洗气瓶的哪端进入气体?
8.收集氯气能用排水法吗?
9.利用排气法收集氯气时应该从哪端进气?
10.多余的氯气能直接排放到空气中吗?
学生实验
二、氯气的实验室制法
实验评价
吸收HCl
二、氯气的实验室制法
干燥H2O
收集Cl2
吸收尾气
形成方法
1.化学原理:
2. 装置的设计:
(3).收集装置:
向上排空气法排饱和食盐水收集
用碱液吸收,常用NaOH溶液
MnO2+4HCl (浓) MnCl2+2H2O+Cl2↑
加热
二、氯气的实验室制法
(1).发生装置:
(2).除杂装置:
(4).尾气处理装置:
洗气瓶
饱和食盐水(除HCl)
浓硫酸(除H2O)
固体+液体 气体
学生实验
三、氯离子的检验
在下列溶液中各滴入几滴AgNO3溶液,再分别加入少量稀HNO3,出现什么现象?
实验现象 解释或离子方程式
加AgNO3 加入稀硝酸
稀盐酸
NaCl溶液
Na2CO3溶液
白色↓
白色↓
白色↓
不溶解
不溶解
产生气泡
Ag++Cl- ==AgCl↓
Ag++Cl- ==AgCl↓
2Ag++==Ag2CO3↓
Ag2CO3+2H+==2Ag++CO2 ↑+H2O
形成方法
试剂:
操作过程及现象:
硝酸银和稀硝酸
在待测液中先加硝酸银,产生白色沉淀,再加稀硝酸,沉淀不溶解
三、氯离子的检验
1. 实验室用下列两种方法制氯气:
①用含HCl 146 g的浓盐酸与足量的MnO2反应;
②用87 g MnO2与足量浓盐酸反应。
所得的氯气( )
B
解析:由化学方程式:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O知,146 g HCl恰好可以与87 g MnO2反应,但是随反应的进行,盐酸的浓度降低,稀盐酸的还原性较弱,不能被MnO2氧化,所以含有146 g HCl的浓盐酸不能与MnO2完全反应,放出的氯气少。
例题讲解
D. 无法比较
A. ①比②多
B. ②比①多
C. 一样多
2. 已知高锰酸钾与浓盐酸在常温下反应能产生氯气。若用下图所示的实验装置来制备纯净、干燥的氯气,并试验其与金属的反应。每个虚线框表示一个单元装置,其中有错误的是( )
例题讲解
解析:①是制备氯气的装置:2KMnO4+16HCl(浓)=== 5Cl2↑+2MnCl2+2KCl+8H2O,不需要加热,正确;②是除去氯气中氯化氢杂质的装置,但是Cl2+2NaOH===NaCl+NaClO+H2O,不能选择NaOH溶液除杂,错误,③是干燥装置,进气管短,出气管却插入液面下,无法对气体进行干燥,也不能使气体进入④,错误;④是用于氯气与金属反应的装置,但其是一个封闭体系,未反应的气体不断蓄积会使容器内压强过大而发生爆炸,错误。综上所述D符合题意。
D
A.①和②处
B.只有②处
C.②和③处
D.②③④处
例题讲解
3. 下列检验Cl-的方法正确的是( )
A. 在某溶液中滴加AgNO3溶液,若产生白色沉淀说明该溶液中有Cl-
B. 在某溶液中先滴加盐酸,再滴加AgNO3溶液,若产生白色沉淀,说明溶液中有Cl-
C. 在某溶液中先滴加AgNO3溶液,产生白色沉淀,再滴加盐酸,沉淀不消失,说明溶液中有Cl-
D. 在某溶液中滴加用HNO3酸化的AgNO3溶液,若产生白色沉淀,说明溶液中有Cl-
解析:可能有等的干扰,A错误;加入盐酸,引入Cl-,B、C错误;硝酸酸化排除干扰,加硝酸银溶液得到不溶于稀硝酸的白色沉淀即为AgCl,由此说明原溶液中有Cl-,D正确。
D
本节内容结束
第二章 海水中的重要元素----钠和氯
第二节 氯及其化合物
氯气的实验室制法
化学1 必修 人民教育出版社
化学2 必修 人民教育出版社
教 学 目 标
核 心 素 养
1 .掌握氯气的实验室制法。
2.掌握氯离子的检验方法。
1.通过小组分工合作完成氯气的实验室制备,理解实验室中气体的制备装置的选择原则,形成从问题出发,依据探究目的设计探究方案,并运用化学实验进行实验探究的化学核心素养。
2.通过对氯离子的检验掌握常见离子的检验方法,形成能基于物质组成提出可能假设,通过分析加以证实的论据推理和模型认知的化学核心素养。
舍勒 【瑞典】
资料卡片
18世纪,人们致力于采矿事业, 瑞典化学家舍勒也把精力放在了软锰矿(主要成分是MnO2)的研究上。
1774年的一天当他把软锰矿粉末和浓盐酸混合加热时,惊奇的看到一种黄绿色的气体冒出。这种呛人的气体不但能使染料褪色,还有许多奇特的性质。
直到1807年,英国化学家戴维对这种气体进行了细致的研究,并于1810年11月在英国皇家学会上正式定名确认上述黄绿色气体是由一种新元素组成,英文定名为“Chlorine”,希腊文的意思是“绿色的”。
戴维 【英国】
思考交流
1. 从氯气的发现到确认为一种新的元素,时间长达三十多年。你从这一史实中得到什么启示?
2. 舍勒发现氯气的方法至今还是实验室制取氯气的主要方法之一。请写出舍勒发现氯气的化学反应方程式。
启示3:科学研究需要有热爱科学的思想和奉献科学的精神。
启示1:科学研究需要有正确的理论作指导,错误的理论只能浪费时间和精力。
启示2:科学研究需要以大量事实为依据,只有大量事实才能推翻错误的理论,建立正确的理论或推动科学理论的发展。
MnO2+4HCl MnCl2+2H2O+Cl2↑
加热
(浓)
方法导引
实验室中制取气体的装置包括发生装置和收集装置,根据实际需要,还可以增加除杂装置和尾气处理装置等。
实验室中制取气体装置的设计
装置的连接顺序一般为:
发生装置 除杂装置 收集装置 尾气处理装置
洗气瓶
交流讨论
MnO2+4HCl MnCl2+2H2O+Cl2↑
加热
(浓)
1.二氧化锰和浓盐酸如何进行混合呢?
2.既可存放盐酸又可分次滴加的仪器是什么?
3.此反应可选择什么反应容器呢?
4.生成的氯气中可能含有哪些杂质呢?
6.饱和食盐水可吸收HCl且同时降低Cl2在水中的溶解,在干燥前还是干燥后?
5.除去气体中杂质的装置是什么?
7.要达到最佳洗涤或干燥效果,从洗气瓶的哪端进入气体?
8.收集氯气能用排水法吗?
9.利用排气法收集氯气时应该从哪端进气?
10.多余的氯气能直接排放到空气中吗?
学生实验
二、氯气的实验室制法
实验评价
吸收HCl
二、氯气的实验室制法
干燥H2O
收集Cl2
吸收尾气
形成方法
1.化学原理:
2. 装置的设计:
(3).收集装置:
向上排空气法排饱和食盐水收集
用碱液吸收,常用NaOH溶液
MnO2+4HCl (浓) MnCl2+2H2O+Cl2↑
加热
二、氯气的实验室制法
(1).发生装置:
(2).除杂装置:
(4).尾气处理装置:
洗气瓶
饱和食盐水(除HCl)
浓硫酸(除H2O)
固体+液体 气体
学生实验
三、氯离子的检验
在下列溶液中各滴入几滴AgNO3溶液,再分别加入少量稀HNO3,出现什么现象?
实验现象 解释或离子方程式
加AgNO3 加入稀硝酸
稀盐酸
NaCl溶液
Na2CO3溶液
白色↓
白色↓
白色↓
不溶解
不溶解
产生气泡
Ag++Cl- ==AgCl↓
Ag++Cl- ==AgCl↓
2Ag++==Ag2CO3↓
Ag2CO3+2H+==2Ag++CO2 ↑+H2O
形成方法
试剂:
操作过程及现象:
硝酸银和稀硝酸
在待测液中先加硝酸银,产生白色沉淀,再加稀硝酸,沉淀不溶解
三、氯离子的检验
1. 实验室用下列两种方法制氯气:
①用含HCl 146 g的浓盐酸与足量的MnO2反应;
②用87 g MnO2与足量浓盐酸反应。
所得的氯气( )
B
解析:由化学方程式:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O知,146 g HCl恰好可以与87 g MnO2反应,但是随反应的进行,盐酸的浓度降低,稀盐酸的还原性较弱,不能被MnO2氧化,所以含有146 g HCl的浓盐酸不能与MnO2完全反应,放出的氯气少。
例题讲解
D. 无法比较
A. ①比②多
B. ②比①多
C. 一样多
2. 已知高锰酸钾与浓盐酸在常温下反应能产生氯气。若用下图所示的实验装置来制备纯净、干燥的氯气,并试验其与金属的反应。每个虚线框表示一个单元装置,其中有错误的是( )
例题讲解
解析:①是制备氯气的装置:2KMnO4+16HCl(浓)=== 5Cl2↑+2MnCl2+2KCl+8H2O,不需要加热,正确;②是除去氯气中氯化氢杂质的装置,但是Cl2+2NaOH===NaCl+NaClO+H2O,不能选择NaOH溶液除杂,错误,③是干燥装置,进气管短,出气管却插入液面下,无法对气体进行干燥,也不能使气体进入④,错误;④是用于氯气与金属反应的装置,但其是一个封闭体系,未反应的气体不断蓄积会使容器内压强过大而发生爆炸,错误。综上所述D符合题意。
D
A.①和②处
B.只有②处
C.②和③处
D.②③④处
例题讲解
3. 下列检验Cl-的方法正确的是( )
A. 在某溶液中滴加AgNO3溶液,若产生白色沉淀说明该溶液中有Cl-
B. 在某溶液中先滴加盐酸,再滴加AgNO3溶液,若产生白色沉淀,说明溶液中有Cl-
C. 在某溶液中先滴加AgNO3溶液,产生白色沉淀,再滴加盐酸,沉淀不消失,说明溶液中有Cl-
D. 在某溶液中滴加用HNO3酸化的AgNO3溶液,若产生白色沉淀,说明溶液中有Cl-
解析:可能有等的干扰,A错误;加入盐酸,引入Cl-,B、C错误;硝酸酸化排除干扰,加硝酸银溶液得到不溶于稀硝酸的白色沉淀即为AgCl,由此说明原溶液中有Cl-,D正确。
D
本节内容结束
