2.1.2胶体 课件(18张)2023-2024学年高一上学期化学鲁科版(2019)必修第一册
文档属性
| 名称 | 2.1.2胶体 课件(18张)2023-2024学年高一上学期化学鲁科版(2019)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-23 00:00:00 | ||
图片预览




文档简介
(共18张PPT)
?
第二章
第一节
元素与物质的分类
第2课时 一种重要的混合物
—胶体
【学习目标】
1.通过阅读课本48页,能够说出分散系的概念、组成和分类以及 胶体的概念和分类。重点
2.通过观看实验视频,能够归纳出胶体的性质, 并能够解释胶体应用的相关问题。 重难点
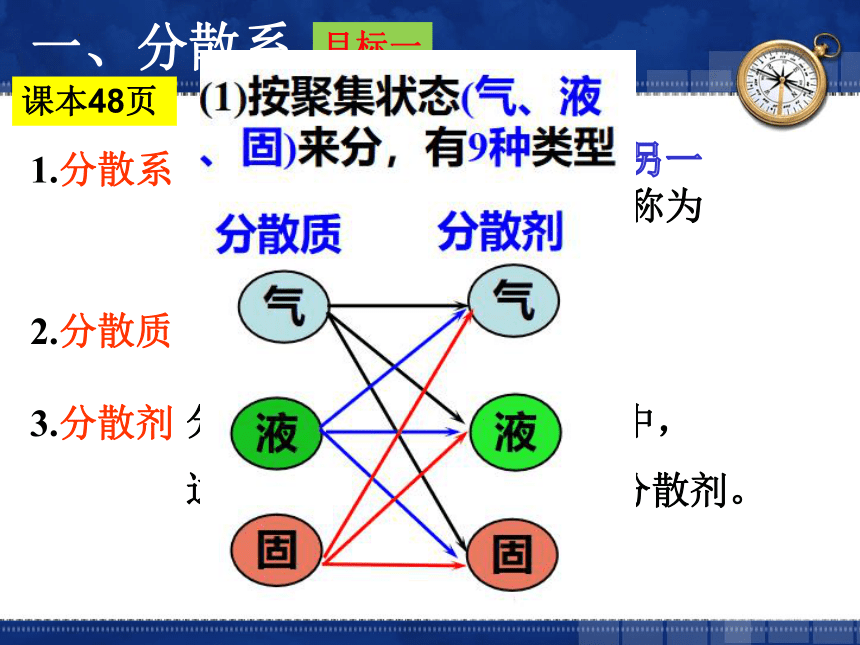
2.分散质
3.分散剂
被分散成微粒的物质。
分散质分散到另一种物质 中,
这种物质(另一种物质)叫分散剂。
由一种或几种物质分散到另一种物质中构成的混合物统称为分散系。
一、分散系
1.分散系
目标一
课本48页
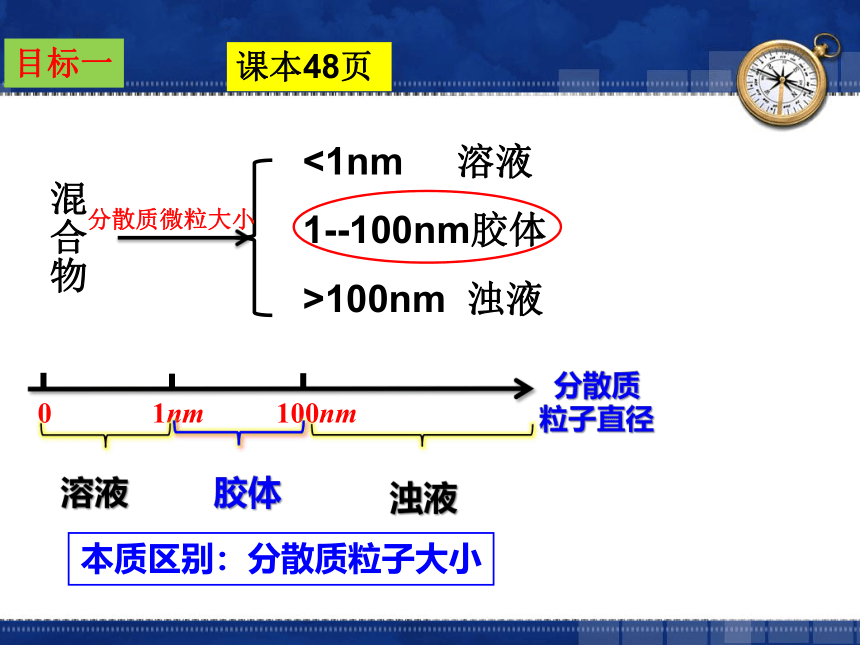
混合物
<1nm 溶液
1- 100nm胶体
>100nm 浊液
分散质微粒大小
0 1nm 100nm
溶液
胶体
浊液
分散质
粒子直径
本质区别:分散质粒子大小
目标一
课本48页
二、胶体
根据分散剂状态
固溶胶:有色玻璃、
烟水晶
液溶胶:AgI胶体、
Fe(OH)3胶体
气溶胶:烟、云、雾
1. 概念: 分散质粒子直径 1nm<d<100nm
之间的分散系
目标一
课本48页
烟水晶有色玻璃晨雾
气溶胶
烟
常见的胶体:
Fe(OH)3胶体、Al(OH)3胶体、AgI胶体、淀粉溶液、蛋清溶液、牛奶、血液、豆浆、墨水、涂料。
2. 胶体的性质和应用
胶体中分散质微粒对可见光散射。
⑴丁达尔现象
当可见光束通过胶体时,能在胶体中形成一条光亮的通路。
原因:
应用:
区别溶液和胶体。
定义:
目标二
课本48页
胶体的性质和应用:
丁达尔现象
Fe(OH)3胶体
CuSO4溶液
牛奶胶体
丁达尔现象
NaCl溶液
目标二
当堂检测
1.下列分散系不能发生丁达尔现象的是( )
A.豆浆 B.牛奶
C.蔗糖溶液 D.烟、云、雾
2 .鉴别胶体和溶液可以采取的方法是( )
A.蒸发 B.从外观观察
C.稀释 D.利用丁达尔效应实验
目标二
使分散质聚集成较大的微粒,在重力作用下
形成沉淀析出。
聚沉方法:
(2)聚沉
电解质溶液中的阳离子或阴离子能中和胶粒所带电荷,使胶粒聚集而沉淀。
原因:
应用:
盐卤点豆腐、明矾净水、黄河三角洲的形成
①加入酸、碱、盐等电解质溶液
②加热或搅拌
③加相反电荷的胶粒
2. 胶体的性质和应用
目标二
课本49页
(3)电泳
胶体中的分散质微粒(胶粒)在直流电的作用下产生定向移动的现象
应用:静电除尘
2. 胶体的性质和应用
目标二
课本49页
(4)胶体的精制——渗析
利用半透膜将胶体与溶液分离的方法。
半透膜:只允许某些分子或离子通过的薄膜(如:动物的肠衣、鸡蛋壳膜、羊皮纸、胶棉薄膜、玻璃纸等)
2. 胶体的性质和应用
目标二
课本48页
滤纸(过滤)
半透膜(渗析)
当堂检测
3.FeCl3溶液和Fe(OH)3胶体共同具备的性质是( )
A.都不稳定,密封静置,会产生沉淀
B.都能产生丁达尔现象
C.分散质微粒都可以透过滤纸
D.加入盐酸先产生沉淀,随后溶解
目标二
分散系 溶液 胶体 浊液
分散质微粒大小
外观特征稳定性
能否透过滤纸
能否透过半透膜
鉴别
1~100nm
>100nm
<1nm
均一
较稳定
不均一
不稳定
均一、透明最稳定
不能
不能
能
能
不能
能
分散系的比较
小结:
渗析
静置分层或沉淀
丁达尔现象
无丁达尔现象
导学案39页
当堂检测
1.溶液、胶体和浊液三种分散系的根本区别( )
A. 丁达尔效应 B. 分散剂不同
C. 能否稳定存在 D. 分散质粒子直径的大小
2.下列事实中,与胶体有关的是( )
A.将植物油倒入水中,用力搅拌形成油水混合物
B.一束可见光射入鸡蛋清液体里,从侧面可以看到一条光亮的“通路”
C.向石灰水中通入二氧化碳产生白色浑浊
D.利用活性炭净水
目标二
目标一
导学案39页
当堂检测
3.下列事实与胶体知识有关的是( )
①郑州美丽夜景中的光柱②明矾净水③卤水点豆腐
④一支钢笔使用不同牌号的蓝黑墨水易出现堵塞
A. ①②④ B.①③④
C.①②③④ D.全部都无关
4.用半透膜把分子或离子从胶体溶液中分离出来的方法是( )
A.电泳 B.电解 C.凝聚 D.渗析
目标二
导学案39页
?
第二章
第一节
元素与物质的分类
第2课时 一种重要的混合物
—胶体
【学习目标】
1.通过阅读课本48页,能够说出分散系的概念、组成和分类以及 胶体的概念和分类。重点
2.通过观看实验视频,能够归纳出胶体的性质, 并能够解释胶体应用的相关问题。 重难点
2.分散质
3.分散剂
被分散成微粒的物质。
分散质分散到另一种物质 中,
这种物质(另一种物质)叫分散剂。
由一种或几种物质分散到另一种物质中构成的混合物统称为分散系。
一、分散系
1.分散系
目标一
课本48页
混合物
<1nm 溶液
1- 100nm胶体
>100nm 浊液
分散质微粒大小
0 1nm 100nm
溶液
胶体
浊液
分散质
粒子直径
本质区别:分散质粒子大小
目标一
课本48页
二、胶体
根据分散剂状态
固溶胶:有色玻璃、
烟水晶
液溶胶:AgI胶体、
Fe(OH)3胶体
气溶胶:烟、云、雾
1. 概念: 分散质粒子直径 1nm<d<100nm
之间的分散系
目标一
课本48页
烟水晶有色玻璃晨雾
气溶胶
烟
常见的胶体:
Fe(OH)3胶体、Al(OH)3胶体、AgI胶体、淀粉溶液、蛋清溶液、牛奶、血液、豆浆、墨水、涂料。
2. 胶体的性质和应用
胶体中分散质微粒对可见光散射。
⑴丁达尔现象
当可见光束通过胶体时,能在胶体中形成一条光亮的通路。
原因:
应用:
区别溶液和胶体。
定义:
目标二
课本48页
胶体的性质和应用:
丁达尔现象
Fe(OH)3胶体
CuSO4溶液
牛奶胶体
丁达尔现象
NaCl溶液
目标二
当堂检测
1.下列分散系不能发生丁达尔现象的是( )
A.豆浆 B.牛奶
C.蔗糖溶液 D.烟、云、雾
2 .鉴别胶体和溶液可以采取的方法是( )
A.蒸发 B.从外观观察
C.稀释 D.利用丁达尔效应实验
目标二
使分散质聚集成较大的微粒,在重力作用下
形成沉淀析出。
聚沉方法:
(2)聚沉
电解质溶液中的阳离子或阴离子能中和胶粒所带电荷,使胶粒聚集而沉淀。
原因:
应用:
盐卤点豆腐、明矾净水、黄河三角洲的形成
①加入酸、碱、盐等电解质溶液
②加热或搅拌
③加相反电荷的胶粒
2. 胶体的性质和应用
目标二
课本49页
(3)电泳
胶体中的分散质微粒(胶粒)在直流电的作用下产生定向移动的现象
应用:静电除尘
2. 胶体的性质和应用
目标二
课本49页
(4)胶体的精制——渗析
利用半透膜将胶体与溶液分离的方法。
半透膜:只允许某些分子或离子通过的薄膜(如:动物的肠衣、鸡蛋壳膜、羊皮纸、胶棉薄膜、玻璃纸等)
2. 胶体的性质和应用
目标二
课本48页
滤纸(过滤)
半透膜(渗析)
当堂检测
3.FeCl3溶液和Fe(OH)3胶体共同具备的性质是( )
A.都不稳定,密封静置,会产生沉淀
B.都能产生丁达尔现象
C.分散质微粒都可以透过滤纸
D.加入盐酸先产生沉淀,随后溶解
目标二
分散系 溶液 胶体 浊液
分散质微粒大小
外观特征稳定性
能否透过滤纸
能否透过半透膜
鉴别
1~100nm
>100nm
<1nm
均一
较稳定
不均一
不稳定
均一、透明最稳定
不能
不能
能
能
不能
能
分散系的比较
小结:
渗析
静置分层或沉淀
丁达尔现象
无丁达尔现象
导学案39页
当堂检测
1.溶液、胶体和浊液三种分散系的根本区别( )
A. 丁达尔效应 B. 分散剂不同
C. 能否稳定存在 D. 分散质粒子直径的大小
2.下列事实中,与胶体有关的是( )
A.将植物油倒入水中,用力搅拌形成油水混合物
B.一束可见光射入鸡蛋清液体里,从侧面可以看到一条光亮的“通路”
C.向石灰水中通入二氧化碳产生白色浑浊
D.利用活性炭净水
目标二
目标一
导学案39页
当堂检测
3.下列事实与胶体知识有关的是( )
①郑州美丽夜景中的光柱②明矾净水③卤水点豆腐
④一支钢笔使用不同牌号的蓝黑墨水易出现堵塞
A. ①②④ B.①③④
C.①②③④ D.全部都无关
4.用半透膜把分子或离子从胶体溶液中分离出来的方法是( )
A.电泳 B.电解 C.凝聚 D.渗析
目标二
导学案39页
