3.1.3铁及其化合物之间的转化关系 课件(17张)2023-2024学年高一上学期化学鲁科版(2019)必修第一册
文档属性
| 名称 | 3.1.3铁及其化合物之间的转化关系 课件(17张)2023-2024学年高一上学期化学鲁科版(2019)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-23 00:00:00 | ||
图片预览





文档简介
(共17张PPT)
回顾:Fe2+、Fe3+的检验方法
药剂:硫酸亚铁片、Vc片各2片/天
辅助治疗:多食用含铁丰富的食物并配合Vc服用
缺铁性贫血
为什么维生素C和补铁剂搭档效果会更好?
铁元素与人体健康
铁元素是人体中含量最高的生命必需微量元素,承担着极其重要的生理功能。血红蛋白分子中含有Fe2+,正是这些Fe2+使血红蛋白分子具有载氧功能,能将肺部吸入的氧气输送到全身各组织,供细胞使用。如果因为某种原因血红蛋白分子中的Fe2+被氧化成Fe3+,这种血红蛋白分子就会丧失载氧能力,使人体出现缺氧症状。
人体内的铁元素主要来源于食物。动物血、肝脏、骨髓以及蛋黄、菠菜、木耳、葡萄、红枣、大豆、芝麻等食物含有丰富的铁元素。研究结果显示,源自食物中的铁元素主要在小肠(尤其是十二指肠)内被吸收,并且人体只能吸收Fe2+。由于维生素C具有还原性,可以将Fe3+还原成Fe2+,所以食用维生素C含量较高的食物有利于人体对铁元素的吸收。对于健康的成年人来说,合理的膳食完全可以满足人体对铁元素的需求。儿童和孕期妇女因需要摄入较多的铁元素,可额外补充。
课本93页身边的化学
铁的多样性
第三课时铁及其化合物之间的转化关系
1.通过绘制铁及其化合物的价-类二维图,能用箭头标明铁及其化合物之间的物质转化关系;(重点)
2.通过应用Fe3+和Fe2+的检验方法,检验补铁剂中铁元素的价态;(重点)
3、通过认识一定条件下铁及其化合物可以互相转化,能总结出Fe、Fe2+、Fe3+间的相互转化关系的转化思路和方法。(难点)
【学习目标】
课本91页
目标一
活动 探究
补铁剂中铁元素价态的检验
铁元素在人体中起着重要的作用。如果人体缺铁,就会出现贫血症状。轻度缺铁性贫血可用饮食疗法治疗,严重缺铁时则需要服用补铁剂。
补铁口服液是常见的补铁剂,其中除了含有铁元素的物质外,还常添加抗氧化物质(如维生素C)、甜味剂、香精等。例如,某补铁口服液100mL中含铁元素20 30mg、维生素C200 300mg。
实验目的
检验某补铁口服液中铁元素的价态。
实验用品
某补铁口服液,H2SO4,NaOH溶液,酸性KmnO4溶液,氯水,KSCN溶液;试管,胶头滴管。
课本92页
实验方案设计及实施
实验步骤 实验现象
实验结论
取少量口服液于小试管中,滴入KSCN溶液,没有明显现象,滴加少量氯水
溶液变为血红色
口服液中铁元素为+2价
取少量口服液于小试管中,滴入酸性KMnO4溶液
KMnO4溶液紫色退去
口服液中铁元素为+2价
取少量口服液于小试管中,滴加NaOH溶液
先有白色沉淀生成迅速变灰绿最后变成红褐色
口服液中铁元素为+2价
课本92页
目标二
0
+3
+2
Fe2+
Fe(OH)2
Fe3+
Fe(OH)3
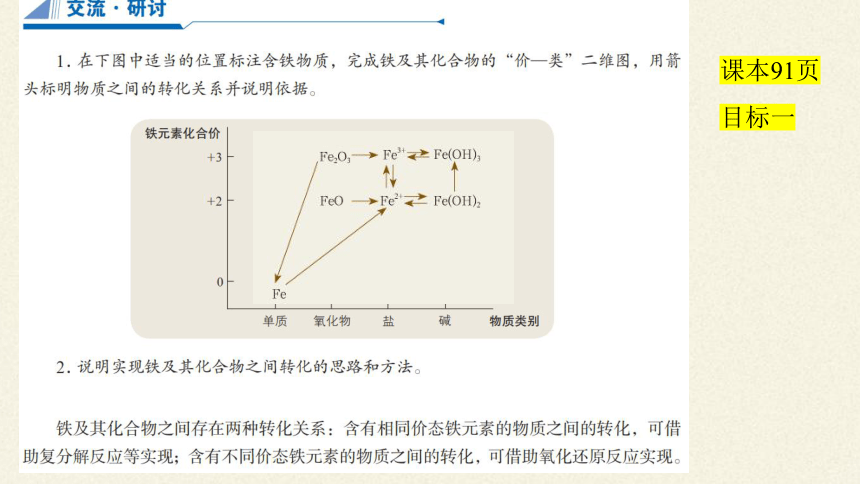
一、铁及其化合物之间的转化思路:
含有不同价态铁元素的物质之间的转化,可借助氧化还原反应实现。
含有相同价态铁元素的物质之间的转化,可借助复分解反应实现;
目标二
Fe
Fe3+
Fe2+
(1)化合价升高:反应物作还原剂,加氧化剂
强氧化剂
强氧化剂
弱氧化剂
二、Fe、Fe2+、Fe3+间的相互转化方法——铁三角
强氧化剂:O2、Cl2、Br2、HNO3、H2O2、酸性KMnO4等
弱氧化剂:I2、H+、Cu2+、Fe3+等
Fe
Fe3+
Fe2+
强还原剂
强还原剂
弱还原剂
(2)化合价降低:反应物作氧化剂,加还原剂
强还原剂:比铁活泼的金属单质如(Al、Zn等)
部分非金属单质C、CO、H2
弱还原剂:Fe、Cu、S2-等
Fe
Fe3+
Fe2+
弱氧化剂 H+、Cu2+、Fe3+
强氧化剂Cl2、O2、HNO3
Fe2O3:C、CO、H2、Al
Fe3+:Al、Zn等还原剂
Fe2+:Al、Zn等还原剂FeO:C、CO
强氧化剂:Cl2、O2、HNO3、H2O2等
Fe、Cu、S2-等还原剂
1.Fe、Fe2+、Fe3+间的相互转化关系——铁三角
学以致用
1、除去下列溶液中所含杂质
①FeCl2(FeCl3):
选用试剂________,
②FeCl3(FeCl2):
选用试剂________,
离子方程式:
______________________________;
Fe
Cl2
2Fe2++Cl2=2Fe3++2Cl-
H2O2
2Fe2++2H++H2O2=2Fe3++2H2O
当堂检测:
在亚铁盐溶液里加铁钉或铁粉防止溶液里的Fe2+
被氧化
2Fe3++Fe=3Fe2+
亚铁盐溶液保存
亚铁盐
0
+3
+2
盐
氢氧化物
氧化物
Fe2+
Fe(OH)2
FeO
Fe3+
Fe(OH)3
Fe2O3
Fe
单质
课本93页
B
1.“缺铁性贫血”中的铁是指( )
A.铁单质 B.铁元素
C.氧化铁 D.四氧化三铁
当堂检测:
2. 下列转化关系不能通过一步反应实现的是( )
A.Fe→FeCl2 B.Fe2O3→Fe(OH)3
C.FeCl3→FeCl2 D.Fe(OH)3→FeCl3
B
3.下列反应的离子方程式正确的是( )
A.Fe与FeCl3溶液反应:Fe+Fe3+===2Fe2+
B.Fe3O4与盐酸反应:Fe3O4+8H+===3Fe3++4H2O
C.Fe(OH)3与稀H2SO4反应:OH-+H+===H2O
D.Fe与CuSO4溶液反应:Fe+Cu2+===Cu+Fe2+
D
① ② ③ ④
将铁钉放入硫酸铜溶液中 向硫酸亚铁溶液 中滴入几滴氯水 将铜丝放入氯化铁溶液中 向FeCl2溶液中滴入KSCN溶液,无明显现象,再滴入氯水,变红
4.已知下述四个实验均能发生化学反应:
下列判断不正确的是( )
A.实验①中铁钉只做还原剂
B.实验②中Fe2+只显还原性
C.实验③中发生的是置换反应
D.上述实验证明:氧化性:Fe3+>Cu2+>Fe2+,Fe2+遇KSCN溶液无红色物质生成
C
回顾:Fe2+、Fe3+的检验方法
药剂:硫酸亚铁片、Vc片各2片/天
辅助治疗:多食用含铁丰富的食物并配合Vc服用
缺铁性贫血
为什么维生素C和补铁剂搭档效果会更好?
铁元素与人体健康
铁元素是人体中含量最高的生命必需微量元素,承担着极其重要的生理功能。血红蛋白分子中含有Fe2+,正是这些Fe2+使血红蛋白分子具有载氧功能,能将肺部吸入的氧气输送到全身各组织,供细胞使用。如果因为某种原因血红蛋白分子中的Fe2+被氧化成Fe3+,这种血红蛋白分子就会丧失载氧能力,使人体出现缺氧症状。
人体内的铁元素主要来源于食物。动物血、肝脏、骨髓以及蛋黄、菠菜、木耳、葡萄、红枣、大豆、芝麻等食物含有丰富的铁元素。研究结果显示,源自食物中的铁元素主要在小肠(尤其是十二指肠)内被吸收,并且人体只能吸收Fe2+。由于维生素C具有还原性,可以将Fe3+还原成Fe2+,所以食用维生素C含量较高的食物有利于人体对铁元素的吸收。对于健康的成年人来说,合理的膳食完全可以满足人体对铁元素的需求。儿童和孕期妇女因需要摄入较多的铁元素,可额外补充。
课本93页身边的化学
铁的多样性
第三课时铁及其化合物之间的转化关系
1.通过绘制铁及其化合物的价-类二维图,能用箭头标明铁及其化合物之间的物质转化关系;(重点)
2.通过应用Fe3+和Fe2+的检验方法,检验补铁剂中铁元素的价态;(重点)
3、通过认识一定条件下铁及其化合物可以互相转化,能总结出Fe、Fe2+、Fe3+间的相互转化关系的转化思路和方法。(难点)
【学习目标】
课本91页
目标一
活动 探究
补铁剂中铁元素价态的检验
铁元素在人体中起着重要的作用。如果人体缺铁,就会出现贫血症状。轻度缺铁性贫血可用饮食疗法治疗,严重缺铁时则需要服用补铁剂。
补铁口服液是常见的补铁剂,其中除了含有铁元素的物质外,还常添加抗氧化物质(如维生素C)、甜味剂、香精等。例如,某补铁口服液100mL中含铁元素20 30mg、维生素C200 300mg。
实验目的
检验某补铁口服液中铁元素的价态。
实验用品
某补铁口服液,H2SO4,NaOH溶液,酸性KmnO4溶液,氯水,KSCN溶液;试管,胶头滴管。
课本92页
实验方案设计及实施
实验步骤 实验现象
实验结论
取少量口服液于小试管中,滴入KSCN溶液,没有明显现象,滴加少量氯水
溶液变为血红色
口服液中铁元素为+2价
取少量口服液于小试管中,滴入酸性KMnO4溶液
KMnO4溶液紫色退去
口服液中铁元素为+2价
取少量口服液于小试管中,滴加NaOH溶液
先有白色沉淀生成迅速变灰绿最后变成红褐色
口服液中铁元素为+2价
课本92页
目标二
0
+3
+2
Fe2+
Fe(OH)2
Fe3+
Fe(OH)3
一、铁及其化合物之间的转化思路:
含有不同价态铁元素的物质之间的转化,可借助氧化还原反应实现。
含有相同价态铁元素的物质之间的转化,可借助复分解反应实现;
目标二
Fe
Fe3+
Fe2+
(1)化合价升高:反应物作还原剂,加氧化剂
强氧化剂
强氧化剂
弱氧化剂
二、Fe、Fe2+、Fe3+间的相互转化方法——铁三角
强氧化剂:O2、Cl2、Br2、HNO3、H2O2、酸性KMnO4等
弱氧化剂:I2、H+、Cu2+、Fe3+等
Fe
Fe3+
Fe2+
强还原剂
强还原剂
弱还原剂
(2)化合价降低:反应物作氧化剂,加还原剂
强还原剂:比铁活泼的金属单质如(Al、Zn等)
部分非金属单质C、CO、H2
弱还原剂:Fe、Cu、S2-等
Fe
Fe3+
Fe2+
弱氧化剂 H+、Cu2+、Fe3+
强氧化剂Cl2、O2、HNO3
Fe2O3:C、CO、H2、Al
Fe3+:Al、Zn等还原剂
Fe2+:Al、Zn等还原剂FeO:C、CO
强氧化剂:Cl2、O2、HNO3、H2O2等
Fe、Cu、S2-等还原剂
1.Fe、Fe2+、Fe3+间的相互转化关系——铁三角
学以致用
1、除去下列溶液中所含杂质
①FeCl2(FeCl3):
选用试剂________,
②FeCl3(FeCl2):
选用试剂________,
离子方程式:
______________________________;
Fe
Cl2
2Fe2++Cl2=2Fe3++2Cl-
H2O2
2Fe2++2H++H2O2=2Fe3++2H2O
当堂检测:
在亚铁盐溶液里加铁钉或铁粉防止溶液里的Fe2+
被氧化
2Fe3++Fe=3Fe2+
亚铁盐溶液保存
亚铁盐
0
+3
+2
盐
氢氧化物
氧化物
Fe2+
Fe(OH)2
FeO
Fe3+
Fe(OH)3
Fe2O3
Fe
单质
课本93页
B
1.“缺铁性贫血”中的铁是指( )
A.铁单质 B.铁元素
C.氧化铁 D.四氧化三铁
当堂检测:
2. 下列转化关系不能通过一步反应实现的是( )
A.Fe→FeCl2 B.Fe2O3→Fe(OH)3
C.FeCl3→FeCl2 D.Fe(OH)3→FeCl3
B
3.下列反应的离子方程式正确的是( )
A.Fe与FeCl3溶液反应:Fe+Fe3+===2Fe2+
B.Fe3O4与盐酸反应:Fe3O4+8H+===3Fe3++4H2O
C.Fe(OH)3与稀H2SO4反应:OH-+H+===H2O
D.Fe与CuSO4溶液反应:Fe+Cu2+===Cu+Fe2+
D
① ② ③ ④
将铁钉放入硫酸铜溶液中 向硫酸亚铁溶液 中滴入几滴氯水 将铜丝放入氯化铁溶液中 向FeCl2溶液中滴入KSCN溶液,无明显现象,再滴入氯水,变红
4.已知下述四个实验均能发生化学反应:
下列判断不正确的是( )
A.实验①中铁钉只做还原剂
B.实验②中Fe2+只显还原性
C.实验③中发生的是置换反应
D.上述实验证明:氧化性:Fe3+>Cu2+>Fe2+,Fe2+遇KSCN溶液无红色物质生成
C
