2.3.4 溶解性 分子的手性 课件(19张)2022-2023学年高二化学人教版(2019)选择性必修2
文档属性
| 名称 | 2.3.4 溶解性 分子的手性 课件(19张)2022-2023学年高二化学人教版(2019)选择性必修2 |

|
|
| 格式 | pptx | ||
| 文件大小 | 9.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-23 00:00:00 | ||
图片预览




文档简介
(共19张PPT)
第二章 分子结构与性质
Autumn
第三节 分子结构与物质的性质
第4课时 溶解性+分子的手性
青蒿素的提取
《肘后备急方》:“青蒿一握,以水二升渍,绞取汁,尽服之”。
屠呦呦团队先后经历了用水、乙醇、乙醚提取青蒿素的过程,最终用乙醚在低温下成功提取了青蒿素,治疗疟疾,挽救了无数人的生命。
为什么需要用乙醚来提取青蒿素,用水不可以呢?
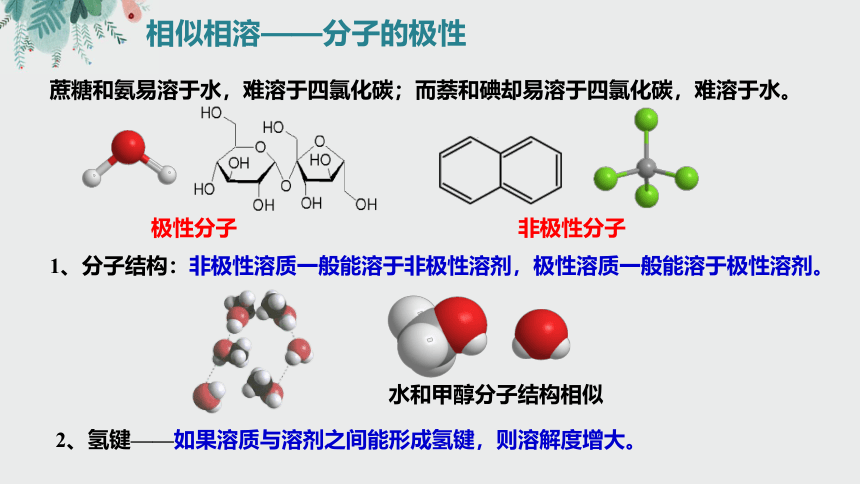
相似相溶——分子的极性
蔗糖和氨易溶于水,难溶于四氯化碳;而萘和碘却易溶于四氯化碳,难溶于水。
极性分子
非极性分子
1、分子结构:非极性溶质一般能溶于非极性溶剂,极性溶质一般能溶于极性溶剂。
水和甲醇分子结构相似
2、氢键——如果溶质与溶剂之间能形成氢键,则溶解度增大。
思考与讨论
分析表中数据,解释溶解度变化规律
名称 甲醇 乙醇 1-丙醇 1-丁醇 1-戊醇
溶解度/g ∞ ∞ ∞ 0.11 0.030
某些物质在293 K,100 g水中的溶解度
相似相溶还适用于分子结构的相似性。C2H5OH中的—OH和H2O中的—OH相近,因而乙醇能与水互溶。戊醇(CH3CH2CH2CH2CH2OH)中的烃基较大,其中的—OH跟水分子的—OH的相似因素小得多了,因而它在水中的溶解度明显减小。
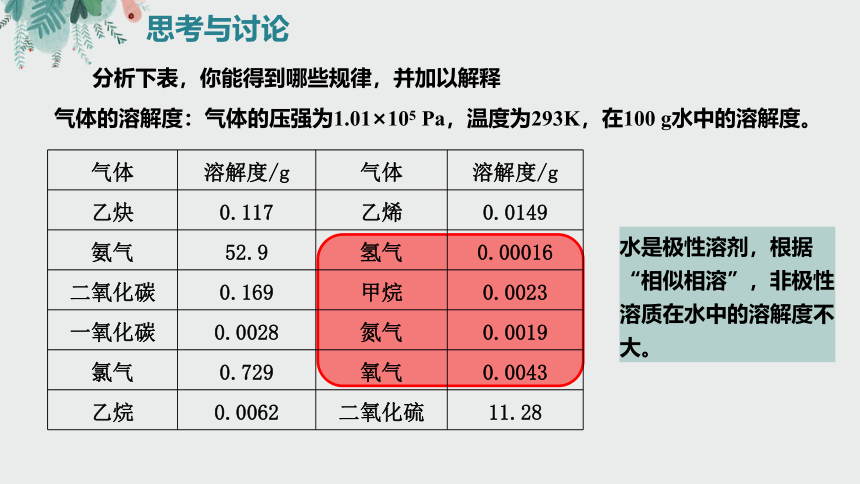
分析下表,你能得到哪些规律,并加以解释
气体的溶解度:气体的压强为1.01×105 Pa,温度为293K,在100 g水中的溶解度。
水是极性溶剂,根据“相似相溶”,非极性溶质在水中的溶解度不大。
气体 溶解度/g 气体 溶解度/g
乙炔 0.117 乙烯 0.0149
氨气 52.9 氢气 0.00016
二氧化碳 0.169 甲烷 0.0023
一氧化碳 0.0028 氮气 0.0019
氯气 0.729 氧气 0.0043
乙烷 0.0062 二氧化硫 11.28
思考与讨论
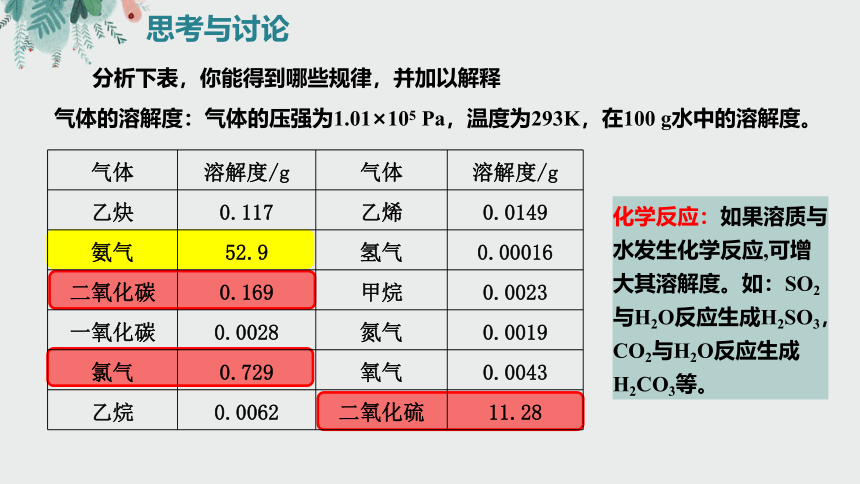
分析下表,你能得到哪些规律,并加以解释
气体的溶解度:气体的压强为1.01×105 Pa,温度为293K,在100 g水中的溶解度。
化学反应:如果溶质与水发生化学反应,可增大其溶解度。如:SO2与H2O反应生成H2SO3,CO2与H2O反应生成H2CO3等。
气体 溶解度/g 气体 溶解度/g
乙炔 0.117 乙烯 0.0149
氨气 52.9 氢气 0.00016
二氧化碳 0.169 甲烷 0.0023
一氧化碳 0.0028 氮气 0.0019
氯气 0.729 氧气 0.0043
乙烷 0.0062 二氧化硫 11.28
思考与讨论
在一个小试管里放入一小粒碘晶体,加入约5 mL蒸馏水,观察碘在水中的溶解性(若有不溶的碘,可将碘水溶液倾倒在另一个试管里继续下面的实验)。在碘水溶液中加入约1 mL四氯化碳(CCl4),振荡试管,观察碘被四氯化碳萃取,形成紫红色的碘的四氯化碳溶液。再向试管里加入1 mL浓碘化钾(KI)水溶液,振荡试管,溶液紫色变浅,这是由于在水溶液里可发生如下反应:I2+I- I3-。
加入 CCl4
加入 KI 溶液
振荡
振荡
I2 溶于水中
溶液呈黄色
溶液分层,下层
溶液呈紫红色
溶液分层,
下层溶液紫红色变浅
思考与讨论
在一个小试管里放入一小粒碘晶体,加入约5 mL蒸馏水,观察碘在水中的溶解性(若有不溶的碘,可将碘水溶液倾倒在另一个试管里继续下面的实验)。在碘水溶液中加入约1 mL四氯化碳(CCl4),振荡试管,观察碘被四氯化碳萃取,形成紫红色的碘的四氯化碳溶液。再向试管里加入1 mL浓碘化钾(KI)水溶液,振荡试管,溶液紫色变浅,这是由于在水溶液里可发生如下反应:I2+I- I3-。
思考与讨论
思考:1、CCl4与水为什么分层?
2、I2为什么从水中转移到CCl4中?
极性分子
非极性分子
自然界中生命体的对称美
思考:你的左右手能够完全重叠么?
1.手性异构体:具有完全相同的组成和原子排列的一对分子,如同左手和右手一样互为镜像,却在三维空间里不能重叠,互称手性异构体(或对映异构体)。
分子的手性
2.手性分子:有手性异构体的分子叫做手性分子。
手性分子在生命科学和药物生产方面有广泛的应用。对于手性药物,一个异构体可能是有效的,而另一个异构体可能是无效甚至是有害的。
镜面
CHFClBr
互为镜像关系的分子不能叠合,不是同种分子
绕轴旋转
不能叠合
手性分子的形成条件
CH2ClBr
手性分子的形成条件
绕轴旋转
能叠合
互为镜像关系的分子能叠合,是同种分子
手性分子的形成条件
同一个碳原子上连有四个不同的原子(基团)
互为镜像的分子在三维空间里不能叠合
互为手性异构体
R1
R3
R2
R4
*
*
*
*
酒石酸
乳酸
镜面
后续更多的研究表明,除了手性碳原子可以产生手性异构。含手性碳原子的单环化合物也可以产生手性异构,例如1,2-二氯环丙烷具有两种同分异构体。
*
含手性轴的化合物也可以产生手性异构。例如丙二烯的中的两个派键平面成直角时,以三个碳的连线为手性轴,可形成一对手性异构体。
手性分子的应用
2001年,诺贝尔化学奖授予三位用手性催化剂生产手性药物的化学家。用他们的合成方法,可以只得到一种或者主要只得到一种手性分子,不得到或者基本上不得到它的手性异构分子,这种独特的合成方法称为手性合成。手性合成的药物生产造福人类并带来巨大的经济效益。
催化剂
催化剂
不产生不匹配的手性产物
合成匹配的手性产物
手性催化剂只催化或者主要催化一种手性分子的合成,可以比喻成握手——手性催化剂像迎宾的主人伸出右手,被催化合成的手性分子像客人,总是伸出右手去握。
课堂评价
2、下列现象不能用“相似相溶”规律解释的是 ( )
A. 氯化氢易溶于水 B. 氯气易溶于NaOH溶液
C. 碘易溶于CCl4 D. 酒精易溶于水
1、已知 O3 的空间结构为 V 形,分子中正电中心和负电中心不重合,则下列关 于 O3 和 O2 在水中的溶解度叙述正确的是( )
A. O3 在水中的溶解度和 O2 一样
B. O3 在水中的溶解度比 O2 小
C. O3 在水中的溶解度比 O2 大
D. 无法比较
C
B
课堂评价
3、下列物质的分子中不具有手性碳原子的是( )
A. B . H2N CH2 COOH
C. CH2OH CH(OH) CHO D. CH3 CH(NH2) COOH
OH
CHCH3
B
4、莽草酸的结构简式如图所示(分子中只有C、H、O三种原子)。 其分子中手性碳原子的个数为( )
A.1 B.2 C.3 D.4
C
第二章 分子结构与性质
Autumn
第三节 分子结构与物质的性质
第4课时 溶解性+分子的手性
青蒿素的提取
《肘后备急方》:“青蒿一握,以水二升渍,绞取汁,尽服之”。
屠呦呦团队先后经历了用水、乙醇、乙醚提取青蒿素的过程,最终用乙醚在低温下成功提取了青蒿素,治疗疟疾,挽救了无数人的生命。
为什么需要用乙醚来提取青蒿素,用水不可以呢?
相似相溶——分子的极性
蔗糖和氨易溶于水,难溶于四氯化碳;而萘和碘却易溶于四氯化碳,难溶于水。
极性分子
非极性分子
1、分子结构:非极性溶质一般能溶于非极性溶剂,极性溶质一般能溶于极性溶剂。
水和甲醇分子结构相似
2、氢键——如果溶质与溶剂之间能形成氢键,则溶解度增大。
思考与讨论
分析表中数据,解释溶解度变化规律
名称 甲醇 乙醇 1-丙醇 1-丁醇 1-戊醇
溶解度/g ∞ ∞ ∞ 0.11 0.030
某些物质在293 K,100 g水中的溶解度
相似相溶还适用于分子结构的相似性。C2H5OH中的—OH和H2O中的—OH相近,因而乙醇能与水互溶。戊醇(CH3CH2CH2CH2CH2OH)中的烃基较大,其中的—OH跟水分子的—OH的相似因素小得多了,因而它在水中的溶解度明显减小。
分析下表,你能得到哪些规律,并加以解释
气体的溶解度:气体的压强为1.01×105 Pa,温度为293K,在100 g水中的溶解度。
水是极性溶剂,根据“相似相溶”,非极性溶质在水中的溶解度不大。
气体 溶解度/g 气体 溶解度/g
乙炔 0.117 乙烯 0.0149
氨气 52.9 氢气 0.00016
二氧化碳 0.169 甲烷 0.0023
一氧化碳 0.0028 氮气 0.0019
氯气 0.729 氧气 0.0043
乙烷 0.0062 二氧化硫 11.28
思考与讨论
分析下表,你能得到哪些规律,并加以解释
气体的溶解度:气体的压强为1.01×105 Pa,温度为293K,在100 g水中的溶解度。
化学反应:如果溶质与水发生化学反应,可增大其溶解度。如:SO2与H2O反应生成H2SO3,CO2与H2O反应生成H2CO3等。
气体 溶解度/g 气体 溶解度/g
乙炔 0.117 乙烯 0.0149
氨气 52.9 氢气 0.00016
二氧化碳 0.169 甲烷 0.0023
一氧化碳 0.0028 氮气 0.0019
氯气 0.729 氧气 0.0043
乙烷 0.0062 二氧化硫 11.28
思考与讨论
在一个小试管里放入一小粒碘晶体,加入约5 mL蒸馏水,观察碘在水中的溶解性(若有不溶的碘,可将碘水溶液倾倒在另一个试管里继续下面的实验)。在碘水溶液中加入约1 mL四氯化碳(CCl4),振荡试管,观察碘被四氯化碳萃取,形成紫红色的碘的四氯化碳溶液。再向试管里加入1 mL浓碘化钾(KI)水溶液,振荡试管,溶液紫色变浅,这是由于在水溶液里可发生如下反应:I2+I- I3-。
加入 CCl4
加入 KI 溶液
振荡
振荡
I2 溶于水中
溶液呈黄色
溶液分层,下层
溶液呈紫红色
溶液分层,
下层溶液紫红色变浅
思考与讨论
在一个小试管里放入一小粒碘晶体,加入约5 mL蒸馏水,观察碘在水中的溶解性(若有不溶的碘,可将碘水溶液倾倒在另一个试管里继续下面的实验)。在碘水溶液中加入约1 mL四氯化碳(CCl4),振荡试管,观察碘被四氯化碳萃取,形成紫红色的碘的四氯化碳溶液。再向试管里加入1 mL浓碘化钾(KI)水溶液,振荡试管,溶液紫色变浅,这是由于在水溶液里可发生如下反应:I2+I- I3-。
思考与讨论
思考:1、CCl4与水为什么分层?
2、I2为什么从水中转移到CCl4中?
极性分子
非极性分子
自然界中生命体的对称美
思考:你的左右手能够完全重叠么?
1.手性异构体:具有完全相同的组成和原子排列的一对分子,如同左手和右手一样互为镜像,却在三维空间里不能重叠,互称手性异构体(或对映异构体)。
分子的手性
2.手性分子:有手性异构体的分子叫做手性分子。
手性分子在生命科学和药物生产方面有广泛的应用。对于手性药物,一个异构体可能是有效的,而另一个异构体可能是无效甚至是有害的。
镜面
CHFClBr
互为镜像关系的分子不能叠合,不是同种分子
绕轴旋转
不能叠合
手性分子的形成条件
CH2ClBr
手性分子的形成条件
绕轴旋转
能叠合
互为镜像关系的分子能叠合,是同种分子
手性分子的形成条件
同一个碳原子上连有四个不同的原子(基团)
互为镜像的分子在三维空间里不能叠合
互为手性异构体
R1
R3
R2
R4
*
*
*
*
酒石酸
乳酸
镜面
后续更多的研究表明,除了手性碳原子可以产生手性异构。含手性碳原子的单环化合物也可以产生手性异构,例如1,2-二氯环丙烷具有两种同分异构体。
*
含手性轴的化合物也可以产生手性异构。例如丙二烯的中的两个派键平面成直角时,以三个碳的连线为手性轴,可形成一对手性异构体。
手性分子的应用
2001年,诺贝尔化学奖授予三位用手性催化剂生产手性药物的化学家。用他们的合成方法,可以只得到一种或者主要只得到一种手性分子,不得到或者基本上不得到它的手性异构分子,这种独特的合成方法称为手性合成。手性合成的药物生产造福人类并带来巨大的经济效益。
催化剂
催化剂
不产生不匹配的手性产物
合成匹配的手性产物
手性催化剂只催化或者主要催化一种手性分子的合成,可以比喻成握手——手性催化剂像迎宾的主人伸出右手,被催化合成的手性分子像客人,总是伸出右手去握。
课堂评价
2、下列现象不能用“相似相溶”规律解释的是 ( )
A. 氯化氢易溶于水 B. 氯气易溶于NaOH溶液
C. 碘易溶于CCl4 D. 酒精易溶于水
1、已知 O3 的空间结构为 V 形,分子中正电中心和负电中心不重合,则下列关 于 O3 和 O2 在水中的溶解度叙述正确的是( )
A. O3 在水中的溶解度和 O2 一样
B. O3 在水中的溶解度比 O2 小
C. O3 在水中的溶解度比 O2 大
D. 无法比较
C
B
课堂评价
3、下列物质的分子中不具有手性碳原子的是( )
A. B . H2N CH2 COOH
C. CH2OH CH(OH) CHO D. CH3 CH(NH2) COOH
OH
CHCH3
B
4、莽草酸的结构简式如图所示(分子中只有C、H、O三种原子)。 其分子中手性碳原子的个数为( )
A.1 B.2 C.3 D.4
C
