3.2.1自然界中的硫 课件(17张)2023-2024学年高一上学期化学鲁科版(2019)必修第一册
文档属性
| 名称 | 3.2.1自然界中的硫 课件(17张)2023-2024学年高一上学期化学鲁科版(2019)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 16.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-23 00:00:00 | ||
图片预览




文档简介
(共17张PPT)
在哥伦比亚东部的普莱斯火山地区,有一条河,全长580多公里,河里鱼虾绝迹,两岸寸草不生。要是哪个不知天高地厚的人喝一口那河里的水,便会高热眩晕,口舌溃烂,五脏俱损甚至死亡。如果有人想到河里去游泳,过不了多久,就会皮开肉绽,一命呜呼,甚至连块骨头也留不下。这条河就是堪称世界五大奇河之一的“雷欧维拉力河”,当地人称它为“谋杀河” !!!
你知道吗
?
第2节 硫的转化
第一课时 自然界中的硫
第3章 物质的性质与转化
1.通过阅读课本97-98页,能说出硫元素在物质中具有不同的价态,并学会从“价—类”二维图的角度分析不同价态硫元素的物质之间的相互转化。
2.通过实验探究,能说出硫的主要性质,并会书写相关的化学方程式。(重难点)
学习目标
SO3
SO2
S
H2S
地下
雌黄
H2S
H2SO4
H2SO3
石膏(CaSO4·2H2O)
芒硝(Na2SO4·10H2O)
地表
O2
H2O
微生物
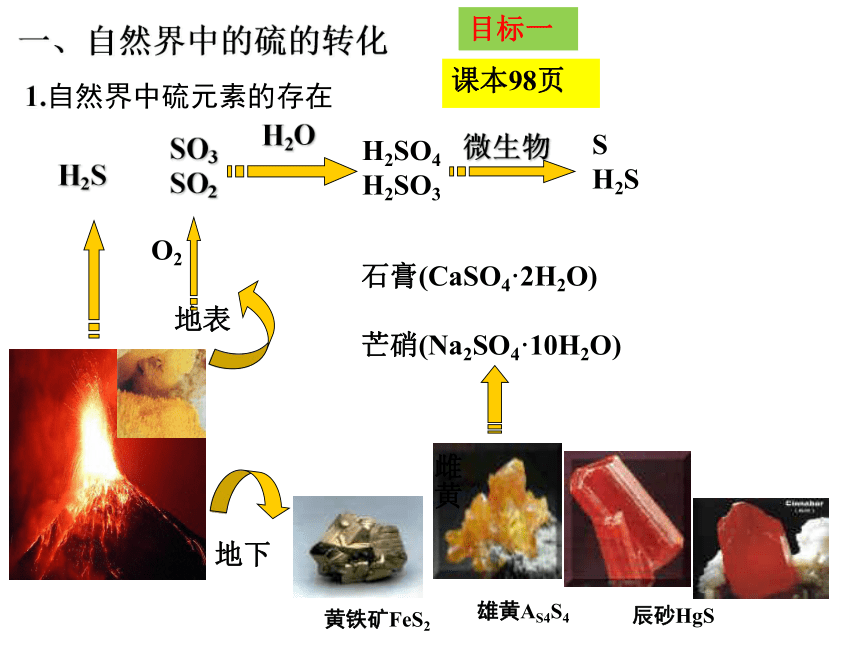
一、自然界中的硫的转化
1.自然界中硫元素的存在
目标一
课本98页
黄铁矿FeS2
辰砂HgS
雄黄AS4S4
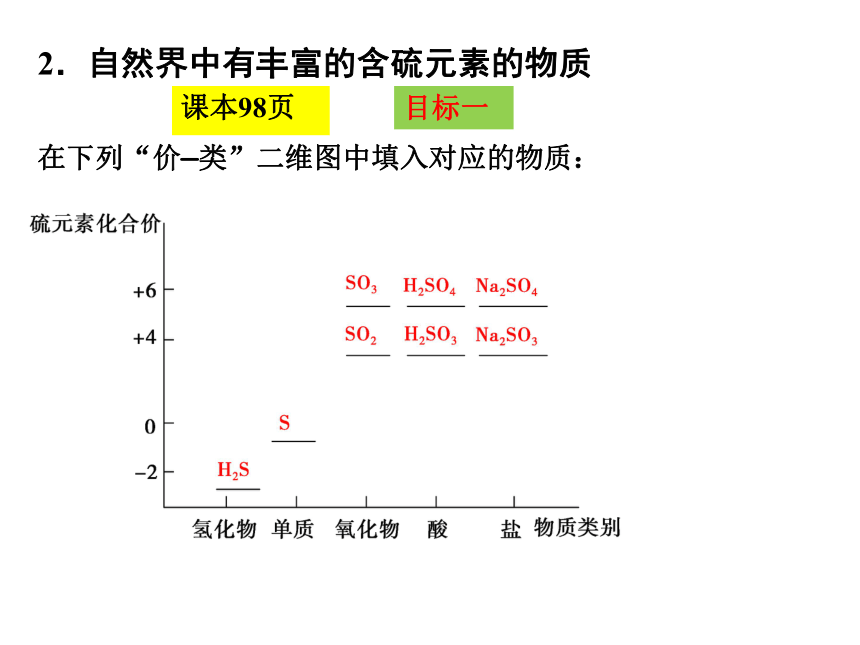
2.自然界中有丰富的含硫元素的物质
在下列“价—类”二维图中填入对应的物质:
目标一
课本98页
1、一种黄色或淡黄色的固体
4、很脆,易研成粉末
3、熔点和沸点都不高
2、不溶于水,微溶于酒 精,易溶于二硫化碳
探究一:硫的物理性质
二、认识硫单质
目标二
课本100页
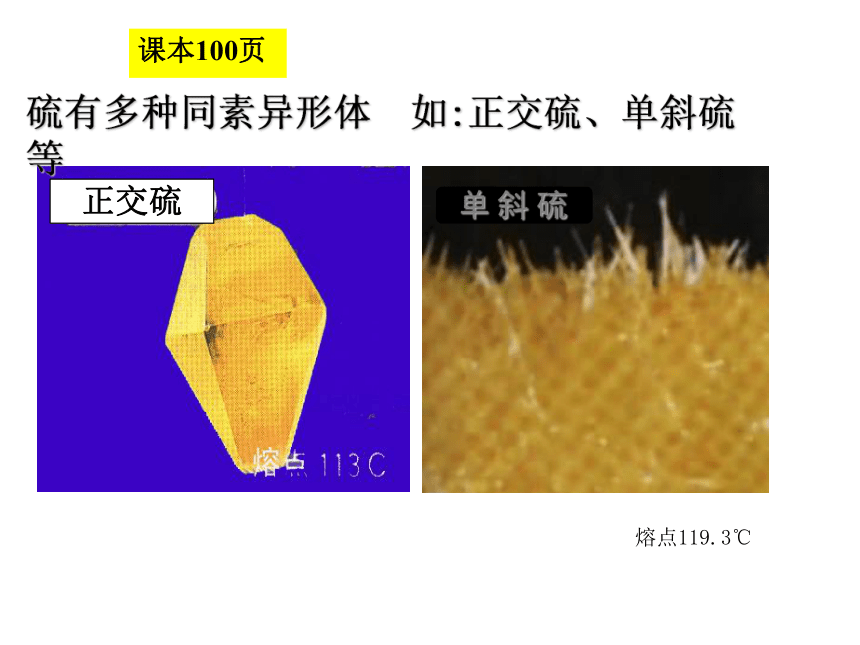
单 斜 硫
熔点119.3℃
硫有多种同素异形体 如:正交硫、单斜硫等
正交硫
课本100页
探究二:硫的化学性质
2、从物质类别的角度,预测硫单质可能与哪几类物质反应?
1、硫元素常见的化合价有哪些?从化合价的角度推测,硫具有怎样的化学性质?
目标二
课本99页
实验操作 实验现象 结论及化学方程式
实验一 把研细的硫粉和铁粉按一定比例混合均匀,在石棉网上堆成“FeS”的形状,用红热的玻璃棒触及一端
实验二 取少量硫粉放入燃烧匙中,在酒精灯火焰上加热至硫粉熔化并燃烧,迅速伸入盛满氧气的集气瓶(底部有少量水)中
混合物一端红热,直到整个混合物红热,结成黑色块状“FeS”
发出明亮的蓝紫色火焰,放出大量的热,生成一种有刺激性气味的气体
观察·思考
Fe + S = FeS
△
+2
S + O2 = SO2
点燃
0
+4
硫具还原性
硫具氧化性
-2
0
目标二
课本99页
[讨论]硫和氯气都能分别与铜、铁反应,试比较反应有何异同。
结论:氯气的氧化性比硫强
Fe + S = FeS
△
+2
Cu + Cl2 = CuCl2
点燃
2Fe + 3Cl2 = 2FeCl3
△
生成高价的金属氯化物
+2
+3
1、硫与金属的反应
△
2Cu + S = Cu2S
生成低价的金属硫化物
+1
目标二
课本100页
2、硫与非金属的反应
S + O2 = SO2
点燃
0
+4
硫作为还原剂
具还原性
H2 + S = H2S
△
C + 2S = CS2
高温
0
-2
-2
0
硫作为氧化剂,具氧化性。
划火柴时常闻到的一股呛鼻的气味,就是火柴头成份中的硫燃烧后产生的二氧化硫。
硫在氧气中燃烧
目标二
课本100页
1. 判断正误
(1)S在O2中燃烧时,若O2不足,则生成SO2;若O2过量,则生成SO3( )
(2)清洗内壁粘有硫的试管时,先用CS2溶解,再用清水冲洗即可( )
(3)斜方硫和单斜硫属于同一种物质。( )
(4)1 mol铁粉与足量硫粉充分反应时转移3NA个电子。( )
(5)硫属于非金属元素,在反应时只有氧化性。( )
(6)氧化性:S>Cl。( )
×
√
【当堂检测】
×
×
×
×
目标二
长白山温泉
广东从化温泉
1、“硫磺”温泉可以医治皮肤病
畅所欲言
你能说出硫在生产、生活中的应用吗
课本100页
2、制造火药,烟花爆竹
S + 2KNO3 + 3C == K2S + 3CO2↑+ N2↑
点燃
3.轮胎、胶管等橡胶制品
4、制造硫酸、化肥、火柴、杀虫剂等
课本100页
课堂小结
【当堂检测】
1.分析 :3S+6KOH == 2K2S+K2SO3+3H2O
氧化剂是 还原剂是 氧化产物是
还原产物
2.下列化合物不能用相应元素的单质直接化合生成的是( )
①CuS ②FeS ③Al2S3 ④Fe2S3 ⑤Cu2S
⑥FeCl2 ⑦H2S ⑧SO3
A.②⑤⑦ B.①④⑥⑧
C.③④ D.④⑥⑧
S
S
K2SO3
K2S
B
目标二
在哥伦比亚东部的普莱斯火山地区,有一条河,全长580多公里,河里鱼虾绝迹,两岸寸草不生。要是哪个不知天高地厚的人喝一口那河里的水,便会高热眩晕,口舌溃烂,五脏俱损甚至死亡。如果有人想到河里去游泳,过不了多久,就会皮开肉绽,一命呜呼,甚至连块骨头也留不下。这条河就是堪称世界五大奇河之一的“雷欧维拉力河”,当地人称它为“谋杀河” !!!
你知道吗
?
第2节 硫的转化
第一课时 自然界中的硫
第3章 物质的性质与转化
1.通过阅读课本97-98页,能说出硫元素在物质中具有不同的价态,并学会从“价—类”二维图的角度分析不同价态硫元素的物质之间的相互转化。
2.通过实验探究,能说出硫的主要性质,并会书写相关的化学方程式。(重难点)
学习目标
SO3
SO2
S
H2S
地下
雌黄
H2S
H2SO4
H2SO3
石膏(CaSO4·2H2O)
芒硝(Na2SO4·10H2O)
地表
O2
H2O
微生物
一、自然界中的硫的转化
1.自然界中硫元素的存在
目标一
课本98页
黄铁矿FeS2
辰砂HgS
雄黄AS4S4
2.自然界中有丰富的含硫元素的物质
在下列“价—类”二维图中填入对应的物质:
目标一
课本98页
1、一种黄色或淡黄色的固体
4、很脆,易研成粉末
3、熔点和沸点都不高
2、不溶于水,微溶于酒 精,易溶于二硫化碳
探究一:硫的物理性质
二、认识硫单质
目标二
课本100页
单 斜 硫
熔点119.3℃
硫有多种同素异形体 如:正交硫、单斜硫等
正交硫
课本100页
探究二:硫的化学性质
2、从物质类别的角度,预测硫单质可能与哪几类物质反应?
1、硫元素常见的化合价有哪些?从化合价的角度推测,硫具有怎样的化学性质?
目标二
课本99页
实验操作 实验现象 结论及化学方程式
实验一 把研细的硫粉和铁粉按一定比例混合均匀,在石棉网上堆成“FeS”的形状,用红热的玻璃棒触及一端
实验二 取少量硫粉放入燃烧匙中,在酒精灯火焰上加热至硫粉熔化并燃烧,迅速伸入盛满氧气的集气瓶(底部有少量水)中
混合物一端红热,直到整个混合物红热,结成黑色块状“FeS”
发出明亮的蓝紫色火焰,放出大量的热,生成一种有刺激性气味的气体
观察·思考
Fe + S = FeS
△
+2
S + O2 = SO2
点燃
0
+4
硫具还原性
硫具氧化性
-2
0
目标二
课本99页
[讨论]硫和氯气都能分别与铜、铁反应,试比较反应有何异同。
结论:氯气的氧化性比硫强
Fe + S = FeS
△
+2
Cu + Cl2 = CuCl2
点燃
2Fe + 3Cl2 = 2FeCl3
△
生成高价的金属氯化物
+2
+3
1、硫与金属的反应
△
2Cu + S = Cu2S
生成低价的金属硫化物
+1
目标二
课本100页
2、硫与非金属的反应
S + O2 = SO2
点燃
0
+4
硫作为还原剂
具还原性
H2 + S = H2S
△
C + 2S = CS2
高温
0
-2
-2
0
硫作为氧化剂,具氧化性。
划火柴时常闻到的一股呛鼻的气味,就是火柴头成份中的硫燃烧后产生的二氧化硫。
硫在氧气中燃烧
目标二
课本100页
1. 判断正误
(1)S在O2中燃烧时,若O2不足,则生成SO2;若O2过量,则生成SO3( )
(2)清洗内壁粘有硫的试管时,先用CS2溶解,再用清水冲洗即可( )
(3)斜方硫和单斜硫属于同一种物质。( )
(4)1 mol铁粉与足量硫粉充分反应时转移3NA个电子。( )
(5)硫属于非金属元素,在反应时只有氧化性。( )
(6)氧化性:S>Cl。( )
×
√
【当堂检测】
×
×
×
×
目标二
长白山温泉
广东从化温泉
1、“硫磺”温泉可以医治皮肤病
畅所欲言
你能说出硫在生产、生活中的应用吗
课本100页
2、制造火药,烟花爆竹
S + 2KNO3 + 3C == K2S + 3CO2↑+ N2↑
点燃
3.轮胎、胶管等橡胶制品
4、制造硫酸、化肥、火柴、杀虫剂等
课本100页
课堂小结
【当堂检测】
1.分析 :3S+6KOH == 2K2S+K2SO3+3H2O
氧化剂是 还原剂是 氧化产物是
还原产物
2.下列化合物不能用相应元素的单质直接化合生成的是( )
①CuS ②FeS ③Al2S3 ④Fe2S3 ⑤Cu2S
⑥FeCl2 ⑦H2S ⑧SO3
A.②⑤⑦ B.①④⑥⑧
C.③④ D.④⑥⑧
S
S
K2SO3
K2S
B
目标二
