3.3.3硝酸 课件(20张)2023-2024学年高一上学期化学鲁科版(2019)必修第一册
文档属性
| 名称 | 3.3.3硝酸 课件(20张)2023-2024学年高一上学期化学鲁科版(2019)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-23 00:00:00 | ||
图片预览








文档简介
(共20张PPT)
引入
9月18日上午,一辆装载了12吨质量分数为63%的
浓硝酸的铁槽车发生严重液体泄漏事故,一瞬间看到车
辆周围升起一团白雾,刺鼻的气味扑面而来……
还不停地冒出浓浓的红棕色的“雾”……
事件中体现了浓硝酸具有哪些性质?
第3课时 硝酸 人类活动对氮循环
和环境的影响
学习目标
1.通过阅读课本119页和实验探究,能说出硝酸的
物理和化学性质,并能写出相关反应的方程式;(重难点)
2.通过学习硝酸的用途以及人类活动对氮循环和环境的
影响,增强节约资源、保护环境的可持续发展的意识。
市售浓硝酸的质量分数为68%-70%。95%以上的浓硝酸称为“发烟硝酸”。
一、硝酸的物理性质
“雾”:硝酸与空气中的水形成的小液滴
颜色状态 气味 挥发性 溶解性
无色液体
刺激性气味
易挥发
低沸点(83℃)
与水任意比互溶
课本119
目标一
1、不稳定性: 见光或受热分解
4HNO3 4NO2↑+ O2↑ + 2H2O
见光或受热
二、硝酸的化学性质
硝酸越浓越易分解
如何保存硝酸?
放在带有玻璃塞的棕色细口瓶中密封保存,并放置于阴凉处!
硝酸分解产生的NO2溶于硝酸中,使得溶液发黄!
久置硝酸为什么会发黄?
目标一
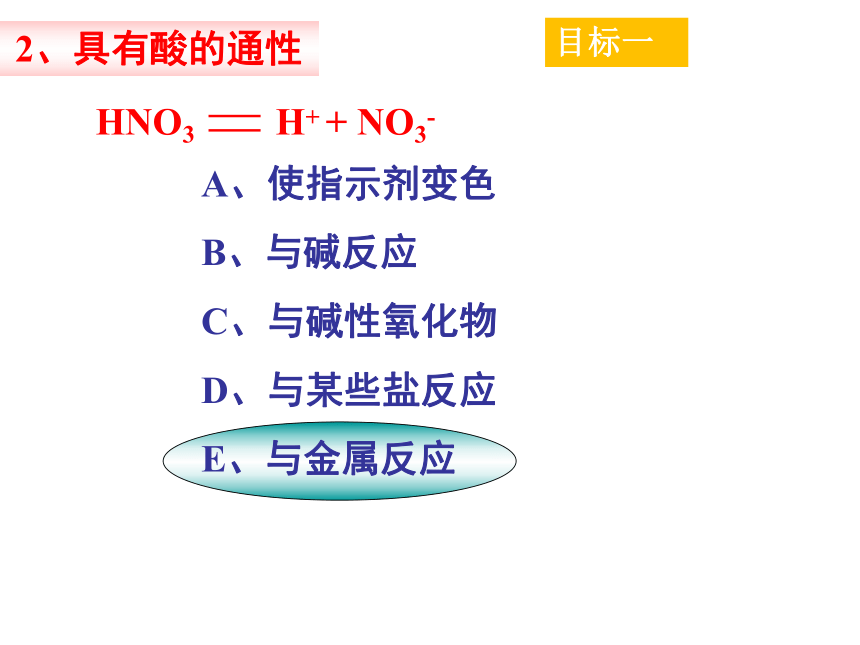
A、使指示剂变色
B、与碱反应
C、与碱性氧化物
D、与某些盐反应
E、与金属反应
2、具有酸的通性
HNO3 H+ + NO3-
目标一
实验:铜与浓、稀硝酸的反应
反应物 现象
Cu+浓HNO3
Cu+稀HNO3
反应剧烈,铜片溶解,溶液变为绿色,生成红棕色气体
反应慢,铜片溶解,溶液变为蓝色,生成无色气体,遇到空气变为红棕色。
Cu+ 4HNO3(浓) = Cu(NO3)2 + 2NO2↑+2H2O
3Cu+8HNO3(稀) = 3Cu(NO3)2+ 2NO↑+ 4H2O
HNO3的作用?
酸性 与 氧化性
3、强氧化性
(1)与金属反应
实验:铁与浓、稀硝酸的反应
反应物 现象
Fe+浓HNO3
Fe+稀HNO3
试管中有无色气体产生
最初反应剧烈,生成红棕色气体。
后来反应停止。
常温下,浓硝酸使铁、铝等金属表面形成致密的氧化膜而钝化。
可以用铁质或铝制容器盛放冷的浓硝酸。
Fe+4HNO3(稀)===Fe(NO3)3+NO↑+2H2O
酸性 与 氧化性
气体遇空气变红棕色
1. 硝酸具有强氧化性,能与除金、铂、钛以外的大多数金属反应。
2. 其还原产物与浓度有关。通常,浓硝酸被还原为NO2 ,稀硝酸被还原为NO。(极稀的硝酸还可能被还原为N2、NH4+) 。
反应不产生氢气。
3. 将变价金属氧化到最高价态。[如:Fe Fe(NO3)3];
4. 常温下,浓硝酸使铁、铝钝化。(加热可反应)
(1)与金属反应
CO2
H3PO4
H2SO4
+ NO2
C
P
S
+ HNO3(浓)
4HNO3(浓)+ C CO2 + 4NO2 + 2H2O
(2) 与非金属单质反应
HNO3的作用?
强氧化性
加热时,浓硝酸能与C、S等非金属单质发生反应,只表现氧化性。
目标一
课本120
硝酸具有强氧化性,所以Fe2+ 、S2-、I-、SO32-等一些还原性的物质不能与硝酸共存!
☆
NO3-在中性和碱性溶液中几乎与所有的离子能共存;
但在酸性溶液中,NO3-+H+具有强氧化性,与Fe2+、SO32-等不能共存!
☆
例:Fe2+
HNO3
Fe3+
SO32-
HNO3
SO42-
例:Fe(NO3)2能在溶液中稳定存在,但如果在溶液中加入盐酸,溶液将由浅绿色变为棕黄色。这说明Fe2+被NO3-/H+氧化成了Fe3+。
(3) 与一些还原性物质反应
目标一
1.下列反应的化学方程式正确的是( )
A.铁与稀硝酸反应:Fe+2HNO3==Fe(NO3)2+H2↑
B.稀硫酸与Ag反应:2Ag+H2SO4==Ag2SO4+H2↑
C.浓硝酸和碳酸钙反应:2HNO3+CaCO3==Ca(NO3)2+ CO2↑+H2O
D.稀硝酸和FeO反应:2HNO3+FeO==Fe(NO3)2+H2O
当堂检测
酸雨
光化学烟雾
1.含氮物质来源及对环境的影响
弊
利
三、人类活动对氮循环和环境的影响
目标二
课本121
酸 雨
酸雨的形成
2NO + O2= 2 NO2
3NO2 + H2O =2HNO3+ NO
酸雨是指PH小于5.6的雨雪或其他形式的降水。分为硝酸型酸雨和硫酸型酸雨。
目标二
光化学烟雾
汽车尾气中的氮氧化物(NXOY)与碳氢化合物在经紫外线照射发生化学反应形成的有毒的浅蓝色烟雾。
光化学烟雾有特殊气味,会刺激眼睛、伤害植物,并能降低大气能见度。
水体富营养化
悲哀的海豚
在人类活动的影响下,生物所需的氮、磷等营养物质大量进入湖泊、河湖、海湾等缓流水体,引起藻类“疯长”并覆盖在水面上,水体溶解氧量下降,水质恶化,鱼类及其他生物大量死亡。
水华
赤潮
2.减少人类活动对氮循环和环境影响的措施
一、物理性质
二、化学性质
1、不稳定性: 4HNO3======4NO2 ↑+O2 ↑+2H2O
2、酸的通性:HNO3=H++NO3-
3、强氧化性
(1)能与大多数的金属反应(铂、金除外)(酸性、强氧化性)
3Cu+8HNO3(稀)====3Cu(NO3)2+2NO↑ +4H2O
Cu+4HNO3(浓)====Cu(NO3)2+2NO2↑+2H2O
常温下铁、铝遇浓硝酸发生钝化现象。
(2)与非金属反应(强氧化性)
C+4HNO3(浓)====CO2↑+4NO2 ↑+2H2O
(3)与还原性离子反应:Fe2+、S2-、SO32-、I-
见光或受热
△
课堂小结
实验室常用铜与浓、稀硝酸的反应制取NO2和NO。
1.现有下列物质,其中必须保存在棕色试剂瓶里(见光分解)的是( )①氯水 ②氨水 ③浓硝酸 ④浓盐酸 ⑤烧碱A.①②③ B.①③④C.仅①③ D.②⑤
2.已知3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O,则下列说法不正确的是( )A.Cu做还原剂,HNO3做氧化剂B.HNO3在该反应中只有部分表现出了氧化性C.每生成22.4 L(标准状况)NO有3 mol的电子转移D.如果有8 mol HNO3被还原,则生成了2 mol NO
当堂检测
3.下列各组离子中,能在水溶液中大量共存的是( )A.Na+、Ag+、Cl-、CO32-B.Na+、Mg2+、Cl-、SO42-
C.K+、SO42-、NO3-、Ba2+D.Fe2+、H+、SO42-、NO3-
引入
9月18日上午,一辆装载了12吨质量分数为63%的
浓硝酸的铁槽车发生严重液体泄漏事故,一瞬间看到车
辆周围升起一团白雾,刺鼻的气味扑面而来……
还不停地冒出浓浓的红棕色的“雾”……
事件中体现了浓硝酸具有哪些性质?
第3课时 硝酸 人类活动对氮循环
和环境的影响
学习目标
1.通过阅读课本119页和实验探究,能说出硝酸的
物理和化学性质,并能写出相关反应的方程式;(重难点)
2.通过学习硝酸的用途以及人类活动对氮循环和环境的
影响,增强节约资源、保护环境的可持续发展的意识。
市售浓硝酸的质量分数为68%-70%。95%以上的浓硝酸称为“发烟硝酸”。
一、硝酸的物理性质
“雾”:硝酸与空气中的水形成的小液滴
颜色状态 气味 挥发性 溶解性
无色液体
刺激性气味
易挥发
低沸点(83℃)
与水任意比互溶
课本119
目标一
1、不稳定性: 见光或受热分解
4HNO3 4NO2↑+ O2↑ + 2H2O
见光或受热
二、硝酸的化学性质
硝酸越浓越易分解
如何保存硝酸?
放在带有玻璃塞的棕色细口瓶中密封保存,并放置于阴凉处!
硝酸分解产生的NO2溶于硝酸中,使得溶液发黄!
久置硝酸为什么会发黄?
目标一
A、使指示剂变色
B、与碱反应
C、与碱性氧化物
D、与某些盐反应
E、与金属反应
2、具有酸的通性
HNO3 H+ + NO3-
目标一
实验:铜与浓、稀硝酸的反应
反应物 现象
Cu+浓HNO3
Cu+稀HNO3
反应剧烈,铜片溶解,溶液变为绿色,生成红棕色气体
反应慢,铜片溶解,溶液变为蓝色,生成无色气体,遇到空气变为红棕色。
Cu+ 4HNO3(浓) = Cu(NO3)2 + 2NO2↑+2H2O
3Cu+8HNO3(稀) = 3Cu(NO3)2+ 2NO↑+ 4H2O
HNO3的作用?
酸性 与 氧化性
3、强氧化性
(1)与金属反应
实验:铁与浓、稀硝酸的反应
反应物 现象
Fe+浓HNO3
Fe+稀HNO3
试管中有无色气体产生
最初反应剧烈,生成红棕色气体。
后来反应停止。
常温下,浓硝酸使铁、铝等金属表面形成致密的氧化膜而钝化。
可以用铁质或铝制容器盛放冷的浓硝酸。
Fe+4HNO3(稀)===Fe(NO3)3+NO↑+2H2O
酸性 与 氧化性
气体遇空气变红棕色
1. 硝酸具有强氧化性,能与除金、铂、钛以外的大多数金属反应。
2. 其还原产物与浓度有关。通常,浓硝酸被还原为NO2 ,稀硝酸被还原为NO。(极稀的硝酸还可能被还原为N2、NH4+) 。
反应不产生氢气。
3. 将变价金属氧化到最高价态。[如:Fe Fe(NO3)3];
4. 常温下,浓硝酸使铁、铝钝化。(加热可反应)
(1)与金属反应
CO2
H3PO4
H2SO4
+ NO2
C
P
S
+ HNO3(浓)
4HNO3(浓)+ C CO2 + 4NO2 + 2H2O
(2) 与非金属单质反应
HNO3的作用?
强氧化性
加热时,浓硝酸能与C、S等非金属单质发生反应,只表现氧化性。
目标一
课本120
硝酸具有强氧化性,所以Fe2+ 、S2-、I-、SO32-等一些还原性的物质不能与硝酸共存!
☆
NO3-在中性和碱性溶液中几乎与所有的离子能共存;
但在酸性溶液中,NO3-+H+具有强氧化性,与Fe2+、SO32-等不能共存!
☆
例:Fe2+
HNO3
Fe3+
SO32-
HNO3
SO42-
例:Fe(NO3)2能在溶液中稳定存在,但如果在溶液中加入盐酸,溶液将由浅绿色变为棕黄色。这说明Fe2+被NO3-/H+氧化成了Fe3+。
(3) 与一些还原性物质反应
目标一
1.下列反应的化学方程式正确的是( )
A.铁与稀硝酸反应:Fe+2HNO3==Fe(NO3)2+H2↑
B.稀硫酸与Ag反应:2Ag+H2SO4==Ag2SO4+H2↑
C.浓硝酸和碳酸钙反应:2HNO3+CaCO3==Ca(NO3)2+ CO2↑+H2O
D.稀硝酸和FeO反应:2HNO3+FeO==Fe(NO3)2+H2O
当堂检测
酸雨
光化学烟雾
1.含氮物质来源及对环境的影响
弊
利
三、人类活动对氮循环和环境的影响
目标二
课本121
酸 雨
酸雨的形成
2NO + O2= 2 NO2
3NO2 + H2O =2HNO3+ NO
酸雨是指PH小于5.6的雨雪或其他形式的降水。分为硝酸型酸雨和硫酸型酸雨。
目标二
光化学烟雾
汽车尾气中的氮氧化物(NXOY)与碳氢化合物在经紫外线照射发生化学反应形成的有毒的浅蓝色烟雾。
光化学烟雾有特殊气味,会刺激眼睛、伤害植物,并能降低大气能见度。
水体富营养化
悲哀的海豚
在人类活动的影响下,生物所需的氮、磷等营养物质大量进入湖泊、河湖、海湾等缓流水体,引起藻类“疯长”并覆盖在水面上,水体溶解氧量下降,水质恶化,鱼类及其他生物大量死亡。
水华
赤潮
2.减少人类活动对氮循环和环境影响的措施
一、物理性质
二、化学性质
1、不稳定性: 4HNO3======4NO2 ↑+O2 ↑+2H2O
2、酸的通性:HNO3=H++NO3-
3、强氧化性
(1)能与大多数的金属反应(铂、金除外)(酸性、强氧化性)
3Cu+8HNO3(稀)====3Cu(NO3)2+2NO↑ +4H2O
Cu+4HNO3(浓)====Cu(NO3)2+2NO2↑+2H2O
常温下铁、铝遇浓硝酸发生钝化现象。
(2)与非金属反应(强氧化性)
C+4HNO3(浓)====CO2↑+4NO2 ↑+2H2O
(3)与还原性离子反应:Fe2+、S2-、SO32-、I-
见光或受热
△
课堂小结
实验室常用铜与浓、稀硝酸的反应制取NO2和NO。
1.现有下列物质,其中必须保存在棕色试剂瓶里(见光分解)的是( )①氯水 ②氨水 ③浓硝酸 ④浓盐酸 ⑤烧碱A.①②③ B.①③④C.仅①③ D.②⑤
2.已知3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O,则下列说法不正确的是( )A.Cu做还原剂,HNO3做氧化剂B.HNO3在该反应中只有部分表现出了氧化性C.每生成22.4 L(标准状况)NO有3 mol的电子转移D.如果有8 mol HNO3被还原,则生成了2 mol NO
当堂检测
3.下列各组离子中,能在水溶液中大量共存的是( )A.Na+、Ag+、Cl-、CO32-B.Na+、Mg2+、Cl-、SO42-
C.K+、SO42-、NO3-、Ba2+D.Fe2+、H+、SO42-、NO3-
