第三单元 物质构成的奥秘 基础知识练习(无答案)
文档属性
| 名称 | 第三单元 物质构成的奥秘 基础知识练习(无答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 368.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-23 00:00:00 | ||
图片预览

文档简介
第三单元 物质构成的奥秘 基础知识
课题1 分子和原子
一、物质是由微观粒子构成
1、构成物质的微观粒子有 、 、________等。
由分子构成的物质有:水(____)、氧气(O2)、氮气(____)、二氧化碳(____);
由原子直接构成的物质有:碳(____)、铁(Fe)、金属汞,俗称水银 (____);
由离子构成的物质有:氯化钠(NaCl),它的构成粒子是_______和_______。
2、分子和原子的基本性质:
① 分子的__________ ; ② 分子总是在__________; ③分子之间是 ;
【交流提升】下列生活中的现象或事实主要可用分子和原子的哪一个性质来解释?选序号A、B 或C填空。
A.分子质量和体积都很小; B.分子总是在不断的运动; C.分子间有间隔 D. 同种分子,性质相同 E. 不同分子,性质不同
1、墙内开花墙外香_______; 2、酒精能挥发______;
3、物质有热胀冷缩的现象_____; 4、一个水分子的质量约是3×10—26千克_____;
5、气态的物质易被压缩,而固体和液体的物质不容易被压缩______。
6、氧气能支持燃烧,二氧化碳却能灭火 _______;7、固体碘和气体碘都能使淀粉变蓝______。
二、分子可分为原子
1、分子的概念:
⑴ 水在蒸发时,水只是从____态变成____态,水分子_______(“有”或“没有”)变化,水的化学性质_______(“有”或“没有”)变化,所以水的蒸发是_______(“物理”或“化学”)变化;
【结论一】由分子构成的物质在发生物理变化时,物质的分子本身_____(“有”或“没有”)变化,这种物质的化学性质也就______(“有”或“没有”)变化;
⑵ 我们在实验室用电解水研究水的组成,反应的文字表达式为:水氢气+氧气。水在通电时,水分子_______(“有” 或“没有”)变化,变成了_________和_________两种不同的分子,水不再保持原来的性质,所以水的通电分解是_____(“物理”或“化学”)变化。
【结论二】由分子构成的物质在发生化学变化时,这种物质的分子_____(“有”或“没有”)变化,会变成其它物质的分子,这种物质的化学性质也就______(“有”或“没有”)变化。
由分子构成的物质,分子是保持该物质 _ 的 __。
【交流提升】保持水化学性质的最小粒子是___________,保持二氧化碳化学性质的最小粒子是__________,
保持铁化学性质的最小粒子是__________。
2、原子的概念:
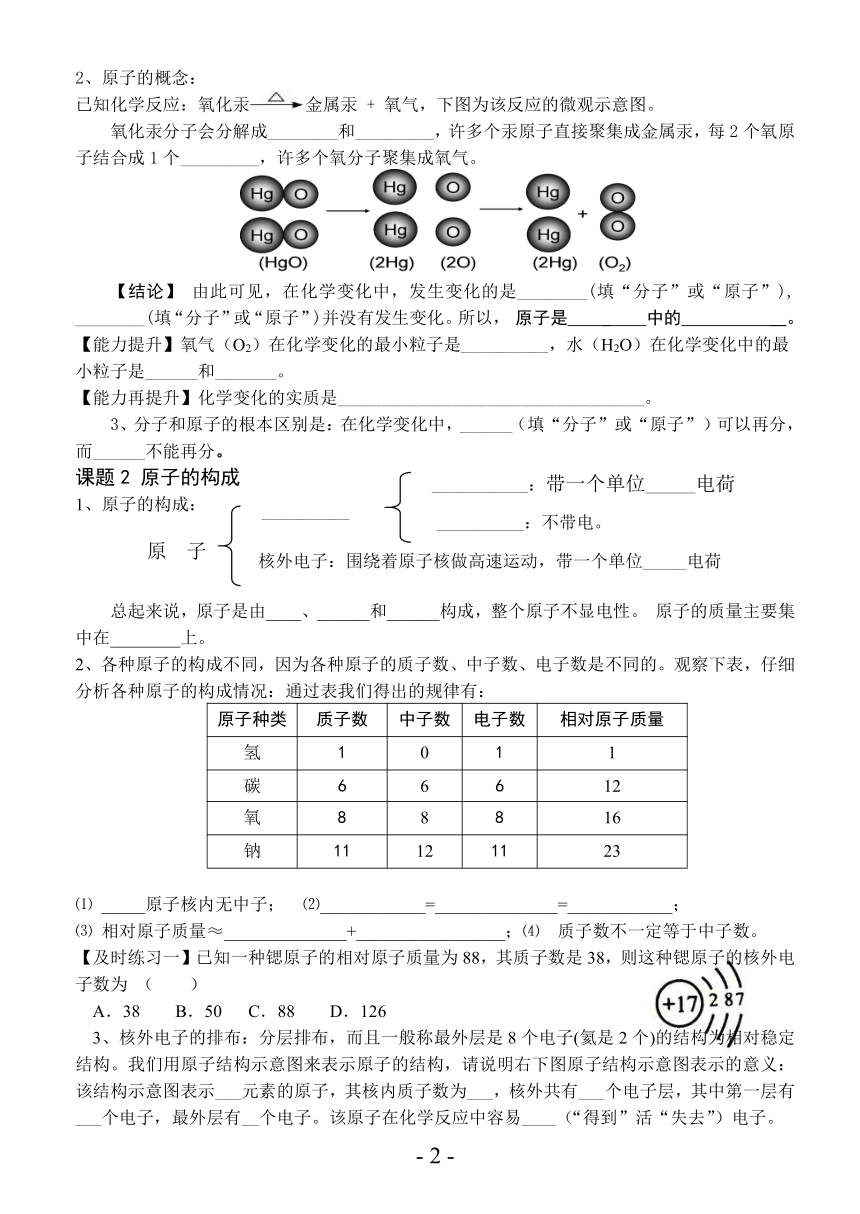
已知化学反应:氧化汞金属汞 + 氧气,下图为该反应的微观示意图。
氧化汞分子会分解成________和_________,许多个汞原子直接聚集成金属汞,每2个氧原子结合成1个_________,许多个氧分子聚集成氧气。
【结论】 由此可见,在化学变化中,发生变化的是________(填“分子”或“原子”), ________(填“分子”或“原子”)并没有发生变化。所以, 原子是 _ 中的 __。
【能力提升】氧气(O2)在化学变化的最小粒子是__________,水(H2O)在化学变化中的最小粒子是______和_______。
【能力再提升】化学变化的实质是___________________________________。
3、分子和原子的根本区别是:在化学变化中,______(填“分子”或“原子”)可以再分,而______不能再分。
课题2 原子的构成
1、原子的构成:
总起来说,原子是由____、______和______构成,整个原子不显电性。 原子的质量主要集中在________上。
2、各种原子的构成不同,因为各种原子的质子数、中子数、电子数是不同的。观察下表,仔细分析各种原子的构成情况:通过表我们得出的规律有:
原子种类 质子数 中子数 电子数 相对原子质量
氢 1 0 1 1
碳 6 6 6 12
氧 8 8 8 16
钠 11 12 11 23
⑴ _____原子核内无中子; ⑵____________=______________=____________;
⑶ 相对原子质量≈______________+_________________;⑷ 质子数不一定等于中子数。
【及时练习一】已知一种锶原子的相对原子质量为88,其质子数是38,则这种锶原子的核外电子数为 ( )
A.38 B.50 C.88 D.126
3、核外电子的排布:分层排布,而且一般称最外层是8个电子(氦是2个)的结构为相对稳定结构。我们用原子结构示意图来表示原子的结构,请说明右下图原子结构示意图表示的意义:该结构示意图表示___元素的原子,其核内质子数为___,核外共有___个电子层,其中第一层有___个电子,最外层有__个电子。该原子在化学反应中容易____(“得到”活“失去”)电子。
4、元素的化学性质与核外电子排布,特别是与________________有密切的关系。
元素分类 最外层电子数 元素化学性质
稀有气体元素 8个(氦为2个) 不易得失电子,相对稳定结构
金属元素 _____4个 易____电子,形成8个电子的相对稳定结构
非金属元素 _____4个 易____电子,形成8个电子的相对稳定结构
5、写出离子符号:
钠离子______;镁离子______; 铝离子______;钾离子_______;钙离子_______; 氯离子______;氧离子______;
硫酸根离子________;碳酸根离子_______;硝酸根离子_________;氢氧根离子________;铵根离子________。
掌握一些离子符号的意义:如Mg2+ 表示镁离子或1个镁离子带两个单位正电荷;2Mg2+ 表示2个镁离子;
Ca2+ 表示_____________________; 符号中数字“2”表示_________________________.
6、阅读1—20号元素原子结构示意图,回答下列问题:
⑴ 图中X=____,Y=____;
⑵ 从左往右,由_____(填“金属”或“非金属”)元素逐渐向______(填“金属”或“非金属”)元素过渡;
⑶ 从左往右,最外层电子数由_____到______逐渐递增;
⑷ 同一竖列, ___________相等;
7、根据下列结构粒子的结构示意图回答问题:
A B C D E F
⑴ 写出示意图表示的粒子符号。(结合元素周期表)
A:_____ B:_____ C:O2- D:_____ E:_____ F:S
⑵ 属于原子的是_______,属于阳离子的是_______,属于阴离子的是______。
⑶ 属于同种元素的是_____;
⑷ 在化学反应里容易失去电子的是______,容易的得到电子的是______,已经达到相对稳定结构的是_______。
⑸ 属于稀有气体元素的是_______;⑹ 具有相同化学性质的元素是_________。
⑺ 具有相同的电子层结构的是________。
课题3 元素
1、元素的概念:
元素是__________(或_________)相同的一类原子的总称。例如,水(H2O)、氧气(O2)、二氧化碳(CO2) 分子中都含有相同的 原子,这些氧原子的原子核内都含有8个质子,化学上将质子数为8的所有氧原子统称为__________。同样,质子数为1的原子统称为氢元素,质子数为6 的原子统称为碳元素,因此元素种类由______________决定。
练习: 氧元素与氢元素最本质的区别在( )
A.质子数不同 B.中子数不同 C.电子数不同 D.相对原子质量不同
2、物质是元素由组成的,例如,水(H2O)由_____元素和_____元素组成。
3、 地壳中含量(质量比)最多的前四位元素_____________________。其中地壳中含量最多的非金属元素是_________,金属元素是__________,这两种元素组成的化合物的化学式为________。
练习:我市著名景点—汤头温泉水富含钾、钙、镁、氟、硅等,这里的“钾、钙、镁、氟、硅”是指_______(填“分子”“原子”或“元素”);
二、元素符号
1、元素符号的意义:①宏观表示___________;②微观表示_______________
2、写出下列符号表示的意义或意义表示的符号:
⑴ O___________、______________;⑵ N___________、______________;
⑶ H___________、______________;⑷ 4O____________;
⑸ 5N____________; ⑹ 6H____________; ⑺ 7Na _____________;
⑻ 2个氧原子_________;⑼ 3个碳原子_________________。
三、元素周期表:
1、元素周期表由7个周期(横行)和16个族(纵行)构成,元素周期表按元素原子的____________递增的顺序给元素编了号,叫做__________。所以从数值上,
原子序数=核电荷数=____________=____________。
2、元素分为____________和____________两种。
3、元素周期表中元素的信息,如右图所示,得到的信息有:
⑴ 该元素的原子序数=核电荷数=____________=____________=53;
⑵ 该元素的符号________;⑶ 该元素的名称为________;
⑷ 该元素的原子的相对原子质量为_______。
⑸ 该元素是_________(填“金属”或“非金属”)元素。
+10
8
2
+161
6
8
2
+111
1
8
2
+121
8
2
+8
8
2
+8
6
2
__________:不带电。
___________:带一个单位_____电荷
__________
核外电子:围绕着原子核做高速运动,带一个单位_____电荷
原 子
53 I
碘
126.9
PAGE
- 3 -
课题1 分子和原子
一、物质是由微观粒子构成
1、构成物质的微观粒子有 、 、________等。
由分子构成的物质有:水(____)、氧气(O2)、氮气(____)、二氧化碳(____);
由原子直接构成的物质有:碳(____)、铁(Fe)、金属汞,俗称水银 (____);
由离子构成的物质有:氯化钠(NaCl),它的构成粒子是_______和_______。
2、分子和原子的基本性质:
① 分子的__________ ; ② 分子总是在__________; ③分子之间是 ;
【交流提升】下列生活中的现象或事实主要可用分子和原子的哪一个性质来解释?选序号A、B 或C填空。
A.分子质量和体积都很小; B.分子总是在不断的运动; C.分子间有间隔 D. 同种分子,性质相同 E. 不同分子,性质不同
1、墙内开花墙外香_______; 2、酒精能挥发______;
3、物质有热胀冷缩的现象_____; 4、一个水分子的质量约是3×10—26千克_____;
5、气态的物质易被压缩,而固体和液体的物质不容易被压缩______。
6、氧气能支持燃烧,二氧化碳却能灭火 _______;7、固体碘和气体碘都能使淀粉变蓝______。
二、分子可分为原子
1、分子的概念:
⑴ 水在蒸发时,水只是从____态变成____态,水分子_______(“有”或“没有”)变化,水的化学性质_______(“有”或“没有”)变化,所以水的蒸发是_______(“物理”或“化学”)变化;
【结论一】由分子构成的物质在发生物理变化时,物质的分子本身_____(“有”或“没有”)变化,这种物质的化学性质也就______(“有”或“没有”)变化;
⑵ 我们在实验室用电解水研究水的组成,反应的文字表达式为:水氢气+氧气。水在通电时,水分子_______(“有” 或“没有”)变化,变成了_________和_________两种不同的分子,水不再保持原来的性质,所以水的通电分解是_____(“物理”或“化学”)变化。
【结论二】由分子构成的物质在发生化学变化时,这种物质的分子_____(“有”或“没有”)变化,会变成其它物质的分子,这种物质的化学性质也就______(“有”或“没有”)变化。
由分子构成的物质,分子是保持该物质 _ 的 __。
【交流提升】保持水化学性质的最小粒子是___________,保持二氧化碳化学性质的最小粒子是__________,
保持铁化学性质的最小粒子是__________。
2、原子的概念:
已知化学反应:氧化汞金属汞 + 氧气,下图为该反应的微观示意图。
氧化汞分子会分解成________和_________,许多个汞原子直接聚集成金属汞,每2个氧原子结合成1个_________,许多个氧分子聚集成氧气。
【结论】 由此可见,在化学变化中,发生变化的是________(填“分子”或“原子”), ________(填“分子”或“原子”)并没有发生变化。所以, 原子是 _ 中的 __。
【能力提升】氧气(O2)在化学变化的最小粒子是__________,水(H2O)在化学变化中的最小粒子是______和_______。
【能力再提升】化学变化的实质是___________________________________。
3、分子和原子的根本区别是:在化学变化中,______(填“分子”或“原子”)可以再分,而______不能再分。
课题2 原子的构成
1、原子的构成:
总起来说,原子是由____、______和______构成,整个原子不显电性。 原子的质量主要集中在________上。
2、各种原子的构成不同,因为各种原子的质子数、中子数、电子数是不同的。观察下表,仔细分析各种原子的构成情况:通过表我们得出的规律有:
原子种类 质子数 中子数 电子数 相对原子质量
氢 1 0 1 1
碳 6 6 6 12
氧 8 8 8 16
钠 11 12 11 23
⑴ _____原子核内无中子; ⑵____________=______________=____________;
⑶ 相对原子质量≈______________+_________________;⑷ 质子数不一定等于中子数。
【及时练习一】已知一种锶原子的相对原子质量为88,其质子数是38,则这种锶原子的核外电子数为 ( )
A.38 B.50 C.88 D.126
3、核外电子的排布:分层排布,而且一般称最外层是8个电子(氦是2个)的结构为相对稳定结构。我们用原子结构示意图来表示原子的结构,请说明右下图原子结构示意图表示的意义:该结构示意图表示___元素的原子,其核内质子数为___,核外共有___个电子层,其中第一层有___个电子,最外层有__个电子。该原子在化学反应中容易____(“得到”活“失去”)电子。
4、元素的化学性质与核外电子排布,特别是与________________有密切的关系。
元素分类 最外层电子数 元素化学性质
稀有气体元素 8个(氦为2个) 不易得失电子,相对稳定结构
金属元素 _____4个 易____电子,形成8个电子的相对稳定结构
非金属元素 _____4个 易____电子,形成8个电子的相对稳定结构
5、写出离子符号:
钠离子______;镁离子______; 铝离子______;钾离子_______;钙离子_______; 氯离子______;氧离子______;
硫酸根离子________;碳酸根离子_______;硝酸根离子_________;氢氧根离子________;铵根离子________。
掌握一些离子符号的意义:如Mg2+ 表示镁离子或1个镁离子带两个单位正电荷;2Mg2+ 表示2个镁离子;
Ca2+ 表示_____________________; 符号中数字“2”表示_________________________.
6、阅读1—20号元素原子结构示意图,回答下列问题:
⑴ 图中X=____,Y=____;
⑵ 从左往右,由_____(填“金属”或“非金属”)元素逐渐向______(填“金属”或“非金属”)元素过渡;
⑶ 从左往右,最外层电子数由_____到______逐渐递增;
⑷ 同一竖列, ___________相等;
7、根据下列结构粒子的结构示意图回答问题:
A B C D E F
⑴ 写出示意图表示的粒子符号。(结合元素周期表)
A:_____ B:_____ C:O2- D:_____ E:_____ F:S
⑵ 属于原子的是_______,属于阳离子的是_______,属于阴离子的是______。
⑶ 属于同种元素的是_____;
⑷ 在化学反应里容易失去电子的是______,容易的得到电子的是______,已经达到相对稳定结构的是_______。
⑸ 属于稀有气体元素的是_______;⑹ 具有相同化学性质的元素是_________。
⑺ 具有相同的电子层结构的是________。
课题3 元素
1、元素的概念:
元素是__________(或_________)相同的一类原子的总称。例如,水(H2O)、氧气(O2)、二氧化碳(CO2) 分子中都含有相同的 原子,这些氧原子的原子核内都含有8个质子,化学上将质子数为8的所有氧原子统称为__________。同样,质子数为1的原子统称为氢元素,质子数为6 的原子统称为碳元素,因此元素种类由______________决定。
练习: 氧元素与氢元素最本质的区别在( )
A.质子数不同 B.中子数不同 C.电子数不同 D.相对原子质量不同
2、物质是元素由组成的,例如,水(H2O)由_____元素和_____元素组成。
3、 地壳中含量(质量比)最多的前四位元素_____________________。其中地壳中含量最多的非金属元素是_________,金属元素是__________,这两种元素组成的化合物的化学式为________。
练习:我市著名景点—汤头温泉水富含钾、钙、镁、氟、硅等,这里的“钾、钙、镁、氟、硅”是指_______(填“分子”“原子”或“元素”);
二、元素符号
1、元素符号的意义:①宏观表示___________;②微观表示_______________
2、写出下列符号表示的意义或意义表示的符号:
⑴ O___________、______________;⑵ N___________、______________;
⑶ H___________、______________;⑷ 4O____________;
⑸ 5N____________; ⑹ 6H____________; ⑺ 7Na _____________;
⑻ 2个氧原子_________;⑼ 3个碳原子_________________。
三、元素周期表:
1、元素周期表由7个周期(横行)和16个族(纵行)构成,元素周期表按元素原子的____________递增的顺序给元素编了号,叫做__________。所以从数值上,
原子序数=核电荷数=____________=____________。
2、元素分为____________和____________两种。
3、元素周期表中元素的信息,如右图所示,得到的信息有:
⑴ 该元素的原子序数=核电荷数=____________=____________=53;
⑵ 该元素的符号________;⑶ 该元素的名称为________;
⑷ 该元素的原子的相对原子质量为_______。
⑸ 该元素是_________(填“金属”或“非金属”)元素。
+10
8
2
+161
6
8
2
+111
1
8
2
+121
8
2
+8
8
2
+8
6
2
__________:不带电。
___________:带一个单位_____电荷
__________
核外电子:围绕着原子核做高速运动,带一个单位_____电荷
原 子
53 I
碘
126.9
PAGE
- 3 -
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
