2023九(上)针对性训练(1.4-1.6)B(含答案)
文档属性
| 名称 | 2023九(上)针对性训练(1.4-1.6)B(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2023-08-25 00:00:00 | ||
图片预览


文档简介
中小学教育资源及组卷应用平台
2023针对性训练 (1.4-1.6)B
一、选择题
1. 实验室的药品要求按物质类别分类放置,部分药品摆放如下:
药品柜 甲 乙 丙 丁
药品 CuO、MnO2 HCl、H2SO4 KOH、Ca(OH)2 Na2CO3、CaCO3
则存放CuSO4的药品柜是( )
A、甲 B、乙 C、丙 D、丁
2.(2023 云南)下列化肥属于钾肥的是( )
A、KCl B、(NH4)2SO4 C、Ca3(PO4)2 D、NH4H2PO4
3. 温州朔门古港遗址被评为2022年全国十大考古考古新发现,出土大量文物,含有多种瓷器、木器等,为“海上丝绸之路”研究提供重要见证,回答下列问题。瓷器出土后需要及时清除、醇洗、除膜、脱盐等环节除去表面杂质,最终覆膜保护。下列过程属于化学变化是( )
A、清除:用毛刷对表面干刷去除杂物
B、醇洗:用酒精使泥土松散,易脱离
C、除膜:用10%稀盐酸除沉积膜碳酸钙
D、脱盐:表面的氯化钠等物质用蒸馏水浸泡除去
4. (2023·金华)在以下探究氢氧化钙溶液性质的实验中,还需借助酸碱指示剂证明化学反应发生的是( )
A B C D
5. 漂白粉可用于游泳池的杀菌消毒,其反应原理为 Ca(ClO)2+H2CO3=2HClO+CaCO3↓,该反应属于( )
A、置换反应 B、复分解反应 C、化合反应 D、分解反应
6.(2023·杭州)有一瓶标签无法辨认的试剂,是碳酸钠溶液或硫酸钠溶液中的一种。仅用下列试剂无法进行鉴别的是( )
A、pH试纸 B、酚酞试液 C、稀硫酸 D、硝酸钡溶液
7.食盐是生活中不可缺少的一种物质,也是科学学习中重要的一种盐。某校以《自然界的盐到餐桌的食盐》为主题进行项目化学习,同学们在这个项目学习中需要完成以下几个项目。科学应用:得到的食盐样品中含有氯化钙,若要除氯化钙杂质,下列所加试剂可行的是( )
A、适量的稀盐酸溶液 B、适量的硝酸银溶液
C、适量的碳酸钠溶液 D、适量的碳酸钾溶液
8.(2023 苏州)常温下,将10mL5%NaOH溶液逐滴加入盛有5mL5%稀盐酸(含2滴酚酞)的锥形瓶中,边滴边振荡。下列有关说法正确的是( )
A、滴加过程中,锥形瓶内溶液中Na+的数目不断增加
B、滴加过程中,溶液恰好由无色变为红色时,溶液pH为7
C、滴加过程中,锥形瓶内溶液温度不断升高
D、滴加结束后,取少量溶液蒸干,所得白色固体是NaCl
9. 向氢氧化钡溶液中逐滴加入稀硫酸,某个量y随稀硫酸的加入的变化情况如图所示,则y表示( )
A、沉淀的质量 B、氢氧化钡的质量
C、溶液的pH D、溶质的质量
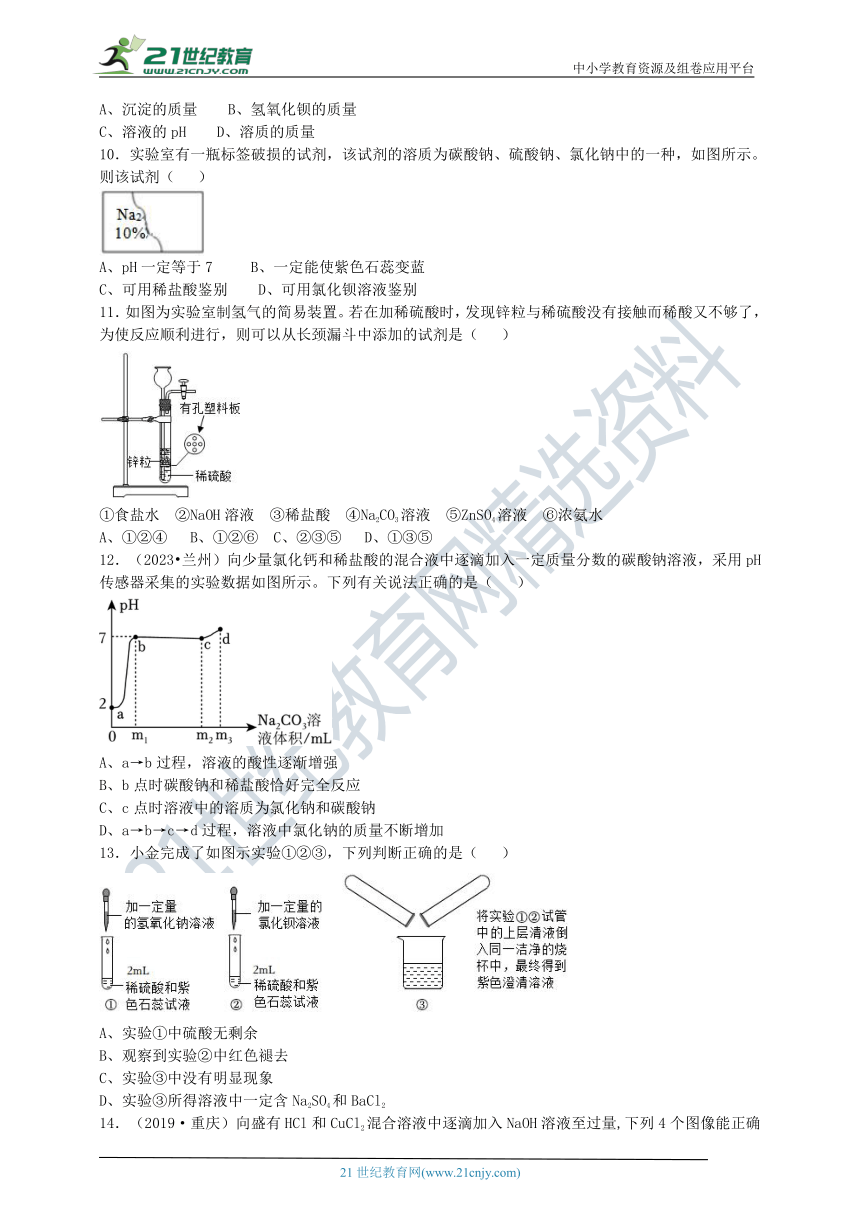
10.实验室有一瓶标签破损的试剂,该试剂的溶质为碳酸钠、硫酸钠、氯化钠中的一种,如图所示。则该试剂( )
A、pH一定等于7 B、一定能使紫色石蕊变蓝
C、可用稀盐酸鉴别 D、可用氯化钡溶液鉴别
11.如图为实验室制氢气的简易装置。若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀酸又不够了,为使反应顺利进行,则可以从长颈漏斗中添加的试剂是( )
①食盐水 ②NaOH溶液 ③稀盐酸 ④Na2CO3溶液 ⑤ZnSO4溶液 ⑥浓氨水
A、①②④ B、①②⑥ C、②③⑤ D、①③⑤
12.(2023 兰州)向少量氯化钙和稀盐酸的混合液中逐滴加入一定质量分数的碳酸钠溶液,采用pH传感器采集的实验数据如图所示。下列有关说法正确的是( )
A、a→b过程,溶液的酸性逐渐增强
B、b点时碳酸钠和稀盐酸恰好完全反应
C、c点时溶液中的溶质为氯化钠和碳酸钠
D、a→b→c→d过程,溶液中氯化钠的质量不断增加
13.小金完成了如图示实验①②③,下列判断正确的是( )
A、实验①中硫酸无剩余
B、观察到实验②中红色褪去
C、实验③中没有明显现象
D、实验③所得溶液中一定含Na2SO4和BaCl2
14.(2019·重庆)向盛有HCl和CuCl2混合溶液中逐滴加入NaOH溶液至过量,下列4个图像能正确反应烧杯内的某些物理量变化趋势的是( )
A、 ①③ B、①②③ C、②④ D、①②④
15.(2023·宁波)有一包固体样品,可能含氯化铁、硫酸钠、氢氧化钡、氢氧化钠中的一种或几种。小宁进行了如下实验:
根据实验现象,下列判断错误的是( )
A、滤液丙中含有氯化铁 B、沉淀乙为氢氧化铁、硫酸钡
C、滤液甲中一定不存在氢氧化钠 D、样品中一定有氯化铁、硫酸钠、氢氧化钡
二、填空题
16.(2023 河南)为了探究氢氧化钠与盐酸是否发生化学反应,某化学小组向滴有几滴酚酞溶液的稀氢氧化钠溶液中滴加稀盐酸并不断搅拌,他们通过溶液颜色的变化,得出了氢氧化钠与盐酸发生了化学反应的结论。溶液颜色的变化过程为______;反应的化学方程式为____________;反应过程中溶液的pH______(填“变大”“不变”或“变小”)。
17.(2023 河北)小明按如图所示进行趣味实验,将U形管开口端放入烧杯内,观察到溶液进入U形管并流入另一端。
(1)烧杯内的溶液呈______色。
(2)二氧化碳与氢氧化钠溶液反应的化学方程式为________________。
(3)U形管开口端放入烧杯后,管内气体压强______(选填“增大”“不变”或“减小”),溶液在管内上升并流入另一端。
18.使用果蔬保鲜剂是果蔬保鲜的一种方法。如图甲是某气调型果蔬保鲜剂,主要成分为消石灰(氢氧化钙)。该保鲜剂使用一段时间后,成分会有怎样的变化呢?小温取一包使用一段时间后的保鲜剂,按图乙步骤进行实验(辅料不参与反应)。
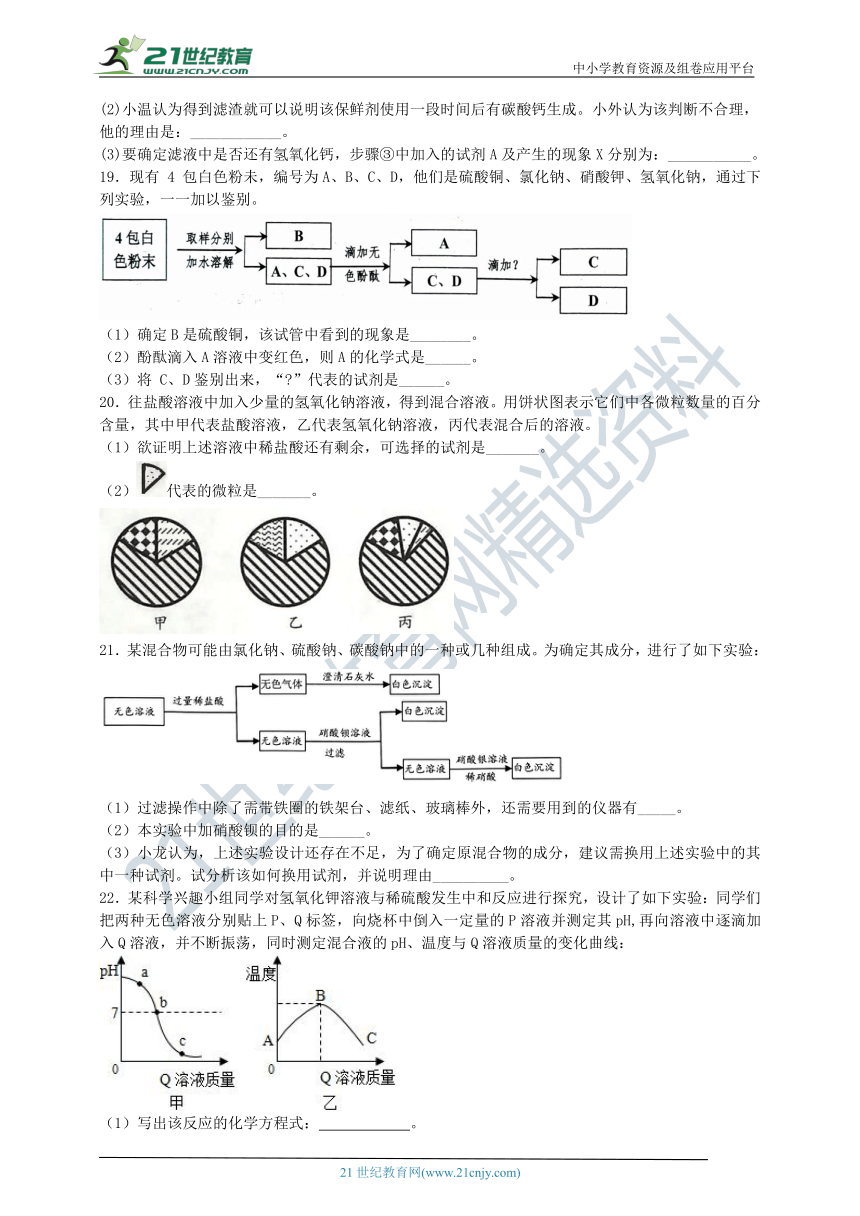
(1)步骤①的操作是:_______________。
(2)小温认为得到滤渣就可以说明该保鲜剂使用一段时间后有碳酸钙生成。小外认为该判断不合理,他的理由是:____________。
(3)要确定滤液中是否还有氢氧化钙,步骤③中加入的试剂A及产生的现象X分别为:___________。
19.现有 4 包白色粉未,编号为A、B、C、D,他们是硫酸铜、氯化钠、硝酸钾、氢氧化钠,通过下列实验,一一加以鉴别。
(1)确定B是硫酸铜,该试管中看到的现象是________。
(2)酚酞滴入A溶液中变红色,则A的化学式是______。
(3)将 C、D鉴别出来,“ ”代表的试剂是______。
20.往盐酸溶液中加入少量的氢氧化钠溶液,得到混合溶液。用饼状图表示它们中各微粒数量的百分含量,其中甲代表盐酸溶液,乙代表氢氧化钠溶液,丙代表混合后的溶液。
(1)欲证明上述溶液中稀盐酸还有剩余,可选择的试剂是_______。
(2)代表的微粒是_______。
21.某混合物可能由氯化钠、硫酸钠、碳酸钠中的一种或几种组成。为确定其成分,进行了如下实验:
(1)过滤操作中除了需带铁圈的铁架台、滤纸、玻璃棒外,还需要用到的仪器有_____。
(2)本实验中加硝酸钡的目的是______。
(3)小龙认为,上述实验设计还存在不足,为了确定原混合物的成分,建议需换用上述实验中的其中一种试剂。试分析该如何换用试剂,并说明理由__________。
22.某科学兴趣小组同学对氢氧化钾溶液与稀硫酸发生中和反应进行探究,设计了如下实验:同学们把两种无色溶液分别贴上P、Q标签,向烧杯中倒入一定量的P溶液并测定其pH,再向溶液中逐滴加入Q溶液,并不断振荡,同时测定混合液的pH、温度与Q溶液质量的变化曲线:
(1)写出该反应的化学方程式: 。
(2)由图甲分析可知:写出c点时杯内溶液中的离子有 (填离子符号)。
(3)分析图乙中BC段温度变化的原因是 。
23.某白色固体可能含有氧化钙、碳酸钠、氢氧化钠、硫酸钠和氯化钡中的一种或多种,某兴趣小组设计了实验对该固体成分进行研究,如下图所示:
(1)由上述实验过程,可确定一定存在的物质是_______。
(2)加入足量的水,溶解过程中放出大量热,能确定存在哪种物质吗?若能,请写出具体物质; 若不能,请说明理由。
三、探究题
24.将NaOH溶液与稀H2SO4混合,观察不到明显现象,为确定其是否反应,小明设计了以下实验探究方案:
(1)方案一:在装有一定量NaOH溶液的烧杯中滴几滴酚酞试液,用滴管逐滴滴加稀H2SO4,并不断振荡。判断两溶液发生了化学反应的现象是________。
(2)方案二:向装有一定量稀H2SO4的试管中滴加NaOH溶液,振荡后再滴加Na2CO3溶液,发现有气泡产生,小明据此判定稀H2SO4与NaOH溶液没有发生化学反应。你认为小明的判断是否正确,并说明理由:_____________________________。
(3)方案三:先用pH试纸测定NaOH溶液的pH,再滴加稀H2SO4,振荡后,再测定混合溶液的pH。若测得pH逐渐减小而且小于7,则能判断NaOH溶液与稀H2SO4 发生了化学反应。方案中“测得pH小于7”是排除___________对实验的干扰。
25.某项目化小组对碳酸钠、碳酸氢钠和稀盐酸反应产生二氧化碳的快慢进行了探究,利用图甲所示装置开展以下实验。
①分别在注射器中加入相同体积、相同浓度且足量的稀盐酸,在相同的具支试管中分别加入相同质量的碳酸钠和碳酸氢钠固体。(已知:NaHCO3+HCl=NaCl+H2O+CO2↑ )
②两位同学同时迅速将注射器中的稀盐酸注入各自试管,并始终用手将活塞按压在底部不动。
③利用“数字化实验”测定试管内的气压变化,得到了如图乙所示的气压变化曲线。(忽略温度变化对试管内气压的影响)
(1)步骤②中始终用手将活塞按压在底部不动的目的是___________。
(2)根据图乙,得出结论____________________________。
(3)在图乙气压变化曲线图中,气压p1大于p2的原因是______________。
四、简答题
26.(2023·宁波)古籍中有记载制烧碱的方法,其核心反应可表示为:Na2CO3+Ca(OH)2=2NaOH+CaCO3↓。小宁模仿古法,以实验室中的Na2CO3、Ca(OH)2固体为原料,制备400g溶质质量分数为10%的NaOH溶液用于制作叶脉书签。
(1)制作叶脉书签时,用NaOH溶液去除叶肉,是利用了NaOH的_____性。
(2)400g溶质质量分数为10%的NaOH溶液中,含NaOH的质量为____g,水的质量为____g。
(3)需称取Na2CO3、Ca(OH)2的质量各为多少?
27.某兴趣小组为测定CuSO4和H2SO4混合溶液中CuSO4的溶质质量分数,进行了如下实验:在烧杯中加入100g该混合溶液,再加入溶质质量分数为20%的NaOH溶液,烧杯中沉淀质量与滴加NaOH溶液质量的关系如图所示:
(1)图中A点对应的溶液中大量存在的分子、离子分别是:____________(用化学符号表示)。
(2)求混合溶液中CuSO4的溶质质量分数。(写出计算过程)
(已知2NaOH+H2SO4═Na2SO4+2H2O,2NaOH+CuSO4═Na2SO4+Cu(OH)2↓)
(3)若改用质量分数为40%的NaOH溶液重新实验,请你在图中大致画出此时烧杯中沉淀质量与滴加NaOH溶液质量的变化曲线,并在曲线上标出当H2SO4、CuSO4恰好完全反应时所消耗的NaOH溶液的具体质量。
参考答案
一、选择题
题号 1 2 3 4 5 6 7 8 9 10
答案 D A C C B D C A D C
题号 11 12 13 14 15
答案 D B A D C
二、填空题
16.溶液由红色变为无色;HCl+NaOH=NaCl+H2O;变小
17.(1)红
(2)2NaOH+CO2=Na2CO3+H2O
(3)减小
18.(1)过滤
(2)氢氧化钙微溶,滤渣也可能是未溶解的氢氧化钙
(3)滴加紫色石蕊,溶液变蓝【(滴加酚酞,溶液变红)、(滴加碳酸钠溶液,产生白色沉淀)、(通入二氧化碳,澄清石灰水变浑浊) 】
19.(1)溶液呈蓝色 (2)NaOH (3)AgNO3溶液
20.(1)紫色石蕊试液(铁粉、碳酸钠粉末) (2)Na+
21.(1)漏斗和烧杯
(2)检验原混合物中是否含有硫酸钠
(3)把稀盐酸换成稀硝酸,防止盐酸中的氯离子对检验氯化钠产生干扰
22.(1)2KOH+H2SO4=K2SO4+2H2O
(2)H+、K+、SO42-
(3)加入的硫酸已经过量,酸碱反应停止
23.(1)碳酸钠 (2)不能,氧化钙和氢氧化钠溶于水都会放出大量热。
三、探究题
24.(1)溶液由红色变成无色
(2)不正确,当稀硫酸有剩余时,滴加碳酸钠溶液也有气泡产生
(3)因稀H2SO4加入,稀释NaOH溶液而引起pH减小
25.(1)保持装置内气体体积一定,防止气体体积变化对压强产生影响。
(2)在相同条件下,碳酸氢钠和稀盐酸反应产生二氧化碳比碳酸钠较快
(3)相同质量的碳酸氢钠和碳酸钠,前者与足量盐酸反应产生的二氧化碳的质量更多。
四、简答题
26.(1)腐蚀
(2)40 360
(3)解:设反应需要Na2CO3的质量为x,Ca(OH)2的质量为y。
Na2CO3+Ca(OH)2=2NaOH+CaCO3↓
106 74 80
x y 40g
==
x=53g y=37g
答:需称取Na2CO3的质量为53g,Ca(OH)2的质量为37g
27.(1)H2O、Na+、SO42-
(2)解:与硫酸铜反应的氢氧化钠溶液的质量为120g-80g=40g
设硫酸铜的质量为x。
2NaOH+CuSO4=Na2SO4+Cu(OH)2↓
80 160
40g×20% x
=
x=16g
混合溶液中CuSO4的溶质质量分数=ⅹ100%=16%
答:混合溶液中CuSO4的溶质质量分数16%。
(3)
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
2023针对性训练 (1.4-1.6)B
一、选择题
1. 实验室的药品要求按物质类别分类放置,部分药品摆放如下:
药品柜 甲 乙 丙 丁
药品 CuO、MnO2 HCl、H2SO4 KOH、Ca(OH)2 Na2CO3、CaCO3
则存放CuSO4的药品柜是( )
A、甲 B、乙 C、丙 D、丁
2.(2023 云南)下列化肥属于钾肥的是( )
A、KCl B、(NH4)2SO4 C、Ca3(PO4)2 D、NH4H2PO4
3. 温州朔门古港遗址被评为2022年全国十大考古考古新发现,出土大量文物,含有多种瓷器、木器等,为“海上丝绸之路”研究提供重要见证,回答下列问题。瓷器出土后需要及时清除、醇洗、除膜、脱盐等环节除去表面杂质,最终覆膜保护。下列过程属于化学变化是( )
A、清除:用毛刷对表面干刷去除杂物
B、醇洗:用酒精使泥土松散,易脱离
C、除膜:用10%稀盐酸除沉积膜碳酸钙
D、脱盐:表面的氯化钠等物质用蒸馏水浸泡除去
4. (2023·金华)在以下探究氢氧化钙溶液性质的实验中,还需借助酸碱指示剂证明化学反应发生的是( )
A B C D
5. 漂白粉可用于游泳池的杀菌消毒,其反应原理为 Ca(ClO)2+H2CO3=2HClO+CaCO3↓,该反应属于( )
A、置换反应 B、复分解反应 C、化合反应 D、分解反应
6.(2023·杭州)有一瓶标签无法辨认的试剂,是碳酸钠溶液或硫酸钠溶液中的一种。仅用下列试剂无法进行鉴别的是( )
A、pH试纸 B、酚酞试液 C、稀硫酸 D、硝酸钡溶液
7.食盐是生活中不可缺少的一种物质,也是科学学习中重要的一种盐。某校以《自然界的盐到餐桌的食盐》为主题进行项目化学习,同学们在这个项目学习中需要完成以下几个项目。科学应用:得到的食盐样品中含有氯化钙,若要除氯化钙杂质,下列所加试剂可行的是( )
A、适量的稀盐酸溶液 B、适量的硝酸银溶液
C、适量的碳酸钠溶液 D、适量的碳酸钾溶液
8.(2023 苏州)常温下,将10mL5%NaOH溶液逐滴加入盛有5mL5%稀盐酸(含2滴酚酞)的锥形瓶中,边滴边振荡。下列有关说法正确的是( )
A、滴加过程中,锥形瓶内溶液中Na+的数目不断增加
B、滴加过程中,溶液恰好由无色变为红色时,溶液pH为7
C、滴加过程中,锥形瓶内溶液温度不断升高
D、滴加结束后,取少量溶液蒸干,所得白色固体是NaCl
9. 向氢氧化钡溶液中逐滴加入稀硫酸,某个量y随稀硫酸的加入的变化情况如图所示,则y表示( )
A、沉淀的质量 B、氢氧化钡的质量
C、溶液的pH D、溶质的质量
10.实验室有一瓶标签破损的试剂,该试剂的溶质为碳酸钠、硫酸钠、氯化钠中的一种,如图所示。则该试剂( )
A、pH一定等于7 B、一定能使紫色石蕊变蓝
C、可用稀盐酸鉴别 D、可用氯化钡溶液鉴别
11.如图为实验室制氢气的简易装置。若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀酸又不够了,为使反应顺利进行,则可以从长颈漏斗中添加的试剂是( )
①食盐水 ②NaOH溶液 ③稀盐酸 ④Na2CO3溶液 ⑤ZnSO4溶液 ⑥浓氨水
A、①②④ B、①②⑥ C、②③⑤ D、①③⑤
12.(2023 兰州)向少量氯化钙和稀盐酸的混合液中逐滴加入一定质量分数的碳酸钠溶液,采用pH传感器采集的实验数据如图所示。下列有关说法正确的是( )
A、a→b过程,溶液的酸性逐渐增强
B、b点时碳酸钠和稀盐酸恰好完全反应
C、c点时溶液中的溶质为氯化钠和碳酸钠
D、a→b→c→d过程,溶液中氯化钠的质量不断增加
13.小金完成了如图示实验①②③,下列判断正确的是( )
A、实验①中硫酸无剩余
B、观察到实验②中红色褪去
C、实验③中没有明显现象
D、实验③所得溶液中一定含Na2SO4和BaCl2
14.(2019·重庆)向盛有HCl和CuCl2混合溶液中逐滴加入NaOH溶液至过量,下列4个图像能正确反应烧杯内的某些物理量变化趋势的是( )
A、 ①③ B、①②③ C、②④ D、①②④
15.(2023·宁波)有一包固体样品,可能含氯化铁、硫酸钠、氢氧化钡、氢氧化钠中的一种或几种。小宁进行了如下实验:
根据实验现象,下列判断错误的是( )
A、滤液丙中含有氯化铁 B、沉淀乙为氢氧化铁、硫酸钡
C、滤液甲中一定不存在氢氧化钠 D、样品中一定有氯化铁、硫酸钠、氢氧化钡
二、填空题
16.(2023 河南)为了探究氢氧化钠与盐酸是否发生化学反应,某化学小组向滴有几滴酚酞溶液的稀氢氧化钠溶液中滴加稀盐酸并不断搅拌,他们通过溶液颜色的变化,得出了氢氧化钠与盐酸发生了化学反应的结论。溶液颜色的变化过程为______;反应的化学方程式为____________;反应过程中溶液的pH______(填“变大”“不变”或“变小”)。
17.(2023 河北)小明按如图所示进行趣味实验,将U形管开口端放入烧杯内,观察到溶液进入U形管并流入另一端。
(1)烧杯内的溶液呈______色。
(2)二氧化碳与氢氧化钠溶液反应的化学方程式为________________。
(3)U形管开口端放入烧杯后,管内气体压强______(选填“增大”“不变”或“减小”),溶液在管内上升并流入另一端。
18.使用果蔬保鲜剂是果蔬保鲜的一种方法。如图甲是某气调型果蔬保鲜剂,主要成分为消石灰(氢氧化钙)。该保鲜剂使用一段时间后,成分会有怎样的变化呢?小温取一包使用一段时间后的保鲜剂,按图乙步骤进行实验(辅料不参与反应)。
(1)步骤①的操作是:_______________。
(2)小温认为得到滤渣就可以说明该保鲜剂使用一段时间后有碳酸钙生成。小外认为该判断不合理,他的理由是:____________。
(3)要确定滤液中是否还有氢氧化钙,步骤③中加入的试剂A及产生的现象X分别为:___________。
19.现有 4 包白色粉未,编号为A、B、C、D,他们是硫酸铜、氯化钠、硝酸钾、氢氧化钠,通过下列实验,一一加以鉴别。
(1)确定B是硫酸铜,该试管中看到的现象是________。
(2)酚酞滴入A溶液中变红色,则A的化学式是______。
(3)将 C、D鉴别出来,“ ”代表的试剂是______。
20.往盐酸溶液中加入少量的氢氧化钠溶液,得到混合溶液。用饼状图表示它们中各微粒数量的百分含量,其中甲代表盐酸溶液,乙代表氢氧化钠溶液,丙代表混合后的溶液。
(1)欲证明上述溶液中稀盐酸还有剩余,可选择的试剂是_______。
(2)代表的微粒是_______。
21.某混合物可能由氯化钠、硫酸钠、碳酸钠中的一种或几种组成。为确定其成分,进行了如下实验:
(1)过滤操作中除了需带铁圈的铁架台、滤纸、玻璃棒外,还需要用到的仪器有_____。
(2)本实验中加硝酸钡的目的是______。
(3)小龙认为,上述实验设计还存在不足,为了确定原混合物的成分,建议需换用上述实验中的其中一种试剂。试分析该如何换用试剂,并说明理由__________。
22.某科学兴趣小组同学对氢氧化钾溶液与稀硫酸发生中和反应进行探究,设计了如下实验:同学们把两种无色溶液分别贴上P、Q标签,向烧杯中倒入一定量的P溶液并测定其pH,再向溶液中逐滴加入Q溶液,并不断振荡,同时测定混合液的pH、温度与Q溶液质量的变化曲线:
(1)写出该反应的化学方程式: 。
(2)由图甲分析可知:写出c点时杯内溶液中的离子有 (填离子符号)。
(3)分析图乙中BC段温度变化的原因是 。
23.某白色固体可能含有氧化钙、碳酸钠、氢氧化钠、硫酸钠和氯化钡中的一种或多种,某兴趣小组设计了实验对该固体成分进行研究,如下图所示:
(1)由上述实验过程,可确定一定存在的物质是_______。
(2)加入足量的水,溶解过程中放出大量热,能确定存在哪种物质吗?若能,请写出具体物质; 若不能,请说明理由。
三、探究题
24.将NaOH溶液与稀H2SO4混合,观察不到明显现象,为确定其是否反应,小明设计了以下实验探究方案:
(1)方案一:在装有一定量NaOH溶液的烧杯中滴几滴酚酞试液,用滴管逐滴滴加稀H2SO4,并不断振荡。判断两溶液发生了化学反应的现象是________。
(2)方案二:向装有一定量稀H2SO4的试管中滴加NaOH溶液,振荡后再滴加Na2CO3溶液,发现有气泡产生,小明据此判定稀H2SO4与NaOH溶液没有发生化学反应。你认为小明的判断是否正确,并说明理由:_____________________________。
(3)方案三:先用pH试纸测定NaOH溶液的pH,再滴加稀H2SO4,振荡后,再测定混合溶液的pH。若测得pH逐渐减小而且小于7,则能判断NaOH溶液与稀H2SO4 发生了化学反应。方案中“测得pH小于7”是排除___________对实验的干扰。
25.某项目化小组对碳酸钠、碳酸氢钠和稀盐酸反应产生二氧化碳的快慢进行了探究,利用图甲所示装置开展以下实验。
①分别在注射器中加入相同体积、相同浓度且足量的稀盐酸,在相同的具支试管中分别加入相同质量的碳酸钠和碳酸氢钠固体。(已知:NaHCO3+HCl=NaCl+H2O+CO2↑ )
②两位同学同时迅速将注射器中的稀盐酸注入各自试管,并始终用手将活塞按压在底部不动。
③利用“数字化实验”测定试管内的气压变化,得到了如图乙所示的气压变化曲线。(忽略温度变化对试管内气压的影响)
(1)步骤②中始终用手将活塞按压在底部不动的目的是___________。
(2)根据图乙,得出结论____________________________。
(3)在图乙气压变化曲线图中,气压p1大于p2的原因是______________。
四、简答题
26.(2023·宁波)古籍中有记载制烧碱的方法,其核心反应可表示为:Na2CO3+Ca(OH)2=2NaOH+CaCO3↓。小宁模仿古法,以实验室中的Na2CO3、Ca(OH)2固体为原料,制备400g溶质质量分数为10%的NaOH溶液用于制作叶脉书签。
(1)制作叶脉书签时,用NaOH溶液去除叶肉,是利用了NaOH的_____性。
(2)400g溶质质量分数为10%的NaOH溶液中,含NaOH的质量为____g,水的质量为____g。
(3)需称取Na2CO3、Ca(OH)2的质量各为多少?
27.某兴趣小组为测定CuSO4和H2SO4混合溶液中CuSO4的溶质质量分数,进行了如下实验:在烧杯中加入100g该混合溶液,再加入溶质质量分数为20%的NaOH溶液,烧杯中沉淀质量与滴加NaOH溶液质量的关系如图所示:
(1)图中A点对应的溶液中大量存在的分子、离子分别是:____________(用化学符号表示)。
(2)求混合溶液中CuSO4的溶质质量分数。(写出计算过程)
(已知2NaOH+H2SO4═Na2SO4+2H2O,2NaOH+CuSO4═Na2SO4+Cu(OH)2↓)
(3)若改用质量分数为40%的NaOH溶液重新实验,请你在图中大致画出此时烧杯中沉淀质量与滴加NaOH溶液质量的变化曲线,并在曲线上标出当H2SO4、CuSO4恰好完全反应时所消耗的NaOH溶液的具体质量。
参考答案
一、选择题
题号 1 2 3 4 5 6 7 8 9 10
答案 D A C C B D C A D C
题号 11 12 13 14 15
答案 D B A D C
二、填空题
16.溶液由红色变为无色;HCl+NaOH=NaCl+H2O;变小
17.(1)红
(2)2NaOH+CO2=Na2CO3+H2O
(3)减小
18.(1)过滤
(2)氢氧化钙微溶,滤渣也可能是未溶解的氢氧化钙
(3)滴加紫色石蕊,溶液变蓝【(滴加酚酞,溶液变红)、(滴加碳酸钠溶液,产生白色沉淀)、(通入二氧化碳,澄清石灰水变浑浊) 】
19.(1)溶液呈蓝色 (2)NaOH (3)AgNO3溶液
20.(1)紫色石蕊试液(铁粉、碳酸钠粉末) (2)Na+
21.(1)漏斗和烧杯
(2)检验原混合物中是否含有硫酸钠
(3)把稀盐酸换成稀硝酸,防止盐酸中的氯离子对检验氯化钠产生干扰
22.(1)2KOH+H2SO4=K2SO4+2H2O
(2)H+、K+、SO42-
(3)加入的硫酸已经过量,酸碱反应停止
23.(1)碳酸钠 (2)不能,氧化钙和氢氧化钠溶于水都会放出大量热。
三、探究题
24.(1)溶液由红色变成无色
(2)不正确,当稀硫酸有剩余时,滴加碳酸钠溶液也有气泡产生
(3)因稀H2SO4加入,稀释NaOH溶液而引起pH减小
25.(1)保持装置内气体体积一定,防止气体体积变化对压强产生影响。
(2)在相同条件下,碳酸氢钠和稀盐酸反应产生二氧化碳比碳酸钠较快
(3)相同质量的碳酸氢钠和碳酸钠,前者与足量盐酸反应产生的二氧化碳的质量更多。
四、简答题
26.(1)腐蚀
(2)40 360
(3)解:设反应需要Na2CO3的质量为x,Ca(OH)2的质量为y。
Na2CO3+Ca(OH)2=2NaOH+CaCO3↓
106 74 80
x y 40g
==
x=53g y=37g
答:需称取Na2CO3的质量为53g,Ca(OH)2的质量为37g
27.(1)H2O、Na+、SO42-
(2)解:与硫酸铜反应的氢氧化钠溶液的质量为120g-80g=40g
设硫酸铜的质量为x。
2NaOH+CuSO4=Na2SO4+Cu(OH)2↓
80 160
40g×20% x
=
x=16g
混合溶液中CuSO4的溶质质量分数=ⅹ100%=16%
答:混合溶液中CuSO4的溶质质量分数16%。
(3)
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
