化学人教版(2019)必修第一册1.1.2.分散系及其分类(共43张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第一册1.1.2.分散系及其分类(共43张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 97.9MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-26 00:00:00 | ||
图片预览










文档简介
(共43张PPT)
分散系及其分类
第2课时
第一节 物质的分类及转化
溶液:
悬浊液:
乳浊液:油滴分散到水里形成的混合物
[相同点]
一种或几种物质分散到另一种物质里,形成的混合物。
新课引入
铜离子分散到水中形成的混合物。
泥土颗粒悬浮于水中形成的混合物
1.分散系的概念与组成
(1)概念:一种或几种物质分散到另一种(或多种)物质里形成的混合物。
(2)组成:
目标一 分散系
分散剂
分散质
(分散系中被分散成粒子的物质)
(微粒分散在其中的物质)
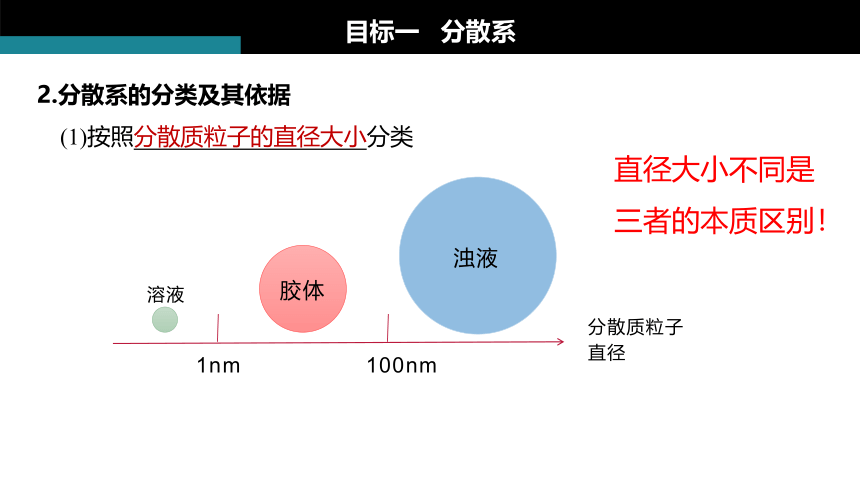
2.分散系的分类及其依据
(1)按照分散质粒子的直径大小分类
目标一 分散系
溶液
胶体
浊液
1nm 100nm
分散质粒子
直径
直径大小不同是三者的本质区别!
练习1
判断正误
(1)氯化钠溶液均一、稳定、透明,不是分散系( )
(2)“冰水混合物”是一种分散系( )
(3)分散系有的是纯净物,有的是混合物( )
(4)分散系可以是固态、液态或气态( )
(5)油水混合物属于乳浊液( )
(6)直径为1~100 nm的粒子称为胶体( )
×
×
×
√
√
×
测一测
练习2
溶液、胶体和浊液三种分散系的本质区别是( )
A.是否是大量分子或离子的集合体
B.是否能通过滤纸
C.分散质粒子直径的大小
D.是否均一、透明、稳定
√
测一测
1.胶体的树状分类
目标二 胶 体
胶体
根据分散剂的状态
气溶胶
液溶胶
固溶胶
Fe(OH)3胶体
分散质粒子的直径为1 100 nm的分散系称为胶体 。
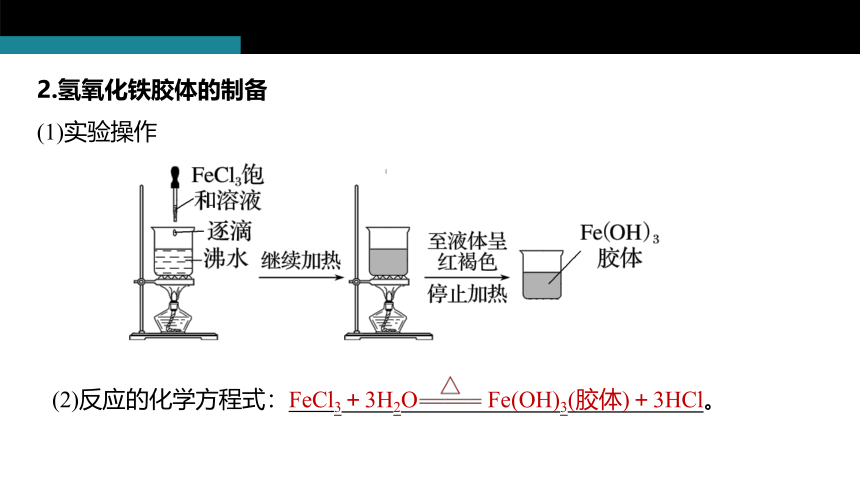
2.氢氧化铁胶体的制备
(1)实验操作
(2)反应的化学方程式:FeCl3+3H2O Fe(OH)3(胶体)+3HCl。
【演示实验】Fe(OH)3胶体的制备
问题:
为什么不用稀溶液?能不能滴入过多氯化铁 饱和溶液?
为什么不用氯化铁与氢氧化钠溶液反应?
为什么不能长时间加热或搅拌?
3.胶体的性质——丁达尔效应
应用:丁达尔效应常用来区分胶体和溶液。
概念:当光束通过胶体时,从入射光的的垂直方向能看到一条光亮的通路,这种现象叫“丁达尔效应”。
成因:光的散射
丁达尔【英国】
(1820~1893)
丁达尔现象
胶体
溶液
浊液
丁达尔现象(微观模型)
可见光波长在102~103纳米数量级
浊液
胶体
溶液
三种分散系中分散质的组成!
【生活中的丁达尔效应】
电影院投射在银幕的光柱
树林中光线透过树叶间隙形成光束
More
生活中的丁达尔效应:
雨过天晴
图2. 夜晚美景
丁达尔现象应用
1、电泳现象
胶体的其他性质
概念:胶体中的分散质微粒在外加电场的作用下产生定向移动的现象。
电泳现象说明:胶体中的分散质微粒(胶粒)带有同种 电荷。
【思考】
(1)为什么胶粒带有电荷?
(2)胶粒所带电荷都相同吗?
(3)胶体带不带电呢?
(4)胶体为什么能稳定存在呢?
Fe(OH)3胶体粒子
正电荷
胶体粒子直径1-100nm
结构
胶体粒子比表面积大
具有吸附性
同种胶体粒子因吸附
带有同种电荷
性质
电泳现象
应用
胶体具有
一定稳定性
电泳技术
分离蛋白质
和DNA
工业上的静电除尘
胶体的聚沉
使胶体凝聚形成沉淀析出的现象
胶体聚沉的应用:
卤水点豆腐、明矾净水、江河入海口处三角洲的形成
使胶体聚沉的方法:
① 加入电解质
② 加入带相反电荷的离子
③ 加热
④ 搅拌
2、胶体的聚沉
胶体的其他性质
学以致用:解释视频中的现象
答:氢氧化铁胶体颗粒遇电解质发生聚沉,而后与盐酸发生复分解反应而溶解。
请你想一想:
要成功制备氢氧化铁胶体并防止其聚沉,实验过程中需要注意哪些问题?
制备过程中不可过度搅拌
加热的时间必须适度
必须使用蒸馏水,也不可以使用氢氧化钠溶液
必须使用饱和溶液?
不可滴入过多饱和氯化铁溶液
4.胶体的分离实验——渗析
透析技术
学习胶体后,请你根据性质决定用途的观点,分析下列图示中现象或是用途与胶体的哪些性质有关,并做出相关注解。
胶体的用途
肥皂的
制取和分离
水泥的硬化
FeCl3溶液
用于伤口止血
土壤的保肥作用
制豆腐
冶金厂大
量的烟尘
用高压电除尘
霞光万道
三角洲的形成
5、应用
分散系(混合物)
浊液
溶液
胶 体
整 合:
(按分散质微粒大小的不同来分)
分散系 溶液 胶体 浊液
分散质微粒直径
分散质微粒
能否透过滤纸
能否透过半透膜
稳定性
< 1nm
1 ~100 nm
>100 nm
单个分子或离子
许多分子集合体
大量分子集合体
能
能
不能
能
不能
不能
稳定
较稳定
不稳定
【小结】:三种分散系的比较
问题:如何分离胶体与溶液、胶体与浊液、以及浊液与溶液的混合物?
1.判断正误(正确的打“√”,错误的打“×”号)。
(1)纳米干冰颗粒分散到CO2气体中形成的是胶体 ( )
(2)直径为1~100nm的粒子是胶体 ( )
(3)溶液和胶体的本质区别是能否产生丁达尔效应 ( )
(4)FeCl3溶液呈电中性,Fe(OH)3胶体带正电( )
(5)江河入海口处易形成三角洲与胶体的性质有关( )
练习2
测一测
×
×
×
×
√
练习1
2、纳米碳酸钙”是一种微粒直径在几纳米到几十纳米的特殊材料,将纳米碳酸钙分散到水中形成分散系,其具有的性质是( )
A.能产生丁达尔效应 B.不能透过滤纸
C.不能与盐酸反应 D.一定是浊液
测一测
A
3.胶体与溶液的根本区别在于 ( )
A.分散系是否有丁达尔现象
B.分散质粒子是否带电荷
C.分散系是否稳定
D.分散质粒子的大小
练习1
D
测一测
4.[双选题]下列有关胶体的说法中正确的是 ( )
A.胶体都是均匀透明的液体
B.胶体一般情况下比较稳定,不易发生沉淀
C.胶体产生丁达尔效应是由胶粒的大小决定的
D.胶体稳定存在的主要原因是布朗运动
练习3
BC
5.下列事实与胶体性质无关的是 ( )
A.水泥厂和冶金厂常用高压直流电除去大量烟尘,减少空气污染
B.将植物油倒入水中用力搅拌形成油水混合物
C.平行光束射入蛋白质溶液里,从侧面可以看到一条光亮的通路
D.Fe(OH)3胶体中滴入稀硫酸,先看到红褐色沉淀而后沉淀溶解
练习4
B
6.(2022·北京汇文中学高一期末)下列分散系中不会出现丁达尔效应的是( )
①氢氧化铁胶体 ②CuSO4溶液 ③雾 ④蔗糖溶液 ⑤FeCl3溶液 ⑥稀豆浆
A.②④⑤ B.③④ C.②④⑥ D.①③④
√
测一测
7.FeCl3溶液、Fe(OH)3胶体、Fe(OH)3浊液是三种重要的分散系,下列叙述不正确的是( )
A.胶体和溶液能透过滤纸,而浊液不能透过滤纸
B.分别用一束光照射三种分散系,只有Fe(OH)3胶体能产生丁达尔效应
C.三种分散系的稳定性:FeCl3溶液>Fe(OH)3胶体>Fe(OH)3浊液
D.根据能否产生丁达尔效应,将分散系分为溶液、浊液和胶体
√
测一测
练习2
8、AlCl3具有与FeCl3类似的性质,写出AlCl3常温下溶于水生成Al(OH)3胶体的化学方程式:___________________________________。
AlCl3+3H2O===Al(OH)3(胶体)+3HCl
测一测
分散系及其分类
第2课时
第一节 物质的分类及转化
溶液:
悬浊液:
乳浊液:油滴分散到水里形成的混合物
[相同点]
一种或几种物质分散到另一种物质里,形成的混合物。
新课引入
铜离子分散到水中形成的混合物。
泥土颗粒悬浮于水中形成的混合物
1.分散系的概念与组成
(1)概念:一种或几种物质分散到另一种(或多种)物质里形成的混合物。
(2)组成:
目标一 分散系
分散剂
分散质
(分散系中被分散成粒子的物质)
(微粒分散在其中的物质)
2.分散系的分类及其依据
(1)按照分散质粒子的直径大小分类
目标一 分散系
溶液
胶体
浊液
1nm 100nm
分散质粒子
直径
直径大小不同是三者的本质区别!
练习1
判断正误
(1)氯化钠溶液均一、稳定、透明,不是分散系( )
(2)“冰水混合物”是一种分散系( )
(3)分散系有的是纯净物,有的是混合物( )
(4)分散系可以是固态、液态或气态( )
(5)油水混合物属于乳浊液( )
(6)直径为1~100 nm的粒子称为胶体( )
×
×
×
√
√
×
测一测
练习2
溶液、胶体和浊液三种分散系的本质区别是( )
A.是否是大量分子或离子的集合体
B.是否能通过滤纸
C.分散质粒子直径的大小
D.是否均一、透明、稳定
√
测一测
1.胶体的树状分类
目标二 胶 体
胶体
根据分散剂的状态
气溶胶
液溶胶
固溶胶
Fe(OH)3胶体
分散质粒子的直径为1 100 nm的分散系称为胶体 。
2.氢氧化铁胶体的制备
(1)实验操作
(2)反应的化学方程式:FeCl3+3H2O Fe(OH)3(胶体)+3HCl。
【演示实验】Fe(OH)3胶体的制备
问题:
为什么不用稀溶液?能不能滴入过多氯化铁 饱和溶液?
为什么不用氯化铁与氢氧化钠溶液反应?
为什么不能长时间加热或搅拌?
3.胶体的性质——丁达尔效应
应用:丁达尔效应常用来区分胶体和溶液。
概念:当光束通过胶体时,从入射光的的垂直方向能看到一条光亮的通路,这种现象叫“丁达尔效应”。
成因:光的散射
丁达尔【英国】
(1820~1893)
丁达尔现象
胶体
溶液
浊液
丁达尔现象(微观模型)
可见光波长在102~103纳米数量级
浊液
胶体
溶液
三种分散系中分散质的组成!
【生活中的丁达尔效应】
电影院投射在银幕的光柱
树林中光线透过树叶间隙形成光束
More
生活中的丁达尔效应:
雨过天晴
图2. 夜晚美景
丁达尔现象应用
1、电泳现象
胶体的其他性质
概念:胶体中的分散质微粒在外加电场的作用下产生定向移动的现象。
电泳现象说明:胶体中的分散质微粒(胶粒)带有同种 电荷。
【思考】
(1)为什么胶粒带有电荷?
(2)胶粒所带电荷都相同吗?
(3)胶体带不带电呢?
(4)胶体为什么能稳定存在呢?
Fe(OH)3胶体粒子
正电荷
胶体粒子直径1-100nm
结构
胶体粒子比表面积大
具有吸附性
同种胶体粒子因吸附
带有同种电荷
性质
电泳现象
应用
胶体具有
一定稳定性
电泳技术
分离蛋白质
和DNA
工业上的静电除尘
胶体的聚沉
使胶体凝聚形成沉淀析出的现象
胶体聚沉的应用:
卤水点豆腐、明矾净水、江河入海口处三角洲的形成
使胶体聚沉的方法:
① 加入电解质
② 加入带相反电荷的离子
③ 加热
④ 搅拌
2、胶体的聚沉
胶体的其他性质
学以致用:解释视频中的现象
答:氢氧化铁胶体颗粒遇电解质发生聚沉,而后与盐酸发生复分解反应而溶解。
请你想一想:
要成功制备氢氧化铁胶体并防止其聚沉,实验过程中需要注意哪些问题?
制备过程中不可过度搅拌
加热的时间必须适度
必须使用蒸馏水,也不可以使用氢氧化钠溶液
必须使用饱和溶液?
不可滴入过多饱和氯化铁溶液
4.胶体的分离实验——渗析
透析技术
学习胶体后,请你根据性质决定用途的观点,分析下列图示中现象或是用途与胶体的哪些性质有关,并做出相关注解。
胶体的用途
肥皂的
制取和分离
水泥的硬化
FeCl3溶液
用于伤口止血
土壤的保肥作用
制豆腐
冶金厂大
量的烟尘
用高压电除尘
霞光万道
三角洲的形成
5、应用
分散系(混合物)
浊液
溶液
胶 体
整 合:
(按分散质微粒大小的不同来分)
分散系 溶液 胶体 浊液
分散质微粒直径
分散质微粒
能否透过滤纸
能否透过半透膜
稳定性
< 1nm
1 ~100 nm
>100 nm
单个分子或离子
许多分子集合体
大量分子集合体
能
能
不能
能
不能
不能
稳定
较稳定
不稳定
【小结】:三种分散系的比较
问题:如何分离胶体与溶液、胶体与浊液、以及浊液与溶液的混合物?
1.判断正误(正确的打“√”,错误的打“×”号)。
(1)纳米干冰颗粒分散到CO2气体中形成的是胶体 ( )
(2)直径为1~100nm的粒子是胶体 ( )
(3)溶液和胶体的本质区别是能否产生丁达尔效应 ( )
(4)FeCl3溶液呈电中性,Fe(OH)3胶体带正电( )
(5)江河入海口处易形成三角洲与胶体的性质有关( )
练习2
测一测
×
×
×
×
√
练习1
2、纳米碳酸钙”是一种微粒直径在几纳米到几十纳米的特殊材料,将纳米碳酸钙分散到水中形成分散系,其具有的性质是( )
A.能产生丁达尔效应 B.不能透过滤纸
C.不能与盐酸反应 D.一定是浊液
测一测
A
3.胶体与溶液的根本区别在于 ( )
A.分散系是否有丁达尔现象
B.分散质粒子是否带电荷
C.分散系是否稳定
D.分散质粒子的大小
练习1
D
测一测
4.[双选题]下列有关胶体的说法中正确的是 ( )
A.胶体都是均匀透明的液体
B.胶体一般情况下比较稳定,不易发生沉淀
C.胶体产生丁达尔效应是由胶粒的大小决定的
D.胶体稳定存在的主要原因是布朗运动
练习3
BC
5.下列事实与胶体性质无关的是 ( )
A.水泥厂和冶金厂常用高压直流电除去大量烟尘,减少空气污染
B.将植物油倒入水中用力搅拌形成油水混合物
C.平行光束射入蛋白质溶液里,从侧面可以看到一条光亮的通路
D.Fe(OH)3胶体中滴入稀硫酸,先看到红褐色沉淀而后沉淀溶解
练习4
B
6.(2022·北京汇文中学高一期末)下列分散系中不会出现丁达尔效应的是( )
①氢氧化铁胶体 ②CuSO4溶液 ③雾 ④蔗糖溶液 ⑤FeCl3溶液 ⑥稀豆浆
A.②④⑤ B.③④ C.②④⑥ D.①③④
√
测一测
7.FeCl3溶液、Fe(OH)3胶体、Fe(OH)3浊液是三种重要的分散系,下列叙述不正确的是( )
A.胶体和溶液能透过滤纸,而浊液不能透过滤纸
B.分别用一束光照射三种分散系,只有Fe(OH)3胶体能产生丁达尔效应
C.三种分散系的稳定性:FeCl3溶液>Fe(OH)3胶体>Fe(OH)3浊液
D.根据能否产生丁达尔效应,将分散系分为溶液、浊液和胶体
√
测一测
练习2
8、AlCl3具有与FeCl3类似的性质,写出AlCl3常温下溶于水生成Al(OH)3胶体的化学方程式:___________________________________。
AlCl3+3H2O===Al(OH)3(胶体)+3HCl
测一测
