1.3.1氧化还原反应 课件(共43张PPT)—2023-2024学年高中化学人教版-2019·高一上学期
文档属性
| 名称 | 1.3.1氧化还原反应 课件(共43张PPT)—2023-2024学年高中化学人教版-2019·高一上学期 |  | |
| 格式 | pptx | ||
| 文件大小 | 8.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-27 00:04:04 | ||
图片预览









文档简介
(共43张PPT)
第一章 物质及其变化
第三节 氧化还原反应
第一课时 氧化还原反应
00
00
人们在分析各种各样的化学反应时发现,在一些化学反应中各反应物所含元素的化合价都没有发生变化,而在另一些化学反应中有些反应物所含的一种或几种元素的化合价发生了变化,这些反应的反应类型是什么?
让我们一起学习氧化还原反应。
00
一
二
三
四
掌握氧化反应、还原反应的概念和实质。
运用元素化合价的升降,理解氧化还原反应的实质是电子的转移。
掌握氧化还原反应中电子转移表示方法。
通过对“氧化还原反应”的学习,培养宏观辨识和微观探析的意识。
学习目标
从三个角度分析氧化还原反应
01
从三个角度分析氧化还原反应
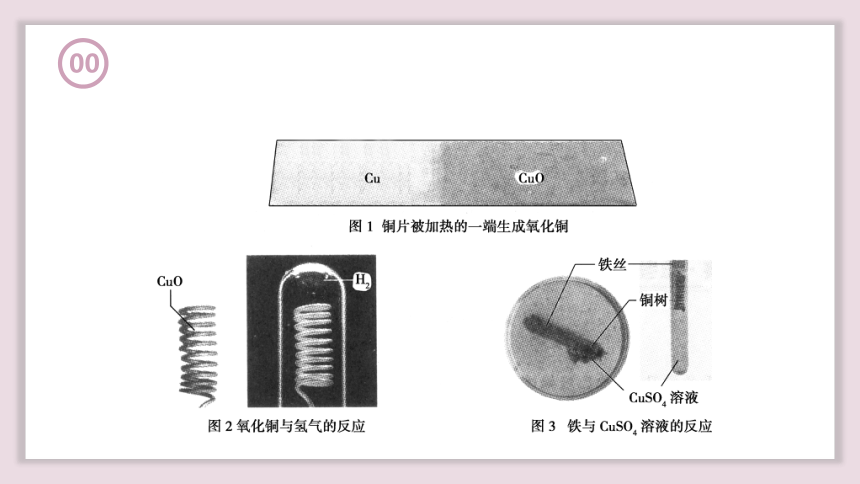
1.从得氧失氧的角度认识:
(1)得氧失氧分析:
01
从三个角度分析氧化还原反应
(2)从得氧失氧的角度分析氧化反应、还原反应。
①氧化反应——__________氧的化学反应。
②还原反应——__________氧的化学反应。
(3)结论:氧化还原反应——有__________的化学反应。
点拨:氧化反应和还原反应同时发生。
得到
失去
得失氧
01
从三个角度分析氧化还原反应
2.从化合价升降的角度认识:
(1)化合价变化分析。
01
从三个角度分析氧化还原反应
(2)从化合价升降的角度分析氧化反应、还原反应。
①氧化反应——化合价__________的化学反应。
②还原反应——化合价__________的化学反应。
(3)结论
氧化还原反应——有________________的化学反应。
点拨:在氧化还原反应中,并不是所有元素的化合价都发生变化。
升高
降低
元素化合价变化
01
从三个角度分析氧化还原反应
3.从电子转移的角度认识:
01
从三个角度分析氧化还原反应
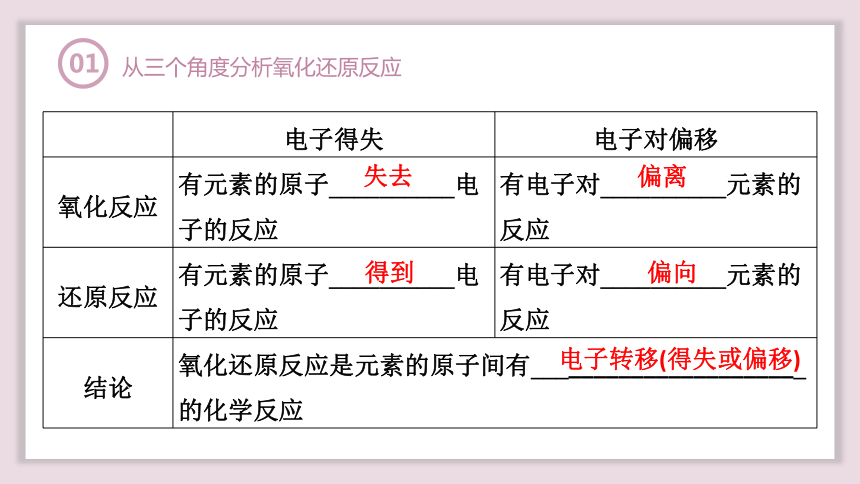
电子得失 电子对偏移
氧化反应 有元素的原子__________电子的反应 有电子对__________元素的反应
还原反应 有元素的原子__________电子的反应 有电子对__________元素的反应
结论 氧化还原反应是元素的原子间有______________________的化学反应
失去
偏离
得到
偏向
电子转移(得失或偏移)
氧化还原反应概念和实质
02
氧化还原反应概念和实质
1.基本概念:
02
氧化还原反应概念和实质
2.特征:__________发生变化。
3.实质:__________(即电子的得失或偏移)。
元素化合价
电子的转移
氧化还原反应与四大基本反应类型的关系
03
氧化还原反应与四大基本反应类型的关系
1.图示关系:
03
氧化还原反应与四大基本反应类型的关系
复分解
置换
04
要点归纳
04
要点归纳
双线桥法:
(1)基本步骤。
04
要点归纳
(2)示例。
用双线桥法表示氢气还原氧化铜的电子转移情况:
04
要点归纳
(3)注意事项。
①箭头、箭尾必须对应化合价变化的同种元素。
②必须注明“得”“失”。
③氧化剂和还原剂得、失电子数目要相等。
04
要点归纳
2.单线桥法:
(1)基本步骤。
04
要点归纳
04
要点归纳
点拨:(1)氧化还原反应中转移电子总数是得到的电子数或失去的电子数,而不是二者的加和。
(2)用双线桥法标电子转移时,电子转移数用a×be-形式表示。
a表示发生氧化或还原反应的原子个数,b表示每个原子得到或失去的电子数,当a或b等于1时,要省略。
04
要点归纳
规律方法指导:
(1)常见元素的主要化合价氟氯溴碘负一价;正一氢银与钾钠。氧的负二先记清;正二镁钙钡和锌。正三是铝正四硅;下面再把变价归。全部金属是正价;一二铜来二三铁。锰正二四与六七;碳的二四要牢记。非金属负主正不齐;氯的负一正一五七。氮磷负三与正五;不同磷三氮二四。硫有负二正四六;边记边用就会熟。
04
要点归纳
(2)常见根价口诀
一价铵根硝酸根;氢卤酸根氢氧根。
高锰酸根氯酸根;高氯酸根醋酸根。
二价硫酸碳酸根;氢硫酸根锰酸根。
暂记铵根为正价;负三有个磷酸根。
05
随堂训练
1.下列关于氧化还原反应的说法中正确的是 ( )
A.氧化还原反应前后元素化合价有升降
B.氧化还原反应前后一定有氧的得失
C.Fe3+→Fe2+的变化过程一定是氧化反应
D.元素化合价升高的反应是还原反应
A
05
随堂训练
C
05
随堂训练
3.下列电子转移表示正确的是 ( )
B
05
随堂训练
4.(2021·成都高一检测)下列变化过程只有通过氧化反应才能实现的是 ( )
A.HCl→H2 B.HCl→FeCl2
C.H2SO4(浓)→SO2 D.Fe→Fe2O3
D
05
随堂训练
C
05
随堂训练
6.碘缺乏病是机体因缺碘导致的疾病,即地方性甲状腺肿大和地方性克汀病,主要病因是环境缺碘,人体摄取碘不足。
05
随堂训练
我国政府对碘缺乏病相当重视,为了消除碘缺乏病,规定在食盐中必须加入适量的碘酸钾。检验食盐中是否加碘,可用如下反应:
KIO3+5KI+3H2SO4===3K2SO4+3I2+3H2O
(1)请分别用单线桥法和双线桥法标出该反应电子转移的方向和数目。
(2)有的同学认为可以用淀粉检验加碘食盐中是否含有碘元素。具体操作为:取适量加碘食盐于水中溶解,然后加入淀粉,溶液变蓝,则说明食盐中含有碘元素,溶液不变蓝,则说明不含有碘元素。该同学的观点是否正确。请说明理由。
05
随堂训练
05
随堂训练
05
随堂训练
05
随堂训练
05
随堂训练
电子转移分析:
05
随堂训练
7.(NH4)2Cr2O7是一种受热易分解的盐,下列各组对(NH4)2Cr2O7受热分解产物的判断可能正确的是 ( )
A.CrO3+NH3+H2
B.Cr2O3+NH3+H2O
C.CrO3+N2+H2O
D.Cr2O3+N2+H2O
D
05
随堂训练
C
05
随堂训练
9.我国“四大发明”在人类发展史上起到了非常重要的作用。
黑火药爆炸的反应为S+2KNO3+3C===K2S+3CO2↑+N2↑。在该反应中,被还原的元素是 ( )
A.N B.C
C.N和S D.N和C
C
05
随堂训练
10.2019年10月1日,我国举行了盛大的阅兵仪式,阅兵式上首次展示了东风—41洲际导弹,它使用到的一种燃料是偏二甲肼(C2H8N2)和四氧化二氮,反应的化学方程式为C2H8N2+2N2O4===3N2↑+2CO2↑+4H2O↑,下列叙述错误的是 ( )
A.此反应是氧化还原反应
B.反应瞬间产生大量高温气体,推动火箭飞行
C.在反应中C2H8N2作氧化剂
D.1个N2O4分子反应,转移8个电子
C
感谢观看
THANK YOU
第一章 物质及其变化
第三节 氧化还原反应
第一课时 氧化还原反应
00
00
人们在分析各种各样的化学反应时发现,在一些化学反应中各反应物所含元素的化合价都没有发生变化,而在另一些化学反应中有些反应物所含的一种或几种元素的化合价发生了变化,这些反应的反应类型是什么?
让我们一起学习氧化还原反应。
00
一
二
三
四
掌握氧化反应、还原反应的概念和实质。
运用元素化合价的升降,理解氧化还原反应的实质是电子的转移。
掌握氧化还原反应中电子转移表示方法。
通过对“氧化还原反应”的学习,培养宏观辨识和微观探析的意识。
学习目标
从三个角度分析氧化还原反应
01
从三个角度分析氧化还原反应
1.从得氧失氧的角度认识:
(1)得氧失氧分析:
01
从三个角度分析氧化还原反应
(2)从得氧失氧的角度分析氧化反应、还原反应。
①氧化反应——__________氧的化学反应。
②还原反应——__________氧的化学反应。
(3)结论:氧化还原反应——有__________的化学反应。
点拨:氧化反应和还原反应同时发生。
得到
失去
得失氧
01
从三个角度分析氧化还原反应
2.从化合价升降的角度认识:
(1)化合价变化分析。
01
从三个角度分析氧化还原反应
(2)从化合价升降的角度分析氧化反应、还原反应。
①氧化反应——化合价__________的化学反应。
②还原反应——化合价__________的化学反应。
(3)结论
氧化还原反应——有________________的化学反应。
点拨:在氧化还原反应中,并不是所有元素的化合价都发生变化。
升高
降低
元素化合价变化
01
从三个角度分析氧化还原反应
3.从电子转移的角度认识:
01
从三个角度分析氧化还原反应
电子得失 电子对偏移
氧化反应 有元素的原子__________电子的反应 有电子对__________元素的反应
还原反应 有元素的原子__________电子的反应 有电子对__________元素的反应
结论 氧化还原反应是元素的原子间有______________________的化学反应
失去
偏离
得到
偏向
电子转移(得失或偏移)
氧化还原反应概念和实质
02
氧化还原反应概念和实质
1.基本概念:
02
氧化还原反应概念和实质
2.特征:__________发生变化。
3.实质:__________(即电子的得失或偏移)。
元素化合价
电子的转移
氧化还原反应与四大基本反应类型的关系
03
氧化还原反应与四大基本反应类型的关系
1.图示关系:
03
氧化还原反应与四大基本反应类型的关系
复分解
置换
04
要点归纳
04
要点归纳
双线桥法:
(1)基本步骤。
04
要点归纳
(2)示例。
用双线桥法表示氢气还原氧化铜的电子转移情况:
04
要点归纳
(3)注意事项。
①箭头、箭尾必须对应化合价变化的同种元素。
②必须注明“得”“失”。
③氧化剂和还原剂得、失电子数目要相等。
04
要点归纳
2.单线桥法:
(1)基本步骤。
04
要点归纳
04
要点归纳
点拨:(1)氧化还原反应中转移电子总数是得到的电子数或失去的电子数,而不是二者的加和。
(2)用双线桥法标电子转移时,电子转移数用a×be-形式表示。
a表示发生氧化或还原反应的原子个数,b表示每个原子得到或失去的电子数,当a或b等于1时,要省略。
04
要点归纳
规律方法指导:
(1)常见元素的主要化合价氟氯溴碘负一价;正一氢银与钾钠。氧的负二先记清;正二镁钙钡和锌。正三是铝正四硅;下面再把变价归。全部金属是正价;一二铜来二三铁。锰正二四与六七;碳的二四要牢记。非金属负主正不齐;氯的负一正一五七。氮磷负三与正五;不同磷三氮二四。硫有负二正四六;边记边用就会熟。
04
要点归纳
(2)常见根价口诀
一价铵根硝酸根;氢卤酸根氢氧根。
高锰酸根氯酸根;高氯酸根醋酸根。
二价硫酸碳酸根;氢硫酸根锰酸根。
暂记铵根为正价;负三有个磷酸根。
05
随堂训练
1.下列关于氧化还原反应的说法中正确的是 ( )
A.氧化还原反应前后元素化合价有升降
B.氧化还原反应前后一定有氧的得失
C.Fe3+→Fe2+的变化过程一定是氧化反应
D.元素化合价升高的反应是还原反应
A
05
随堂训练
C
05
随堂训练
3.下列电子转移表示正确的是 ( )
B
05
随堂训练
4.(2021·成都高一检测)下列变化过程只有通过氧化反应才能实现的是 ( )
A.HCl→H2 B.HCl→FeCl2
C.H2SO4(浓)→SO2 D.Fe→Fe2O3
D
05
随堂训练
C
05
随堂训练
6.碘缺乏病是机体因缺碘导致的疾病,即地方性甲状腺肿大和地方性克汀病,主要病因是环境缺碘,人体摄取碘不足。
05
随堂训练
我国政府对碘缺乏病相当重视,为了消除碘缺乏病,规定在食盐中必须加入适量的碘酸钾。检验食盐中是否加碘,可用如下反应:
KIO3+5KI+3H2SO4===3K2SO4+3I2+3H2O
(1)请分别用单线桥法和双线桥法标出该反应电子转移的方向和数目。
(2)有的同学认为可以用淀粉检验加碘食盐中是否含有碘元素。具体操作为:取适量加碘食盐于水中溶解,然后加入淀粉,溶液变蓝,则说明食盐中含有碘元素,溶液不变蓝,则说明不含有碘元素。该同学的观点是否正确。请说明理由。
05
随堂训练
05
随堂训练
05
随堂训练
05
随堂训练
05
随堂训练
电子转移分析:
05
随堂训练
7.(NH4)2Cr2O7是一种受热易分解的盐,下列各组对(NH4)2Cr2O7受热分解产物的判断可能正确的是 ( )
A.CrO3+NH3+H2
B.Cr2O3+NH3+H2O
C.CrO3+N2+H2O
D.Cr2O3+N2+H2O
D
05
随堂训练
C
05
随堂训练
9.我国“四大发明”在人类发展史上起到了非常重要的作用。
黑火药爆炸的反应为S+2KNO3+3C===K2S+3CO2↑+N2↑。在该反应中,被还原的元素是 ( )
A.N B.C
C.N和S D.N和C
C
05
随堂训练
10.2019年10月1日,我国举行了盛大的阅兵仪式,阅兵式上首次展示了东风—41洲际导弹,它使用到的一种燃料是偏二甲肼(C2H8N2)和四氧化二氮,反应的化学方程式为C2H8N2+2N2O4===3N2↑+2CO2↑+4H2O↑,下列叙述错误的是 ( )
A.此反应是氧化还原反应
B.反应瞬间产生大量高温气体,推动火箭飞行
C.在反应中C2H8N2作氧化剂
D.1个N2O4分子反应,转移8个电子
C
感谢观看
THANK YOU
