2023-2024学年鲁科版高中化学选择性必修2 2.2.1共价键与分子的空间结构 运用杂化理论,探索大π键——重难点突破 课件(共17张PPT)
文档属性
| 名称 | 2023-2024学年鲁科版高中化学选择性必修2 2.2.1共价键与分子的空间结构 运用杂化理论,探索大π键——重难点突破 课件(共17张PPT) |
|
|
| 格式 | pptx | ||
| 文件大小 | 7.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-29 00:00:00 | ||
图片预览



文档简介
(共17张PPT)
2.2.1 共价键与分子的空间结构
鲁科版化学选择性必修2
《物质结构与性质》
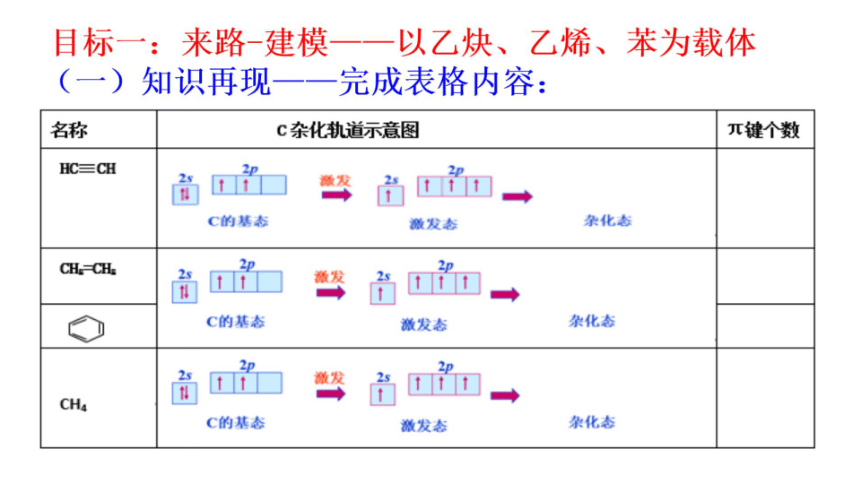
运用杂化理论,探索大键一重难点突破
参与成建
的电子数
参与成建
的原子数
乳山市第一中学
滕平平
学习目标:
1、通过知识再现,探析π键的形成条件,构建π键模型。
(宏观辨识与微观探析)
2、以山东高考题为素材,能运用π键模型解决环状化合物的相关
问题。(证据推理与模型认知)
3、以全国卷考题为载体,能运用π键模型探究非环状化合物中的
大键。(科学探究与创新意识)
重点:兀键模型的构建过程。
难点:运用杂化理论去解决大兀键的相关知识。
目标三
目标二
去路一出模
目标一
思路一用模
来路—建模
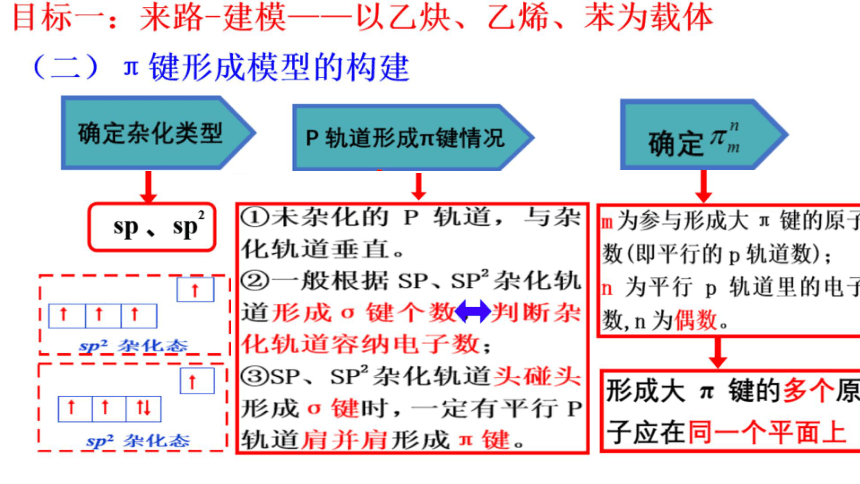
目标一:来路-建模一一以乙炔、乙烯、苯为载体
(一)知识再现一一完成表格内容:
名称
C杂化轨道示意图
π键个数
HC三CH
2p
2
激发
25
C的基态
澈发态
杂化态
CH-CH:
2p
5
2p
2
激发
C的基态
激发态
杂化态
2p
2p
2s
澈发
CHa
C的基态
激发态
杂化态
目标一:来路-建模
一一以乙炔、乙烯、苯为载体
(二)π键形成模型的构建
确定杂化类型
P轨道形成π键情况
确定π
①少未杂化的P轨道,与杂
m为参与形成大π键的原子
化轨道垂直。
数(即平行的p轨道数);
②一般根据SP、SP2杂化轨
五
为平行p轨道里的电子
道形成·键个数→判断杂
数,n为偶数。
化轨道容纳电子数:
③SP、SP杂化轨道头碰头
形成大π键的多个原
形成·键时,一定有平行P
sp2杂化态_1
轨道肩并肩形成π键。
子应在同一个平面上
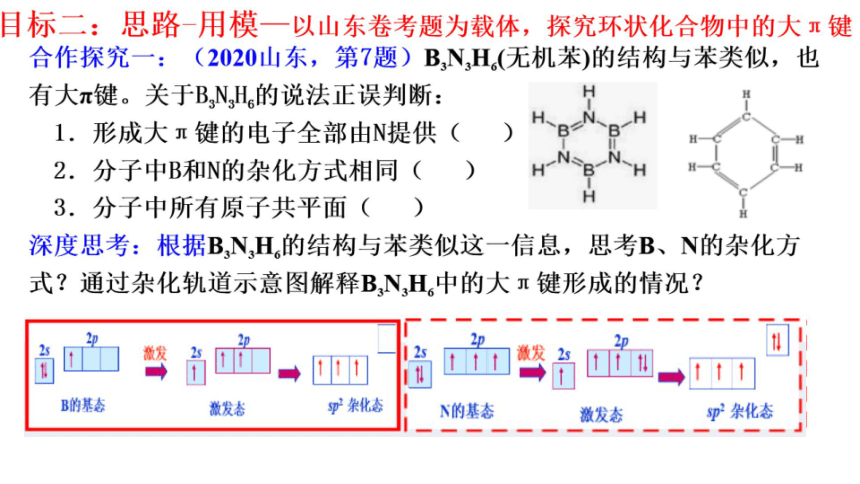
目标二:思路-用模一以山东卷考题为载体,探究环状化合物中的大π键
合作探究一:(2020山东,第7题)B,NH(无机苯)的结构与苯类似,也
有大π键。关于B,N,H的说法正误判断:
1.形成大π键的电子全部由N提供(
2.分子中B和N的杂化方式相同(
3.分子中所有原子共平面(
深度思考:根据B,N,H的结构与苯类似这一信息,思考B、N的杂化方
式?通过杂化轨道示意图解释BNH,中的大π键形成的情况?
2p
2p
2p
11t
B的基态
激发态
sp2杂化态
N的基态
激发态
sp2杂化态
目标二:思路-用模一以山东卷考题为载体,探究环状化合物中的大π键
合作探究二:
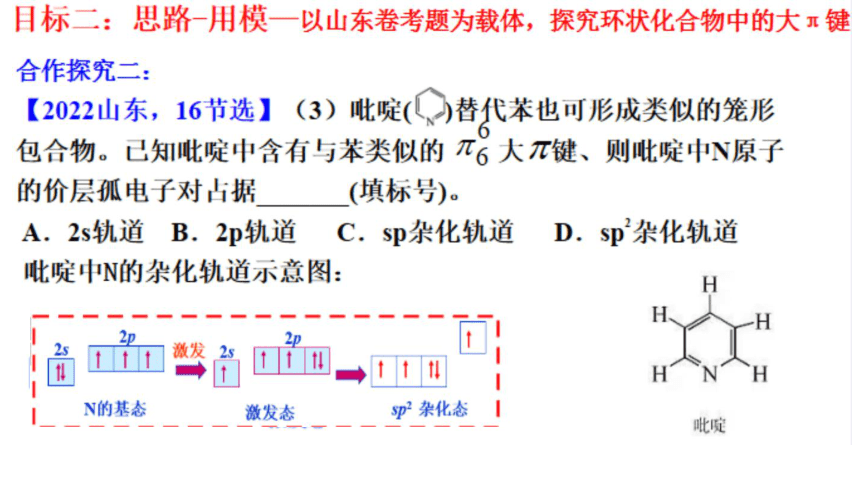
【2022山东,16节选】(3)吡啶(〔)替代苯也可形成类似的笼形
包合物。已知吡啶中含有与苯类似的兀6大元键、则吡啶中原子
的价层孤电子对占据
(填标号)
A.2s轨道B.2p轨道
C.sp朵化轨道
D.sp杂化轨道
吡啶中N的杂化轨道示意图:
N的基态
澈发态
杂化态
吡啶
2.2.1 共价键与分子的空间结构
鲁科版化学选择性必修2
《物质结构与性质》
运用杂化理论,探索大键一重难点突破
参与成建
的电子数
参与成建
的原子数
乳山市第一中学
滕平平
学习目标:
1、通过知识再现,探析π键的形成条件,构建π键模型。
(宏观辨识与微观探析)
2、以山东高考题为素材,能运用π键模型解决环状化合物的相关
问题。(证据推理与模型认知)
3、以全国卷考题为载体,能运用π键模型探究非环状化合物中的
大键。(科学探究与创新意识)
重点:兀键模型的构建过程。
难点:运用杂化理论去解决大兀键的相关知识。
目标三
目标二
去路一出模
目标一
思路一用模
来路—建模
目标一:来路-建模一一以乙炔、乙烯、苯为载体
(一)知识再现一一完成表格内容:
名称
C杂化轨道示意图
π键个数
HC三CH
2p
2
激发
25
C的基态
澈发态
杂化态
CH-CH:
2p
5
2p
2
激发
C的基态
激发态
杂化态
2p
2p
2s
澈发
CHa
C的基态
激发态
杂化态
目标一:来路-建模
一一以乙炔、乙烯、苯为载体
(二)π键形成模型的构建
确定杂化类型
P轨道形成π键情况
确定π
①少未杂化的P轨道,与杂
m为参与形成大π键的原子
化轨道垂直。
数(即平行的p轨道数);
②一般根据SP、SP2杂化轨
五
为平行p轨道里的电子
道形成·键个数→判断杂
数,n为偶数。
化轨道容纳电子数:
③SP、SP杂化轨道头碰头
形成大π键的多个原
形成·键时,一定有平行P
sp2杂化态_1
轨道肩并肩形成π键。
子应在同一个平面上
目标二:思路-用模一以山东卷考题为载体,探究环状化合物中的大π键
合作探究一:(2020山东,第7题)B,NH(无机苯)的结构与苯类似,也
有大π键。关于B,N,H的说法正误判断:
1.形成大π键的电子全部由N提供(
2.分子中B和N的杂化方式相同(
3.分子中所有原子共平面(
深度思考:根据B,N,H的结构与苯类似这一信息,思考B、N的杂化方
式?通过杂化轨道示意图解释BNH,中的大π键形成的情况?
2p
2p
2p
11t
B的基态
激发态
sp2杂化态
N的基态
激发态
sp2杂化态
目标二:思路-用模一以山东卷考题为载体,探究环状化合物中的大π键
合作探究二:
【2022山东,16节选】(3)吡啶(〔)替代苯也可形成类似的笼形
包合物。已知吡啶中含有与苯类似的兀6大元键、则吡啶中原子
的价层孤电子对占据
(填标号)
A.2s轨道B.2p轨道
C.sp朵化轨道
D.sp杂化轨道
吡啶中N的杂化轨道示意图:
N的基态
澈发态
杂化态
吡啶
