2023-2024学年人教版九年级化学上册 第三单元 课题3 元素 预习案(含解析)
文档属性
| 名称 | 2023-2024学年人教版九年级化学上册 第三单元 课题3 元素 预习案(含解析) |

|
|
| 格式 | doc | ||
| 文件大小 | 3.7MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-29 00:00:00 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
课题3 元素
1. 认识物质是由元素组成的,知道质子数相同的一类原子属于同种元素。(化学观念)
2. 能对元素进行简单分类,了解元素符号所表示的意义。(化学观念)
3. 识记并正确书写常见元素的名称和符号。(化学观念)
4. 初步认识元素周期表,能根据元素的原子序数在元素周期表中查到指定元素的相关信息。(科学思维)
5.初步认识元素性质与原子核外电子排布(特别是最外层电子数)的密切关系。(科学思维)
知识点一 元素
物质是由 组成的,如氧气是由氧元素组成的,过氧化氢是由氢元素和氧元素组成的,加碘食盐中含有碘元素等。元素是组成物质的基本成分。
过氧化氢分子和二氧化碳分子中都含氧原子,这些氧原子的原子核内都含有8个质子,即核电荷数为8,化学上将质子数(即核电荷数)为8的所有氧原子统称为 。同样,将质子数为 1的所有氢原子统称为 ,将质子数为6的所有碳原子统称为 。
1.元素的定义:元素是 (即核电荷数)相同的一类原子的总称。
决定元素的种类,即元素原子 不同,元素种类不同。
【说明】
(1)具有相同质子数的微粒不一定是同种元素,微粒可能是分子、原子或离子。如水分子(H2O)和氖原子(Ne)都有10个质子,但不属于同种元素。
(2)这里所说的“一类原子”包括两种情况:①质子数相同、中子数不同的原子,如碳12、碳13、碳14,它们都属于碳元素;②质子数相同、电子数不同的单核粒子属于同种元素,如Na和Na+都属于钠元素。
(3)元素是一个 (填宏观或微观),只讲 ,不讲个数。
(4)物质发生化学变化时, 的种类发生变化, 的种类不变, 的种类也不会改变。
(5)元素的性质,尤其是化学性质,主要由 决定。通常,最外层电子数 ,化学性质 。
2.元素的种类
物质的种类非常多,已知的有上亿种,但是,组成这些物质的元素并不多,到目前为止,已经发现的元素只有一百多种。
3.元素与原子的比较
项目 元素 原子
概念 具有相同 (即核电荷数)的一类原子的总称。一种元素可包含几种原子。如氢元素包含、、 中的最小粒子
区别 宏观概念,只讲 ,不讲个数 微观概念,既讲种类,又讲个数
使用范围 描述物质 组成,如二氧化硫是由硫元素和氧元素组成的 用来描述由原子直接构成的 和 的构成。如铁是由铁原子构成的,1个水分子是由 2个氢原子和1个氧原子构成的
联系 只要质子数(即核电荷数)相同的一类原子就属于同一种元素。 是元素的最小单位,元素则是原子的一个归类“集体”,即元素和原子是总体和个体的关系
4.元素的存在
(1)空气中含量居前两位的元素是 、 (按体积分数计算,氮气约占 ,氧气约占 )。
(2)生物细胞中含量居前四位的元素如下表所示。
元素 氮
质量分数 /% 65 18 10 3
(3)地壳中各种元素的含量分布如图所示。
地壳中含量居于前四位的元素是 。
(4)海水中含量居于前四位的元素是 。
【考点例题】
例1.(2023 九台区一模)患贫血病的人可以多吃韭菜,因为韭菜是一种含铁量很高的蔬菜,每100克韭菜中含铁8.9毫克。这里的铁指的是( )
A.铁元素 B.铁单质 C.氧化铁 D.铁的化合物
【变式精选】
【变式一】(2023 沂源县一模)元素之间的根本区别是原子的( )
A.核内质子数不同 B.核外电子数不同
C.核内中子数不同 D.相对原子质量不同
【变式二】(2023 梁溪区二模)地壳中含量第二的非金属元素是( )
A.Si B.O C.Al D.Fe
知识点二 宏观元素与微观粒子
1.物质、元素、分子、原子等概念的区别及联系
关于物质、元素、分子、原子的区别和联系可进行简单的归纳,如下所示。
2.“宏观”与“微观”的区别和联系
元素是 概念,只有 之分,没有 之别。在讨论物质的组成时,一般用“某物质由什么元素组成”来描述,其中只涉及类别而没有数量多少的含义;而分子、 、 等是微观概念,既有种类之分又有数量之别,当讨论物质的微观结构时,一般用“某物质由什么分子(或原子、离子)构成”“每个某分子是由多少个某原子构成的”来描述。一般是元素与“组成”匹配,而分子、原子、离子与“构成”匹配。
注意物质的描述过程中“宏观与宏观”“微观与微观”对应。
【考点例题】
例1.思维导图有助于建构知识,如图是小金建立的有关物质宏观组成和微观构成的思维导图,其中“▲”应填入的是( )
A.原子 B.中子 C.元素 D.质子
【变式精选】
【变式二】下列说法中正确的是( )
A.二氧化碳由二个氧元素和一个碳元素组成
B.二氧化碳由碳、氧两种元素组成
C.二氧化碳由碳和氧气两种单质组成
D.二氧化碳由氧分子和碳原子构成
知识点三 元素符号
1.元素符号的规定
国际上统一采用元素拉丁文名称的第一个字母(大写)来表示元素,如果几种元素拉丁文名称的第一个字母相同,就附加一个小写字母来区别,如N表示氮元素,Na表示钠元素。
2.元素符号的写法
(1)由一个字母表示的元素符号要 ,如 H、C、K、S 等。
(2)由两个字母表示的元素符号,第一个字母大写,第二个字母小写,如 Na、Mg、Cu 等。书写这类元素符号时,特别注意要辨清第一个字母相同的一些类似的元素符号,如 Cu、Ca、Cl等。
(3)常见元素符号规范写法如下:
3.元素符号的含义
(1)意义
①微观意义:表示这种元素的一个
②宏观意义:表示一种
如H的意义:表示氢元素(宏观)、表示一个氢原子(微观)
(2) 对于由原子直接构成的物质,元素符号还表示一种 。例如,Fe可以表示铁元素、一个铁原子、铁这种物质。
(3) 元素符号前面加化学计量数时,只能表示多个原子,不再表示这种元素,因为元素只讲种类不讲个数。如2N,只能表示两个氮原子,而不再表示氮元素,该符号只有微观含义。
4.元素的分类
元素分为三类:一是 元素;二是 元素;三是 元素。
(1)金属元素:汉字名称偏旁为“钅”的元素,加上金和汞。由金属元素组成的金属,通常状况下为固体,只有汞(通常状况下为液体)除外,另外,金属由原子直接构成。
(2)非金属元素:通常状况下,非金属元素有三种状态一是中文名称有“气”字头的,是气态非金属元素;二是中文名称有“氵”字旁的,是液态非金属元素;三是中文名称有“石”字旁的,是固态非金属元素。
(3)稀有气体元素:通常状况下,稀有气体为气体,它们的中文名称中都有“气”字头,它们是由原子直接构成的,如氨(He)。
【考点例题】
例1.下列属于非金属元素的是( )
A.Zn B.Ag C.N D.Na
【变式精选】
【变式一】(2023 柳州三模)元素“Cu”的名称是( )
A.铜 B.硅 C.钙 D.碳
【变式二】氯的元素符号是 ;该元素符号表示的意义是 。
知识点四 元素周期表
1.元素周期表
根据元素的原子结构和性质,将已知的一百多种元素按 (数值上等于核电荷数)科学有序地排列起来所得的表,叫做元素周期表。
元素周期表中对金属元素、非金属元素(包括稀有气体元素)用不同的颜色做了区分,并标上了元素的相对原子质量。
2.元素周期表的结构
(1)横行(周期):元素周期表中每一横行代表一个周期,共有 7个横行,即 周期。
(2)纵列(族):元素周期表共有 18 个纵列,每1个纵列叫做一个族,第 8,9、10 三个纵列共同组成一个族,所以有 。
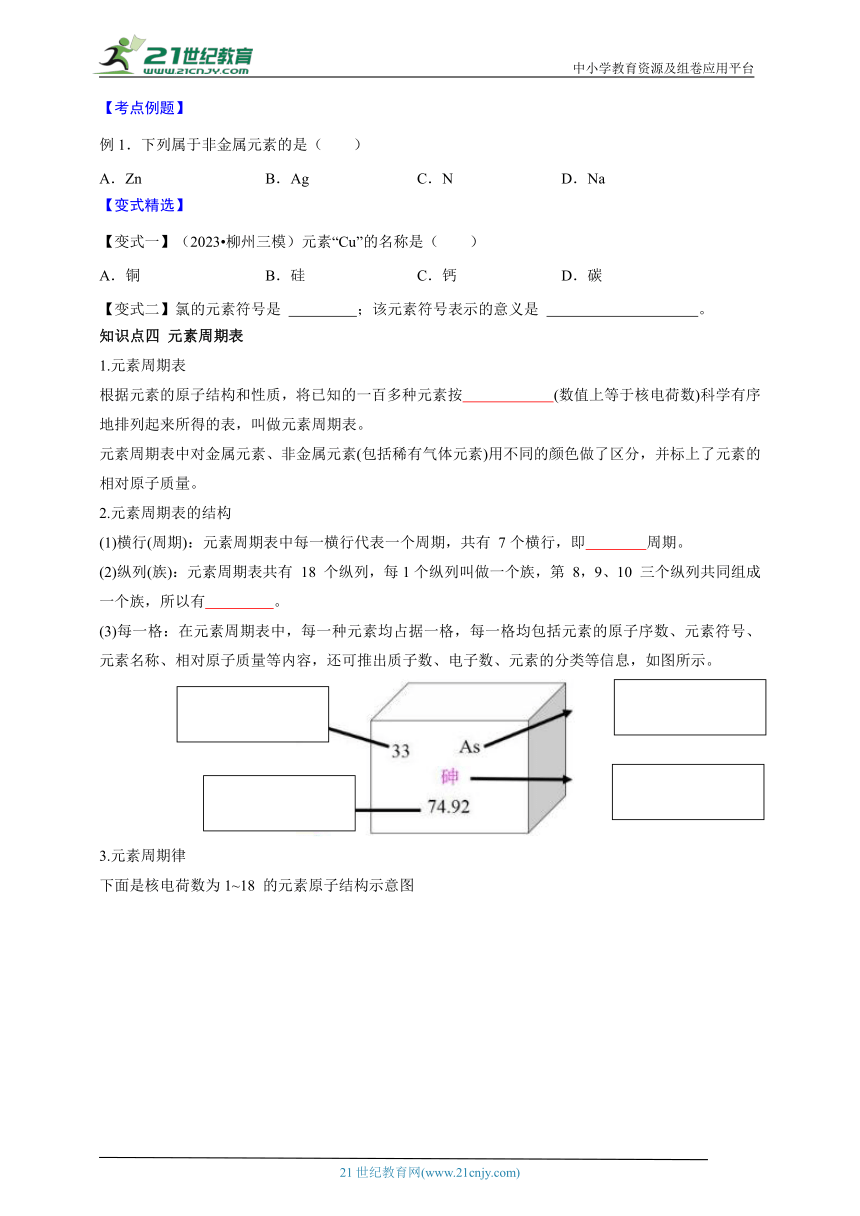
(3)每一格:在元素周期表中,每一种元素均占据一格,每一格均包括元素的原子序数、元素符号、元素名称、相对原子质量等内容,还可推出质子数、电子数、元素的分类等信息,如图所示。
3.元素周期律
下面是核电荷数为1~18 的元素原子结构示意图
根据表格,你能找到哪些规律
(1)每一横行(同一周期 ),从左到右 即 依次增加,最 层电子数依次增加, 相同。
(2)每一横行(同一周期)开头的元素是 元素(第一周期除外),靠近尾部的元素是 元素,结尾的是 元素。
(3)每一纵列(同一族),从上到下 依次增加,最外层电子数 ( He 除外),化学性质 。
4.元素周期表的意义
(1)是学习和研究化学知识的重要工具。
(2)为寻找新元素提供了理论依据。
(3)由于元素周期表中位置越靠近的元素性质越相似,启发人们在元素周期表的一定区域内寻找新物质(如半导体材料、农药、催化剂等)。
【考点例题】
例1.如图是钠元素和氯元素在元素周期表中的信息和两种原子的结构示意图,下列有关说法不正确的是( )
A.钠元素和氯元素处在同一族
B.二者组成的化合物是由离子构成的
C.一个钠原子质量比一个氯原子质量小
D.钠元素和氯元素的本质区别是质子数不同
【变式精选】
【变式一】(2023 长丰县一模)如图是元素周期表中碘元素的部分信息、碘原子的结构示意图。下列说法正确的是( )
A.碘的相对原子质量为126.9g,原子核内质子数为53
B.碘原子核外共有53个电子,最外层有7个电子
C.碘是人体必需的微量元素,缺碘会引起皮肤角质化
D.碘元素属于非金属元素,碘原子在化学反应中易失电子
知识点一 元素(共7小题)
1.(2023 泸水市模拟)在我们的日常生活中出现了“加碘食盐”、“高钙牛奶”、“富硒茶叶”、“含氟牙膏”等商品.这里的碘、铁、钙、硒、氟应理解为( )
A.分子 B.单质 C.元素 D.氧化物
2.(2023春 行唐县期末)科学家发现某些原子具有放射性,即原子能自动地放射出一些固定的粒子。据此推断,当一种元素的原子经放射后,变成了另一种元素的原子,它一定放射了( )
A.中子 B.质子 C.电子 D.离子
3.(2023 凤庆县二模)根据下表信息可知碳﹣12、碳﹣14都属于碳元素,判断依据是( )
质子数 核外电子数 最外层电子数 电子层数
碳﹣12 6 6 4 2
碳﹣14 6 6 4 2
A.质子数相同 B.核外电子数相同
C.最外层电子数相同 D.电子层数相同
4.(2023 东城区二模)地壳中含量最多的元素是( )
A.O B.Si C.Fe D.Al
5.(2023 绥江县二模)铁元素在地壳中含量居( )
A.第一位 B.第二位 C.第三位 D.第四位
6.(2023 秦淮区二模)在地壳中的含量居于第三位的元素是( )
A.铝 B.硅 C.氧 D.铁
7.(2023 海南模拟)“化学”一词最早出于清朝的《化学鉴原》一书,该书把地壳中含量第二的元素翻译成“矽(xī)”,如今把这种“矽”元素命名为( )
A.氧 B.硅 C.铝 D.铁
知识点二 宏观元素与微观粒子(共5小题)
8.(2023 凤凰县三模)“宏观辨识与微观探析”是化学学科核心素养之一。下列有关元素和原子、分子的认识不正确的是( )
A.原子是由分子构成的
B.元素是质子数相同的一类原子的总称
C.原子是化学变化中的最小粒子
D.分子是不断运动的
9.(2023 市南区一模)思维导图有助于建构知识,如图是有关物质宏观组成和微观构成的思维导图,其中“▲”处应填入的是( )
A.离子 B.电子 C.质子 D.中子
10.(2023 桂林一模)在H2、H2SO4、H2O、H2O2四种物质的分子中都含有( )
A.氢原子 B.1个氢分子 C.2个氢元素 D.氢气
(多选)11.(2022秋 讷河市期末)下列说法正确的是( )
A.二氧化碳是由碳元素和氧元素组成的
B.二氧化碳是由一个碳元素和一个氧元素组成的
C.二氧化碳是由一个碳原子和一个氧分子组成的
D.一个二氧化碳分子是由一个碳原子和两个氧原子构成的
12.(2023 莒南县二模)在宏观、微观和符号之间建立联系是化学学科的特点。
(1)物质的组成及构成关系如图所示,图中①表示的是 。
(2)由一种元素组成的物质 (填“一定”或“不一定”)是纯净物。
(3)下面是几种粒子的结构示意图,回答下列问题。
A﹣E共有 种元素。
知识点三 元素符号(共6小题)
13.(2023 鹤城区校级模拟)下列符号既能表示一种元素,又能表示一个原子的是( )
A.O2 B.Mg2+ C.H D.2N2
14.(2023 松山区三模)下列各组元素中,元素符号的第一个字母不相同的一组是( )
A.锰、锌 B.氩、金 C.铅、铂 D.氦、汞
15.(2023 宜州区二模)元素“Ca”的名称是( )
A.钙 B.碳 C.铜 D.氯
16.(2023 赣州三模)南昌海昏侯墓遗址公园展示了玉石文物,下列玉石组成的元素中属于非金属元素的是( )
A.Al B.Na C.K D.Si
17.(2023 崇明区二模)属于金属元素的是( )
A.碳 B.氢 C.氦 D.镁
18.(2022春 东阳市校级月考)元素符号的意义:
(1)宏观上表示 ,如“N”表示氮元素,“O”表示氧元素。每种元素只能有一种元素符号。
(2)微观上表示这种元素的 ,如“N”表示1 个氮原子,“O”表示1 个氧原子。如果物质直接由原子构成,则该元素符号还表示一种物质,如“Fe”表示铁这种物质。
知识点四 元素周期表(共5小题)
19.(2023 红河州一模)景泰蓝作为一种美术工艺品,其制法即于铜器表面上以各色珐琅质涂成花纹,花纹的四周嵌以铜丝或金银丝,再用高火度烧即成。如图是元素周期表中银元素的信息示意图,对图中信息理解不正确的是( )
A.银元素的符号为Ag
B.银的原子序数为47
C.银是一种金属元素
D.一个银原子的质量为107.9g
20.(2023 瑶海区三模)2022年10月31日,梦天实验舱(搭具直上动型直原子钟、冷原子键光钟)成功发射,氢和锶在元素周期表中的信息如图,下列说法正确的是( )
A.氢和锶都属于金属元素
B.1个氢原子的质量为1.008g
C.锶原子的核外电子数38
D.氢元素与锶元素的本质区别是原子质量不同
21.(2023 姜堰区二模)第31届“世界大学生运动会”将在成都开幕。碲化镉发电玻璃将成为本次大运会的“黑科技”。碲元素的信息如图,下列说法正确的是( )
A.碲属于金属元素
B.碲原子中子数为52
C.碲原子核外电子数为52
D.碲原子相对原子质量为127.6g
22.(2023 咸安区模拟)如图是钠元素和氯元素在元素周期表中的信息和有关的4种粒子结构示意图,下列说法正确的是( )
A.钠、氯都属于金属元素
B.氯化钠是由a、d两种粒子构成的
C.氯的相对原子质量是35.45g
D.a表示的是一种阴离子
23.(2022 哈尔滨模拟)下列微观粒子图所表示的元素在元素周期表中同一纵行的是( )
A.①② B.①②③ C.①③⑤ D.①③④
B.
1. (2023 金昌)某食品营养成分表中标有钠、钙、铁的含量,这里的“钠、钙、铁”指的是( )
A.原子 B.分子 C.元素 D.单质
2. (2023 扬州)重氢可应用于光导纤维制备,重氢和氢都属于氢元素,是因为它们的原子具有相同的( )
A.质子数 B.中子数
C.体积 D.相对原子质量
3. (2023 宜昌)缺铁会引起贫血,这里的“铁”应理解为( )
A.元素 B.原子 C.分子 D.单质
4. (2023 自贡)在宏观、微观和符号之间建立联系是学习化学的重要思维方式。
(1)从宏观角度分析,氧气是由氧 (填“元素”或“原子”)组成的。
(2)中国科学院院士张青莲教授于1983年当选为国际原子量委员会委员,他主持测定了多种元素相对原子质量的新值,其中相对原子质量确定为152的铕元素的原子序数为63,则铕原子的核外电子数为 。
(3)根据下列粒子的结构示意图,回答下列问题:
①属于非金属元素的有 (填数字)种。
②与氧元素具有相似化学性质的是 (填元素符号)。
③由镁和氯两种元素组成化合物的化学式为 。
5. (2023 天门)中国芯彰显中国“智”造,芯片的基材主要是高纯硅。硅元素在元素周期表中的信息及硅原子的结构示意图如图。下列说法不正确的是( )
A.硅元素属于金属元素
B.硅的相对原子质量为28.09
C.硅元素位于元素周期表中第三周期
D.硅原子核外有3个电子层,最外层有4个电子
6. (2023 河南)我国化学家张青莲教授主持测定了铟、锑、铈等元素的相对原子质量的新值。铈元素在元素周期表中的相关信息如图所示,下列有关说法不正确的是( )
A.铈属于金属元素
B.铈的元素符号是Ce
C.铈的相对原子质量为140.1g
D.铈原子的质子数为58
7. (2023 新疆)硒是人体必需的微量元素,具有防癌抗癌的作用。结合如图分析,下列说法错误的是( )
A.硒元素属于金属元素
B.硒原子的质子数是34
C.硒元素的相对原子质量为78.96
D.硒原子核外有4个电子层
答案和解析
5. 认识物质是由元素组成的,知道质子数相同的一类原子属于同种元素。(化学观念)
6. 能对元素进行简单分类,了解元素符号所表示的意义。(化学观念)
7. 识记并正确书写常见元素的名称和符号。(化学观念)
8. 初步认识元素周期表,能根据元素的原子序数在元素周期表中查到指定元素的相关信息。(科学思维)
5.初步认识元素性质与原子核外电子排布(特别是最外层电子数)的密切关系。(科学思维)
知识点一 元素
物质是由元素组成的,如氧气是由氧元素组成的,过氧化氢是由氢元素和氧元素组成的,加碘食盐中含有碘元素等。元素是组成物质的基本成分。
过氧化氢分子和二氧化碳分子中都含氧原子,这些氧原子的原子核内都含有8个质子,即核电荷数为8,化学上将质子数(即核电荷数)为8的所有氧原子统称为氧元素。同样,将质子数为 1的所有氢原子统称为氢元素,将质子数为6的所有碳原子统称为碳元素。
1.元素的定义:元素是质子数(即核电荷数)相同的一类原子的总称。
质子数决定元素的种类,即元素原子质子数不同,元素种类不同。
【说明】
(1)具有相同质子数的微粒不一定是同种元素,微粒可能是分子、原子或离子。如水分子(H2O)和氖原子(Ne)都有10个质子,但不属于同种元素。
(2)这里所说的“一类原子”包括两种情况:①质子数相同、中子数不同的原子,如碳12、碳13、碳14,它们都属于碳元素;②质子数相同、电子数不同的单核粒子属于同种元素,如Na和Na+都属于钠元素。
(3)元素是一个宏观(填宏观或微观)概念,只讲种类,不讲个数。
(4)物质发生化学变化时,分子的种类发生变化,原子的种类不变,元素的种类也不会改变。
(5)元素的性质,尤其是化学性质,主要由最外层电子数决定。通常,最外层电子数相同,化学性质相似。
2.元素的种类
物质的种类非常多,已知的有上亿种,但是,组成这些物质的元素并不多,到目前为止,已经发现的元素只有一百多种。
3.元素与原子的比较
项目 元素 原子
概念 具有相同质子数(即核电荷数)的一类原子的总称。一种元素可包含几种原子。如氢元素包含、、 化学变化中的最小粒子
区别 宏观概念,只讲种类,不讲个数 微观概念,既讲种类,又讲个数
使用范围 描述物质宏观组成,如二氧化硫是由硫元素和氧元素组成的 用来描述由原子直接构成的物质和分子的构成。如铁是由铁原子构成的,1个水分子是由 2个氢原子和1个氧原子构成的
联系 只要质子数(即核电荷数)相同的一类原子就属于同一种元素。原子是元素的最小单位,元素则是原子的一个归类“集体”,即元素和原子是总体和个体的关系
4.元素的存在
(1)空气中含量居前两位的元素是氮、氧(按体积分数计算,氮气约占 78%,氧气约占 21%)。
(2)生物细胞中含量居前四位的元素如下表所示。
元素 氧 碳 氢 氮
质量分数 /% 65 18 10 3
(4)地壳中各种元素的含量分布如图所示。
地壳中含量居于前四位的元素是氧、硅、铝、铁。
(4)海水中含量居于前四位的元素是氧、氢、氯、钠。
【考点例题】
例1.(2023 九台区一模)患贫血病的人可以多吃韭菜,因为韭菜是一种含铁量很高的蔬菜,每100克韭菜中含铁8.9毫克。这里的铁指的是( )
A.铁元素 B.铁单质 C.氧化铁 D.铁的化合物
【答案】A
【解析】解:在韭菜中,铁是以无机盐的形式存在的,这里的“铁”不是以单质、分子、原子等形式存在,这里所指的“铁”是强调存在的元素,与具体形态无关。
故选:A。
【变式精选】
【变式一】(2023 沂源县一模)元素之间的根本区别是原子的( )
A.核内质子数不同 B.核外电子数不同
C.核内中子数不同 D.相对原子质量不同
【答案】A
【解析】解:根据不同种元素之间的本质区别是质子数不同,故选A。
【变式二】(2023 梁溪区二模)地壳中含量第二的非金属元素是( )
A.Si B.O C.Al D.Fe
【答案】A
【解析】解:地壳含量较多的元素(前四种)按含量从高到低的排序为:氧、硅、铝、铁,所以地壳中含量居第二位的非金属元素是硅元素,硅元素符号是:Si。
故选:A。
知识点二 宏观元素与微观粒子
1.物质、元素、分子、原子等概念的区别及联系
关于物质、元素、分子、原子的区别和联系可进行简单的归纳,如下所示。
2.“宏观”与“微观”的区别和联系
元素是宏观概念,只有种类之分,没有个数之别。在讨论物质的组成时,一般用“某物质由什么元素组成”来描述,其中只涉及类别而没有数量多少的含义;而分子、原子、离子等是微观概念,既有种类之分又有数量之别,当讨论物质的微观结构时,一般用“某物质由什么分子(或原子、离子)构成”“每个某分子是由多少个某原子构成的”来描述。一般是元素与“组成”匹配,而分子、原子、离子与“构成”匹配。
注意物质的描述过程中“宏观与宏观”“微观与微观”对应。
【考点例题】
例1.思维导图有助于建构知识,如图是小金建立的有关物质宏观组成和微观构成的思维导图,其中“▲”应填入的是( )
A.原子 B.中子 C.元素 D.质子
【答案】C
【解析】解:宏观上物质是由元素组成的;具有相同核电荷数的一类原子总称为元素,其中“▲”应填入的是元素。
故选:C。
【变式精选】
【变式二】下列说法中正确的是( )
A.二氧化碳由二个氧元素和一个碳元素组成
B.二氧化碳由碳、氧两种元素组成
C.二氧化碳由碳和氧气两种单质组成
D.二氧化碳由氧分子和碳原子构成
【答案】B
【解析】解:A、元素只讲种类,不讲个数,故选项说法错误。
B、二氧化碳由碳、氧两种元素组成,故选项说法正确。
C、物质是由元素组成的,二氧化碳由碳、氧两种元素组成,不含碳和氧气两种单质,故选项说法错误。
D、二氧化碳是由二氧化碳分子构成的,不含氧分子,故选项说法错误。
故选:B。
知识点三 元素符号
1.元素符号的规定
国际上统一采用元素拉丁文名称的第一个字母(大写)来表示元素,如果几种元素拉丁文名称的第一个字母相同,就附加一个小写字母来区别,如N表示氮元素,Na表示钠元素。
2.元素符号的写法
(1)由一个字母表示的元素符号要大写,如 H、C、K、S 等。
(2)由两个字母表示的元素符号,第一个字母大写,第二个字母小写,如 Na、Mg、Cu 等。书写这类元素符号时,特别注意要辨清第一个字母相同的一些类似的元素符号,如 Cu、Ca、Cl等。
(3)常见元素符号规范写法如下:
3.元素符号的含义
(1)意义
①微观意义:表示这种元素的一个原子
②宏观意义:表示一种元素
如H的意义:表示氢元素(宏观)、表示一个氢原子(微观)
(4) 对于由原子直接构成的物质,元素符号还表示一种物质。例如,Fe可以表示铁元素、一个铁原子、铁这种物质。
(5) 元素符号前面加化学计量数时,只能表示多个原子,不再表示这种元素,因为元素只讲种类不讲个数。如2N,只能表示两个氮原子,而不再表示氮元素,该符号只有微观含义。
4.元素的分类
元素分为三类:一是金属元素;二是非金属元素;三是稀有气体元素。
(1)金属元素:汉字名称偏旁为“钅”的元素,加上金和汞。由金属元素组成的金属,通常状况下为固体,只有汞(通常状况下为液体)除外,另外,金属由原子直接构成。
(2)非金属元素:通常状况下,非金属元素有三种状态一是中文名称有“气”字头的,是气态非金属元素;二是中文名称有“氵”字旁的,是液态非金属元素;三是中文名称有“石”字旁的,是固态非金属元素。
(3)稀有气体元素:通常状况下,稀有气体为气体,它们的中文名称中都有“气”字头,它们是由原子直接构成的,如氨(He)。
【考点例题】
例1.下列属于非金属元素的是( )
A.Zn B.Ag C.N D.Na
【答案】C
【解析】解:A、Zn为锌元素的元素符号,带“钅”字旁,属于金属元素,故A错误;
B、Ag为银元素的元素符号,带“钅”字旁,属于金属元素,故B错误;
C、N为氮元素的元素符号,带“气”字头,属于非金属元素,故C正确;
D、Na为金元素的元素符号,带“钅”字旁,属于金属元素,故D错误。
故选:C。
【变式精选】
【变式一】(2023 柳州三模)元素“Cu”的名称是( )
A.铜 B.硅 C.钙 D.碳
【答案】A
【解析】解:A、元素“Cu”的名称是铜,故选项正确。
B、硅的元素符号为Si,故选项错误。
C、钙的元素符号为Ca,故选项错误。
D、碳的元素符号为C,故选项错误。
故选:A。
【变式二】氯的元素符号是 ;该元素符号表示的意义是 。
【答案】Cl;表示氯元素,表示1个氯原子。
【解析】解:氯的元素符号为Cl,第一个字母大写,第二个字母小写;
元素符号宏观上表示元素,微观上表示该元素的一个原子,所以该元素符号表示的意义是表示氯元素,表示1个氯原子。
知识点四 元素周期表
1.元素周期表
根据元素的原子结构和性质,将已知的一百多种元素按原子序数(数值上等于核电荷数)科学有序地排列起来所得的表,叫做元素周期表。
元素周期表中对金属元素、非金属元素(包括稀有气体元素)用不同的颜色做了区分,并标上了元素的相对原子质量。
2.元素周期表的结构
(1)横行(周期):元素周期表中每一横行代表一个周期,共有 7个横行,即7个周期。
(2)纵列(族):元素周期表共有 18 个纵列,每1个纵列叫做一个族,第 8,9、10 三个纵列共同组成一个族,所以有16个族。
(3)每一格:在元素周期表中,每一种元素均占据一格,每一格均包括元素的原子序数、元素符号、元素名称、相对原子质量等内容,还可推出质子数、电子数、元素的分类等信息,如图所示。
3.元素周期律
下面是核电荷数为1~18 的元素原子结构示意图
根据表格,你能找到哪些规律
(1)每一横行(同一周期 ),从左到右核电荷数即质子数依次增加,最外层电子数依次增加,电子层数相同。
(2)每一横行(同一周期)开头的元素是金属元素(第一周期除外),靠近尾部的元素是非金属元素,结尾的是稀有气体元素。
(3)每一纵列(同一族),从上到下电子层数依次增加,最外层电子数相同( He 除外),化学性质相似。
4.元素周期表的意义
(1)是学习和研究化学知识的重要工具。
(2)为寻找新元素提供了理论依据。
(3)由于元素周期表中位置越靠近的元素性质越相似,启发人们在元素周期表的一定区域内寻找新物质(如半导体材料、农药、催化剂等)。
【考点例题】
例1.如图是钠元素和氯元素在元素周期表中的信息和两种原子的结构示意图,下列有关说法不正确的是( )
A.钠元素和氯元素处在同一族
B.二者组成的化合物是由离子构成的
C.一个钠原子质量比一个氯原子质量小
D.钠元素和氯元素的本质区别是质子数不同
【答案】A
【解析】解:A.钠原子和氯原子核外具有相同的电子层数,故位于同一周期,最外层电子数不同,故不属于同一族,故错误;
B.钠原子易失去最外层的电子而形成钠离子,氯原子易得到电子而形成氯离子,二者组成的氯化钠是由钠离子和氯离子构成的,故正确;
C.由元素周期表可知,钠元素的相对原子质量小于氯元素的相对原子质量,所以一个钠原子质量比一个氯原子质量小,故正确;
D.不同的元素本质区别是质子数不同,故正确。
故选:A。
【变式精选】
【变式一】(2023 长丰县一模)如图是元素周期表中碘元素的部分信息、碘原子的结构示意图。下列说法正确的是( )
A.碘的相对原子质量为126.9g,原子核内质子数为53
B.碘原子核外共有53个电子,最外层有7个电子
C.碘是人体必需的微量元素,缺碘会引起皮肤角质化
D.碘元素属于非金属元素,碘原子在化学反应中易失电子
【答案】B
【解析】解:A、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为126.9,相对原子质量单位是“1”,不是“克”;原子结构示意图中,圆圈内数字表示核内质子数,原子核内质子数为53;故选项说法错误。
B、由碘原子的结构示意图,碘原子核外共有53个电子,最外层有7个电子,故选项说法正确。
C、碘是人体必需的微量元素,碘是合成甲状腺激素的主要元素,缺乏会患甲状腺肿大,故选项说法错误。
D、碘元素带“石”字旁,属于固态非金属元素,最外层电子数是7,在化学反应中易得到1个电子而形成阴离子,故选项说法错误。
故选:B。
知识点一 元素(共7小题)
1.(2023 泸水市模拟)在我们的日常生活中出现了“加碘食盐”、“高钙牛奶”、“富硒茶叶”、“含氟牙膏”等商品.这里的碘、铁、钙、硒、氟应理解为( )
A.分子 B.单质 C.元素 D.氧化物
【答案】C
【解析】解:“加碘食盐”、“高钙牛奶”、“富硒茶叶”、“含氟牙膏”等商品中的“碘、铁、钙、硒、氟”等不是以单质、氧化物、分子、原子等形式存在,这里所指的“碘、铁、钙、硒、氟”是强调存在的元素,与具体形态无关。
故选:C。
2.(2023春 行唐县期末)科学家发现某些原子具有放射性,即原子能自动地放射出一些固定的粒子。据此推断,当一种元素的原子经放射后,变成了另一种元素的原子,它一定放射了( )
A.中子 B.质子 C.电子 D.离子
【答案】B
【解析】解:元素是质子数(即核电荷数)相同的一类原子的总称,即原子的种类由其所含质子数决定,因此当一种元素的原子经放射后,变成了另一种元素的原子,则核内质子数发生了改变,则它一定放射了质子。
故选:B。
3.(2023 凤庆县二模)根据下表信息可知碳﹣12、碳﹣14都属于碳元素,判断依据是( )
质子数 核外电子数 最外层电子数 电子层数
碳﹣12 6 6 4 2
碳﹣14 6 6 4 2
A.质子数相同 B.核外电子数相同
C.最外层电子数相同 D.电子层数相同
【答案】A
【解析】解:决定元素种类的是核内质子数,碳﹣12、碳﹣14都属于碳元素是因为核内质子数相同,故A正确。
故选:A。
4.(2023 东城区二模)地壳中含量最多的元素是( )
A.O B.Si C.Fe D.Al
【答案】A
【解析】解:地壳中各元素及含量由多到少的顺序是氧、硅、铝、铁、钙、钠、钾、镁、氢;所以含量最多的元素为氧元素。
故选:A。
5.(2023 绥江县二模)铁元素在地壳中含量居( )
A.第一位 B.第二位 C.第三位 D.第四位
【答案】D
【解析】解:地壳含量较多的元素(前四种)按含量从高到低的排序为:氧、硅、铝、铁,则铁元素在地壳中含量居第四位。
故选:D。
6.(2023 秦淮区二模)在地壳中的含量居于第三位的元素是( )
A.铝 B.硅 C.氧 D.铁
【答案】A
【解析】解:地壳含量较多的元素按含量从高到低的排序为:氧、硅、铝、铁、钙、钠、钾、镁,居于第三位的元素是铝。
故选:A。
7.(2023 海南模拟)“化学”一词最早出于清朝的《化学鉴原》一书,该书把地壳中含量第二的元素翻译成“矽(xī)”,如今把这种“矽”元素命名为( )
A.氧 B.硅 C.铝 D.铁
【答案】B
【解析】解:《化学鉴原》一书把地壳中含量第二的元素翻译成“矽(xī)”,地壳含量较多的元素(前四种)按含量从高到低的排序为:氧、硅、铝、铁,则如今把这种“矽”元素命名为硅。
故选:B。
知识点二 宏观元素与微观粒子(共5小题)
8.(2023 凤凰县三模)“宏观辨识与微观探析”是化学学科核心素养之一。下列有关元素和原子、分子的认识不正确的是( )
A.原子是由分子构成的
B.元素是质子数相同的一类原子的总称
C.原子是化学变化中的最小粒子
D.分子是不断运动的
【答案】A
【解析】解:A.分子是由原子构成的,故A错误;
B.元素是质子数(或核电荷数)相同的一类原子的总称,故B正确;
C.原子是化学变化中的最小粒子,故C正确;
D.分子是不断运动的,故D正确;
故选:A。
9.(2023 市南区一模)思维导图有助于建构知识,如图是有关物质宏观组成和微观构成的思维导图,其中“▲”处应填入的是( )
A.离子 B.电子 C.质子 D.中子
【答案】A
【解析】解:原子构成分子,原子也可以直接构成物质;原子通过得失电子变成离子;具有相同核电荷数的一类原子总称为元素,其中“▲”应填入的是离子。
故选:A。
10.(2023 桂林一模)在H2、H2SO4、H2O、H2O2四种物质的分子中都含有( )
A.氢原子 B.1个氢分子 C.2个氢元素 D.氢气
【答案】A
【解析】解:A、H2、H2SO4、H2O、H2O2四种物质的分子中都含有氢原子,故A正确;
B、只有氢气中含有氢分子,其他物质不含有氢分子,故B错误;
C、元素只讲种类,不讲个数,故C错误;
D、H2、H2SO4、H2O、H2O2四种物质的分子中不含有氢气,而含有氢原子,故D错误。
故选:A。
(多选)11.(2022秋 讷河市期末)下列说法正确的是( )
A.二氧化碳是由碳元素和氧元素组成的
B.二氧化碳是由一个碳元素和一个氧元素组成的
C.二氧化碳是由一个碳原子和一个氧分子组成的
D.一个二氧化碳分子是由一个碳原子和两个氧原子构成的
【答案】AD
【解析】解:A、物质由元素组成,二氧化碳是由碳元素和氧元素组成的,故选项说法正确。
B、二氧化碳由碳元素和氧元素组成,元素只讲种类、不讲个数,故选项说法错误。
C、二氧化碳是由二氧化碳分子构成的,分子是由原子构成的,1个二氧化碳分子是由1个碳原子和2个氧原子构成的,故选项说法错误。
D、分子由原子构成,1个二氧化碳分子是由1个碳原子和2个氧原子构成的,故选项说法正确。
故选:AD。
12.(2023 莒南县二模)在宏观、微观和符号之间建立联系是化学学科的特点。
(1)物质的组成及构成关系如图所示,图中①表示的是 。
(2)由一种元素组成的物质 (填“一定”或“不一定”)是纯净物。
(3)下面是几种粒子的结构示意图,回答下列问题。
A﹣E共有 种元素。
【答案】(1)离子;
(2)不一定;
(3)4。
【解析】解:(1)氯化钠是由钠离子和氯离子构成的,原子得失电子可以转化为离子,离子可以构成物质,因此图中①表示的是离子;
(2)由一种元素组成的物质不一定是纯净物,可能为混合物,如氧气和臭氧的混合物等
(3)具有相同核电荷数或质子数的一类原子的总成为元素,因此A﹣E共有4种元素;
知识点三 元素符号(共6小题)
13.(2023 鹤城区校级模拟)下列符号既能表示一种元素,又能表示一个原子的是( )
A.O2 B.Mg2+ C.H D.2N2
【答案】C
【解析】解:A.这是氧气的化学式,不能表示氧元素,也不能表示一个氧原子,故错误;
B.这是镁离子的符号,不能表示镁元素,也不能表示一个镁原子,故错误;
C.这是氢元素的元素符号,可以表示氢元素,还可以表示1个氢原子,故正确;
D.这个化学符号只能表示2个氮分子,不能表示一种元素,也不能表示一个原子,故错误。
故选:C。
14.(2023 松山区三模)下列各组元素中,元素符号的第一个字母不相同的一组是( )
A.锰、锌 B.氩、金 C.铅、铂 D.氦、汞
【答案】A
【解析】解:A、锰、锌元素的元素符号分别是Mn、Zn,第一个字母不同,故A正确;
B、氩、金元素的元素符号分别是Ar、Au,第一个字母相同,故B错误;
C、铅、铂元素的元素符号分别是Pb、Pt,第一个字母相同,故C错误;
D、氦、汞元素的元素符号分别是He、Hg,第一个字母相同,故D错误。
故选:A。
15.(2023 宜州区二模)元素“Ca”的名称是( )
A.钙 B.碳 C.铜 D.氯
【答案】A
【解析】解:A、钙的元素符号是Ca,故选项正确。
B、碳的元素符号是C,故选项错误。
C、铜的元素符号是Cu,故选项错误。
D、氯的元素符号是Cl,故选项错误。
故选:A。
16.(2023 赣州三模)南昌海昏侯墓遗址公园展示了玉石文物,下列玉石组成的元素中属于非金属元素的是( )
A.Al B.Na C.K D.Si
【答案】D
【解析】解:根据常见元素的分类可知,铝、钠、钾都是金属元素,硅是非金属元素,故选:D。
17.(2023 崇明区二模)属于金属元素的是( )
A.碳 B.氢 C.氦 D.镁
【答案】D
【解析】解:在金属元素中,通常状况下绝大多数都是固态金属元素,只有汞例外,它是液态金属元素;在非金属元素中,中文名称带有“石”字旁的是固态非金属元素,带有“气”字头的是气态非金属元素,带有“氵”字旁的是液态非金属元素;对于稀有气体元素来说,主要是指氦、氖、氩、氪、氙等,有时也把它们归类到非金属元素中。
A、碳属于非金属元素,故A错误;
B、氢属于非金属元素,故B错误;
C、氦属于非金属元素,故C错误;
D、镁属于金属元素,故D正确。
故选:D。
18.(2022春 东阳市校级月考)元素符号的意义:
(1)宏观上表示 ,如“N”表示氮元素,“O”表示氧元素。每种元素只能有一种元素符号。
(2)微观上表示这种元素的 ,如“N”表示1 个氮原子,“O”表示1 个氧原子。如果物质直接由原子构成,则该元素符号还表示一种物质,如“Fe”表示铁这种物质。
【答案】(1)一种元素;
(2)一个原子。
【解析】解:一般情况下元素符号具有两种意义,宏观上表示一种元素;微观上表示该元素的一个原子;
由原子直接构成的物质,则该元素符号还表示一种物质。
知识点四 元素周期表(共5小题)
19.(2023 红河州一模)景泰蓝作为一种美术工艺品,其制法即于铜器表面上以各色珐琅质涂成花纹,花纹的四周嵌以铜丝或金银丝,再用高火度烧即成。如图是元素周期表中银元素的信息示意图,对图中信息理解不正确的是( )
A.银元素的符号为Ag
B.银的原子序数为47
C.银是一种金属元素
D.一个银原子的质量为107.9g
【答案】D
【解析】解:A.根据元素周期表中的一格可知,右上角的字母表示该元素的元素符号,则银元素的符号为Ag,故A正确;
B.元素名称的左上角数字表示原子序数,则银的原子序数为47,故B正确;
C.银字带“钅”字旁,属于金属元素,故C正确;
D.根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,属于银原子的相对原子质量为107.9,故D错误;
故选:D。
20.(2023 瑶海区三模)2022年10月31日,梦天实验舱(搭具直上动型直原子钟、冷原子键光钟)成功发射,氢和锶在元素周期表中的信息如图,下列说法正确的是( )
A.氢和锶都属于金属元素
B.1个氢原子的质量为1.008g
C.锶原子的核外电子数38
D.氢元素与锶元素的本质区别是原子质量不同
【答案】C
【解析】解:A、由元素名称可知,氢带“气”字头,属于非金属元素;锶带“钅”字旁,属于金属元素,故选项说法错误。
B、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为1.008,而不是1个氢原子的质量为1.008g,故选项说法错误。
C、根据元素周期表中的一格可知,左上角的数字表示原子序数,该元素的原子序数为38,根据原子中原子序数=核电荷数=质子数=核外电子数,则该元素的原子核外电子数为38,故选项说法正确。
D、元素是具有相同质子数(即核电荷数)的一类原子的总称,不同种元素的本质区别是质子数(即核电荷数)不同,不是原子质量不同,故选项说法错误。
故选:C。
21.(2023 姜堰区二模)第31届“世界大学生运动会”将在成都开幕。碲化镉发电玻璃将成为本次大运会的“黑科技”。碲元素的信息如图,下列说法正确的是( )
A.碲属于金属元素
B.碲原子中子数为52
C.碲原子核外电子数为52
D.碲原子相对原子质量为127.6g
【答案】C
【解析】解:A、碲带“石”字旁,属于非金属元素,故选项说法错误。
B、根据元素周期表中的一格可知,左上角的数字表示原子序数,该元素的原子序数为52;根据原子中原子序数=核电荷数=质子数,则该原子的核内质子数为52;相对原子质量为127.6,不是质子数的两倍,则原子核内中子数不等于52,故选项说法错误。
C、根据元素周期表中的一格可知,左上角的数字表示原子序数,该元素的原子序数为52;根据原子中原子序数=核电荷数=质子数,则该元素的原子核内质子数为52,故选项说法正确。
D、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为127.6,相对原子质量单位是“1”,不是“g”,常省略不写,错误。
故选:C。
22.(2023 咸安区模拟)如图是钠元素和氯元素在元素周期表中的信息和有关的4种粒子结构示意图,下列说法正确的是( )
A.钠、氯都属于金属元素
B.氯化钠是由a、d两种粒子构成的
C.氯的相对原子质量是35.45g
D.a表示的是一种阴离子
【答案】B
【解析】解:A、钠带“钅”字旁,属于金属元素;氯有“气”字头,属于非金属元素,故选项说法错误。
B、氯化钠是由钠离子和氯离子构成的,a、d两种粒子分别是钠离子、氯离子,故选项说法正确。
C、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为35.45,相对原子质量单位是“1”,不是“克”,故选项说法错误。
D、a质子数=11,核外电子数=10,质子数>核外电子数,为阳离子,故选项说法错误。
故选:B。
23.(2022 哈尔滨模拟)下列微观粒子图所表示的元素在元素周期表中同一纵行的是( )
A.①② B.①②③ C.①③⑤ D.①③④
【答案】A
【解析】解:由元素周期表的规律,从原子结构方面看:同一纵行,原子最外层电子数相同,从上到下电子层数逐渐增加;①②最外层电子数均为7,表示元素周期表中同一纵行的原子。
故选:A。
8. (2023 金昌)某食品营养成分表中标有钠、钙、铁的含量,这里的“钠、钙、铁”指的是( )
A.原子 B.分子 C.元素 D.单质
【答案】C
【解析】解:某食品营养成分表中标有钠、钙、铁的含量,这里的“钠、钙、铁”指的是元素。
故选:C。
9. (2023 扬州)重氢可应用于光导纤维制备,重氢和氢都属于氢元素,是因为它们的原子具有相同的( )
A.质子数 B.中子数
C.体积 D.相对原子质量
【答案】A
【解析】解:元素是质子数(即核电荷数)相同的一类原子的总称,同种元素的原子质子数相同,重氢和氢都属于氢元素,是因为它们的原子具有相同的质子数。
故选:A。
10. (2023 宜昌)缺铁会引起贫血,这里的“铁”应理解为( )
A.元素 B.原子 C.分子 D.单质
【答案】A
【解析】解:缺铁性贫血中的“铁”不是以单质、分子、原子等形式存在,这里所指的“铁”是强调存在的元素,与具体形态无关。
故选:A。
11. (2023 自贡)在宏观、微观和符号之间建立联系是学习化学的重要思维方式。
(1)从宏观角度分析,氧气是由氧 (填“元素”或“原子”)组成的。
(2)中国科学院院士张青莲教授于1983年当选为国际原子量委员会委员,他主持测定了多种元素相对原子质量的新值,其中相对原子质量确定为152的铕元素的原子序数为63,则铕原子的核外电子数为 。
(3)根据下列粒子的结构示意图,回答下列问题:
①属于非金属元素的有 (填数字)种。
②与氧元素具有相似化学性质的是 (填元素符号)。
③由镁和氯两种元素组成化合物的化学式为 。
【答案】(1)元素;
(2)63;
(3)①3;②S;③MgCl2。
【解析】解:(1)从宏观角度分析,氧气是由氧元素组成的;
(2)原子序数=核电荷数=核外电子数,因此相对原子质量为152的铕元素的原子序数为63,则铕原子的核外电子数为63;
(3)①带有气字旁的字属于非金属元素,因此O(氧)、S(硫)、氯(氯)均为非金属元素,共有3种;
②元素的化学性质是由粒子的最外层电子数决定的,最外层电子数相同,化学性质相似,因此与氧元素具有相似化学性质的是硫元素,符号为S;
③镁原子易失去最外层的2个电子,形成带有2个单位的镁离子,化合价为+2价;氯原子易得到1个电子,形成带有1个单位负电荷的氯离子,化合价为﹣1价;根据化合价法则可知,两种元素组成化合物的化学式为MgCl2;
12. (2023 天门)中国芯彰显中国“智”造,芯片的基材主要是高纯硅。硅元素在元素周期表中的信息及硅原子的结构示意图如图。下列说法不正确的是( )
A.硅元素属于金属元素
B.硅的相对原子质量为28.09
C.硅元素位于元素周期表中第三周期
D.硅原子核外有3个电子层,最外层有4个电子
【答案】A
【解析】解:A.硅字带有石字旁,属于非金属元素,故错误;
B.元素名称的正下方数字表示相对原子质量,因此硅的相对原子质量为28.09,故正确;
C.周期数=原子电子层数,根据硅原子结构可知,硅元素位于元素周期表中第三周期,故正确;
D.根据硅原子结构可知,硅原子核外有3个电子层,最外层有4个电子,故正确;
故选:A。
13. (2023 河南)我国化学家张青莲教授主持测定了铟、锑、铈等元素的相对原子质量的新值。铈元素在元素周期表中的相关信息如图所示,下列有关说法不正确的是( )
A.铈属于金属元素
B.铈的元素符号是Ce
C.铈的相对原子质量为140.1g
D.铈原子的质子数为58
【答案】C
【解析】解:A.铈字带有钅字旁,属于金属元素,故正确;
B.根据图示信息可知,铈的元素符号是Ce,故正确;
C.铈的相对原子质量为140.1,单位应为“1”,不是“g”,故错误;
D.元素名称左上角的数字表示原子序数,原子序数=质子数,因此铈原子的质子数为58,故正确;
故选:C。
14. (2023 新疆)硒是人体必需的微量元素,具有防癌抗癌的作用。结合如图分析,下列说法错误的是( )
A.硒元素属于金属元素
B.硒原子的质子数是34
C.硒元素的相对原子质量为78.96
D.硒原子核外有4个电子层
【答案】A
【解析】解:A.硒字带有石字旁,属于非金属元素,故错误;
B.元素名称左上角的数字表示原子序数,原子序数=质子数,因此硒原子的质子数是34,故正确;
C.元素名称的正下方的数字表示相对原子质量,因此硒元素的相对原子质量为78.96,故正确;
D.根据硒原子的结构示意图可知,硒原子核外有4个电子层,故正确;
故选:A。
目标导航
教材全解
精选精练
真题检测
目标导航
教材全解
精选精练
真题检测
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
课题3 元素
1. 认识物质是由元素组成的,知道质子数相同的一类原子属于同种元素。(化学观念)
2. 能对元素进行简单分类,了解元素符号所表示的意义。(化学观念)
3. 识记并正确书写常见元素的名称和符号。(化学观念)
4. 初步认识元素周期表,能根据元素的原子序数在元素周期表中查到指定元素的相关信息。(科学思维)
5.初步认识元素性质与原子核外电子排布(特别是最外层电子数)的密切关系。(科学思维)
知识点一 元素
物质是由 组成的,如氧气是由氧元素组成的,过氧化氢是由氢元素和氧元素组成的,加碘食盐中含有碘元素等。元素是组成物质的基本成分。
过氧化氢分子和二氧化碳分子中都含氧原子,这些氧原子的原子核内都含有8个质子,即核电荷数为8,化学上将质子数(即核电荷数)为8的所有氧原子统称为 。同样,将质子数为 1的所有氢原子统称为 ,将质子数为6的所有碳原子统称为 。
1.元素的定义:元素是 (即核电荷数)相同的一类原子的总称。
决定元素的种类,即元素原子 不同,元素种类不同。
【说明】
(1)具有相同质子数的微粒不一定是同种元素,微粒可能是分子、原子或离子。如水分子(H2O)和氖原子(Ne)都有10个质子,但不属于同种元素。
(2)这里所说的“一类原子”包括两种情况:①质子数相同、中子数不同的原子,如碳12、碳13、碳14,它们都属于碳元素;②质子数相同、电子数不同的单核粒子属于同种元素,如Na和Na+都属于钠元素。
(3)元素是一个 (填宏观或微观),只讲 ,不讲个数。
(4)物质发生化学变化时, 的种类发生变化, 的种类不变, 的种类也不会改变。
(5)元素的性质,尤其是化学性质,主要由 决定。通常,最外层电子数 ,化学性质 。
2.元素的种类
物质的种类非常多,已知的有上亿种,但是,组成这些物质的元素并不多,到目前为止,已经发现的元素只有一百多种。
3.元素与原子的比较
项目 元素 原子
概念 具有相同 (即核电荷数)的一类原子的总称。一种元素可包含几种原子。如氢元素包含、、 中的最小粒子
区别 宏观概念,只讲 ,不讲个数 微观概念,既讲种类,又讲个数
使用范围 描述物质 组成,如二氧化硫是由硫元素和氧元素组成的 用来描述由原子直接构成的 和 的构成。如铁是由铁原子构成的,1个水分子是由 2个氢原子和1个氧原子构成的
联系 只要质子数(即核电荷数)相同的一类原子就属于同一种元素。 是元素的最小单位,元素则是原子的一个归类“集体”,即元素和原子是总体和个体的关系
4.元素的存在
(1)空气中含量居前两位的元素是 、 (按体积分数计算,氮气约占 ,氧气约占 )。
(2)生物细胞中含量居前四位的元素如下表所示。
元素 氮
质量分数 /% 65 18 10 3
(3)地壳中各种元素的含量分布如图所示。
地壳中含量居于前四位的元素是 。
(4)海水中含量居于前四位的元素是 。
【考点例题】
例1.(2023 九台区一模)患贫血病的人可以多吃韭菜,因为韭菜是一种含铁量很高的蔬菜,每100克韭菜中含铁8.9毫克。这里的铁指的是( )
A.铁元素 B.铁单质 C.氧化铁 D.铁的化合物
【变式精选】
【变式一】(2023 沂源县一模)元素之间的根本区别是原子的( )
A.核内质子数不同 B.核外电子数不同
C.核内中子数不同 D.相对原子质量不同
【变式二】(2023 梁溪区二模)地壳中含量第二的非金属元素是( )
A.Si B.O C.Al D.Fe
知识点二 宏观元素与微观粒子
1.物质、元素、分子、原子等概念的区别及联系
关于物质、元素、分子、原子的区别和联系可进行简单的归纳,如下所示。
2.“宏观”与“微观”的区别和联系
元素是 概念,只有 之分,没有 之别。在讨论物质的组成时,一般用“某物质由什么元素组成”来描述,其中只涉及类别而没有数量多少的含义;而分子、 、 等是微观概念,既有种类之分又有数量之别,当讨论物质的微观结构时,一般用“某物质由什么分子(或原子、离子)构成”“每个某分子是由多少个某原子构成的”来描述。一般是元素与“组成”匹配,而分子、原子、离子与“构成”匹配。
注意物质的描述过程中“宏观与宏观”“微观与微观”对应。
【考点例题】
例1.思维导图有助于建构知识,如图是小金建立的有关物质宏观组成和微观构成的思维导图,其中“▲”应填入的是( )
A.原子 B.中子 C.元素 D.质子
【变式精选】
【变式二】下列说法中正确的是( )
A.二氧化碳由二个氧元素和一个碳元素组成
B.二氧化碳由碳、氧两种元素组成
C.二氧化碳由碳和氧气两种单质组成
D.二氧化碳由氧分子和碳原子构成
知识点三 元素符号
1.元素符号的规定
国际上统一采用元素拉丁文名称的第一个字母(大写)来表示元素,如果几种元素拉丁文名称的第一个字母相同,就附加一个小写字母来区别,如N表示氮元素,Na表示钠元素。
2.元素符号的写法
(1)由一个字母表示的元素符号要 ,如 H、C、K、S 等。
(2)由两个字母表示的元素符号,第一个字母大写,第二个字母小写,如 Na、Mg、Cu 等。书写这类元素符号时,特别注意要辨清第一个字母相同的一些类似的元素符号,如 Cu、Ca、Cl等。
(3)常见元素符号规范写法如下:
3.元素符号的含义
(1)意义
①微观意义:表示这种元素的一个
②宏观意义:表示一种
如H的意义:表示氢元素(宏观)、表示一个氢原子(微观)
(2) 对于由原子直接构成的物质,元素符号还表示一种 。例如,Fe可以表示铁元素、一个铁原子、铁这种物质。
(3) 元素符号前面加化学计量数时,只能表示多个原子,不再表示这种元素,因为元素只讲种类不讲个数。如2N,只能表示两个氮原子,而不再表示氮元素,该符号只有微观含义。
4.元素的分类
元素分为三类:一是 元素;二是 元素;三是 元素。
(1)金属元素:汉字名称偏旁为“钅”的元素,加上金和汞。由金属元素组成的金属,通常状况下为固体,只有汞(通常状况下为液体)除外,另外,金属由原子直接构成。
(2)非金属元素:通常状况下,非金属元素有三种状态一是中文名称有“气”字头的,是气态非金属元素;二是中文名称有“氵”字旁的,是液态非金属元素;三是中文名称有“石”字旁的,是固态非金属元素。
(3)稀有气体元素:通常状况下,稀有气体为气体,它们的中文名称中都有“气”字头,它们是由原子直接构成的,如氨(He)。
【考点例题】
例1.下列属于非金属元素的是( )
A.Zn B.Ag C.N D.Na
【变式精选】
【变式一】(2023 柳州三模)元素“Cu”的名称是( )
A.铜 B.硅 C.钙 D.碳
【变式二】氯的元素符号是 ;该元素符号表示的意义是 。
知识点四 元素周期表
1.元素周期表
根据元素的原子结构和性质,将已知的一百多种元素按 (数值上等于核电荷数)科学有序地排列起来所得的表,叫做元素周期表。
元素周期表中对金属元素、非金属元素(包括稀有气体元素)用不同的颜色做了区分,并标上了元素的相对原子质量。
2.元素周期表的结构
(1)横行(周期):元素周期表中每一横行代表一个周期,共有 7个横行,即 周期。
(2)纵列(族):元素周期表共有 18 个纵列,每1个纵列叫做一个族,第 8,9、10 三个纵列共同组成一个族,所以有 。
(3)每一格:在元素周期表中,每一种元素均占据一格,每一格均包括元素的原子序数、元素符号、元素名称、相对原子质量等内容,还可推出质子数、电子数、元素的分类等信息,如图所示。
3.元素周期律
下面是核电荷数为1~18 的元素原子结构示意图
根据表格,你能找到哪些规律
(1)每一横行(同一周期 ),从左到右 即 依次增加,最 层电子数依次增加, 相同。
(2)每一横行(同一周期)开头的元素是 元素(第一周期除外),靠近尾部的元素是 元素,结尾的是 元素。
(3)每一纵列(同一族),从上到下 依次增加,最外层电子数 ( He 除外),化学性质 。
4.元素周期表的意义
(1)是学习和研究化学知识的重要工具。
(2)为寻找新元素提供了理论依据。
(3)由于元素周期表中位置越靠近的元素性质越相似,启发人们在元素周期表的一定区域内寻找新物质(如半导体材料、农药、催化剂等)。
【考点例题】
例1.如图是钠元素和氯元素在元素周期表中的信息和两种原子的结构示意图,下列有关说法不正确的是( )
A.钠元素和氯元素处在同一族
B.二者组成的化合物是由离子构成的
C.一个钠原子质量比一个氯原子质量小
D.钠元素和氯元素的本质区别是质子数不同
【变式精选】
【变式一】(2023 长丰县一模)如图是元素周期表中碘元素的部分信息、碘原子的结构示意图。下列说法正确的是( )
A.碘的相对原子质量为126.9g,原子核内质子数为53
B.碘原子核外共有53个电子,最外层有7个电子
C.碘是人体必需的微量元素,缺碘会引起皮肤角质化
D.碘元素属于非金属元素,碘原子在化学反应中易失电子
知识点一 元素(共7小题)
1.(2023 泸水市模拟)在我们的日常生活中出现了“加碘食盐”、“高钙牛奶”、“富硒茶叶”、“含氟牙膏”等商品.这里的碘、铁、钙、硒、氟应理解为( )
A.分子 B.单质 C.元素 D.氧化物
2.(2023春 行唐县期末)科学家发现某些原子具有放射性,即原子能自动地放射出一些固定的粒子。据此推断,当一种元素的原子经放射后,变成了另一种元素的原子,它一定放射了( )
A.中子 B.质子 C.电子 D.离子
3.(2023 凤庆县二模)根据下表信息可知碳﹣12、碳﹣14都属于碳元素,判断依据是( )
质子数 核外电子数 最外层电子数 电子层数
碳﹣12 6 6 4 2
碳﹣14 6 6 4 2
A.质子数相同 B.核外电子数相同
C.最外层电子数相同 D.电子层数相同
4.(2023 东城区二模)地壳中含量最多的元素是( )
A.O B.Si C.Fe D.Al
5.(2023 绥江县二模)铁元素在地壳中含量居( )
A.第一位 B.第二位 C.第三位 D.第四位
6.(2023 秦淮区二模)在地壳中的含量居于第三位的元素是( )
A.铝 B.硅 C.氧 D.铁
7.(2023 海南模拟)“化学”一词最早出于清朝的《化学鉴原》一书,该书把地壳中含量第二的元素翻译成“矽(xī)”,如今把这种“矽”元素命名为( )
A.氧 B.硅 C.铝 D.铁
知识点二 宏观元素与微观粒子(共5小题)
8.(2023 凤凰县三模)“宏观辨识与微观探析”是化学学科核心素养之一。下列有关元素和原子、分子的认识不正确的是( )
A.原子是由分子构成的
B.元素是质子数相同的一类原子的总称
C.原子是化学变化中的最小粒子
D.分子是不断运动的
9.(2023 市南区一模)思维导图有助于建构知识,如图是有关物质宏观组成和微观构成的思维导图,其中“▲”处应填入的是( )
A.离子 B.电子 C.质子 D.中子
10.(2023 桂林一模)在H2、H2SO4、H2O、H2O2四种物质的分子中都含有( )
A.氢原子 B.1个氢分子 C.2个氢元素 D.氢气
(多选)11.(2022秋 讷河市期末)下列说法正确的是( )
A.二氧化碳是由碳元素和氧元素组成的
B.二氧化碳是由一个碳元素和一个氧元素组成的
C.二氧化碳是由一个碳原子和一个氧分子组成的
D.一个二氧化碳分子是由一个碳原子和两个氧原子构成的
12.(2023 莒南县二模)在宏观、微观和符号之间建立联系是化学学科的特点。
(1)物质的组成及构成关系如图所示,图中①表示的是 。
(2)由一种元素组成的物质 (填“一定”或“不一定”)是纯净物。
(3)下面是几种粒子的结构示意图,回答下列问题。
A﹣E共有 种元素。
知识点三 元素符号(共6小题)
13.(2023 鹤城区校级模拟)下列符号既能表示一种元素,又能表示一个原子的是( )
A.O2 B.Mg2+ C.H D.2N2
14.(2023 松山区三模)下列各组元素中,元素符号的第一个字母不相同的一组是( )
A.锰、锌 B.氩、金 C.铅、铂 D.氦、汞
15.(2023 宜州区二模)元素“Ca”的名称是( )
A.钙 B.碳 C.铜 D.氯
16.(2023 赣州三模)南昌海昏侯墓遗址公园展示了玉石文物,下列玉石组成的元素中属于非金属元素的是( )
A.Al B.Na C.K D.Si
17.(2023 崇明区二模)属于金属元素的是( )
A.碳 B.氢 C.氦 D.镁
18.(2022春 东阳市校级月考)元素符号的意义:
(1)宏观上表示 ,如“N”表示氮元素,“O”表示氧元素。每种元素只能有一种元素符号。
(2)微观上表示这种元素的 ,如“N”表示1 个氮原子,“O”表示1 个氧原子。如果物质直接由原子构成,则该元素符号还表示一种物质,如“Fe”表示铁这种物质。
知识点四 元素周期表(共5小题)
19.(2023 红河州一模)景泰蓝作为一种美术工艺品,其制法即于铜器表面上以各色珐琅质涂成花纹,花纹的四周嵌以铜丝或金银丝,再用高火度烧即成。如图是元素周期表中银元素的信息示意图,对图中信息理解不正确的是( )
A.银元素的符号为Ag
B.银的原子序数为47
C.银是一种金属元素
D.一个银原子的质量为107.9g
20.(2023 瑶海区三模)2022年10月31日,梦天实验舱(搭具直上动型直原子钟、冷原子键光钟)成功发射,氢和锶在元素周期表中的信息如图,下列说法正确的是( )
A.氢和锶都属于金属元素
B.1个氢原子的质量为1.008g
C.锶原子的核外电子数38
D.氢元素与锶元素的本质区别是原子质量不同
21.(2023 姜堰区二模)第31届“世界大学生运动会”将在成都开幕。碲化镉发电玻璃将成为本次大运会的“黑科技”。碲元素的信息如图,下列说法正确的是( )
A.碲属于金属元素
B.碲原子中子数为52
C.碲原子核外电子数为52
D.碲原子相对原子质量为127.6g
22.(2023 咸安区模拟)如图是钠元素和氯元素在元素周期表中的信息和有关的4种粒子结构示意图,下列说法正确的是( )
A.钠、氯都属于金属元素
B.氯化钠是由a、d两种粒子构成的
C.氯的相对原子质量是35.45g
D.a表示的是一种阴离子
23.(2022 哈尔滨模拟)下列微观粒子图所表示的元素在元素周期表中同一纵行的是( )
A.①② B.①②③ C.①③⑤ D.①③④
B.
1. (2023 金昌)某食品营养成分表中标有钠、钙、铁的含量,这里的“钠、钙、铁”指的是( )
A.原子 B.分子 C.元素 D.单质
2. (2023 扬州)重氢可应用于光导纤维制备,重氢和氢都属于氢元素,是因为它们的原子具有相同的( )
A.质子数 B.中子数
C.体积 D.相对原子质量
3. (2023 宜昌)缺铁会引起贫血,这里的“铁”应理解为( )
A.元素 B.原子 C.分子 D.单质
4. (2023 自贡)在宏观、微观和符号之间建立联系是学习化学的重要思维方式。
(1)从宏观角度分析,氧气是由氧 (填“元素”或“原子”)组成的。
(2)中国科学院院士张青莲教授于1983年当选为国际原子量委员会委员,他主持测定了多种元素相对原子质量的新值,其中相对原子质量确定为152的铕元素的原子序数为63,则铕原子的核外电子数为 。
(3)根据下列粒子的结构示意图,回答下列问题:
①属于非金属元素的有 (填数字)种。
②与氧元素具有相似化学性质的是 (填元素符号)。
③由镁和氯两种元素组成化合物的化学式为 。
5. (2023 天门)中国芯彰显中国“智”造,芯片的基材主要是高纯硅。硅元素在元素周期表中的信息及硅原子的结构示意图如图。下列说法不正确的是( )
A.硅元素属于金属元素
B.硅的相对原子质量为28.09
C.硅元素位于元素周期表中第三周期
D.硅原子核外有3个电子层,最外层有4个电子
6. (2023 河南)我国化学家张青莲教授主持测定了铟、锑、铈等元素的相对原子质量的新值。铈元素在元素周期表中的相关信息如图所示,下列有关说法不正确的是( )
A.铈属于金属元素
B.铈的元素符号是Ce
C.铈的相对原子质量为140.1g
D.铈原子的质子数为58
7. (2023 新疆)硒是人体必需的微量元素,具有防癌抗癌的作用。结合如图分析,下列说法错误的是( )
A.硒元素属于金属元素
B.硒原子的质子数是34
C.硒元素的相对原子质量为78.96
D.硒原子核外有4个电子层
答案和解析
5. 认识物质是由元素组成的,知道质子数相同的一类原子属于同种元素。(化学观念)
6. 能对元素进行简单分类,了解元素符号所表示的意义。(化学观念)
7. 识记并正确书写常见元素的名称和符号。(化学观念)
8. 初步认识元素周期表,能根据元素的原子序数在元素周期表中查到指定元素的相关信息。(科学思维)
5.初步认识元素性质与原子核外电子排布(特别是最外层电子数)的密切关系。(科学思维)
知识点一 元素
物质是由元素组成的,如氧气是由氧元素组成的,过氧化氢是由氢元素和氧元素组成的,加碘食盐中含有碘元素等。元素是组成物质的基本成分。
过氧化氢分子和二氧化碳分子中都含氧原子,这些氧原子的原子核内都含有8个质子,即核电荷数为8,化学上将质子数(即核电荷数)为8的所有氧原子统称为氧元素。同样,将质子数为 1的所有氢原子统称为氢元素,将质子数为6的所有碳原子统称为碳元素。
1.元素的定义:元素是质子数(即核电荷数)相同的一类原子的总称。
质子数决定元素的种类,即元素原子质子数不同,元素种类不同。
【说明】
(1)具有相同质子数的微粒不一定是同种元素,微粒可能是分子、原子或离子。如水分子(H2O)和氖原子(Ne)都有10个质子,但不属于同种元素。
(2)这里所说的“一类原子”包括两种情况:①质子数相同、中子数不同的原子,如碳12、碳13、碳14,它们都属于碳元素;②质子数相同、电子数不同的单核粒子属于同种元素,如Na和Na+都属于钠元素。
(3)元素是一个宏观(填宏观或微观)概念,只讲种类,不讲个数。
(4)物质发生化学变化时,分子的种类发生变化,原子的种类不变,元素的种类也不会改变。
(5)元素的性质,尤其是化学性质,主要由最外层电子数决定。通常,最外层电子数相同,化学性质相似。
2.元素的种类
物质的种类非常多,已知的有上亿种,但是,组成这些物质的元素并不多,到目前为止,已经发现的元素只有一百多种。
3.元素与原子的比较
项目 元素 原子
概念 具有相同质子数(即核电荷数)的一类原子的总称。一种元素可包含几种原子。如氢元素包含、、 化学变化中的最小粒子
区别 宏观概念,只讲种类,不讲个数 微观概念,既讲种类,又讲个数
使用范围 描述物质宏观组成,如二氧化硫是由硫元素和氧元素组成的 用来描述由原子直接构成的物质和分子的构成。如铁是由铁原子构成的,1个水分子是由 2个氢原子和1个氧原子构成的
联系 只要质子数(即核电荷数)相同的一类原子就属于同一种元素。原子是元素的最小单位,元素则是原子的一个归类“集体”,即元素和原子是总体和个体的关系
4.元素的存在
(1)空气中含量居前两位的元素是氮、氧(按体积分数计算,氮气约占 78%,氧气约占 21%)。
(2)生物细胞中含量居前四位的元素如下表所示。
元素 氧 碳 氢 氮
质量分数 /% 65 18 10 3
(4)地壳中各种元素的含量分布如图所示。
地壳中含量居于前四位的元素是氧、硅、铝、铁。
(4)海水中含量居于前四位的元素是氧、氢、氯、钠。
【考点例题】
例1.(2023 九台区一模)患贫血病的人可以多吃韭菜,因为韭菜是一种含铁量很高的蔬菜,每100克韭菜中含铁8.9毫克。这里的铁指的是( )
A.铁元素 B.铁单质 C.氧化铁 D.铁的化合物
【答案】A
【解析】解:在韭菜中,铁是以无机盐的形式存在的,这里的“铁”不是以单质、分子、原子等形式存在,这里所指的“铁”是强调存在的元素,与具体形态无关。
故选:A。
【变式精选】
【变式一】(2023 沂源县一模)元素之间的根本区别是原子的( )
A.核内质子数不同 B.核外电子数不同
C.核内中子数不同 D.相对原子质量不同
【答案】A
【解析】解:根据不同种元素之间的本质区别是质子数不同,故选A。
【变式二】(2023 梁溪区二模)地壳中含量第二的非金属元素是( )
A.Si B.O C.Al D.Fe
【答案】A
【解析】解:地壳含量较多的元素(前四种)按含量从高到低的排序为:氧、硅、铝、铁,所以地壳中含量居第二位的非金属元素是硅元素,硅元素符号是:Si。
故选:A。
知识点二 宏观元素与微观粒子
1.物质、元素、分子、原子等概念的区别及联系
关于物质、元素、分子、原子的区别和联系可进行简单的归纳,如下所示。
2.“宏观”与“微观”的区别和联系
元素是宏观概念,只有种类之分,没有个数之别。在讨论物质的组成时,一般用“某物质由什么元素组成”来描述,其中只涉及类别而没有数量多少的含义;而分子、原子、离子等是微观概念,既有种类之分又有数量之别,当讨论物质的微观结构时,一般用“某物质由什么分子(或原子、离子)构成”“每个某分子是由多少个某原子构成的”来描述。一般是元素与“组成”匹配,而分子、原子、离子与“构成”匹配。
注意物质的描述过程中“宏观与宏观”“微观与微观”对应。
【考点例题】
例1.思维导图有助于建构知识,如图是小金建立的有关物质宏观组成和微观构成的思维导图,其中“▲”应填入的是( )
A.原子 B.中子 C.元素 D.质子
【答案】C
【解析】解:宏观上物质是由元素组成的;具有相同核电荷数的一类原子总称为元素,其中“▲”应填入的是元素。
故选:C。
【变式精选】
【变式二】下列说法中正确的是( )
A.二氧化碳由二个氧元素和一个碳元素组成
B.二氧化碳由碳、氧两种元素组成
C.二氧化碳由碳和氧气两种单质组成
D.二氧化碳由氧分子和碳原子构成
【答案】B
【解析】解:A、元素只讲种类,不讲个数,故选项说法错误。
B、二氧化碳由碳、氧两种元素组成,故选项说法正确。
C、物质是由元素组成的,二氧化碳由碳、氧两种元素组成,不含碳和氧气两种单质,故选项说法错误。
D、二氧化碳是由二氧化碳分子构成的,不含氧分子,故选项说法错误。
故选:B。
知识点三 元素符号
1.元素符号的规定
国际上统一采用元素拉丁文名称的第一个字母(大写)来表示元素,如果几种元素拉丁文名称的第一个字母相同,就附加一个小写字母来区别,如N表示氮元素,Na表示钠元素。
2.元素符号的写法
(1)由一个字母表示的元素符号要大写,如 H、C、K、S 等。
(2)由两个字母表示的元素符号,第一个字母大写,第二个字母小写,如 Na、Mg、Cu 等。书写这类元素符号时,特别注意要辨清第一个字母相同的一些类似的元素符号,如 Cu、Ca、Cl等。
(3)常见元素符号规范写法如下:
3.元素符号的含义
(1)意义
①微观意义:表示这种元素的一个原子
②宏观意义:表示一种元素
如H的意义:表示氢元素(宏观)、表示一个氢原子(微观)
(4) 对于由原子直接构成的物质,元素符号还表示一种物质。例如,Fe可以表示铁元素、一个铁原子、铁这种物质。
(5) 元素符号前面加化学计量数时,只能表示多个原子,不再表示这种元素,因为元素只讲种类不讲个数。如2N,只能表示两个氮原子,而不再表示氮元素,该符号只有微观含义。
4.元素的分类
元素分为三类:一是金属元素;二是非金属元素;三是稀有气体元素。
(1)金属元素:汉字名称偏旁为“钅”的元素,加上金和汞。由金属元素组成的金属,通常状况下为固体,只有汞(通常状况下为液体)除外,另外,金属由原子直接构成。
(2)非金属元素:通常状况下,非金属元素有三种状态一是中文名称有“气”字头的,是气态非金属元素;二是中文名称有“氵”字旁的,是液态非金属元素;三是中文名称有“石”字旁的,是固态非金属元素。
(3)稀有气体元素:通常状况下,稀有气体为气体,它们的中文名称中都有“气”字头,它们是由原子直接构成的,如氨(He)。
【考点例题】
例1.下列属于非金属元素的是( )
A.Zn B.Ag C.N D.Na
【答案】C
【解析】解:A、Zn为锌元素的元素符号,带“钅”字旁,属于金属元素,故A错误;
B、Ag为银元素的元素符号,带“钅”字旁,属于金属元素,故B错误;
C、N为氮元素的元素符号,带“气”字头,属于非金属元素,故C正确;
D、Na为金元素的元素符号,带“钅”字旁,属于金属元素,故D错误。
故选:C。
【变式精选】
【变式一】(2023 柳州三模)元素“Cu”的名称是( )
A.铜 B.硅 C.钙 D.碳
【答案】A
【解析】解:A、元素“Cu”的名称是铜,故选项正确。
B、硅的元素符号为Si,故选项错误。
C、钙的元素符号为Ca,故选项错误。
D、碳的元素符号为C,故选项错误。
故选:A。
【变式二】氯的元素符号是 ;该元素符号表示的意义是 。
【答案】Cl;表示氯元素,表示1个氯原子。
【解析】解:氯的元素符号为Cl,第一个字母大写,第二个字母小写;
元素符号宏观上表示元素,微观上表示该元素的一个原子,所以该元素符号表示的意义是表示氯元素,表示1个氯原子。
知识点四 元素周期表
1.元素周期表
根据元素的原子结构和性质,将已知的一百多种元素按原子序数(数值上等于核电荷数)科学有序地排列起来所得的表,叫做元素周期表。
元素周期表中对金属元素、非金属元素(包括稀有气体元素)用不同的颜色做了区分,并标上了元素的相对原子质量。
2.元素周期表的结构
(1)横行(周期):元素周期表中每一横行代表一个周期,共有 7个横行,即7个周期。
(2)纵列(族):元素周期表共有 18 个纵列,每1个纵列叫做一个族,第 8,9、10 三个纵列共同组成一个族,所以有16个族。
(3)每一格:在元素周期表中,每一种元素均占据一格,每一格均包括元素的原子序数、元素符号、元素名称、相对原子质量等内容,还可推出质子数、电子数、元素的分类等信息,如图所示。
3.元素周期律
下面是核电荷数为1~18 的元素原子结构示意图
根据表格,你能找到哪些规律
(1)每一横行(同一周期 ),从左到右核电荷数即质子数依次增加,最外层电子数依次增加,电子层数相同。
(2)每一横行(同一周期)开头的元素是金属元素(第一周期除外),靠近尾部的元素是非金属元素,结尾的是稀有气体元素。
(3)每一纵列(同一族),从上到下电子层数依次增加,最外层电子数相同( He 除外),化学性质相似。
4.元素周期表的意义
(1)是学习和研究化学知识的重要工具。
(2)为寻找新元素提供了理论依据。
(3)由于元素周期表中位置越靠近的元素性质越相似,启发人们在元素周期表的一定区域内寻找新物质(如半导体材料、农药、催化剂等)。
【考点例题】
例1.如图是钠元素和氯元素在元素周期表中的信息和两种原子的结构示意图,下列有关说法不正确的是( )
A.钠元素和氯元素处在同一族
B.二者组成的化合物是由离子构成的
C.一个钠原子质量比一个氯原子质量小
D.钠元素和氯元素的本质区别是质子数不同
【答案】A
【解析】解:A.钠原子和氯原子核外具有相同的电子层数,故位于同一周期,最外层电子数不同,故不属于同一族,故错误;
B.钠原子易失去最外层的电子而形成钠离子,氯原子易得到电子而形成氯离子,二者组成的氯化钠是由钠离子和氯离子构成的,故正确;
C.由元素周期表可知,钠元素的相对原子质量小于氯元素的相对原子质量,所以一个钠原子质量比一个氯原子质量小,故正确;
D.不同的元素本质区别是质子数不同,故正确。
故选:A。
【变式精选】
【变式一】(2023 长丰县一模)如图是元素周期表中碘元素的部分信息、碘原子的结构示意图。下列说法正确的是( )
A.碘的相对原子质量为126.9g,原子核内质子数为53
B.碘原子核外共有53个电子,最外层有7个电子
C.碘是人体必需的微量元素,缺碘会引起皮肤角质化
D.碘元素属于非金属元素,碘原子在化学反应中易失电子
【答案】B
【解析】解:A、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为126.9,相对原子质量单位是“1”,不是“克”;原子结构示意图中,圆圈内数字表示核内质子数,原子核内质子数为53;故选项说法错误。
B、由碘原子的结构示意图,碘原子核外共有53个电子,最外层有7个电子,故选项说法正确。
C、碘是人体必需的微量元素,碘是合成甲状腺激素的主要元素,缺乏会患甲状腺肿大,故选项说法错误。
D、碘元素带“石”字旁,属于固态非金属元素,最外层电子数是7,在化学反应中易得到1个电子而形成阴离子,故选项说法错误。
故选:B。
知识点一 元素(共7小题)
1.(2023 泸水市模拟)在我们的日常生活中出现了“加碘食盐”、“高钙牛奶”、“富硒茶叶”、“含氟牙膏”等商品.这里的碘、铁、钙、硒、氟应理解为( )
A.分子 B.单质 C.元素 D.氧化物
【答案】C
【解析】解:“加碘食盐”、“高钙牛奶”、“富硒茶叶”、“含氟牙膏”等商品中的“碘、铁、钙、硒、氟”等不是以单质、氧化物、分子、原子等形式存在,这里所指的“碘、铁、钙、硒、氟”是强调存在的元素,与具体形态无关。
故选:C。
2.(2023春 行唐县期末)科学家发现某些原子具有放射性,即原子能自动地放射出一些固定的粒子。据此推断,当一种元素的原子经放射后,变成了另一种元素的原子,它一定放射了( )
A.中子 B.质子 C.电子 D.离子
【答案】B
【解析】解:元素是质子数(即核电荷数)相同的一类原子的总称,即原子的种类由其所含质子数决定,因此当一种元素的原子经放射后,变成了另一种元素的原子,则核内质子数发生了改变,则它一定放射了质子。
故选:B。
3.(2023 凤庆县二模)根据下表信息可知碳﹣12、碳﹣14都属于碳元素,判断依据是( )
质子数 核外电子数 最外层电子数 电子层数
碳﹣12 6 6 4 2
碳﹣14 6 6 4 2
A.质子数相同 B.核外电子数相同
C.最外层电子数相同 D.电子层数相同
【答案】A
【解析】解:决定元素种类的是核内质子数,碳﹣12、碳﹣14都属于碳元素是因为核内质子数相同,故A正确。
故选:A。
4.(2023 东城区二模)地壳中含量最多的元素是( )
A.O B.Si C.Fe D.Al
【答案】A
【解析】解:地壳中各元素及含量由多到少的顺序是氧、硅、铝、铁、钙、钠、钾、镁、氢;所以含量最多的元素为氧元素。
故选:A。
5.(2023 绥江县二模)铁元素在地壳中含量居( )
A.第一位 B.第二位 C.第三位 D.第四位
【答案】D
【解析】解:地壳含量较多的元素(前四种)按含量从高到低的排序为:氧、硅、铝、铁,则铁元素在地壳中含量居第四位。
故选:D。
6.(2023 秦淮区二模)在地壳中的含量居于第三位的元素是( )
A.铝 B.硅 C.氧 D.铁
【答案】A
【解析】解:地壳含量较多的元素按含量从高到低的排序为:氧、硅、铝、铁、钙、钠、钾、镁,居于第三位的元素是铝。
故选:A。
7.(2023 海南模拟)“化学”一词最早出于清朝的《化学鉴原》一书,该书把地壳中含量第二的元素翻译成“矽(xī)”,如今把这种“矽”元素命名为( )
A.氧 B.硅 C.铝 D.铁
【答案】B
【解析】解:《化学鉴原》一书把地壳中含量第二的元素翻译成“矽(xī)”,地壳含量较多的元素(前四种)按含量从高到低的排序为:氧、硅、铝、铁,则如今把这种“矽”元素命名为硅。
故选:B。
知识点二 宏观元素与微观粒子(共5小题)
8.(2023 凤凰县三模)“宏观辨识与微观探析”是化学学科核心素养之一。下列有关元素和原子、分子的认识不正确的是( )
A.原子是由分子构成的
B.元素是质子数相同的一类原子的总称
C.原子是化学变化中的最小粒子
D.分子是不断运动的
【答案】A
【解析】解:A.分子是由原子构成的,故A错误;
B.元素是质子数(或核电荷数)相同的一类原子的总称,故B正确;
C.原子是化学变化中的最小粒子,故C正确;
D.分子是不断运动的,故D正确;
故选:A。
9.(2023 市南区一模)思维导图有助于建构知识,如图是有关物质宏观组成和微观构成的思维导图,其中“▲”处应填入的是( )
A.离子 B.电子 C.质子 D.中子
【答案】A
【解析】解:原子构成分子,原子也可以直接构成物质;原子通过得失电子变成离子;具有相同核电荷数的一类原子总称为元素,其中“▲”应填入的是离子。
故选:A。
10.(2023 桂林一模)在H2、H2SO4、H2O、H2O2四种物质的分子中都含有( )
A.氢原子 B.1个氢分子 C.2个氢元素 D.氢气
【答案】A
【解析】解:A、H2、H2SO4、H2O、H2O2四种物质的分子中都含有氢原子,故A正确;
B、只有氢气中含有氢分子,其他物质不含有氢分子,故B错误;
C、元素只讲种类,不讲个数,故C错误;
D、H2、H2SO4、H2O、H2O2四种物质的分子中不含有氢气,而含有氢原子,故D错误。
故选:A。
(多选)11.(2022秋 讷河市期末)下列说法正确的是( )
A.二氧化碳是由碳元素和氧元素组成的
B.二氧化碳是由一个碳元素和一个氧元素组成的
C.二氧化碳是由一个碳原子和一个氧分子组成的
D.一个二氧化碳分子是由一个碳原子和两个氧原子构成的
【答案】AD
【解析】解:A、物质由元素组成,二氧化碳是由碳元素和氧元素组成的,故选项说法正确。
B、二氧化碳由碳元素和氧元素组成,元素只讲种类、不讲个数,故选项说法错误。
C、二氧化碳是由二氧化碳分子构成的,分子是由原子构成的,1个二氧化碳分子是由1个碳原子和2个氧原子构成的,故选项说法错误。
D、分子由原子构成,1个二氧化碳分子是由1个碳原子和2个氧原子构成的,故选项说法正确。
故选:AD。
12.(2023 莒南县二模)在宏观、微观和符号之间建立联系是化学学科的特点。
(1)物质的组成及构成关系如图所示,图中①表示的是 。
(2)由一种元素组成的物质 (填“一定”或“不一定”)是纯净物。
(3)下面是几种粒子的结构示意图,回答下列问题。
A﹣E共有 种元素。
【答案】(1)离子;
(2)不一定;
(3)4。
【解析】解:(1)氯化钠是由钠离子和氯离子构成的,原子得失电子可以转化为离子,离子可以构成物质,因此图中①表示的是离子;
(2)由一种元素组成的物质不一定是纯净物,可能为混合物,如氧气和臭氧的混合物等
(3)具有相同核电荷数或质子数的一类原子的总成为元素,因此A﹣E共有4种元素;
知识点三 元素符号(共6小题)
13.(2023 鹤城区校级模拟)下列符号既能表示一种元素,又能表示一个原子的是( )
A.O2 B.Mg2+ C.H D.2N2
【答案】C
【解析】解:A.这是氧气的化学式,不能表示氧元素,也不能表示一个氧原子,故错误;
B.这是镁离子的符号,不能表示镁元素,也不能表示一个镁原子,故错误;
C.这是氢元素的元素符号,可以表示氢元素,还可以表示1个氢原子,故正确;
D.这个化学符号只能表示2个氮分子,不能表示一种元素,也不能表示一个原子,故错误。
故选:C。
14.(2023 松山区三模)下列各组元素中,元素符号的第一个字母不相同的一组是( )
A.锰、锌 B.氩、金 C.铅、铂 D.氦、汞
【答案】A
【解析】解:A、锰、锌元素的元素符号分别是Mn、Zn,第一个字母不同,故A正确;
B、氩、金元素的元素符号分别是Ar、Au,第一个字母相同,故B错误;
C、铅、铂元素的元素符号分别是Pb、Pt,第一个字母相同,故C错误;
D、氦、汞元素的元素符号分别是He、Hg,第一个字母相同,故D错误。
故选:A。
15.(2023 宜州区二模)元素“Ca”的名称是( )
A.钙 B.碳 C.铜 D.氯
【答案】A
【解析】解:A、钙的元素符号是Ca,故选项正确。
B、碳的元素符号是C,故选项错误。
C、铜的元素符号是Cu,故选项错误。
D、氯的元素符号是Cl,故选项错误。
故选:A。
16.(2023 赣州三模)南昌海昏侯墓遗址公园展示了玉石文物,下列玉石组成的元素中属于非金属元素的是( )
A.Al B.Na C.K D.Si
【答案】D
【解析】解:根据常见元素的分类可知,铝、钠、钾都是金属元素,硅是非金属元素,故选:D。
17.(2023 崇明区二模)属于金属元素的是( )
A.碳 B.氢 C.氦 D.镁
【答案】D
【解析】解:在金属元素中,通常状况下绝大多数都是固态金属元素,只有汞例外,它是液态金属元素;在非金属元素中,中文名称带有“石”字旁的是固态非金属元素,带有“气”字头的是气态非金属元素,带有“氵”字旁的是液态非金属元素;对于稀有气体元素来说,主要是指氦、氖、氩、氪、氙等,有时也把它们归类到非金属元素中。
A、碳属于非金属元素,故A错误;
B、氢属于非金属元素,故B错误;
C、氦属于非金属元素,故C错误;
D、镁属于金属元素,故D正确。
故选:D。
18.(2022春 东阳市校级月考)元素符号的意义:
(1)宏观上表示 ,如“N”表示氮元素,“O”表示氧元素。每种元素只能有一种元素符号。
(2)微观上表示这种元素的 ,如“N”表示1 个氮原子,“O”表示1 个氧原子。如果物质直接由原子构成,则该元素符号还表示一种物质,如“Fe”表示铁这种物质。
【答案】(1)一种元素;
(2)一个原子。
【解析】解:一般情况下元素符号具有两种意义,宏观上表示一种元素;微观上表示该元素的一个原子;
由原子直接构成的物质,则该元素符号还表示一种物质。
知识点四 元素周期表(共5小题)
19.(2023 红河州一模)景泰蓝作为一种美术工艺品,其制法即于铜器表面上以各色珐琅质涂成花纹,花纹的四周嵌以铜丝或金银丝,再用高火度烧即成。如图是元素周期表中银元素的信息示意图,对图中信息理解不正确的是( )
A.银元素的符号为Ag
B.银的原子序数为47
C.银是一种金属元素
D.一个银原子的质量为107.9g
【答案】D
【解析】解:A.根据元素周期表中的一格可知,右上角的字母表示该元素的元素符号,则银元素的符号为Ag,故A正确;
B.元素名称的左上角数字表示原子序数,则银的原子序数为47,故B正确;
C.银字带“钅”字旁,属于金属元素,故C正确;
D.根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,属于银原子的相对原子质量为107.9,故D错误;
故选:D。
20.(2023 瑶海区三模)2022年10月31日,梦天实验舱(搭具直上动型直原子钟、冷原子键光钟)成功发射,氢和锶在元素周期表中的信息如图,下列说法正确的是( )
A.氢和锶都属于金属元素
B.1个氢原子的质量为1.008g
C.锶原子的核外电子数38
D.氢元素与锶元素的本质区别是原子质量不同
【答案】C
【解析】解:A、由元素名称可知,氢带“气”字头,属于非金属元素;锶带“钅”字旁,属于金属元素,故选项说法错误。
B、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为1.008,而不是1个氢原子的质量为1.008g,故选项说法错误。
C、根据元素周期表中的一格可知,左上角的数字表示原子序数,该元素的原子序数为38,根据原子中原子序数=核电荷数=质子数=核外电子数,则该元素的原子核外电子数为38,故选项说法正确。
D、元素是具有相同质子数(即核电荷数)的一类原子的总称,不同种元素的本质区别是质子数(即核电荷数)不同,不是原子质量不同,故选项说法错误。
故选:C。
21.(2023 姜堰区二模)第31届“世界大学生运动会”将在成都开幕。碲化镉发电玻璃将成为本次大运会的“黑科技”。碲元素的信息如图,下列说法正确的是( )
A.碲属于金属元素
B.碲原子中子数为52
C.碲原子核外电子数为52
D.碲原子相对原子质量为127.6g
【答案】C
【解析】解:A、碲带“石”字旁,属于非金属元素,故选项说法错误。
B、根据元素周期表中的一格可知,左上角的数字表示原子序数,该元素的原子序数为52;根据原子中原子序数=核电荷数=质子数,则该原子的核内质子数为52;相对原子质量为127.6,不是质子数的两倍,则原子核内中子数不等于52,故选项说法错误。
C、根据元素周期表中的一格可知,左上角的数字表示原子序数,该元素的原子序数为52;根据原子中原子序数=核电荷数=质子数,则该元素的原子核内质子数为52,故选项说法正确。
D、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为127.6,相对原子质量单位是“1”,不是“g”,常省略不写,错误。
故选:C。
22.(2023 咸安区模拟)如图是钠元素和氯元素在元素周期表中的信息和有关的4种粒子结构示意图,下列说法正确的是( )
A.钠、氯都属于金属元素
B.氯化钠是由a、d两种粒子构成的
C.氯的相对原子质量是35.45g
D.a表示的是一种阴离子
【答案】B
【解析】解:A、钠带“钅”字旁,属于金属元素;氯有“气”字头,属于非金属元素,故选项说法错误。
B、氯化钠是由钠离子和氯离子构成的,a、d两种粒子分别是钠离子、氯离子,故选项说法正确。
C、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为35.45,相对原子质量单位是“1”,不是“克”,故选项说法错误。
D、a质子数=11,核外电子数=10,质子数>核外电子数,为阳离子,故选项说法错误。
故选:B。
23.(2022 哈尔滨模拟)下列微观粒子图所表示的元素在元素周期表中同一纵行的是( )
A.①② B.①②③ C.①③⑤ D.①③④
【答案】A
【解析】解:由元素周期表的规律,从原子结构方面看:同一纵行,原子最外层电子数相同,从上到下电子层数逐渐增加;①②最外层电子数均为7,表示元素周期表中同一纵行的原子。
故选:A。
8. (2023 金昌)某食品营养成分表中标有钠、钙、铁的含量,这里的“钠、钙、铁”指的是( )
A.原子 B.分子 C.元素 D.单质
【答案】C
【解析】解:某食品营养成分表中标有钠、钙、铁的含量,这里的“钠、钙、铁”指的是元素。
故选:C。
9. (2023 扬州)重氢可应用于光导纤维制备,重氢和氢都属于氢元素,是因为它们的原子具有相同的( )
A.质子数 B.中子数
C.体积 D.相对原子质量
【答案】A
【解析】解:元素是质子数(即核电荷数)相同的一类原子的总称,同种元素的原子质子数相同,重氢和氢都属于氢元素,是因为它们的原子具有相同的质子数。
故选:A。
10. (2023 宜昌)缺铁会引起贫血,这里的“铁”应理解为( )
A.元素 B.原子 C.分子 D.单质
【答案】A
【解析】解:缺铁性贫血中的“铁”不是以单质、分子、原子等形式存在,这里所指的“铁”是强调存在的元素,与具体形态无关。
故选:A。
11. (2023 自贡)在宏观、微观和符号之间建立联系是学习化学的重要思维方式。
(1)从宏观角度分析,氧气是由氧 (填“元素”或“原子”)组成的。
(2)中国科学院院士张青莲教授于1983年当选为国际原子量委员会委员,他主持测定了多种元素相对原子质量的新值,其中相对原子质量确定为152的铕元素的原子序数为63,则铕原子的核外电子数为 。
(3)根据下列粒子的结构示意图,回答下列问题:
①属于非金属元素的有 (填数字)种。
②与氧元素具有相似化学性质的是 (填元素符号)。
③由镁和氯两种元素组成化合物的化学式为 。
【答案】(1)元素;
(2)63;
(3)①3;②S;③MgCl2。
【解析】解:(1)从宏观角度分析,氧气是由氧元素组成的;
(2)原子序数=核电荷数=核外电子数,因此相对原子质量为152的铕元素的原子序数为63,则铕原子的核外电子数为63;
(3)①带有气字旁的字属于非金属元素,因此O(氧)、S(硫)、氯(氯)均为非金属元素,共有3种;
②元素的化学性质是由粒子的最外层电子数决定的,最外层电子数相同,化学性质相似,因此与氧元素具有相似化学性质的是硫元素,符号为S;
③镁原子易失去最外层的2个电子,形成带有2个单位的镁离子,化合价为+2价;氯原子易得到1个电子,形成带有1个单位负电荷的氯离子,化合价为﹣1价;根据化合价法则可知,两种元素组成化合物的化学式为MgCl2;
12. (2023 天门)中国芯彰显中国“智”造,芯片的基材主要是高纯硅。硅元素在元素周期表中的信息及硅原子的结构示意图如图。下列说法不正确的是( )
A.硅元素属于金属元素
B.硅的相对原子质量为28.09
C.硅元素位于元素周期表中第三周期
D.硅原子核外有3个电子层,最外层有4个电子
【答案】A
【解析】解:A.硅字带有石字旁,属于非金属元素,故错误;
B.元素名称的正下方数字表示相对原子质量,因此硅的相对原子质量为28.09,故正确;
C.周期数=原子电子层数,根据硅原子结构可知,硅元素位于元素周期表中第三周期,故正确;
D.根据硅原子结构可知,硅原子核外有3个电子层,最外层有4个电子,故正确;
故选:A。
13. (2023 河南)我国化学家张青莲教授主持测定了铟、锑、铈等元素的相对原子质量的新值。铈元素在元素周期表中的相关信息如图所示,下列有关说法不正确的是( )
A.铈属于金属元素
B.铈的元素符号是Ce
C.铈的相对原子质量为140.1g
D.铈原子的质子数为58
【答案】C
【解析】解:A.铈字带有钅字旁,属于金属元素,故正确;
B.根据图示信息可知,铈的元素符号是Ce,故正确;
C.铈的相对原子质量为140.1,单位应为“1”,不是“g”,故错误;
D.元素名称左上角的数字表示原子序数,原子序数=质子数,因此铈原子的质子数为58,故正确;
故选:C。
14. (2023 新疆)硒是人体必需的微量元素,具有防癌抗癌的作用。结合如图分析,下列说法错误的是( )
A.硒元素属于金属元素
B.硒原子的质子数是34
C.硒元素的相对原子质量为78.96
D.硒原子核外有4个电子层
【答案】A
【解析】解:A.硒字带有石字旁,属于非金属元素,故错误;
B.元素名称左上角的数字表示原子序数,原子序数=质子数,因此硒原子的质子数是34,故正确;
C.元素名称的正下方的数字表示相对原子质量,因此硒元素的相对原子质量为78.96,故正确;
D.根据硒原子的结构示意图可知,硒原子核外有4个电子层,故正确;
故选:A。
目标导航
教材全解
精选精练
真题检测
目标导航
教材全解
精选精练
真题检测
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
