1.1.3物质的转化 课件(共27张ppt)化学人教版(2019)必修第一册
文档属性
| 名称 | 1.1.3物质的转化 课件(共27张ppt)化学人教版(2019)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 656.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-29 00:00:00 | ||
图片预览





文档简介
(共27张PPT)
第1章 物质及其变化
第一节 物质的分类及转化
第3课时 物质的转化
贝壳的主要成分为碳酸钙,那么碳酸钙在日常生活、实验室有什么应用呢
1.实验室可以利用碳酸钙与盐酸反应制备二氧化碳气体。
2.在建筑房屋时,可利用碳酸钙生产石灰乳(碳酸钙加热生成氧化钙,氧化钙和水化合可制得石灰乳)。
导入一
一、酸、碱、盐的性质
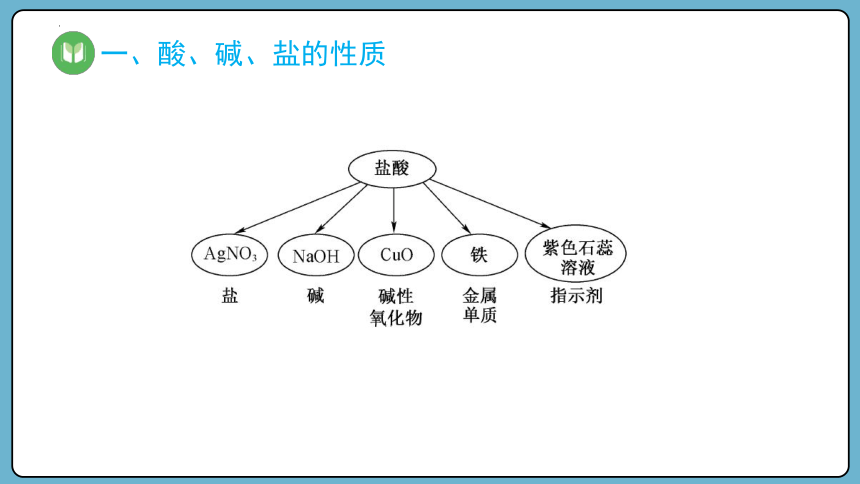
盐酸能与哪些物质反应,举例说明并书写反应的化学方程式。
盐酸可以与Fe、NaOH、CuO、AgNO3 等物质反应,反应的化学方程式:
一、酸、碱、盐的性质
一、酸、碱、盐的性质
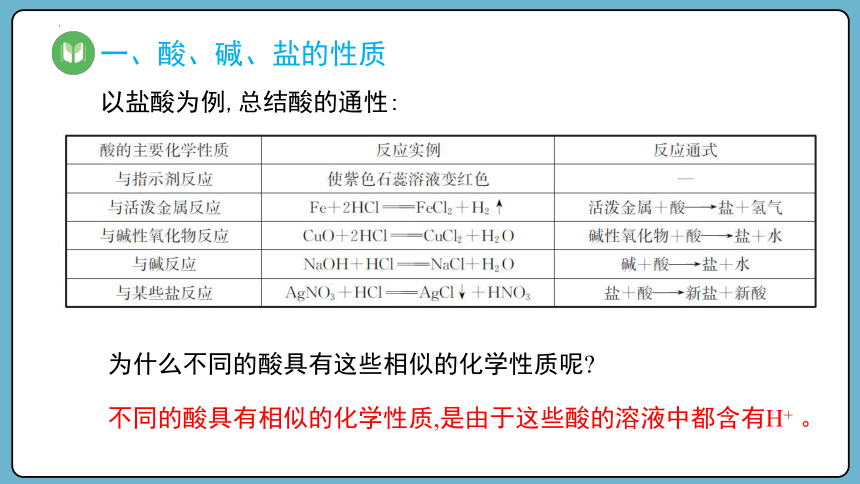
以盐酸为例,总结酸的通性:
为什么不同的酸具有这些相似的化学性质呢
不同的酸具有相似的化学性质,是由于这些酸的溶液中都含有H+ 。
小试牛刀 1.指出下表中各物质的类别:
2.找出上述能与氢氧化钙反应的物质,并书写反应的化学方程式。
HNO3、CO2、Na2CO3、CuCl2
碱
酸
氧化物
单质
盐
盐
氧化物
(1)Ca(OH)2+2HNO3 Ca(NO3)2+2H2O
(2)Ca(OH)2+CO2 CaCO3↓+H2O
(3)Ca(OH)2+Na2CO3 CaCO3↓+2NaOH
(4)Ca(OH)2+CuCl2 Cu(OH)2↓+CaCl2
一、酸、碱、盐的性质
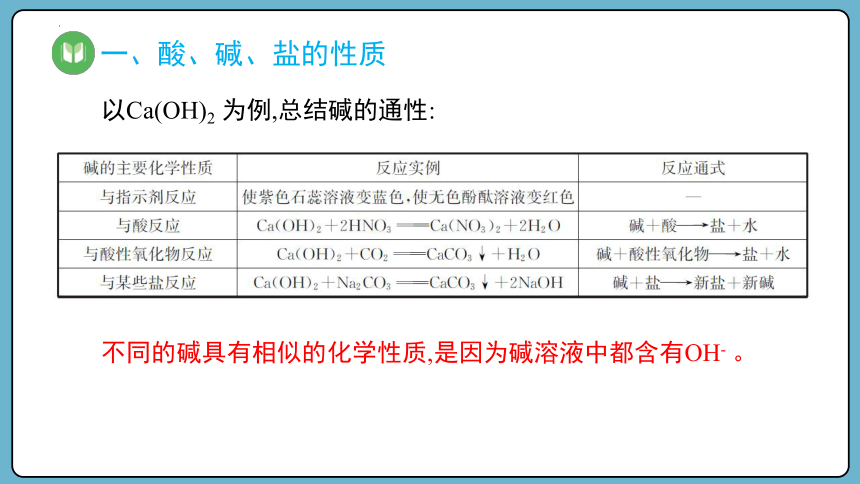
以Ca(OH)2 为例,总结碱的通性:
不同的碱具有相似的化学性质,是因为碱溶液中都含有OH- 。
一、酸、碱、盐的性质
小试牛刀 写出下列反应的化学方程式:
(1)碳酸钠溶液与①氯化钙溶液、②稀盐酸、③氢氧化钡溶液。
(2)硫酸铜溶液与①硝酸钡溶液、②氢氧化钠溶液、③单质铁。
(1)①CaCl2+Na2CO3 CaCO3↓+2NaCl
②Na2CO3+2HCl 2NaCl+H2O+CO2↑
③Na2CO3+Ba(OH)2 BaCO3↓+2NaOH
(2)①CuSO4+Ba(NO3)2 BaSO4↓+Cu(NO3)2
②CuSO4+2NaOH Cu(OH)2↓+Na2SO4
③Fe+CuSO4 FeSO4+Cu
一、酸、碱、盐的性质
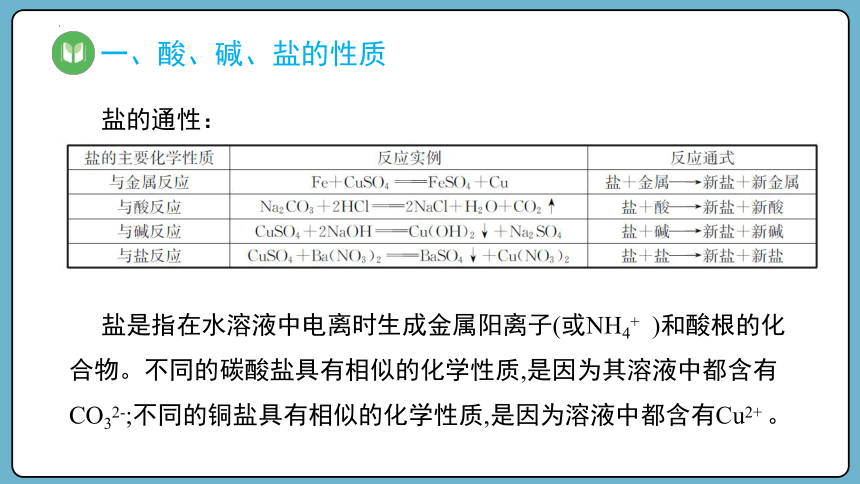
盐的通性:
盐是指在水溶液中电离时生成金属阳离子(或NH4+ )和酸根的化合物。不同的碳酸盐具有相似的化学性质,是因为其溶液中都含有CO32-;不同的铜盐具有相似的化学性质,是因为溶液中都含有Cu2+ 。
一、酸、碱、盐的性质
小试牛刀 基于物质分类寻找具有相同或相似性质的物质,预测其性质。SO2 和CO2同为酸性氧化物,试根据酸性氧化物具有的通性(或CO2 的性质),回答下列问题:
(1)请写出SO2 与生石灰反应的化学方程式:_____________________。
(2)SO2 的实验室制法与CO2 的实验室制法具有许多相似之处,请写出H2SO4 和Na2SO3 反应制取SO2 的化学方程式:___________________________________。
(3)将足量的SO2 通入澄清石灰水中的现象是______________________ 。
溶液先变浑浊,后变澄清
SO2+CaO CaSO3
H2SO4+Na2SO3 Na2SO4+SO2↑+H2O
一、酸、碱、盐的性质
1.由金属单质到盐的转化关系:
2. 由非金属单质到盐的转化关系:
一、酸、碱、盐的性质
二、物质的转化
小试牛刀 1.以钙为例,用化学方程式表示钙及其化合物之间的转化关系(如图),并指明反应类型。
①2Ca+O2 2CaO,化合反应
②CaO+H2O Ca(OH)2,化合反应
③CaO+ CO2 CaCO3,化合反应
④Ca(OH)2+Na2CO3 CaCO3↓+2NaOH,复分解反应
⑤Ca(OH)2+2HCl CaCl2+2H2O,复分解反应
⑥CaCO3+2HCl CaCl2+CO2↑+H2O,复分解反应
2.碳及其化合物间的转化关系如图所示,写出图中序号所示转化所需反应物的化学式。
①O2 ②H2O ③Ca(OH)2 ④CaO ⑤Ca(OH)2(答案合理即可)
二、物质的转化
对于上述转化关系,从物质分类的角度看, 有什么规律
1.物质可以依据其组成进行分类,而组成相似的物质在性质上也有相似性,可以基于这种规律预测物质间的转化关系。
2.某些类别的物质之间较易发生化学反应,如酸性物质和碱性物质之间较易发生反应,其中以酸碱中和反应最为典型。
二、物质的转化
体现单质、酸、碱、盐、氧化物之间的转化关系的“八圈图”:
二、物质的转化
“八圈图”中7类物质体现的化学性质:
二、物质的转化
三、物质转化的应用
小试牛刀 以工业上制取NaOH为例,讨论下列问题:
(1)选用两种方法制取氢氧化钠,并写出相关反应的化学方程式。
(2)从原料来源、成本等角度考虑工业上能否用上述两种方法制取氢氧化钠 现在主要采用什么方法制取氢氧化钠
(2)方法①不能用来制取氢氧化钠,因为Na2O作为原料,来源少、成本高。过去曾采用方法②,现在工业上主要采用电解饱和食盐水的方法制取氢氧化钠。
②Na2CO3 + Ca(OH)2 CaCO3 ↓ + 2NaOH。
(1)①Na2O + H2O 2NaOH;
三、物质转化的应用
工业生产中最适当方法的选择:
三、物质转化的应用
总结
课堂练习
1.中华文化源远流长、博大精深。下列有关诗词中蕴含的化学知识不正确的是( )
A.曹植的“磁石引铁,于金不连”———“磁石”能吸引铁,不能吸引金
B.苏轼的“庭下如积水空明,水中藻、荇交横,盖竹柏影也”———句中对月光
的描述体现了丁达尔效应
C.杨万里的“庐山山南刷铜绿”———铜锈俗称“铜绿”,其主要成分为铜的氧
化物
D.杜牧的“折戟沉沙铁未销”———铁生锈的条件是与水和氧气同时接触
C
2.在一定条件下,能跟某些酸、碱、盐发生反应的物质是 ( )
A. Na2CO3 B. CuO
C. CaCO3 D. CO2
课堂练习
A
3.某同学总结了碱的化学性质如图所示,发现碱与酸一样,也有一些相似的化学性质。“———”表示两类物质间能发生反应。已知:CaCl2+Na2CO3 2NaCl+CaCO3↓。
请回答下列问题:
课堂练习
(1)不同的碱具有相似的化学性质,原因是______________________。
(2)已知熟石灰能与二氧化碳反应,根据三氧化硫与二氧化碳的类
别相同,推断三氧化硫也能与氢氧化钙溶液反应,反应的化学方程
式为__________________________。
碱溶液中都含有OH-
课堂练习
SO3+Ca(OH)2 CaSO4↓+H2O
(3)根据图中关系可知NaOH 必须密封保存,否则在空气中容易变质,如果要除去在空气中已变质的氢氧化钠溶液中的杂质,应选择适量的_____(填序号)。
A.稀盐酸 B.稀硫酸
C.CaCl2 溶液 D.Ca(OH)2 溶液
以上混合物静置后再通过______(填操作名称),即可达到实验目的,写出除杂的化学方程式:________________________________。
课堂练习
过滤
D
Ca(OH)2 + Na2CO3 CaCO3↓ + 2NaOH
(4)若碱为氢氧化钠,请写出一个符合性质②的化学方程式:________________________________ ,基本反应类型为_____________。
课堂练习
2NaOH+CuSO4 Cu(OH)2↓+Na2SO4
复分解反应
谢谢!
第1章 物质及其变化
第一节 物质的分类及转化
第3课时 物质的转化
贝壳的主要成分为碳酸钙,那么碳酸钙在日常生活、实验室有什么应用呢
1.实验室可以利用碳酸钙与盐酸反应制备二氧化碳气体。
2.在建筑房屋时,可利用碳酸钙生产石灰乳(碳酸钙加热生成氧化钙,氧化钙和水化合可制得石灰乳)。
导入一
一、酸、碱、盐的性质
盐酸能与哪些物质反应,举例说明并书写反应的化学方程式。
盐酸可以与Fe、NaOH、CuO、AgNO3 等物质反应,反应的化学方程式:
一、酸、碱、盐的性质
一、酸、碱、盐的性质
以盐酸为例,总结酸的通性:
为什么不同的酸具有这些相似的化学性质呢
不同的酸具有相似的化学性质,是由于这些酸的溶液中都含有H+ 。
小试牛刀 1.指出下表中各物质的类别:
2.找出上述能与氢氧化钙反应的物质,并书写反应的化学方程式。
HNO3、CO2、Na2CO3、CuCl2
碱
酸
氧化物
单质
盐
盐
氧化物
(1)Ca(OH)2+2HNO3 Ca(NO3)2+2H2O
(2)Ca(OH)2+CO2 CaCO3↓+H2O
(3)Ca(OH)2+Na2CO3 CaCO3↓+2NaOH
(4)Ca(OH)2+CuCl2 Cu(OH)2↓+CaCl2
一、酸、碱、盐的性质
以Ca(OH)2 为例,总结碱的通性:
不同的碱具有相似的化学性质,是因为碱溶液中都含有OH- 。
一、酸、碱、盐的性质
小试牛刀 写出下列反应的化学方程式:
(1)碳酸钠溶液与①氯化钙溶液、②稀盐酸、③氢氧化钡溶液。
(2)硫酸铜溶液与①硝酸钡溶液、②氢氧化钠溶液、③单质铁。
(1)①CaCl2+Na2CO3 CaCO3↓+2NaCl
②Na2CO3+2HCl 2NaCl+H2O+CO2↑
③Na2CO3+Ba(OH)2 BaCO3↓+2NaOH
(2)①CuSO4+Ba(NO3)2 BaSO4↓+Cu(NO3)2
②CuSO4+2NaOH Cu(OH)2↓+Na2SO4
③Fe+CuSO4 FeSO4+Cu
一、酸、碱、盐的性质
盐的通性:
盐是指在水溶液中电离时生成金属阳离子(或NH4+ )和酸根的化合物。不同的碳酸盐具有相似的化学性质,是因为其溶液中都含有CO32-;不同的铜盐具有相似的化学性质,是因为溶液中都含有Cu2+ 。
一、酸、碱、盐的性质
小试牛刀 基于物质分类寻找具有相同或相似性质的物质,预测其性质。SO2 和CO2同为酸性氧化物,试根据酸性氧化物具有的通性(或CO2 的性质),回答下列问题:
(1)请写出SO2 与生石灰反应的化学方程式:_____________________。
(2)SO2 的实验室制法与CO2 的实验室制法具有许多相似之处,请写出H2SO4 和Na2SO3 反应制取SO2 的化学方程式:___________________________________。
(3)将足量的SO2 通入澄清石灰水中的现象是______________________ 。
溶液先变浑浊,后变澄清
SO2+CaO CaSO3
H2SO4+Na2SO3 Na2SO4+SO2↑+H2O
一、酸、碱、盐的性质
1.由金属单质到盐的转化关系:
2. 由非金属单质到盐的转化关系:
一、酸、碱、盐的性质
二、物质的转化
小试牛刀 1.以钙为例,用化学方程式表示钙及其化合物之间的转化关系(如图),并指明反应类型。
①2Ca+O2 2CaO,化合反应
②CaO+H2O Ca(OH)2,化合反应
③CaO+ CO2 CaCO3,化合反应
④Ca(OH)2+Na2CO3 CaCO3↓+2NaOH,复分解反应
⑤Ca(OH)2+2HCl CaCl2+2H2O,复分解反应
⑥CaCO3+2HCl CaCl2+CO2↑+H2O,复分解反应
2.碳及其化合物间的转化关系如图所示,写出图中序号所示转化所需反应物的化学式。
①O2 ②H2O ③Ca(OH)2 ④CaO ⑤Ca(OH)2(答案合理即可)
二、物质的转化
对于上述转化关系,从物质分类的角度看, 有什么规律
1.物质可以依据其组成进行分类,而组成相似的物质在性质上也有相似性,可以基于这种规律预测物质间的转化关系。
2.某些类别的物质之间较易发生化学反应,如酸性物质和碱性物质之间较易发生反应,其中以酸碱中和反应最为典型。
二、物质的转化
体现单质、酸、碱、盐、氧化物之间的转化关系的“八圈图”:
二、物质的转化
“八圈图”中7类物质体现的化学性质:
二、物质的转化
三、物质转化的应用
小试牛刀 以工业上制取NaOH为例,讨论下列问题:
(1)选用两种方法制取氢氧化钠,并写出相关反应的化学方程式。
(2)从原料来源、成本等角度考虑工业上能否用上述两种方法制取氢氧化钠 现在主要采用什么方法制取氢氧化钠
(2)方法①不能用来制取氢氧化钠,因为Na2O作为原料,来源少、成本高。过去曾采用方法②,现在工业上主要采用电解饱和食盐水的方法制取氢氧化钠。
②Na2CO3 + Ca(OH)2 CaCO3 ↓ + 2NaOH。
(1)①Na2O + H2O 2NaOH;
三、物质转化的应用
工业生产中最适当方法的选择:
三、物质转化的应用
总结
课堂练习
1.中华文化源远流长、博大精深。下列有关诗词中蕴含的化学知识不正确的是( )
A.曹植的“磁石引铁,于金不连”———“磁石”能吸引铁,不能吸引金
B.苏轼的“庭下如积水空明,水中藻、荇交横,盖竹柏影也”———句中对月光
的描述体现了丁达尔效应
C.杨万里的“庐山山南刷铜绿”———铜锈俗称“铜绿”,其主要成分为铜的氧
化物
D.杜牧的“折戟沉沙铁未销”———铁生锈的条件是与水和氧气同时接触
C
2.在一定条件下,能跟某些酸、碱、盐发生反应的物质是 ( )
A. Na2CO3 B. CuO
C. CaCO3 D. CO2
课堂练习
A
3.某同学总结了碱的化学性质如图所示,发现碱与酸一样,也有一些相似的化学性质。“———”表示两类物质间能发生反应。已知:CaCl2+Na2CO3 2NaCl+CaCO3↓。
请回答下列问题:
课堂练习
(1)不同的碱具有相似的化学性质,原因是______________________。
(2)已知熟石灰能与二氧化碳反应,根据三氧化硫与二氧化碳的类
别相同,推断三氧化硫也能与氢氧化钙溶液反应,反应的化学方程
式为__________________________。
碱溶液中都含有OH-
课堂练习
SO3+Ca(OH)2 CaSO4↓+H2O
(3)根据图中关系可知NaOH 必须密封保存,否则在空气中容易变质,如果要除去在空气中已变质的氢氧化钠溶液中的杂质,应选择适量的_____(填序号)。
A.稀盐酸 B.稀硫酸
C.CaCl2 溶液 D.Ca(OH)2 溶液
以上混合物静置后再通过______(填操作名称),即可达到实验目的,写出除杂的化学方程式:________________________________。
课堂练习
过滤
D
Ca(OH)2 + Na2CO3 CaCO3↓ + 2NaOH
(4)若碱为氢氧化钠,请写出一个符合性质②的化学方程式:________________________________ ,基本反应类型为_____________。
课堂练习
2NaOH+CuSO4 Cu(OH)2↓+Na2SO4
复分解反应
谢谢!
