2023年普通高校招收华侨港澳台考生考试化学试题(PDF版无答案)
文档属性
| 名称 | 2023年普通高校招收华侨港澳台考生考试化学试题(PDF版无答案) |

|
|
| 格式 | |||
| 文件大小 | 549.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-29 00:00:00 | ||
图片预览

文档简介
2023 年中华人民共和国普通高等学校
联合招收华侨港澳台学生入学考试
化 学
可能用到的原子量 H l C 12 N 14 O 16 Mg 24 Al 27 Si 28 Cl 35.5
一、选择题:本题共 15 小题,每小题 4 分,共 60 分。在每小题给出的四个选项中,只有
一项是符合题目要求的。
1.下列试剂与标签不对应的是 ( )
A.四氯化碳 B.冰醋酸 C.高锰酸钾 D.丁烷
2.下列消毒剂不是利用其氧化性进行消毒的是 ( )
A.0.5%过氧乙酸溶液 B.1%次氯酸钠溶液
C.75%乙醇溶液 D.3%双氧水溶液
3.下列物质水解能生成果糖即是 ( )
A.淀粉 B.纤维素 C.蔗糖 D.麦芽糖
4.下列属于非极性分子的是 ( )
A.对二甲苯 B.苯甲酸 C.对硝基甲苯 D.苯甲醚
5.工业制合块的反应为 CaC2+2H2O=C2H2↑+Ca(OH)2,下列说法错误的是 ( )
A.CaC 为离子化合物 B.Ca2+的结构示意图为
C.C2H2含有极性和非极性共价键 D.H2O的电子式
6.关于 HF + OD-= F +HOD (D为氘),下列说法正确的是 ( )
A.HOD 与 H O的质量数相同 B.HF和 DF为同分异构体
C.H和 D的电子数相同 D.OD- 和 OH 的中子数相同
7.向 X溶液加入等体积的 Y 溶液后,导电性显著增加且酸碱性显著改变的是 ( )
X(0.01mol·L ) Y(0.01mol·L )
A. Na2CO3 HAc
B. Na2SO3 氯水
C. NH4Cl AgNO3
D. H2SO4 BaS
2023年华侨港澳台联考真题化学试卷 1
{#{QQABIYCAogiAABBAABgCUQHCCAEQkBECAIgGwAAMMAAByAFABAA=}#}
8.能正确表达下列反应的离子方程式为 ( )
A.碘化亚铁溶液与浓硫酸反应:2Fe2+ +SO42- + 4H+ =2Fe3+ +SO2↑+2H2O
B.硫酸铝溶液与过量的浓氨水反应:Al3+ + 3NH3·H2O=Al(OH)3↓+3NH4+
C.硫酸铜溶液与碘化钾溶液反应:2Cu2+ + 2I- = 2Cu+ + I2
D..硫酸锌溶液和硫化钡溶液反应:Zn2+ + Ba2+ + 2S2- + 2H2O=ZnS·Ba(OH)2↓ +H2S↑
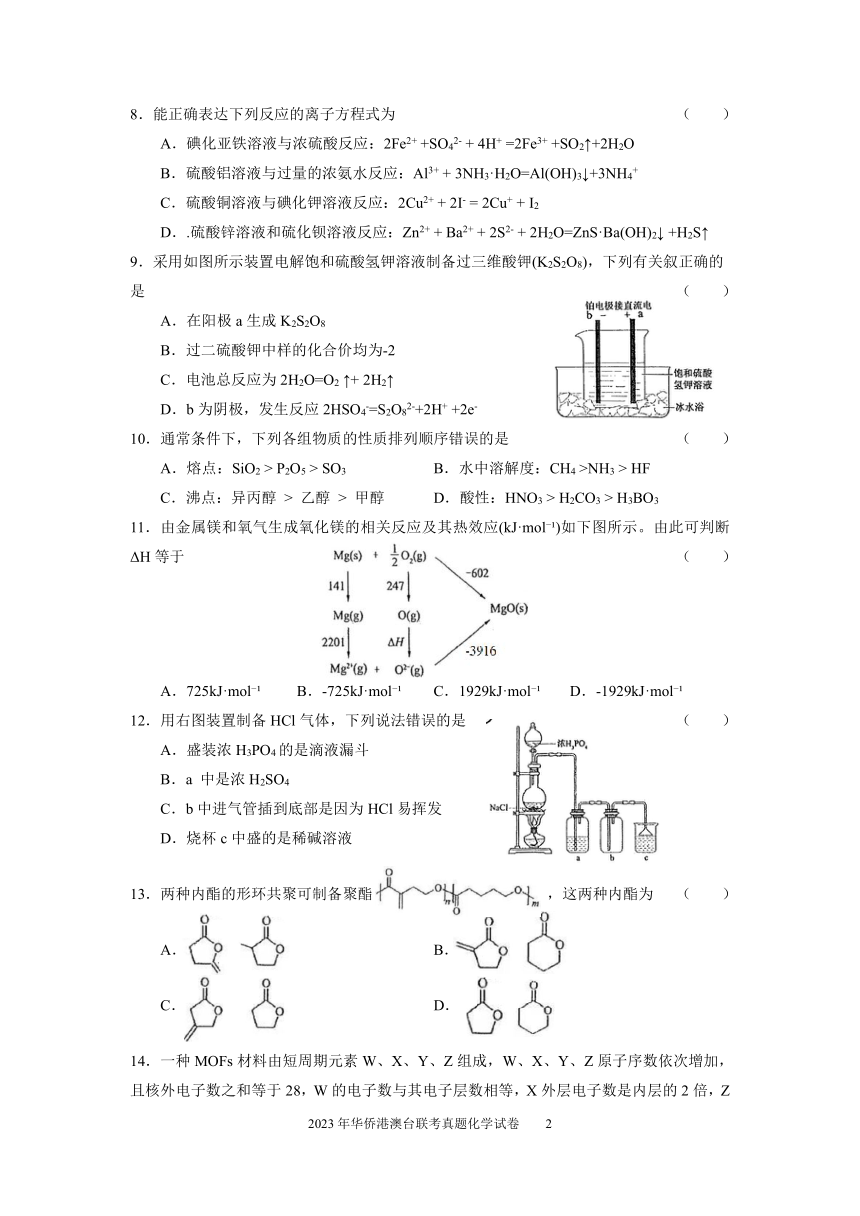
9.采用如图所示装置电解饱和硫酸氢钾溶液制备过三维酸钾(K2S2O8),下列有关叙正确的
是 ( )
A.在阳极 a生成 K2S2O8
B.过二硫酸钾中样的化合价均为-2
C.电池总反应为 2H2O=O2 ↑+ 2H2↑
D.b为阴极,发生反应 2HSO4-=S2O82-+2H+ +2e-
10.通常条件下,下列各组物质的性质排列顺序错误的是 ( )
A.熔点:SiO2 > P2O5 > SO3 B.水中溶解度:CH4 >NH3 > HF
C.沸点:异丙醇 > 乙醇 > 甲醇 D.酸性:HNO3 > H2CO3 > H3BO3
11.由金属镁和氧气生成氧化镁的相关反应及其热效应(kJ·mol )如下图所示。由此可判断
ΔH等于 ( )
A.725kJ·mol B.-725kJ·mol C.1929kJ·mol D.-1929kJ·mol
12.用右图装置制备 HCl气体,下列说法错误的是 ( )
A.盛装浓 H3PO4的是滴液漏斗
B.a 中是浓 H2SO4
C.b中进气管插到底部是因为 HCl易挥发
D.烧杯 c中盛的是稀碱溶液
13.两种内酯的形环共聚可制备聚酯 ,这两种内酯为 ( )
A. B.
C. D.
14.一种MOFs材料由短周期元素W、X、Y、Z组成,W、X、Y、Z原子序数依次增加,
且核外电子数之和等于 28,W的电子数与其电子层数相等,X外层电子数是内层的 2倍,Z
2023年华侨港澳台联考真题化学试卷 2
{#{QQABIYCAogiAABBAABgCUQHCCAEQkBECAIgGwAAMMAAByAFABAA=}#}
的价层电子数与其电子层数相等。下列叙述不正确的是 ( )
A.W、X、Y是组成葡萄糖的元素 B.W与 Y可由成显弱酸性的化合物
C.W、Y、Z可以组成配合物阴离子 D.X单质的导电性均高于 Z单质的
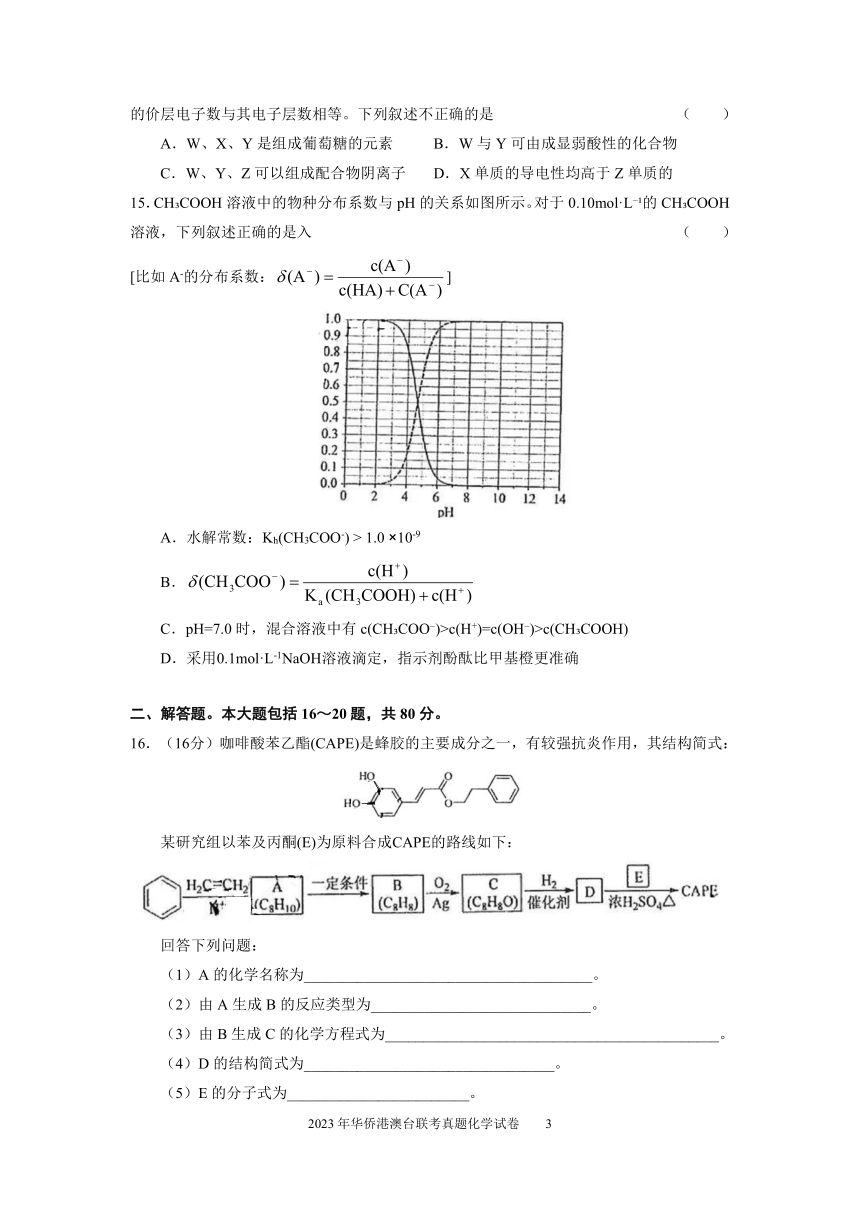
15.CH COOH溶液中的物种分布系数与 pH的关系如图所示。对于 0.10mol·L 的 CH COOH
溶液,下列叙述正确的是入 ( )
c(A )[比如 A-的分布系数: (A ) ]
c(HA) C(A )
A.水解常数:Kh(CH3COO-) > 1.0 ×10-9
B. (CH COO ) c(H )3 K a (CH3COOH) c(H
)
C.pH=7.0时,混合溶液中有 c(CH COO )>c(H+)=c(OH )>c(CH COOH)
D.采用0.1mol·L-1NaOH溶液滴定,指示剂酚酞比甲基橙更准确
二、解答题。本大题包括 16~20 题,共 80 分。
16.(16分)咖啡酸苯乙酯(CAPE)是蜂胶的主要成分之一,有较强抗炎作用,其结构简式:
某研究组以苯及丙酮(E)为原料合成CAPE的路线如下:
回答下列问题:
(1)A的化学名称为______________________________________。
(2)由 A生成 B的反应类型为_____________________________。
(3)由 B生成 C的化学方程式为____________________________________________。
(4)D的结构简式为_________________________________。
(5)E的分子式为________________________。
2023年华侨港澳台联考真题化学试卷 3
{#{QQABIYCAogiAABBAABgCUQHCCAEQkBECAIgGwAAMMAAByAFABAA=}#}
(6)F为 E的芳香同分异构体,1 mol F与足量饱和 NaHCO 溶液反应可产生 2 mol CO ,
F可能的结构共有_________种,其中核磁共振氢谱有 4组峰,且峰面积比为 3∶2∶2∶1的
有__________________(写结构简式)。
17.(16分)无水三氯化铝是重要的化学试剂(三氯化铝易升华,升华点 178℃),可作为有
机合成的催化剂。一种工业制法如下图所示:
(1)制备反应前,应该预通入一段时间的氯气,目的是_____________________。
(2)反应炉中发生的主要反应是_____________________,为使反应更快进行,可采取
的措施是__________________________________________。
(3)进入捕集器的混合气体有_________(填“增加”“降低”或“不变”);降温,AlCl 变为
固体,该变化称为________________________。
(4)吸收器中的溶液可由电解食盐水制得,吸收器中发生反应的化学方程式为:
________________________________________。
(5)三氯化铝在潮湿的空气中不稳定,其原因是:________________________________。
因此,进入反应炉的氯气需要_____________________。
18.(16分)乙酰苯胺可作为退热剂。纯乙酰苯胺为由色晶体,熔点 114.3℃,微溶于水,
易溶于有机溶剂。某粗乙酰苯胺含少量不溶于水的杂质,可通过重结晶提纯。乙酰苯胺在水
中的溶解度如下表:
t/℃ 20 50 80 100
溶解度/(g/100mL) 0.46 0.84 3.45 5.5
回答下列问题:
(1)重结晶时,加水量应根据粗乙酰苯胺的量和其在_______℃时的溶解度计算确定。
(2)若加热时不慎碰倒酒精灯而使酒精洒出起火,应立即用__________覆盖。
(3)下列玻璃仪器中,重结晶实验不需要的是__________(填名称)
(4)加热溶解后进行热过滤,若滤纸上有较多晶体析出,可能的原因有____________
_______________________________________________________________________________
(答出两条)。不能将滤纸上析出的晶体合并到滤液中,原因是___________________________
2023年华侨港澳台联考真题化学试卷 4
{#{QQABIYCAogiAABBAABgCUQHCCAEQkBECAIgGwAAMMAAByAFABAA=}#}
________________________________________________。
(5)结晶时,如果想要得到较大的晶体,可采取的方法有________。(填标号)
A.搅拌 B.快速降温 C.缓慢降温
过滤后,可用来洗涤晶体的是________。(填标号)
A.乙醇 B.冷水 C.热水
19.(16分)在 326℃的密闭刚性容器中,1,3—丁二烯(C H )在催化剂 A 作用下发生二聚
反应:2C4H6(g)=C8H12(g) ΔH=-80kJ·mol-1。不同时刻测得容器中的压强如下表所示。
t/min 0 3.25 12.18 24.55 42.50 68.05 ∞
p/kPa 84.25 82.45 77.87 72.85 67.89 63.26 47.61
回答下列问题(列出计算表达式即可):
(1)成立 t=24.55min 时,C H (g)的转化率α=___________%。
(2)3.25~24.55min之间的 (C8H12 ) =___________________kPa·min-1。
(3)该反应的平衡常数 K =__________kPa 。
(4)若提高反应温度,则平衡时容器中的压强_________________(填大于”“小于”或“等
于”)47.61kPa。
(5)保持反应温度不变,改用催化剂 B,发现平衡时容器中的压强小于 47.61kPa。分
析可能的原因是___________________________________________________。
20.(16分)[C(NH ) ][SO F]是一种新型的紫外非线性晶体材料。回答下列问题:
(1)组成[C(NH ) ][SO F]的所有元素中,电负性最大的是____________,基态原
子p轨道为半充满的元素是________________________。(填元素符号)
(2)[C(NH ) ] 中碳原子形成 σ 键的轨道重叠方式为____________(填标号)
A. B. C. D.
其中碳原子的杂化类型为____________。碳原子杂化方式与[C(NH ) ] 中的碳相同,且
只含有一个碳原子的有机物结构简式为_______________________________。(写出两个)
(3)[C(NH ) ][SO F]的晶体类型为______________,[SO F] 的空间构型为____________。
晶体中单层[C(NH )3][SO3F]结构如图所示,其中[C(NH) ]与[SO F] 之间的作用力包括_______
______________________________。
2023年华侨港澳台联考真题化学试卷 5
{#{QQABIYCAogiAABBAABgCUQHCCAEQkBECAIgGwAAMMAAByAFABAA=}#}
三、计算题,共 10 分。
21.(10分)
Cds既是一种颜料,又是一种感光材料。常采用向可溶性镉盐溶液中通入 H S气体使其
饱和(c(H2S)=0.1mol·L-1),调节液的 pH来生产 CdS。欲使沉淀的滤液中 c(Cd2+)达到国家
II类地表水质量控制标准 c(Cd2+)≤10-7.4mol·L-1(≤0.005 mg·L ),计算沉淀时应控制溶液的
最低 pH为多少?
已知:Ka1(H2S)=10-7.0、Ka2(H2S)=10-12.9及 Ksp(CdS)=10-26.1。
2023年华侨港澳台联考真题化学试卷 6
{#{QQABIYCAogiAABBAABgCUQHCCAEQkBECAIgGwAAMMAAByAFABAA=}#}
联合招收华侨港澳台学生入学考试
化 学
可能用到的原子量 H l C 12 N 14 O 16 Mg 24 Al 27 Si 28 Cl 35.5
一、选择题:本题共 15 小题,每小题 4 分,共 60 分。在每小题给出的四个选项中,只有
一项是符合题目要求的。
1.下列试剂与标签不对应的是 ( )
A.四氯化碳 B.冰醋酸 C.高锰酸钾 D.丁烷
2.下列消毒剂不是利用其氧化性进行消毒的是 ( )
A.0.5%过氧乙酸溶液 B.1%次氯酸钠溶液
C.75%乙醇溶液 D.3%双氧水溶液
3.下列物质水解能生成果糖即是 ( )
A.淀粉 B.纤维素 C.蔗糖 D.麦芽糖
4.下列属于非极性分子的是 ( )
A.对二甲苯 B.苯甲酸 C.对硝基甲苯 D.苯甲醚
5.工业制合块的反应为 CaC2+2H2O=C2H2↑+Ca(OH)2,下列说法错误的是 ( )
A.CaC 为离子化合物 B.Ca2+的结构示意图为
C.C2H2含有极性和非极性共价键 D.H2O的电子式
6.关于 HF + OD-= F +HOD (D为氘),下列说法正确的是 ( )
A.HOD 与 H O的质量数相同 B.HF和 DF为同分异构体
C.H和 D的电子数相同 D.OD- 和 OH 的中子数相同
7.向 X溶液加入等体积的 Y 溶液后,导电性显著增加且酸碱性显著改变的是 ( )
X(0.01mol·L ) Y(0.01mol·L )
A. Na2CO3 HAc
B. Na2SO3 氯水
C. NH4Cl AgNO3
D. H2SO4 BaS
2023年华侨港澳台联考真题化学试卷 1
{#{QQABIYCAogiAABBAABgCUQHCCAEQkBECAIgGwAAMMAAByAFABAA=}#}
8.能正确表达下列反应的离子方程式为 ( )
A.碘化亚铁溶液与浓硫酸反应:2Fe2+ +SO42- + 4H+ =2Fe3+ +SO2↑+2H2O
B.硫酸铝溶液与过量的浓氨水反应:Al3+ + 3NH3·H2O=Al(OH)3↓+3NH4+
C.硫酸铜溶液与碘化钾溶液反应:2Cu2+ + 2I- = 2Cu+ + I2
D..硫酸锌溶液和硫化钡溶液反应:Zn2+ + Ba2+ + 2S2- + 2H2O=ZnS·Ba(OH)2↓ +H2S↑
9.采用如图所示装置电解饱和硫酸氢钾溶液制备过三维酸钾(K2S2O8),下列有关叙正确的
是 ( )
A.在阳极 a生成 K2S2O8
B.过二硫酸钾中样的化合价均为-2
C.电池总反应为 2H2O=O2 ↑+ 2H2↑
D.b为阴极,发生反应 2HSO4-=S2O82-+2H+ +2e-
10.通常条件下,下列各组物质的性质排列顺序错误的是 ( )
A.熔点:SiO2 > P2O5 > SO3 B.水中溶解度:CH4 >NH3 > HF
C.沸点:异丙醇 > 乙醇 > 甲醇 D.酸性:HNO3 > H2CO3 > H3BO3
11.由金属镁和氧气生成氧化镁的相关反应及其热效应(kJ·mol )如下图所示。由此可判断
ΔH等于 ( )
A.725kJ·mol B.-725kJ·mol C.1929kJ·mol D.-1929kJ·mol
12.用右图装置制备 HCl气体,下列说法错误的是 ( )
A.盛装浓 H3PO4的是滴液漏斗
B.a 中是浓 H2SO4
C.b中进气管插到底部是因为 HCl易挥发
D.烧杯 c中盛的是稀碱溶液
13.两种内酯的形环共聚可制备聚酯 ,这两种内酯为 ( )
A. B.
C. D.
14.一种MOFs材料由短周期元素W、X、Y、Z组成,W、X、Y、Z原子序数依次增加,
且核外电子数之和等于 28,W的电子数与其电子层数相等,X外层电子数是内层的 2倍,Z
2023年华侨港澳台联考真题化学试卷 2
{#{QQABIYCAogiAABBAABgCUQHCCAEQkBECAIgGwAAMMAAByAFABAA=}#}
的价层电子数与其电子层数相等。下列叙述不正确的是 ( )
A.W、X、Y是组成葡萄糖的元素 B.W与 Y可由成显弱酸性的化合物
C.W、Y、Z可以组成配合物阴离子 D.X单质的导电性均高于 Z单质的
15.CH COOH溶液中的物种分布系数与 pH的关系如图所示。对于 0.10mol·L 的 CH COOH
溶液,下列叙述正确的是入 ( )
c(A )[比如 A-的分布系数: (A ) ]
c(HA) C(A )
A.水解常数:Kh(CH3COO-) > 1.0 ×10-9
B. (CH COO ) c(H )3 K a (CH3COOH) c(H
)
C.pH=7.0时,混合溶液中有 c(CH COO )>c(H+)=c(OH )>c(CH COOH)
D.采用0.1mol·L-1NaOH溶液滴定,指示剂酚酞比甲基橙更准确
二、解答题。本大题包括 16~20 题,共 80 分。
16.(16分)咖啡酸苯乙酯(CAPE)是蜂胶的主要成分之一,有较强抗炎作用,其结构简式:
某研究组以苯及丙酮(E)为原料合成CAPE的路线如下:
回答下列问题:
(1)A的化学名称为______________________________________。
(2)由 A生成 B的反应类型为_____________________________。
(3)由 B生成 C的化学方程式为____________________________________________。
(4)D的结构简式为_________________________________。
(5)E的分子式为________________________。
2023年华侨港澳台联考真题化学试卷 3
{#{QQABIYCAogiAABBAABgCUQHCCAEQkBECAIgGwAAMMAAByAFABAA=}#}
(6)F为 E的芳香同分异构体,1 mol F与足量饱和 NaHCO 溶液反应可产生 2 mol CO ,
F可能的结构共有_________种,其中核磁共振氢谱有 4组峰,且峰面积比为 3∶2∶2∶1的
有__________________(写结构简式)。
17.(16分)无水三氯化铝是重要的化学试剂(三氯化铝易升华,升华点 178℃),可作为有
机合成的催化剂。一种工业制法如下图所示:
(1)制备反应前,应该预通入一段时间的氯气,目的是_____________________。
(2)反应炉中发生的主要反应是_____________________,为使反应更快进行,可采取
的措施是__________________________________________。
(3)进入捕集器的混合气体有_________(填“增加”“降低”或“不变”);降温,AlCl 变为
固体,该变化称为________________________。
(4)吸收器中的溶液可由电解食盐水制得,吸收器中发生反应的化学方程式为:
________________________________________。
(5)三氯化铝在潮湿的空气中不稳定,其原因是:________________________________。
因此,进入反应炉的氯气需要_____________________。
18.(16分)乙酰苯胺可作为退热剂。纯乙酰苯胺为由色晶体,熔点 114.3℃,微溶于水,
易溶于有机溶剂。某粗乙酰苯胺含少量不溶于水的杂质,可通过重结晶提纯。乙酰苯胺在水
中的溶解度如下表:
t/℃ 20 50 80 100
溶解度/(g/100mL) 0.46 0.84 3.45 5.5
回答下列问题:
(1)重结晶时,加水量应根据粗乙酰苯胺的量和其在_______℃时的溶解度计算确定。
(2)若加热时不慎碰倒酒精灯而使酒精洒出起火,应立即用__________覆盖。
(3)下列玻璃仪器中,重结晶实验不需要的是__________(填名称)
(4)加热溶解后进行热过滤,若滤纸上有较多晶体析出,可能的原因有____________
_______________________________________________________________________________
(答出两条)。不能将滤纸上析出的晶体合并到滤液中,原因是___________________________
2023年华侨港澳台联考真题化学试卷 4
{#{QQABIYCAogiAABBAABgCUQHCCAEQkBECAIgGwAAMMAAByAFABAA=}#}
________________________________________________。
(5)结晶时,如果想要得到较大的晶体,可采取的方法有________。(填标号)
A.搅拌 B.快速降温 C.缓慢降温
过滤后,可用来洗涤晶体的是________。(填标号)
A.乙醇 B.冷水 C.热水
19.(16分)在 326℃的密闭刚性容器中,1,3—丁二烯(C H )在催化剂 A 作用下发生二聚
反应:2C4H6(g)=C8H12(g) ΔH=-80kJ·mol-1。不同时刻测得容器中的压强如下表所示。
t/min 0 3.25 12.18 24.55 42.50 68.05 ∞
p/kPa 84.25 82.45 77.87 72.85 67.89 63.26 47.61
回答下列问题(列出计算表达式即可):
(1)成立 t=24.55min 时,C H (g)的转化率α=___________%。
(2)3.25~24.55min之间的 (C8H12 ) =___________________kPa·min-1。
(3)该反应的平衡常数 K =__________kPa 。
(4)若提高反应温度,则平衡时容器中的压强_________________(填大于”“小于”或“等
于”)47.61kPa。
(5)保持反应温度不变,改用催化剂 B,发现平衡时容器中的压强小于 47.61kPa。分
析可能的原因是___________________________________________________。
20.(16分)[C(NH ) ][SO F]是一种新型的紫外非线性晶体材料。回答下列问题:
(1)组成[C(NH ) ][SO F]的所有元素中,电负性最大的是____________,基态原
子p轨道为半充满的元素是________________________。(填元素符号)
(2)[C(NH ) ] 中碳原子形成 σ 键的轨道重叠方式为____________(填标号)
A. B. C. D.
其中碳原子的杂化类型为____________。碳原子杂化方式与[C(NH ) ] 中的碳相同,且
只含有一个碳原子的有机物结构简式为_______________________________。(写出两个)
(3)[C(NH ) ][SO F]的晶体类型为______________,[SO F] 的空间构型为____________。
晶体中单层[C(NH )3][SO3F]结构如图所示,其中[C(NH) ]与[SO F] 之间的作用力包括_______
______________________________。
2023年华侨港澳台联考真题化学试卷 5
{#{QQABIYCAogiAABBAABgCUQHCCAEQkBECAIgGwAAMMAAByAFABAA=}#}
三、计算题,共 10 分。
21.(10分)
Cds既是一种颜料,又是一种感光材料。常采用向可溶性镉盐溶液中通入 H S气体使其
饱和(c(H2S)=0.1mol·L-1),调节液的 pH来生产 CdS。欲使沉淀的滤液中 c(Cd2+)达到国家
II类地表水质量控制标准 c(Cd2+)≤10-7.4mol·L-1(≤0.005 mg·L ),计算沉淀时应控制溶液的
最低 pH为多少?
已知:Ka1(H2S)=10-7.0、Ka2(H2S)=10-12.9及 Ksp(CdS)=10-26.1。
2023年华侨港澳台联考真题化学试卷 6
{#{QQABIYCAogiAABBAABgCUQHCCAEQkBECAIgGwAAMMAAByAFABAA=}#}
同课章节目录
