2023-2024学年科粤版初中化学第5单元第3节二氧化碳的性质和制法 导学案(含答案)
文档属性
| 名称 | 2023-2024学年科粤版初中化学第5单元第3节二氧化碳的性质和制法 导学案(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 3.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-29 00:00:00 | ||
图片预览


文档简介
5.3二氧化碳性质与制取
[课前复习]
1.“吸烟有害于健康。”我国政府规定:公共室内禁止吸烟。烟草燃烧释放的有害物质中,能与血红蛋白结合引起中毒的是( )
A.尼古丁 B.一氧化碳 C.焦油 D.甲醛
2.下列叙述中,与常温下碳单质的化学稳定性无关的是( )
A.将木桩埋入地下的一段用火烤焦
B.档案材料一般用碳素墨水填写
C.古代用墨书写绘制的字画经久不变色
D.用石墨制铅笔芯
3.下列物质的用途,既利用了碳的物理性质,又利用了化学性质的是( )
A.用焦炭炼钢 B.用活性炭作吸附剂 C.用墨写字保存时间长 D.用木炭制燃料
4.一种无色气体X,能在空气中燃烧生成另一种无色气体Y,Y和灼热的木炭反应又只生成气体X,则X是( )y.co*m】
A.O2 B.H2 C.CH4 D.CO
5.关于C60的说法正确的是( )
A.它是一种新型的碳的化合物B.它是一种新型的碳单质
C.它是由碳原子直接构成的D.它的相对分子质量是60
6.金刚石、石墨、木炭和C60都是由碳元素组成的单质,下列关于碳的单质的叙述正确的是( )21纪
A.都是黑色固体
B.在氧气中充分燃烧时都生成二氧化碳
C.碳原子的排列方式相同
D.一定条件下,石墨转化成金刚石是物理变化
7.防毒面具的滤毒罐中用来吸附毒气的物质是( )
A.炭黑 B.活性炭 C.木炭 D.石墨
8.中华炭雕(主要成分是木炭)是一种集观赏与空气净化于一体的工艺品,关于它的说法错误的是( )
A.炭雕摆设要远离火种
B.炭雕艺术品可以长久保存
C.炭雕是轻质透明的固体
D.炭雕能吸附室内有害气体
9.下列对一些事实的解释错误的是( )
事实 解释
A 书写档案规定必须使用碳素墨水 碳的化学性质稳定
B 石墨能够作电池的电极材料 石墨能够导电
C 焦炭可以把铁从它的氧化物矿石里还原出来 焦炭具有氧化性
D 制糖工业中用活性炭来脱色制白糖 活性炭具有吸附性
10.以石墨为原料,先制备氧化石墨,再经过热还原制备石墨烯。石墨烯硬度大,导电性能好,有韧性,可弯曲。下列关于金刚石、石墨、C60和石墨烯四种物质的叙述中错误的是( )2·1·c·n·j·y
A.将石墨变成石墨烯发生了化学变化
B.四种物质碳原子的排列方式不同
C.四种物质完全燃烧后的产物都是CO2
D.石墨烯是一种新型的化合物
[新授课]
[学习目标]1、认识二氧化碳的主要物理和化学性质;
2、了解二氧化碳对人类生活和生产的意义。
3、了解掌握二氧化碳的实验室制法。
一、二氧化碳有何性质
1.物理性质
(1)通常情况下,二氧化碳是一种______色、______味的气体。(2)密度比空气的________。
(3)溶解性____________。(4)固体二氧化碳俗称________,干冰升华吸热。
2.化学性质
[实验一] 在大烧杯中放置一个铁皮架,架上固定两支点燃的蜡烛,通过喇叭形纸筒将一瓶二氧化碳向烧杯内倾倒。
现象:________层的蜡烛先熄灭,________层的蜡烛后熄灭。
结论:①二氧化碳__________,也不能______________________;
②二氧化碳的密度________________。
[实验二] (1)往集满二氧化碳的软质塑料瓶里注入约 瓶蒸
馏水,立即旋紧瓶盖,充分振荡,如右图所示,观察到____________,
原因是二氧化碳_______________________________。
(2)将瓶内液体倒数毫升至试管中,向试管中滴入紫色石蕊溶液,振荡,观察到紫色石蕊溶液______,原因是________________,反应的化学方程式为____________________。
(3)将上述试管加热,观察到溶液变为紫色,因为碳酸不稳定易分解,反应的化学方程式为___________。
某同学设计了如下一组实验,取四朵紫色石蕊试液染色的干燥纸花,
分别按下图进行实验。
(1)各步实验中观察到纸花的颜色变化情况是:
I.纸花 II.纸花 III.纸花 IV.纸花
总结:二氧化碳与水发生反应,生成的 能使紫色的石蕊试液变
二氧化碳与水的反应方程式:
碳酸不稳定,易分解,化学方程式为
[实验三] 如右图所示,取一支盛澄清石灰水的试管,通过玻璃管,往石灰水里吹一会儿气。
现象:澄清石灰水________。
结论:CO2与澄清石灰水反应,有______________生成,该反应的
化学方程式为________________________________,用此反应可以鉴定
二氧化碳。
二、 二氧化碳对人类生活和环境有何影响
1.二氧化碳有广泛的用途
写出各用途对应的二氧化碳的性质。
人工降雨____________________________;
灭 火____________________________;
2.二氧化碳对人类和环境的影响
虽然二氧化碳______毒性,但不能____________,人在二氧化碳浓度偏高的环境中,会感到气闷、头痛乃至窒息死亡;大气中二氧化碳含量持续上升,产生了越来越严重的____________。结果导致全球变暖,带来了严重的环境问题。
三 、自然界中的碳循环
[注意] CO2 不是空气污染物。CO2会参与大气中的碳循环,是氧气的间接来源。
四、二氧化碳制取
1.实验室常用大理石和稀盐酸反应制取二氧化碳。
(1)反应的化学方程式为:_________________________________________;
(2)碳酸不稳定,分解生成二氧化碳和水_____________________________;
(3)总的化学方程式为:___________________________________________。
2.确定二氧化碳气体发生装置应考虑的因素
(1)反应物的状态 —— ________________________;
(2)反应发生的条件 —— ______________________。
3.确定二氧化碳气体收集装置应考虑的因素
(1)二氧化碳的密度—— ______________________;
(2)二氧化碳的溶解性 —— ___________________;
(3)二氧化碳能否与水反应 —— ________________。
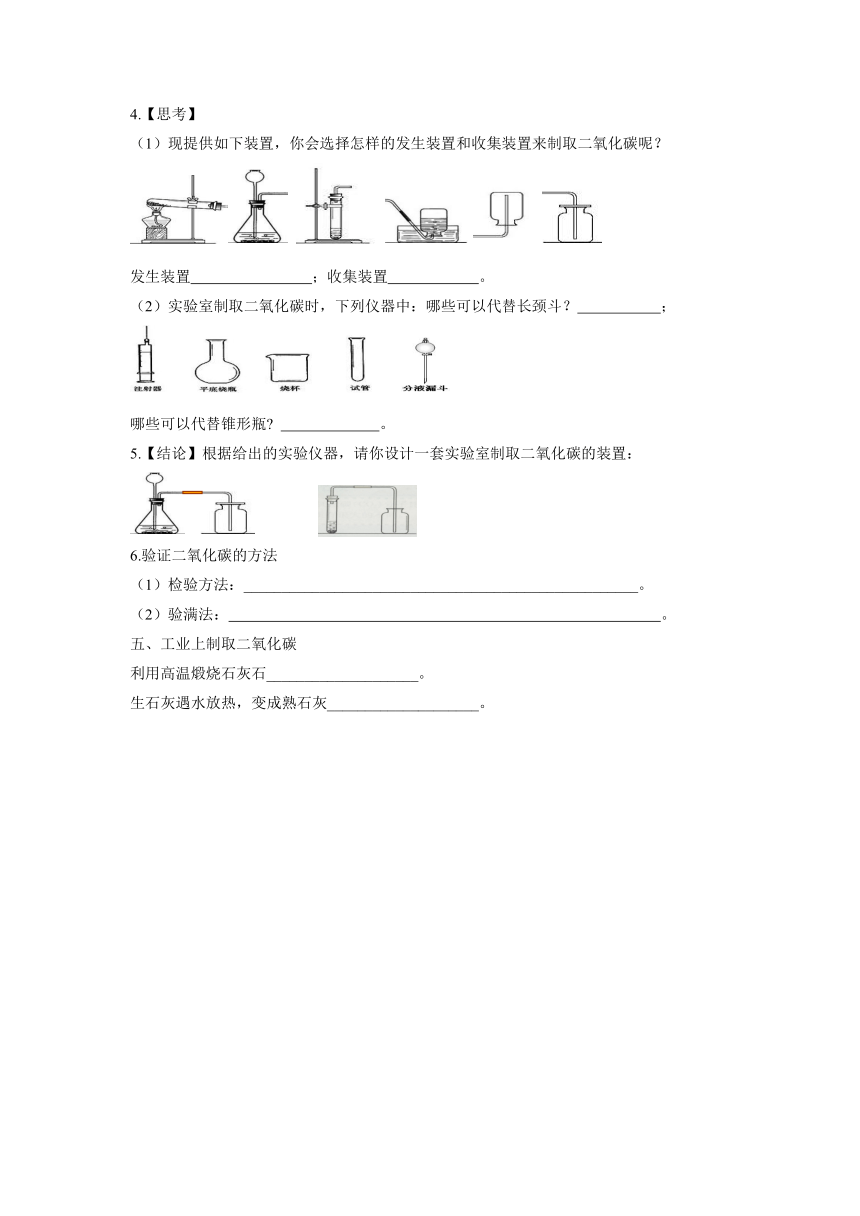
4.【思考】
(1)现提供如下装置,你会选择怎样的发生装置和收集装置来制取二氧化碳呢?
发生装置 ;收集装置 。
(2)实验室制取二氧化碳时,下列仪器中:哪些可以代替长颈斗? ;
哪些可以代替锥形瓶 。
5.【结论】根据给出的实验仪器,请你设计一套实验室制取二氧化碳的装置:
6.验证二氧化碳的方法
(1)检验方法:____________________________________________________。
(2)验满法: 。
五、工业上制取二氧化碳
利用高温煅烧石灰石____________________。
生石灰遇水放热,变成熟石灰____________________。
例题精讲:
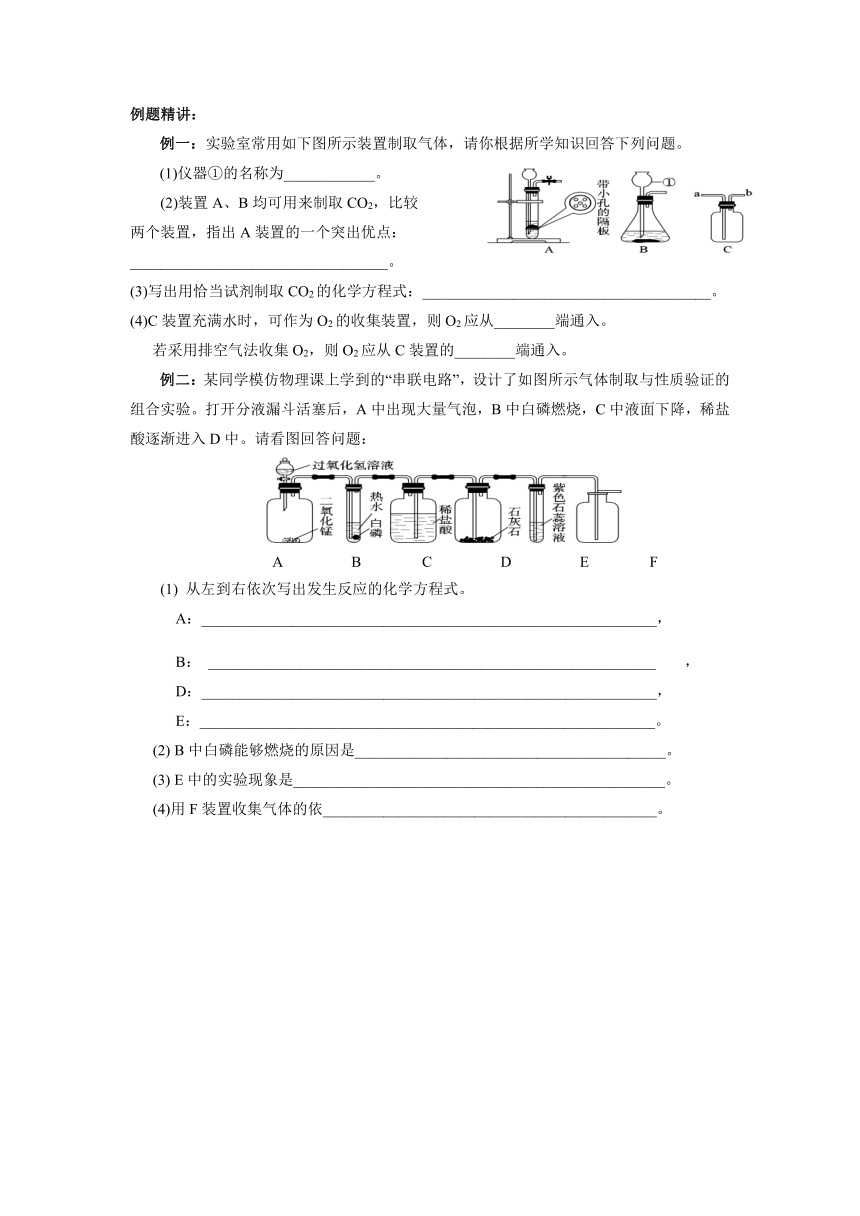
例一:实验室常用如下图所示装置制取气体,请你根据所学知识回答下列问题。
(1)仪器①的名称为____________。
(2)装置A、B均可用来制取CO2,比较
两个装置,指出A装置的一个突出优点:
__________________________________。
(3)写出用恰当试剂制取CO2的化学方程式:______________________________________。
(4)C装置充满水时,可作为O2的收集装置,则O2应从________端通入。
若采用排空气法收集O2,则O2应从C装置的________端通入。
例二:某同学模仿物理课上学到的“串联电路”,设计了如图所示气体制取与性质验证的组合实验。打开分液漏斗活塞后,A中出现大量气泡,B中白磷燃烧,C中液面下降,稀盐酸逐渐进入D中。请看图回答问题:
A B C D E F
(1) 从左到右依次写出发生反应的化学方程式。
A:____________________________________________________________,
B: ___________________________________________________________,
D:____________________________________________________________,
E:____________________________________________________________。
(2) B中白磷能够燃烧的原因是_________________________________________。
(3) E中的实验现象是_________________________________________________。
(4)用F装置收集气体的依____________________________________________。
例三:为测定石灰石样品中碳酸钙的质量分数,某学
习小组进行了如下实验探究,取10 g石灰石样品放入烧杯
中,加入稀盐酸至不再产生气泡为止(石灰石中的杂质不溶
于水,也不反应),并绘制了加入稀盐酸的质量与放出气体
质量的坐标图,如右图所示。
(1)碳酸钙完全反应用去稀盐酸的质量为____ g。
(2)计算该石灰石样品中碳酸钙的质量分数。
5.3二氧化碳性质与制取答案
[课前复习]
1.“吸烟有害于健康。”我国政府规定:从2010年5月1日起,公共室内禁止吸烟。烟草燃烧释放的有害物质中,能与血红蛋白结合引起中毒的是( B )
A.尼古丁 B.一氧化碳C.焦油 D.甲醛
2.下列叙述中,与常温下碳单质的化学稳定性无关的是( D )
A.将木桩埋入地下的一段用火烤焦B.档案材料一般用碳素墨水填写
C.古代用墨书写绘制的字画经久不变色D.用石墨制铅笔芯
3.下列物质的用途,既利用了碳的物理性质,又利用了化学性质的是( C )
A.用焦炭炼钢B.用活性炭作吸附剂C.用墨写字保存时间长D.用木炭制燃料
4.一种无色气体X,能在空气中燃烧生成另一种无色气体Y,Y和灼热的木炭反应又只生成气体X,则X是( D )【来源:21cnj*y.co*m】
A.O2 B.H2 C.CH4 D.CO
5.关于C60的说法正确的是( B )
A.它是一种新型的碳的化合物B.它是一种新型的碳单质
C.它是由碳原子直接构成的D.它的相对分子质量是60
6.金刚石、石墨、木炭和C60都是由碳元素组成的单质,下列关于碳的单质的叙述正确的是( B )21
纪A.都是黑色固体B.在氧气中充分燃烧时都生成二氧化碳
C.碳原子的排列方式相同D.一定条件下,石墨转化成金刚石是物理变化
7.防毒面具的滤毒罐中用来吸附毒气的物质是( B )
A.炭黑 B.活性炭C.木炭 D.石墨
8.中华炭雕(主要成分是木炭)是一种集观赏与空气净化于一体的工艺品,关于它的说法错误的是( C )
A.炭雕摆设要远离火种B.炭雕艺术品可以长久保存
C.炭雕是轻质透明的固体D.炭雕能吸附室内有害气体
9.下列对一些事实的解释错误的是( C )
事实 解释
A 书写档案规定必须使用碳素墨水 碳的化学性质稳定
B 石墨能够作电池的电极材料 石墨能够导电
C 焦炭可以把铁从它的氧化物矿石里还原出来 焦炭具有氧化性
D 制糖工业中用活性炭来脱色制白糖 活性炭具有吸附性
10.以石墨为原料,先制备氧化石墨,再经过热还原制备石墨烯。石墨烯硬度大,导电性能好,有韧性,可弯曲。下列关于金刚石、石墨、C60和石墨烯四种物质的叙述中错误的是( B )2·1·c·n·j·y
A.将石墨变成石墨烯发生了化学变化B.四种物质碳原子的排列方式不同
C.四种物质完全燃烧后的产物都是CO2D.石墨烯是一种新型的化合物
[新授课]
[学习目标]1、认识二氧化碳的主要物理和化学性质;
2、了解二氧化碳对人类生活和生产的意义。
3、了解掌握二氧化碳的实验室制法。
一、二氧化碳有何性质
1.物理性质
(1)通常情况下,二氧化碳是一种无色、无味的气体。(2)密度比空气的大。
(3)溶解性能溶于水。(4)固体二氧化碳俗称干冰,干冰升华吸热。
2.化学性质
[实验一] 在大烧杯中放置一个铁皮架,架上固定两支点燃的蜡烛,通过喇叭形纸筒将一瓶二氧化碳向烧杯内倾倒。
现象:下 层的蜡烛先熄灭,上层的蜡烛后熄灭。
结论:①二氧化碳不能燃烧,也不能支持燃烧;
②二氧化碳的密度比空气密度大。
[实验二] (1)往集满二氧化碳的软质塑料瓶里注入约 瓶蒸
馏水,立即旋紧瓶盖,充分振荡,如右图所示,观察到软塑料瓶变瘪,
原因是二氧化碳二氧化碳溶于水,瓶内气压变小。
(2)将瓶内液体倒数毫升至试管中,向试管中滴入紫色石蕊溶液,振荡,观察到
紫色石蕊溶液变红,原因是CO2与水反应生成碳酸,反应的化学方程式为
CO2 +H2O==H2CO3。
将上述试管加热,观察到溶液变为紫色,因为碳酸不稳定易分解,反应的化学方程式为
H2CO3== CO2 ↑ +H2O 。
某同学设计了如下一组实验,取四朵紫色石蕊试液染色的干燥纸花,
分别按下图进行实验。
(1)各步实验中观察到纸花的颜色变化情况是:
I.纸花 变红 II.纸花 不变色 III.纸花 不变色 IV.纸花 变红
总结:二氧化碳与水发生反应,生成的 碳酸 能使紫色的石蕊试液变 变红
二氧化碳与水的反应方程式:CO2 +H2O==H2CO3
碳酸不稳定,易分解,化学方程式为H2CO3== CO2 ↑ +H2O
[实验三] 如右图所示,取一支盛澄清石灰水的试管,通过玻璃管,往石灰水里吹一会儿气。
现象:澄清石灰水变浑浊。
结论:CO2与澄清石灰水反应,有不容白色固体生成,该反应的
化学方程式为CO2+Ca(OH)2==CaCO3↓+H2O,用此反应可以鉴定二氧化碳。
二、 二氧化碳对人类生活和环境有何影响
1.二氧化碳有广泛的用途
写出各用途对应的二氧化碳的性质。
人工降雨升华吸热;
灭 火密度比空气密度大;
2.二氧化碳对人类和环境的影响
虽然二氧化碳无毒性,但不能供给呼吸,人在二氧化碳浓度偏高的环境中,会感到气闷、头痛乃至窒息死亡;大气中二氧化碳含量持续上升,产生了越来越严重的温室效应加剧。结果导致全球变暖,带来了严重的环境问题。
三 、自然界中的碳循环
氧气
二氧化碳
[注意] CO2 不是空气污染物。CO2会参与大气中的碳循环,是氧气的间接来源。
四、二氧化碳制取
1.实验室常用大理石和稀盐酸反应制取二氧化碳。
(1)反应的化学方程式为:2HCl+CaCO3===CaCl2+ H2CO3;
(2)碳酸不稳定,分解生成二氧化碳和水H2CO3==CO2 ↑ +H2O;
(3)总的化学方程式为:2HCl+ CaCO3===CaCl2+ CO2 ↑ +H2O。
2.确定二氧化碳气体发生装置应考虑的因素
(1)反应物的状态 —— 固体和液体;
(2)反应发生的条件 —— 常温。
3.确定二氧化碳气体收集装置应考虑的因素
(1)二氧化碳的密度—— 大于空气密度;
(2)二氧化碳的溶解性 —— 能溶于水;
(3)二氧化碳能否与水反应 —— CO2 +H2O==H2CO3。
4.【思考】
(1)现提供如下装置,你会选择怎样的发生装置和收集装置来制取二氧化碳呢?
发生装置 B或 C ;收集装置 F 。
(2)实验室制取二氧化碳时,下列仪器中:哪些可以代替长颈斗? AE ;
哪些可以代替锥形瓶 BD 。
5.【结论】根据给出的实验仪器,请你设计一套实验室制取二氧化碳的装置:
6.验证二氧化碳的方法
(1)检验方法:将生成气体通入澄清石灰水,若石灰水变浑浊,证明是二氧化碳。
(2)验满法: 将燃着的小木条放在集气瓶口,若小木条熄灭,说明收集已满 。
五、工业上制取二氧化碳
利用高温煅烧石灰石CaCO3CaO+ CO2 ↑。
生石灰遇水放热,变成熟石灰 CaO +H2O ===Ca(OH)2。
例题精讲:
例一:实验室常用如下图所示装置制取气体,请你根据所学知识回答下列问题。
(1)仪器①的名称为长颈漏斗。
(2)装置A、B均可用来制取CO2,比较
两个装置,指出A装置的一个突出优点:
随时控制反应的发生和停止。
(3)写出用恰当试剂制取CO2的化学方程式:2HCl+CaCO3=== CaCl2+ CO2 ↑ +H2O 。
(4)C装置充满水时,可作为O2的收集装置,则O2应从b端通入。
若采用排空气法收集O2,则O2应从C装置的a端通入。
例二:某同学模仿物理课上学到的“串联电路”,设计了如图所示气体制取与性质验证的组合实验。打开分液漏斗活塞后,A中出现大量气泡,B中白磷燃烧,C中液面下降,稀盐酸逐渐进入D中。请看图回答问题:
A B C D E F
(1) 从左到右依次写出发生反应的化学方程式。
A:2H2O2 2H2O+O2↑,
B: 4 P+5O2 2 P2O5 ,
D:2HCl+ CaCO3===CaCl2+ CO2 ↑ +H2O,
E: CO2 +H2O==H2CO3。
(2) B中白磷能够燃烧的原因是与氧气充分接触且温度达到着火点。
(3) E中的实验现象是紫色石蕊溶液变红。
(4)用F装置收集气体的依据是二氧化碳密度比空气大。
例三:为测定石灰石样品中碳酸钙的质量分数,某学
习小组进行了如下实验探究,取10 g石灰石样品放入烧杯
中,加入稀盐酸至不再产生气泡为止(石灰石中的杂质不溶
于水,也不反应),并绘制了加入稀盐酸的质量与放出气体
质量的坐标图,如右图所示。
(1)碳酸钙完全反应用去稀盐酸的质量为84.32 g。
(2)计算该石灰石样品中碳酸钙的质量分数。80%
A B C D E F
A B C D E
A B C D E F
A B C D E
[课前复习]
1.“吸烟有害于健康。”我国政府规定:公共室内禁止吸烟。烟草燃烧释放的有害物质中,能与血红蛋白结合引起中毒的是( )
A.尼古丁 B.一氧化碳 C.焦油 D.甲醛
2.下列叙述中,与常温下碳单质的化学稳定性无关的是( )
A.将木桩埋入地下的一段用火烤焦
B.档案材料一般用碳素墨水填写
C.古代用墨书写绘制的字画经久不变色
D.用石墨制铅笔芯
3.下列物质的用途,既利用了碳的物理性质,又利用了化学性质的是( )
A.用焦炭炼钢 B.用活性炭作吸附剂 C.用墨写字保存时间长 D.用木炭制燃料
4.一种无色气体X,能在空气中燃烧生成另一种无色气体Y,Y和灼热的木炭反应又只生成气体X,则X是( )y.co*m】
A.O2 B.H2 C.CH4 D.CO
5.关于C60的说法正确的是( )
A.它是一种新型的碳的化合物B.它是一种新型的碳单质
C.它是由碳原子直接构成的D.它的相对分子质量是60
6.金刚石、石墨、木炭和C60都是由碳元素组成的单质,下列关于碳的单质的叙述正确的是( )21纪
A.都是黑色固体
B.在氧气中充分燃烧时都生成二氧化碳
C.碳原子的排列方式相同
D.一定条件下,石墨转化成金刚石是物理变化
7.防毒面具的滤毒罐中用来吸附毒气的物质是( )
A.炭黑 B.活性炭 C.木炭 D.石墨
8.中华炭雕(主要成分是木炭)是一种集观赏与空气净化于一体的工艺品,关于它的说法错误的是( )
A.炭雕摆设要远离火种
B.炭雕艺术品可以长久保存
C.炭雕是轻质透明的固体
D.炭雕能吸附室内有害气体
9.下列对一些事实的解释错误的是( )
事实 解释
A 书写档案规定必须使用碳素墨水 碳的化学性质稳定
B 石墨能够作电池的电极材料 石墨能够导电
C 焦炭可以把铁从它的氧化物矿石里还原出来 焦炭具有氧化性
D 制糖工业中用活性炭来脱色制白糖 活性炭具有吸附性
10.以石墨为原料,先制备氧化石墨,再经过热还原制备石墨烯。石墨烯硬度大,导电性能好,有韧性,可弯曲。下列关于金刚石、石墨、C60和石墨烯四种物质的叙述中错误的是( )2·1·c·n·j·y
A.将石墨变成石墨烯发生了化学变化
B.四种物质碳原子的排列方式不同
C.四种物质完全燃烧后的产物都是CO2
D.石墨烯是一种新型的化合物
[新授课]
[学习目标]1、认识二氧化碳的主要物理和化学性质;
2、了解二氧化碳对人类生活和生产的意义。
3、了解掌握二氧化碳的实验室制法。
一、二氧化碳有何性质
1.物理性质
(1)通常情况下,二氧化碳是一种______色、______味的气体。(2)密度比空气的________。
(3)溶解性____________。(4)固体二氧化碳俗称________,干冰升华吸热。
2.化学性质
[实验一] 在大烧杯中放置一个铁皮架,架上固定两支点燃的蜡烛,通过喇叭形纸筒将一瓶二氧化碳向烧杯内倾倒。
现象:________层的蜡烛先熄灭,________层的蜡烛后熄灭。
结论:①二氧化碳__________,也不能______________________;
②二氧化碳的密度________________。
[实验二] (1)往集满二氧化碳的软质塑料瓶里注入约 瓶蒸
馏水,立即旋紧瓶盖,充分振荡,如右图所示,观察到____________,
原因是二氧化碳_______________________________。
(2)将瓶内液体倒数毫升至试管中,向试管中滴入紫色石蕊溶液,振荡,观察到紫色石蕊溶液______,原因是________________,反应的化学方程式为____________________。
(3)将上述试管加热,观察到溶液变为紫色,因为碳酸不稳定易分解,反应的化学方程式为___________。
某同学设计了如下一组实验,取四朵紫色石蕊试液染色的干燥纸花,
分别按下图进行实验。
(1)各步实验中观察到纸花的颜色变化情况是:
I.纸花 II.纸花 III.纸花 IV.纸花
总结:二氧化碳与水发生反应,生成的 能使紫色的石蕊试液变
二氧化碳与水的反应方程式:
碳酸不稳定,易分解,化学方程式为
[实验三] 如右图所示,取一支盛澄清石灰水的试管,通过玻璃管,往石灰水里吹一会儿气。
现象:澄清石灰水________。
结论:CO2与澄清石灰水反应,有______________生成,该反应的
化学方程式为________________________________,用此反应可以鉴定
二氧化碳。
二、 二氧化碳对人类生活和环境有何影响
1.二氧化碳有广泛的用途
写出各用途对应的二氧化碳的性质。
人工降雨____________________________;
灭 火____________________________;
2.二氧化碳对人类和环境的影响
虽然二氧化碳______毒性,但不能____________,人在二氧化碳浓度偏高的环境中,会感到气闷、头痛乃至窒息死亡;大气中二氧化碳含量持续上升,产生了越来越严重的____________。结果导致全球变暖,带来了严重的环境问题。
三 、自然界中的碳循环
[注意] CO2 不是空气污染物。CO2会参与大气中的碳循环,是氧气的间接来源。
四、二氧化碳制取
1.实验室常用大理石和稀盐酸反应制取二氧化碳。
(1)反应的化学方程式为:_________________________________________;
(2)碳酸不稳定,分解生成二氧化碳和水_____________________________;
(3)总的化学方程式为:___________________________________________。
2.确定二氧化碳气体发生装置应考虑的因素
(1)反应物的状态 —— ________________________;
(2)反应发生的条件 —— ______________________。
3.确定二氧化碳气体收集装置应考虑的因素
(1)二氧化碳的密度—— ______________________;
(2)二氧化碳的溶解性 —— ___________________;
(3)二氧化碳能否与水反应 —— ________________。
4.【思考】
(1)现提供如下装置,你会选择怎样的发生装置和收集装置来制取二氧化碳呢?
发生装置 ;收集装置 。
(2)实验室制取二氧化碳时,下列仪器中:哪些可以代替长颈斗? ;
哪些可以代替锥形瓶 。
5.【结论】根据给出的实验仪器,请你设计一套实验室制取二氧化碳的装置:
6.验证二氧化碳的方法
(1)检验方法:____________________________________________________。
(2)验满法: 。
五、工业上制取二氧化碳
利用高温煅烧石灰石____________________。
生石灰遇水放热,变成熟石灰____________________。
例题精讲:
例一:实验室常用如下图所示装置制取气体,请你根据所学知识回答下列问题。
(1)仪器①的名称为____________。
(2)装置A、B均可用来制取CO2,比较
两个装置,指出A装置的一个突出优点:
__________________________________。
(3)写出用恰当试剂制取CO2的化学方程式:______________________________________。
(4)C装置充满水时,可作为O2的收集装置,则O2应从________端通入。
若采用排空气法收集O2,则O2应从C装置的________端通入。
例二:某同学模仿物理课上学到的“串联电路”,设计了如图所示气体制取与性质验证的组合实验。打开分液漏斗活塞后,A中出现大量气泡,B中白磷燃烧,C中液面下降,稀盐酸逐渐进入D中。请看图回答问题:
A B C D E F
(1) 从左到右依次写出发生反应的化学方程式。
A:____________________________________________________________,
B: ___________________________________________________________,
D:____________________________________________________________,
E:____________________________________________________________。
(2) B中白磷能够燃烧的原因是_________________________________________。
(3) E中的实验现象是_________________________________________________。
(4)用F装置收集气体的依____________________________________________。
例三:为测定石灰石样品中碳酸钙的质量分数,某学
习小组进行了如下实验探究,取10 g石灰石样品放入烧杯
中,加入稀盐酸至不再产生气泡为止(石灰石中的杂质不溶
于水,也不反应),并绘制了加入稀盐酸的质量与放出气体
质量的坐标图,如右图所示。
(1)碳酸钙完全反应用去稀盐酸的质量为____ g。
(2)计算该石灰石样品中碳酸钙的质量分数。
5.3二氧化碳性质与制取答案
[课前复习]
1.“吸烟有害于健康。”我国政府规定:从2010年5月1日起,公共室内禁止吸烟。烟草燃烧释放的有害物质中,能与血红蛋白结合引起中毒的是( B )
A.尼古丁 B.一氧化碳C.焦油 D.甲醛
2.下列叙述中,与常温下碳单质的化学稳定性无关的是( D )
A.将木桩埋入地下的一段用火烤焦B.档案材料一般用碳素墨水填写
C.古代用墨书写绘制的字画经久不变色D.用石墨制铅笔芯
3.下列物质的用途,既利用了碳的物理性质,又利用了化学性质的是( C )
A.用焦炭炼钢B.用活性炭作吸附剂C.用墨写字保存时间长D.用木炭制燃料
4.一种无色气体X,能在空气中燃烧生成另一种无色气体Y,Y和灼热的木炭反应又只生成气体X,则X是( D )【来源:21cnj*y.co*m】
A.O2 B.H2 C.CH4 D.CO
5.关于C60的说法正确的是( B )
A.它是一种新型的碳的化合物B.它是一种新型的碳单质
C.它是由碳原子直接构成的D.它的相对分子质量是60
6.金刚石、石墨、木炭和C60都是由碳元素组成的单质,下列关于碳的单质的叙述正确的是( B )21
纪A.都是黑色固体B.在氧气中充分燃烧时都生成二氧化碳
C.碳原子的排列方式相同D.一定条件下,石墨转化成金刚石是物理变化
7.防毒面具的滤毒罐中用来吸附毒气的物质是( B )
A.炭黑 B.活性炭C.木炭 D.石墨
8.中华炭雕(主要成分是木炭)是一种集观赏与空气净化于一体的工艺品,关于它的说法错误的是( C )
A.炭雕摆设要远离火种B.炭雕艺术品可以长久保存
C.炭雕是轻质透明的固体D.炭雕能吸附室内有害气体
9.下列对一些事实的解释错误的是( C )
事实 解释
A 书写档案规定必须使用碳素墨水 碳的化学性质稳定
B 石墨能够作电池的电极材料 石墨能够导电
C 焦炭可以把铁从它的氧化物矿石里还原出来 焦炭具有氧化性
D 制糖工业中用活性炭来脱色制白糖 活性炭具有吸附性
10.以石墨为原料,先制备氧化石墨,再经过热还原制备石墨烯。石墨烯硬度大,导电性能好,有韧性,可弯曲。下列关于金刚石、石墨、C60和石墨烯四种物质的叙述中错误的是( B )2·1·c·n·j·y
A.将石墨变成石墨烯发生了化学变化B.四种物质碳原子的排列方式不同
C.四种物质完全燃烧后的产物都是CO2D.石墨烯是一种新型的化合物
[新授课]
[学习目标]1、认识二氧化碳的主要物理和化学性质;
2、了解二氧化碳对人类生活和生产的意义。
3、了解掌握二氧化碳的实验室制法。
一、二氧化碳有何性质
1.物理性质
(1)通常情况下,二氧化碳是一种无色、无味的气体。(2)密度比空气的大。
(3)溶解性能溶于水。(4)固体二氧化碳俗称干冰,干冰升华吸热。
2.化学性质
[实验一] 在大烧杯中放置一个铁皮架,架上固定两支点燃的蜡烛,通过喇叭形纸筒将一瓶二氧化碳向烧杯内倾倒。
现象:下 层的蜡烛先熄灭,上层的蜡烛后熄灭。
结论:①二氧化碳不能燃烧,也不能支持燃烧;
②二氧化碳的密度比空气密度大。
[实验二] (1)往集满二氧化碳的软质塑料瓶里注入约 瓶蒸
馏水,立即旋紧瓶盖,充分振荡,如右图所示,观察到软塑料瓶变瘪,
原因是二氧化碳二氧化碳溶于水,瓶内气压变小。
(2)将瓶内液体倒数毫升至试管中,向试管中滴入紫色石蕊溶液,振荡,观察到
紫色石蕊溶液变红,原因是CO2与水反应生成碳酸,反应的化学方程式为
CO2 +H2O==H2CO3。
将上述试管加热,观察到溶液变为紫色,因为碳酸不稳定易分解,反应的化学方程式为
H2CO3== CO2 ↑ +H2O 。
某同学设计了如下一组实验,取四朵紫色石蕊试液染色的干燥纸花,
分别按下图进行实验。
(1)各步实验中观察到纸花的颜色变化情况是:
I.纸花 变红 II.纸花 不变色 III.纸花 不变色 IV.纸花 变红
总结:二氧化碳与水发生反应,生成的 碳酸 能使紫色的石蕊试液变 变红
二氧化碳与水的反应方程式:CO2 +H2O==H2CO3
碳酸不稳定,易分解,化学方程式为H2CO3== CO2 ↑ +H2O
[实验三] 如右图所示,取一支盛澄清石灰水的试管,通过玻璃管,往石灰水里吹一会儿气。
现象:澄清石灰水变浑浊。
结论:CO2与澄清石灰水反应,有不容白色固体生成,该反应的
化学方程式为CO2+Ca(OH)2==CaCO3↓+H2O,用此反应可以鉴定二氧化碳。
二、 二氧化碳对人类生活和环境有何影响
1.二氧化碳有广泛的用途
写出各用途对应的二氧化碳的性质。
人工降雨升华吸热;
灭 火密度比空气密度大;
2.二氧化碳对人类和环境的影响
虽然二氧化碳无毒性,但不能供给呼吸,人在二氧化碳浓度偏高的环境中,会感到气闷、头痛乃至窒息死亡;大气中二氧化碳含量持续上升,产生了越来越严重的温室效应加剧。结果导致全球变暖,带来了严重的环境问题。
三 、自然界中的碳循环
氧气
二氧化碳
[注意] CO2 不是空气污染物。CO2会参与大气中的碳循环,是氧气的间接来源。
四、二氧化碳制取
1.实验室常用大理石和稀盐酸反应制取二氧化碳。
(1)反应的化学方程式为:2HCl+CaCO3===CaCl2+ H2CO3;
(2)碳酸不稳定,分解生成二氧化碳和水H2CO3==CO2 ↑ +H2O;
(3)总的化学方程式为:2HCl+ CaCO3===CaCl2+ CO2 ↑ +H2O。
2.确定二氧化碳气体发生装置应考虑的因素
(1)反应物的状态 —— 固体和液体;
(2)反应发生的条件 —— 常温。
3.确定二氧化碳气体收集装置应考虑的因素
(1)二氧化碳的密度—— 大于空气密度;
(2)二氧化碳的溶解性 —— 能溶于水;
(3)二氧化碳能否与水反应 —— CO2 +H2O==H2CO3。
4.【思考】
(1)现提供如下装置,你会选择怎样的发生装置和收集装置来制取二氧化碳呢?
发生装置 B或 C ;收集装置 F 。
(2)实验室制取二氧化碳时,下列仪器中:哪些可以代替长颈斗? AE ;
哪些可以代替锥形瓶 BD 。
5.【结论】根据给出的实验仪器,请你设计一套实验室制取二氧化碳的装置:
6.验证二氧化碳的方法
(1)检验方法:将生成气体通入澄清石灰水,若石灰水变浑浊,证明是二氧化碳。
(2)验满法: 将燃着的小木条放在集气瓶口,若小木条熄灭,说明收集已满 。
五、工业上制取二氧化碳
利用高温煅烧石灰石CaCO3CaO+ CO2 ↑。
生石灰遇水放热,变成熟石灰 CaO +H2O ===Ca(OH)2。
例题精讲:
例一:实验室常用如下图所示装置制取气体,请你根据所学知识回答下列问题。
(1)仪器①的名称为长颈漏斗。
(2)装置A、B均可用来制取CO2,比较
两个装置,指出A装置的一个突出优点:
随时控制反应的发生和停止。
(3)写出用恰当试剂制取CO2的化学方程式:2HCl+CaCO3=== CaCl2+ CO2 ↑ +H2O 。
(4)C装置充满水时,可作为O2的收集装置,则O2应从b端通入。
若采用排空气法收集O2,则O2应从C装置的a端通入。
例二:某同学模仿物理课上学到的“串联电路”,设计了如图所示气体制取与性质验证的组合实验。打开分液漏斗活塞后,A中出现大量气泡,B中白磷燃烧,C中液面下降,稀盐酸逐渐进入D中。请看图回答问题:
A B C D E F
(1) 从左到右依次写出发生反应的化学方程式。
A:2H2O2 2H2O+O2↑,
B: 4 P+5O2 2 P2O5 ,
D:2HCl+ CaCO3===CaCl2+ CO2 ↑ +H2O,
E: CO2 +H2O==H2CO3。
(2) B中白磷能够燃烧的原因是与氧气充分接触且温度达到着火点。
(3) E中的实验现象是紫色石蕊溶液变红。
(4)用F装置收集气体的依据是二氧化碳密度比空气大。
例三:为测定石灰石样品中碳酸钙的质量分数,某学
习小组进行了如下实验探究,取10 g石灰石样品放入烧杯
中,加入稀盐酸至不再产生气泡为止(石灰石中的杂质不溶
于水,也不反应),并绘制了加入稀盐酸的质量与放出气体
质量的坐标图,如右图所示。
(1)碳酸钙完全反应用去稀盐酸的质量为84.32 g。
(2)计算该石灰石样品中碳酸钙的质量分数。80%
A B C D E F
A B C D E
A B C D E F
A B C D E
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
