化学人教版(2019)必修第一册3.1.3铁盐和亚铁盐(共35张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第一册3.1.3铁盐和亚铁盐(共35张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 87.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-29 00:00:00 | ||
图片预览










文档简介
(共35张PPT)
meiyangyang8602
meiyangyang8602
人体中的铁元素
铁在成人体中的含量为4~5g,是人体必需微量元素中含量最多的一种。人体内的含铁化合物主要分为两类,即功能性铁和储存铁。功能性铁参与氧的运输,其余的铁与一些酶结合,分布于身体各器官。体内缺铁将会导致人的记忆能力、免疫能力和对温度的适应能力等生理功能下降。如果体内的铁不足以供给生命活动的需要,就会发生贫血。
为了满足生理需要,成人每天铁的适宜摄入量为15~20mg。动物内脏、肉类、鱼类、蛋类等动物性食物中的铁容易被吸收。一般蔬菜中铁的含量较少,吸收率也低,但我国膳食中一般食用蔬菜量很大,仍为铁的重要来源。我国已经实施在某些酱油中加入铁强化剂的措施,以减少缺铁性贫血问题的发生。
【资料卡片】P70
如何合理补铁?
meiyangyang8602
meiyangyang8602
生活中的富铁食品
补铁补的是几价铁?
第一节
铁及其化合物
第三章 铁 金属材料
赵健
第3课时 铁盐和亚铁盐
meiyangyang8602
meiyangyang8602
meiyangyang8602
meiyangyang8602
生活中的富铁食品
菠菜中铁元素的含量测定
课本P76
检验食品中的铁元素
meiyangyang8602
meiyangyang8602
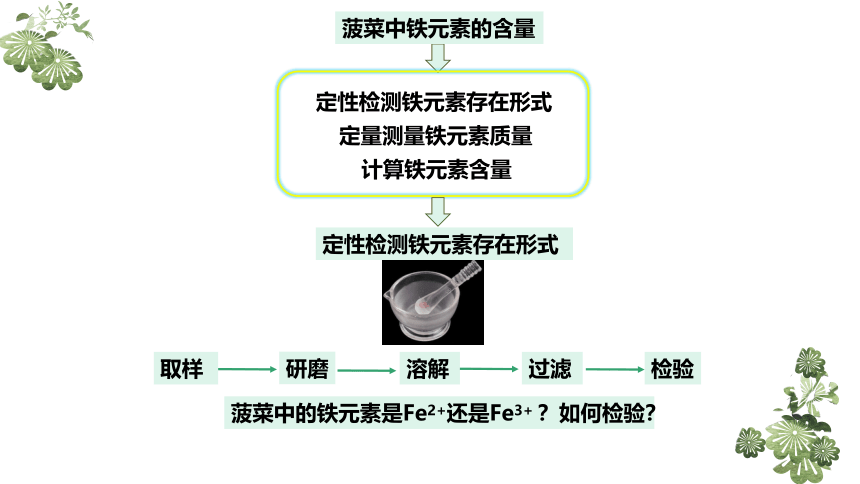
菠菜中铁元素的含量
定性检测铁元素存在形式
定量测量铁元素质量
计算铁元素含量
定性检测铁元素存在形式
取样
研磨
溶解
过滤
检验
菠菜中的铁元素是Fe2+还是Fe3+ ?如何检验?
meiyangyang8602
请你猜测!
菠菜中的铁元素是Fe2+还是Fe3+ ?
猜想1:只含有Fe2+
猜想2:只含有Fe3+
猜想3:含有Fe2+和Fe3+
综合考虑:应该含有Fe2+和Fe3+
针对猜想,请同学们设计实验加以验证
溶解水配成溶液,你认为样品中铁元素有哪些存在形式
O2
亚铁离子被O2氧化,铁元素可能以铁离子形式存在
Fe2+
Fe3+
01
Fe2+、Fe3+的检验
赵健
meiyangyang8602
meiyangyang8602
meiyangyang8602
meiyangyang8602
学习方法引导
课本P74
铁盐和亚铁盐具有什么样的化学性质?
meiyangyang8602
meiyangyang8602
铁盐和亚铁盐
硫酸亚铁
硫酸亚铁溶液
氯化亚铁
硫酸铁
硫酸铁溶液
氯化铁
氯化铁溶液
Fe3+:棕黄色
Fe2+:浅绿色
meiyangyang8602
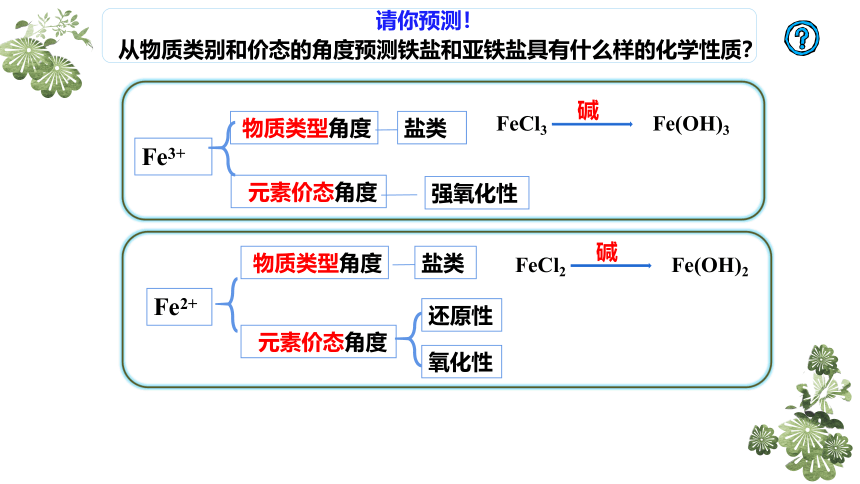
请你预测!
从物质类别和价态的角度预测铁盐和亚铁盐具有什么样的化学性质?
Fe3+
物质类型角度
元素价态角度
强氧化性
盐类
Fe2+
物质类型角度
元素价态角度
氧化性
盐类
还原性
FeCl3
碱
Fe(OH)3
FeCl2
碱
Fe(OH)2
meiyangyang8602
meiyangyang8602
Fe2+、Fe3+的检验
Fe(OH)3 Fe(OH)2
实验 操作
实验现象及方程式
有红褐色沉淀
Fe3++3OH-=Fe(OH)3↓
Fe2++2OH-=Fe(OH)2↓
从物质类别的角度
meiyangyang8602
meiyangyang8602
Fe2+、Fe3+的检验
[实验3-2]
在两支试管中分别加入少量的FeCl3溶液和FeCl2溶液,各滴入几滴KSCN溶液。观察并记录现象。
课本P72
meiyangyang8602
meiyangyang8602
Fe2+、Fe3+的检验
[实验3-2]
在两支试管中分别加入少量的FeCl3溶液和FeCl2溶液,各滴入几滴KSCN溶液。观察并记录现象。
课本P72
滴入KSCN溶液 原理
FeCl3溶液
FeCl2溶液 ——
滴入
KSCN溶液
滴入
KSCN溶液
溶液变为红色
溶液无明显变化
Fe3+ + 3SCN- = Fe(SCN)3
(红色)
?
meiyangyang8602
meiyangyang8602
Fe2+、Fe3+的检验
Fe3+ + 3SCN- = Fe(SCN)3 (红色液体)
检验Fe3+最灵敏的方法
2Fe2++Cl2= 2Fe3+ +2Cl-
检验Fe2+的方法
?
滴入
KSCN溶液
FeCl3
滴入
KSCN溶液
FeCl2
滴入
氯水
Fe3+ + 3SCN- = Fe(SCN)3 (红色液体)
meiyangyang8602
meiyangyang8602
Fe2+、Fe3+的检验
从元素化合价的角度
在给定试剂中选择合适试剂,设计实验方案并预测实验现象
试剂:FeCl3溶液、FeCl2溶液、KSCN溶液、新制氯水、H2O2溶液、
酸性KMnO4溶液、KI-淀粉试纸、铁粉、铜片
性质预测 所选试剂 预期实验现象及结论 相关离子方程式
既具有还原性,又具有氧化性
氧化性
+2
+3
FeCl2
FeCl3
请你设计试验方案
meiyangyang8602
Fe2+、Fe3+的检验
设计试验方案
确认Fe2+存在 ,利用Fe2+还原性
2Fe2++Cl2= 2Fe3+ +2Cl-
?
滴入
KSCN溶液
FeCl2
滴入
氯水
Fe3+ + 3SCN- = Fe(SCN)3 (红色液体)
滴入双氧水
①先加KSCN溶液,再加氯水或双氧水
取少量样品溶液于试管,滴加少量酸性高锰酸钾溶液,如果紫红色褪色,则溶液中含有Fe2+ ;如果无明显变化,则溶液中不含Fe2+
5Fe2++MnO4-+8H+= 5Fe3+ +Mn2++4H2O
②加KMnO4(H+)溶液
meiyangyang8602
Fe2+、Fe3+的检验
确认Fe2+存在 ,利用Fe2+还原性
meiyangyang8602
请你解释!
请你解释一下日常生活中出现的现象为什么?
苹果 “生锈”
亚铁盐很容易被氧化为铁盐
赵健
02
Fe2+和Fe3+的转化
meiyangyang8602
meiyangyang8602
meiyangyang8602
请你思考!
你还知道哪些试剂能将亚铁盐变成铁盐?写出反应的离子方程式
Fe2+ Fe3+
氧化剂
(还原剂具有还原性)
氧化剂:O2、 Cl2、H2O2、HNO3、KMnO4 等
meiyangyang8602
请你思考!
如果将铁盐转变成亚铁盐选择什么试剂?写出反应的离子方程式
如何用Fe3+制备Fe2+?
加铁粉 (利用Fe3+的氧化性、Fe的还原性)
现象预测:溶液棕黄变浅绿
Fe3+
Fe2+
还原剂
请你设计试验方案
meiyangyang8602
meiyangyang8602
Fe2+、Fe3+的转化
[实验3-3]
在盛有2 mL FeCl3溶液的试管中加入少量铁粉,振荡试管。充分反应后,滴入几滴KSCN溶液,观察并记录现象。把上层清液倒入另一支试管中,再滴入几滴氯水,又发生了什么变化?
课本P73
meiyangyang8602
FeCl3溶液
加入过量
铁粉
溶液由棕黄色变为浅绿色
无明显现象
溶液呈红色
2Fe3++Fe=3Fe2+
2Fe2++Cl2=2Fe3++2Cl-
meiyangyang8602
Fe2+、Fe3+的转化
滴入
KSCN溶液
取上层清液
滴入氯水
meiyangyang8602
Fe2+、Fe3+的转化
电子工业上常用覆铜板制作印刷电路板,原理是:利用FeCl3溶液做腐蚀液,把覆铜板上不需要的铜腐蚀掉。预先设计好的电路在铜板上用蜡或不透水的物料覆盖,以保护铜线路不被腐蚀。
课本P74
思考与讨论(1)在上述实验中,发生 了什么化学反应, 生成的主要产 物是什么?请运用氧化还原反应的规律进行分析并尝试写出反应的化学方程式。
(2)为使使用后的“腐蚀液” 能得到充分利用,如何处理使用后的“腐蚀液”
meiyangyang8602meiyangyang8602Fe2+、Fe3+的转化
meiyangyang8602
meiyangyang8602
Fe2+、Fe3+的转化
1. 写出反应原理的化学方程式并用双线桥表示电子转移?
2. 为使使用后的“腐蚀液” 能得到充分利用,如何回收得到 Cu 和 FeCl 3
meiyangyang8602
meiyangyang8602
Fe2+、Fe3+的转化
思考与讨论
(1)Fe、FeSO4和Fe2(SO4)3三种物质中,哪种物质可做氧化剂,哪种可做还原剂,哪种既可做氧化剂又可做还原剂?举例写出相应反应的化学方程式,并加以说明。
(2)请你用图示的方法归纳Fe、Fe2+和Fe3+三者之间的相互转化关系,并与同学讨论。
Fe2+ Fe3+
氧化剂
还原剂
还原剂:Zn、Fe、Cu、S2-、I-等
氧化剂:O2、 Cl2、H2O2、HNO3、KMnO4 等
meiyangyang8602
物质类别
氧化物
碱
盐
单质
元素价态
0
+2
+3
+6
Fe(OH)3
Fe3+
Fe(OH)2
Fe2+
FeO
Fe
Fe3O4
Fe2O3
铁及其化合物的价类二维图
meiyangyang8602
Fe、Fe3+与Fe2+的相互转化
Fe
Fe2+
Fe3+
还原剂 如Fe、Zn、Cu、I- 、 S2-、H2S2-等
强氧化剂 如Cl2、H2O2、O2、HNO3、KMnO4等
弱氧化剂 如H+、Cu2+、S、I2 等
强还原剂 如Zn、Al、CO、H2等
强氧化剂 如Cl2、Br2、HNO3、浓硫酸等
强还原剂 如Zn、Al、CO、H2等
meiyangyang8602
meiyangyang8602
菠菜中铁元素的含量
定性检测铁元素存在形式
定量测量铁元素质量
计算铁元素含量
定量测量铁元素质量
溶液中Fe2+、Fe3+的质量不易直接测量,可以将离子转化为沉淀,通过测量沉淀的质量来计算铁元素的质量。
Fe3++3OH-=Fe(OH)3↓
Fe2++2OH-=Fe(OH)2↓
meiyangyang8602
菠菜中铁元素的含量
定量测量铁元素质量
方案1:沉淀法,将铁元素转化为Fe(OH)3,过滤、洗涤、干燥后称量,计算铁元素含量
Fe3+溶液
Fe2+溶液
OH-
OH-
Fe(OH)3
Fe(OH)2
O2
Fe2O3
方案2:将铁元素转化为Fe(OH)3过滤、洗涤、干燥后灼烧,称量Fe2O3质量后计算铁元素含量
Fe3+溶液
Fe2+溶液
OH-
Fe(OH)3
Fe2O3
meiyangyang8602
菠菜中铁元素的含量
定量测量铁元素质量
氧化剂
方案3:用氧化剂将补铁剂中亚铁盐全部氧化为铁盐,加碱沉淀后过滤、洗涤、干燥灼烧后称量氧化铁质量,再进行计算。
铁元素的质量分数
m(Fe2O3)×
56×2
56×2+16×3
m(样品)
meiyangyang8602
菠菜中铁元素的含量
meiyangyang8602
练习
FeCl2
Fe(OH)2
Fe(OH)3
FeCl3
KNO3
AgCl
KCl
FeCl2
KOH
Fe
H2
(2)写出E转变成F的化学方程式:
(3)向G溶液中加入A,写出反应的离子方程式:
KCl
(1)写出B和D的化学式:B ;D
课本77--6
meiyangyang8602
练习
2,某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液.在FeCl2溶液中需加入少量铁屑,其目的是___________________。
(2)甲组同学取2mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为________________________________。
(5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为__________________________;
一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成。
防止Fe2+被氧化
2Fe2++Cl2=2Fe3++2Cl-
H2O2+2Fe2++2H+=2Fe3++2H2O
meiyangyang8602
meiyangyang8602
人体中的铁元素
铁在成人体中的含量为4~5g,是人体必需微量元素中含量最多的一种。人体内的含铁化合物主要分为两类,即功能性铁和储存铁。功能性铁参与氧的运输,其余的铁与一些酶结合,分布于身体各器官。体内缺铁将会导致人的记忆能力、免疫能力和对温度的适应能力等生理功能下降。如果体内的铁不足以供给生命活动的需要,就会发生贫血。
为了满足生理需要,成人每天铁的适宜摄入量为15~20mg。动物内脏、肉类、鱼类、蛋类等动物性食物中的铁容易被吸收。一般蔬菜中铁的含量较少,吸收率也低,但我国膳食中一般食用蔬菜量很大,仍为铁的重要来源。我国已经实施在某些酱油中加入铁强化剂的措施,以减少缺铁性贫血问题的发生。
【资料卡片】P70
如何合理补铁?
meiyangyang8602
meiyangyang8602
生活中的富铁食品
补铁补的是几价铁?
第一节
铁及其化合物
第三章 铁 金属材料
赵健
第3课时 铁盐和亚铁盐
meiyangyang8602
meiyangyang8602
meiyangyang8602
meiyangyang8602
生活中的富铁食品
菠菜中铁元素的含量测定
课本P76
检验食品中的铁元素
meiyangyang8602
meiyangyang8602
菠菜中铁元素的含量
定性检测铁元素存在形式
定量测量铁元素质量
计算铁元素含量
定性检测铁元素存在形式
取样
研磨
溶解
过滤
检验
菠菜中的铁元素是Fe2+还是Fe3+ ?如何检验?
meiyangyang8602
请你猜测!
菠菜中的铁元素是Fe2+还是Fe3+ ?
猜想1:只含有Fe2+
猜想2:只含有Fe3+
猜想3:含有Fe2+和Fe3+
综合考虑:应该含有Fe2+和Fe3+
针对猜想,请同学们设计实验加以验证
溶解水配成溶液,你认为样品中铁元素有哪些存在形式
O2
亚铁离子被O2氧化,铁元素可能以铁离子形式存在
Fe2+
Fe3+
01
Fe2+、Fe3+的检验
赵健
meiyangyang8602
meiyangyang8602
meiyangyang8602
meiyangyang8602
学习方法引导
课本P74
铁盐和亚铁盐具有什么样的化学性质?
meiyangyang8602
meiyangyang8602
铁盐和亚铁盐
硫酸亚铁
硫酸亚铁溶液
氯化亚铁
硫酸铁
硫酸铁溶液
氯化铁
氯化铁溶液
Fe3+:棕黄色
Fe2+:浅绿色
meiyangyang8602
请你预测!
从物质类别和价态的角度预测铁盐和亚铁盐具有什么样的化学性质?
Fe3+
物质类型角度
元素价态角度
强氧化性
盐类
Fe2+
物质类型角度
元素价态角度
氧化性
盐类
还原性
FeCl3
碱
Fe(OH)3
FeCl2
碱
Fe(OH)2
meiyangyang8602
meiyangyang8602
Fe2+、Fe3+的检验
Fe(OH)3 Fe(OH)2
实验 操作
实验现象及方程式
有红褐色沉淀
Fe3++3OH-=Fe(OH)3↓
Fe2++2OH-=Fe(OH)2↓
从物质类别的角度
meiyangyang8602
meiyangyang8602
Fe2+、Fe3+的检验
[实验3-2]
在两支试管中分别加入少量的FeCl3溶液和FeCl2溶液,各滴入几滴KSCN溶液。观察并记录现象。
课本P72
meiyangyang8602
meiyangyang8602
Fe2+、Fe3+的检验
[实验3-2]
在两支试管中分别加入少量的FeCl3溶液和FeCl2溶液,各滴入几滴KSCN溶液。观察并记录现象。
课本P72
滴入KSCN溶液 原理
FeCl3溶液
FeCl2溶液 ——
滴入
KSCN溶液
滴入
KSCN溶液
溶液变为红色
溶液无明显变化
Fe3+ + 3SCN- = Fe(SCN)3
(红色)
?
meiyangyang8602
meiyangyang8602
Fe2+、Fe3+的检验
Fe3+ + 3SCN- = Fe(SCN)3 (红色液体)
检验Fe3+最灵敏的方法
2Fe2++Cl2= 2Fe3+ +2Cl-
检验Fe2+的方法
?
滴入
KSCN溶液
FeCl3
滴入
KSCN溶液
FeCl2
滴入
氯水
Fe3+ + 3SCN- = Fe(SCN)3 (红色液体)
meiyangyang8602
meiyangyang8602
Fe2+、Fe3+的检验
从元素化合价的角度
在给定试剂中选择合适试剂,设计实验方案并预测实验现象
试剂:FeCl3溶液、FeCl2溶液、KSCN溶液、新制氯水、H2O2溶液、
酸性KMnO4溶液、KI-淀粉试纸、铁粉、铜片
性质预测 所选试剂 预期实验现象及结论 相关离子方程式
既具有还原性,又具有氧化性
氧化性
+2
+3
FeCl2
FeCl3
请你设计试验方案
meiyangyang8602
Fe2+、Fe3+的检验
设计试验方案
确认Fe2+存在 ,利用Fe2+还原性
2Fe2++Cl2= 2Fe3+ +2Cl-
?
滴入
KSCN溶液
FeCl2
滴入
氯水
Fe3+ + 3SCN- = Fe(SCN)3 (红色液体)
滴入双氧水
①先加KSCN溶液,再加氯水或双氧水
取少量样品溶液于试管,滴加少量酸性高锰酸钾溶液,如果紫红色褪色,则溶液中含有Fe2+ ;如果无明显变化,则溶液中不含Fe2+
5Fe2++MnO4-+8H+= 5Fe3+ +Mn2++4H2O
②加KMnO4(H+)溶液
meiyangyang8602
Fe2+、Fe3+的检验
确认Fe2+存在 ,利用Fe2+还原性
meiyangyang8602
请你解释!
请你解释一下日常生活中出现的现象为什么?
苹果 “生锈”
亚铁盐很容易被氧化为铁盐
赵健
02
Fe2+和Fe3+的转化
meiyangyang8602
meiyangyang8602
meiyangyang8602
请你思考!
你还知道哪些试剂能将亚铁盐变成铁盐?写出反应的离子方程式
Fe2+ Fe3+
氧化剂
(还原剂具有还原性)
氧化剂:O2、 Cl2、H2O2、HNO3、KMnO4 等
meiyangyang8602
请你思考!
如果将铁盐转变成亚铁盐选择什么试剂?写出反应的离子方程式
如何用Fe3+制备Fe2+?
加铁粉 (利用Fe3+的氧化性、Fe的还原性)
现象预测:溶液棕黄变浅绿
Fe3+
Fe2+
还原剂
请你设计试验方案
meiyangyang8602
meiyangyang8602
Fe2+、Fe3+的转化
[实验3-3]
在盛有2 mL FeCl3溶液的试管中加入少量铁粉,振荡试管。充分反应后,滴入几滴KSCN溶液,观察并记录现象。把上层清液倒入另一支试管中,再滴入几滴氯水,又发生了什么变化?
课本P73
meiyangyang8602
FeCl3溶液
加入过量
铁粉
溶液由棕黄色变为浅绿色
无明显现象
溶液呈红色
2Fe3++Fe=3Fe2+
2Fe2++Cl2=2Fe3++2Cl-
meiyangyang8602
Fe2+、Fe3+的转化
滴入
KSCN溶液
取上层清液
滴入氯水
meiyangyang8602
Fe2+、Fe3+的转化
电子工业上常用覆铜板制作印刷电路板,原理是:利用FeCl3溶液做腐蚀液,把覆铜板上不需要的铜腐蚀掉。预先设计好的电路在铜板上用蜡或不透水的物料覆盖,以保护铜线路不被腐蚀。
课本P74
思考与讨论(1)在上述实验中,发生 了什么化学反应, 生成的主要产 物是什么?请运用氧化还原反应的规律进行分析并尝试写出反应的化学方程式。
(2)为使使用后的“腐蚀液” 能得到充分利用,如何处理使用后的“腐蚀液”
meiyangyang8602meiyangyang8602Fe2+、Fe3+的转化
meiyangyang8602
meiyangyang8602
Fe2+、Fe3+的转化
1. 写出反应原理的化学方程式并用双线桥表示电子转移?
2. 为使使用后的“腐蚀液” 能得到充分利用,如何回收得到 Cu 和 FeCl 3
meiyangyang8602
meiyangyang8602
Fe2+、Fe3+的转化
思考与讨论
(1)Fe、FeSO4和Fe2(SO4)3三种物质中,哪种物质可做氧化剂,哪种可做还原剂,哪种既可做氧化剂又可做还原剂?举例写出相应反应的化学方程式,并加以说明。
(2)请你用图示的方法归纳Fe、Fe2+和Fe3+三者之间的相互转化关系,并与同学讨论。
Fe2+ Fe3+
氧化剂
还原剂
还原剂:Zn、Fe、Cu、S2-、I-等
氧化剂:O2、 Cl2、H2O2、HNO3、KMnO4 等
meiyangyang8602
物质类别
氧化物
碱
盐
单质
元素价态
0
+2
+3
+6
Fe(OH)3
Fe3+
Fe(OH)2
Fe2+
FeO
Fe
Fe3O4
Fe2O3
铁及其化合物的价类二维图
meiyangyang8602
Fe、Fe3+与Fe2+的相互转化
Fe
Fe2+
Fe3+
还原剂 如Fe、Zn、Cu、I- 、 S2-、H2S2-等
强氧化剂 如Cl2、H2O2、O2、HNO3、KMnO4等
弱氧化剂 如H+、Cu2+、S、I2 等
强还原剂 如Zn、Al、CO、H2等
强氧化剂 如Cl2、Br2、HNO3、浓硫酸等
强还原剂 如Zn、Al、CO、H2等
meiyangyang8602
meiyangyang8602
菠菜中铁元素的含量
定性检测铁元素存在形式
定量测量铁元素质量
计算铁元素含量
定量测量铁元素质量
溶液中Fe2+、Fe3+的质量不易直接测量,可以将离子转化为沉淀,通过测量沉淀的质量来计算铁元素的质量。
Fe3++3OH-=Fe(OH)3↓
Fe2++2OH-=Fe(OH)2↓
meiyangyang8602
菠菜中铁元素的含量
定量测量铁元素质量
方案1:沉淀法,将铁元素转化为Fe(OH)3,过滤、洗涤、干燥后称量,计算铁元素含量
Fe3+溶液
Fe2+溶液
OH-
OH-
Fe(OH)3
Fe(OH)2
O2
Fe2O3
方案2:将铁元素转化为Fe(OH)3过滤、洗涤、干燥后灼烧,称量Fe2O3质量后计算铁元素含量
Fe3+溶液
Fe2+溶液
OH-
Fe(OH)3
Fe2O3
meiyangyang8602
菠菜中铁元素的含量
定量测量铁元素质量
氧化剂
方案3:用氧化剂将补铁剂中亚铁盐全部氧化为铁盐,加碱沉淀后过滤、洗涤、干燥灼烧后称量氧化铁质量,再进行计算。
铁元素的质量分数
m(Fe2O3)×
56×2
56×2+16×3
m(样品)
meiyangyang8602
菠菜中铁元素的含量
meiyangyang8602
练习
FeCl2
Fe(OH)2
Fe(OH)3
FeCl3
KNO3
AgCl
KCl
FeCl2
KOH
Fe
H2
(2)写出E转变成F的化学方程式:
(3)向G溶液中加入A,写出反应的离子方程式:
KCl
(1)写出B和D的化学式:B ;D
课本77--6
meiyangyang8602
练习
2,某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1mol/L的溶液.在FeCl2溶液中需加入少量铁屑,其目的是___________________。
(2)甲组同学取2mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为________________________________。
(5)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为__________________________;
一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成。
防止Fe2+被氧化
2Fe2++Cl2=2Fe3++2Cl-
H2O2+2Fe2++2H+=2Fe3++2H2O
