3.1.2铁的重要化合物 课件(共29张ppt)化学人教版(2019)必修第一册
文档属性
| 名称 | 3.1.2铁的重要化合物 课件(共29张ppt)化学人教版(2019)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 26.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-29 00:00:00 | ||
图片预览






文档简介
(共29张PPT)
meiyangyang8602
请你说说!
根据生活和学习经验,尽可能说说你所了解的铁的氧化物有哪些?
meiyangyang8602
丹霞地貌的岩层因Fe2O3而呈红色
meiyangyang8602
meiyangyang8602
请你说说!
根据生活和学习经验,尽可能说说你所了解的铁的氧化物有哪些?
第一节
铁及其化合物
第三章 铁 金属材料
赵健
第2课时 铁的重要化合物
meiyangyang8602
meiyangyang8602
meiyangyang8602
meiyangyang8602
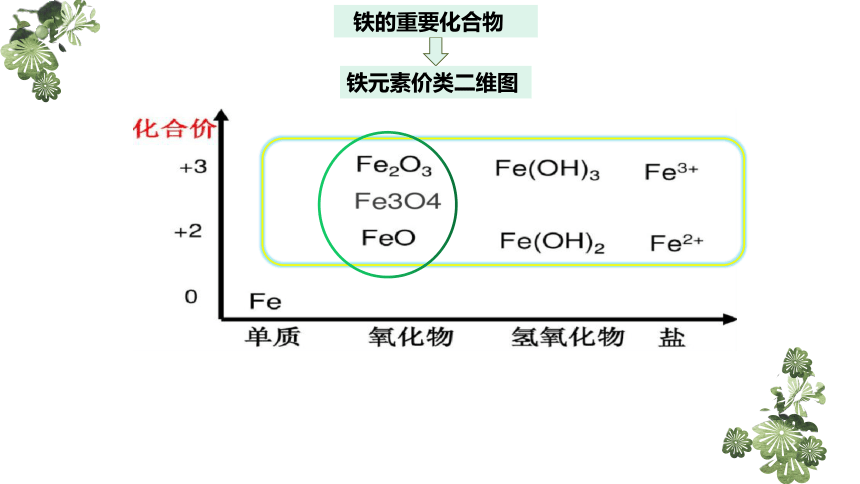
铁的重要化合物
铁元素价类二维图
01
铁的氧化物
赵健
meiyangyang8602
meiyangyang8602
meiyangyang8602
meiyangyang8602
铁的氧化物
Fe2O3
氧化铁是一种红棕色粉末,俗称铁红,常用作油漆、涂料等的红色颜料
FeO
氧化亚铁是一种黑色粉末,不稳定,受热会转化为四氧化三铁
Fe3O4
四氧化三铁是具有磁性的黑色晶体,俗称磁性氧化铁
6FeO + O2 2Fe3O4
铁的氧化物都不溶于水、常温下也不与水反应
铁的氧化物的性质如何?
meiyangyang8602
请你回忆!
你还记得基于物质类别及化合价研究金属氧化物的性质吗?
1. 按性质划分,铁的氧化物属于哪个类别的氧化物?
Fe2O3
碱性氧化物
碱性氧化物
FeO
+3
氧化性
+2
氧化性
还原性
Fe3O4
+3
+2
氧化性
还原性
2. 按元素价态从氧化性和还原性角度分析,铁的氧化物具有什么性?
meiyangyang8602
meiyangyang8602
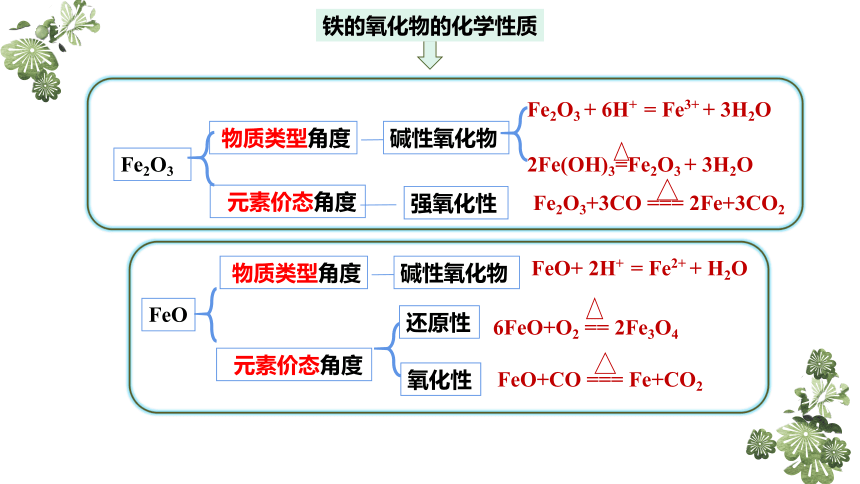
铁的氧化物的化学性质
Fe2O3
物质类型角度
元素价态角度
强氧化性
碱性氧化物
Fe2O3 + 6H+ = Fe3+ + 3H2O
2Fe(OH)3=Fe2O3 + 3H2O
Fe2O3+3CO === 2Fe+3CO2
FeO
物质类型角度
元素价态角度
氧化性
碱性氧化物
FeO+ 2H+ = Fe2+ + H2O
FeO+CO === Fe+CO2
还原性
6FeO+O2 == 2Fe3O4
meiyangyang8602
meiyangyang8602
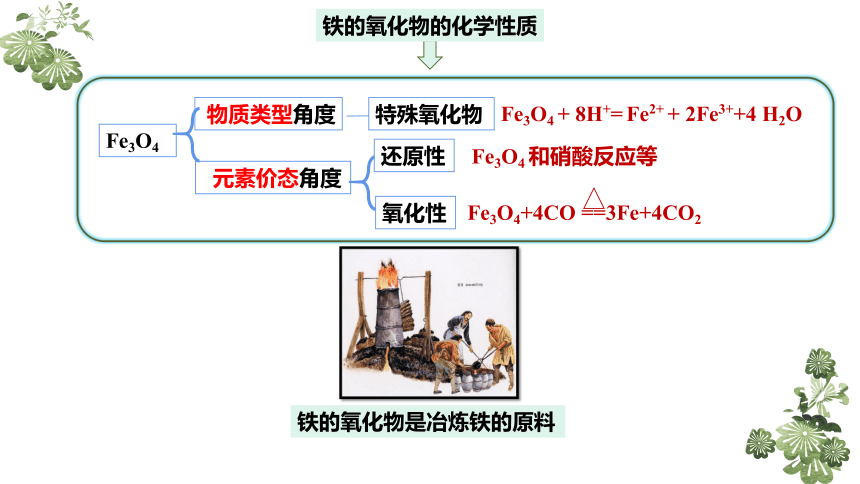
铁的氧化物的化学性质
Fe3O4
物质类型角度
元素价态角度
特殊氧化物
Fe3O4 + 8H+= Fe2+ + 2Fe3++4 H2O
氧化性
还原性
Fe3O4+4CO ==3Fe+4CO2
Fe3O4 和硝酸反应等
铁的氧化物是冶炼铁的原料
meiyangyang8602
练习
1、下列物质常用作红色油漆和涂料的是 ( )
A.FeO B.Fe2O3 C.Fe3O4 D.Al2O3
2、除去铁制品上的铁锈可选用 ( )
A.NaOH溶液 B.稀盐酸 C.CuSO4溶液 D.NaCl溶液
3、下列关于氧化铁和氧化亚铁的叙述中不正确的是( )
A.所含铁元素化合价都是+2价 B.都能与酸反应生成盐和水
C.都能与水反应生成氢氧化物 D.都能被一氧化碳还原为铁
B
B
A
练习
4,下列关于铁的氧化物说法错误的是( )
A.铁的氧化物在通常状况下都是有色固体
B.四氧化三铁是一种复杂的铁的氧化物,它与盐酸反应后的溶液中同时存在Fe2+和Fe3+
C.FeO在空气中加热生成Fe2O3
D.工业上常使用铁的氧化物作原料冶炼铁
C
5,下列变化过程中,不能一步实现的是( )
A.Fe FeCl3
B.Fe Fe3O4
C.Fe Fe3O4
D.Fe FeCl3
D
练习
物质类别(x)
单质
氧化物
碱
盐
元素
价态(y)
0
+2
+3
Fe(OH)3
Fe3+
Fe(OH)2
Fe2+
FeO
Fe
Fe3O4
Fe2O3
?
meiyangyang8602
铁的重要化合物
赵健
02
铁的氢氧化物
meiyangyang8602
meiyangyang8602
meiyangyang8602
meiyangyang8602
铁的氢氧化物
Fe(OH)3 、Fe(OH)2
如何制备Fe(OH)3 、Fe(OH)2
金属的氢氧化物通常有以下几种方案:
1.单质和水反应
2.氧化物和水反应
3.可溶性盐和碱溶液反应
meiyangyang8602
铁的氢氧化物
制备Fe(OH)3 、Fe(OH)2
从物质类别的角度
亚铁盐
铁 盐
FeSO4
FeCl3
碱
Fe(OH)2
碱
Fe(OH)3
请你设计试验方案
meiyangyang8602
meiyangyang8602
制备Fe(OH)3 、Fe(OH)2
课本P71
[实验3-1]
在两支试管中分别加入少量的FeCl3溶液和FeSO4溶液,然后各滴入NaOH溶液。观察并描述发生的现象。
Fe(OH)3 Fe(OH)2
实验 操作
实验 现象
meiyangyang8602
制备Fe(OH)3 、Fe(OH)2
meiyangyang8602
meiyangyang8602
meiyangyang8602
制备Fe(OH)3 、Fe(OH)2
Fe(OH)3 Fe(OH)2
实验 操作
实验现象及方程式
有红褐色沉淀
Fe3++3OH-=Fe(OH)3↓
Fe2++2OH-=Fe(OH)2↓
Fe(OH)2
Fe(OH)3
?
O2
4Fe(OH)2+O2+2H2O=4Fe(OH)3
meiyangyang8602
请你思考!
制取 Fe(OH)2 实验过程中要注意哪些问题?如何改进实验操作?
【分析】 Fe(OH)2会被O2氧化,因此制取Fe(OH)2的关键是防止O2的干扰,需要做到:溶液中不含O2; 生成的Fe(OH)2隔绝O2
1. 使用新配制的FeSO4溶液(可加入少量铁屑)
2. 把NaOH溶液或配制溶液用的蒸馏水加热煮沸除去溶解氧
3. 滴入溶液时将胶头滴管伸入液面以下
4Fe(OH)2+O2+2H2O=4Fe(OH)3
胶头滴管伸入液面以下
现配现用
加热煮沸
meiyangyang8602
meiyangyang8602
制取 Fe(OH)2 实验改进
Fe(OH)2被氧化的原因
反应试剂中溶有氧气
配制试剂的蒸馏水要煮沸
试剂与空气接触
①在Fe(OH)2溶液的液面上加少量苯(或植物油)
②胶头滴管插入液面下加入NaOH溶液
改进方法
改进装置
meiyangyang8602
meiyangyang8602
制取 Fe(OH)2 实验改进
操作:
先滴加 ,
然后 ,
当氢气纯净后,再滴加 。
收集氢气并验纯
NaOH溶液
稀硫酸
改进方案二
meiyangyang8602
制取 Fe(OH)2 实验改进
改进方案三
meiyangyang8602meiyangyang8602制取Fe(OH)2实验改进NaOH溶液操作:先止水夹,在试管Ⅱ出口处,当后,止水夹。产生的氢气使Ⅰ中压强,将生成的硫酸亚铁溶液从长导管入.改进方案三稀H2SO4铁屑打开收集氢气并验纯关闭增大Ⅱ中氢气纯净
meiyangyang8602
meiyangyang8602
制取 Fe(OH)2 实验改进
改进方案四
铁粉
稀硫酸
NaOH溶液
操作:
先 活塞a,在锥形瓶出口处 ,当 后, 活塞a。产生的氢气使A中压强 ,将生成的硫酸亚铁溶液从长导管排入 .
打开
收集氢气并验纯
关闭
增大
B中
氢气纯净
meiyangyang8602
铁的氢氧化物
名 称 Fe(OH)2 Fe(OH)3
物理性质
化学性质
制法
Fe2++2OH- =Fe(OH)2↓
Fe3++3OH- =Fe(OH)3↓
红褐色固体、不溶于水
Fe(OH)3+3H+=Fe3++3H2O
Fe(OH)2+2H+=Fe2++2H2O
4Fe(OH)2+O2+2H2O=4Fe(OH)3
2Fe(OH)3==Fe2O3+3H2O
△
白色固体、不溶于水
meiyangyang8602
meiyangyang8602
练习
1, 下列各图示中,能较长时间观察到Fe(OH)2白色沉淀的是( )
①②④
meiyangyang8602
练习
2,某同学欲利用如图装置制取能较长时间存在的 Fe(OH)2,其中实验所用溶液现配现用且蒸馏水先加热煮沸。下列分析正确的是( )
A.蒸馏烧瓶中反应的离子方程式是
2Fe+6H+===3Fe2++3H2↑
B.实验开始时应先关闭止水夹a、
打开 b,再向烧瓶中加入稀盐酸
C.反应一段时间后可在烧瓶中观察到白色沉淀
D.反应结束后若关闭 b 及分液漏斗活塞,则 Fe(OH)2可较长时间存在
D
meiyangyang8602
练习
3,已知A为常见的金属单质,根据如图所示的关系,下列叙述中正确的是( )
A.A为Fe,B为FeO
B.C→D溶液的颜色变化:浅绿色→棕黄色
C.④的离子方程式:
D.⑤的离子方程式:
B
meiyangyang8602
请你说说!
根据生活和学习经验,尽可能说说你所了解的铁的氧化物有哪些?
meiyangyang8602
丹霞地貌的岩层因Fe2O3而呈红色
meiyangyang8602
meiyangyang8602
请你说说!
根据生活和学习经验,尽可能说说你所了解的铁的氧化物有哪些?
第一节
铁及其化合物
第三章 铁 金属材料
赵健
第2课时 铁的重要化合物
meiyangyang8602
meiyangyang8602
meiyangyang8602
meiyangyang8602
铁的重要化合物
铁元素价类二维图
01
铁的氧化物
赵健
meiyangyang8602
meiyangyang8602
meiyangyang8602
meiyangyang8602
铁的氧化物
Fe2O3
氧化铁是一种红棕色粉末,俗称铁红,常用作油漆、涂料等的红色颜料
FeO
氧化亚铁是一种黑色粉末,不稳定,受热会转化为四氧化三铁
Fe3O4
四氧化三铁是具有磁性的黑色晶体,俗称磁性氧化铁
6FeO + O2 2Fe3O4
铁的氧化物都不溶于水、常温下也不与水反应
铁的氧化物的性质如何?
meiyangyang8602
请你回忆!
你还记得基于物质类别及化合价研究金属氧化物的性质吗?
1. 按性质划分,铁的氧化物属于哪个类别的氧化物?
Fe2O3
碱性氧化物
碱性氧化物
FeO
+3
氧化性
+2
氧化性
还原性
Fe3O4
+3
+2
氧化性
还原性
2. 按元素价态从氧化性和还原性角度分析,铁的氧化物具有什么性?
meiyangyang8602
meiyangyang8602
铁的氧化物的化学性质
Fe2O3
物质类型角度
元素价态角度
强氧化性
碱性氧化物
Fe2O3 + 6H+ = Fe3+ + 3H2O
2Fe(OH)3=Fe2O3 + 3H2O
Fe2O3+3CO === 2Fe+3CO2
FeO
物质类型角度
元素价态角度
氧化性
碱性氧化物
FeO+ 2H+ = Fe2+ + H2O
FeO+CO === Fe+CO2
还原性
6FeO+O2 == 2Fe3O4
meiyangyang8602
meiyangyang8602
铁的氧化物的化学性质
Fe3O4
物质类型角度
元素价态角度
特殊氧化物
Fe3O4 + 8H+= Fe2+ + 2Fe3++4 H2O
氧化性
还原性
Fe3O4+4CO ==3Fe+4CO2
Fe3O4 和硝酸反应等
铁的氧化物是冶炼铁的原料
meiyangyang8602
练习
1、下列物质常用作红色油漆和涂料的是 ( )
A.FeO B.Fe2O3 C.Fe3O4 D.Al2O3
2、除去铁制品上的铁锈可选用 ( )
A.NaOH溶液 B.稀盐酸 C.CuSO4溶液 D.NaCl溶液
3、下列关于氧化铁和氧化亚铁的叙述中不正确的是( )
A.所含铁元素化合价都是+2价 B.都能与酸反应生成盐和水
C.都能与水反应生成氢氧化物 D.都能被一氧化碳还原为铁
B
B
A
练习
4,下列关于铁的氧化物说法错误的是( )
A.铁的氧化物在通常状况下都是有色固体
B.四氧化三铁是一种复杂的铁的氧化物,它与盐酸反应后的溶液中同时存在Fe2+和Fe3+
C.FeO在空气中加热生成Fe2O3
D.工业上常使用铁的氧化物作原料冶炼铁
C
5,下列变化过程中,不能一步实现的是( )
A.Fe FeCl3
B.Fe Fe3O4
C.Fe Fe3O4
D.Fe FeCl3
D
练习
物质类别(x)
单质
氧化物
碱
盐
元素
价态(y)
0
+2
+3
Fe(OH)3
Fe3+
Fe(OH)2
Fe2+
FeO
Fe
Fe3O4
Fe2O3
?
meiyangyang8602
铁的重要化合物
赵健
02
铁的氢氧化物
meiyangyang8602
meiyangyang8602
meiyangyang8602
meiyangyang8602
铁的氢氧化物
Fe(OH)3 、Fe(OH)2
如何制备Fe(OH)3 、Fe(OH)2
金属的氢氧化物通常有以下几种方案:
1.单质和水反应
2.氧化物和水反应
3.可溶性盐和碱溶液反应
meiyangyang8602
铁的氢氧化物
制备Fe(OH)3 、Fe(OH)2
从物质类别的角度
亚铁盐
铁 盐
FeSO4
FeCl3
碱
Fe(OH)2
碱
Fe(OH)3
请你设计试验方案
meiyangyang8602
meiyangyang8602
制备Fe(OH)3 、Fe(OH)2
课本P71
[实验3-1]
在两支试管中分别加入少量的FeCl3溶液和FeSO4溶液,然后各滴入NaOH溶液。观察并描述发生的现象。
Fe(OH)3 Fe(OH)2
实验 操作
实验 现象
meiyangyang8602
制备Fe(OH)3 、Fe(OH)2
meiyangyang8602
meiyangyang8602
meiyangyang8602
制备Fe(OH)3 、Fe(OH)2
Fe(OH)3 Fe(OH)2
实验 操作
实验现象及方程式
有红褐色沉淀
Fe3++3OH-=Fe(OH)3↓
Fe2++2OH-=Fe(OH)2↓
Fe(OH)2
Fe(OH)3
?
O2
4Fe(OH)2+O2+2H2O=4Fe(OH)3
meiyangyang8602
请你思考!
制取 Fe(OH)2 实验过程中要注意哪些问题?如何改进实验操作?
【分析】 Fe(OH)2会被O2氧化,因此制取Fe(OH)2的关键是防止O2的干扰,需要做到:溶液中不含O2; 生成的Fe(OH)2隔绝O2
1. 使用新配制的FeSO4溶液(可加入少量铁屑)
2. 把NaOH溶液或配制溶液用的蒸馏水加热煮沸除去溶解氧
3. 滴入溶液时将胶头滴管伸入液面以下
4Fe(OH)2+O2+2H2O=4Fe(OH)3
胶头滴管伸入液面以下
现配现用
加热煮沸
meiyangyang8602
meiyangyang8602
制取 Fe(OH)2 实验改进
Fe(OH)2被氧化的原因
反应试剂中溶有氧气
配制试剂的蒸馏水要煮沸
试剂与空气接触
①在Fe(OH)2溶液的液面上加少量苯(或植物油)
②胶头滴管插入液面下加入NaOH溶液
改进方法
改进装置
meiyangyang8602
meiyangyang8602
制取 Fe(OH)2 实验改进
操作:
先滴加 ,
然后 ,
当氢气纯净后,再滴加 。
收集氢气并验纯
NaOH溶液
稀硫酸
改进方案二
meiyangyang8602
制取 Fe(OH)2 实验改进
改进方案三
meiyangyang8602meiyangyang8602制取Fe(OH)2实验改进NaOH溶液操作:先止水夹,在试管Ⅱ出口处,当后,止水夹。产生的氢气使Ⅰ中压强,将生成的硫酸亚铁溶液从长导管入.改进方案三稀H2SO4铁屑打开收集氢气并验纯关闭增大Ⅱ中氢气纯净
meiyangyang8602
meiyangyang8602
制取 Fe(OH)2 实验改进
改进方案四
铁粉
稀硫酸
NaOH溶液
操作:
先 活塞a,在锥形瓶出口处 ,当 后, 活塞a。产生的氢气使A中压强 ,将生成的硫酸亚铁溶液从长导管排入 .
打开
收集氢气并验纯
关闭
增大
B中
氢气纯净
meiyangyang8602
铁的氢氧化物
名 称 Fe(OH)2 Fe(OH)3
物理性质
化学性质
制法
Fe2++2OH- =Fe(OH)2↓
Fe3++3OH- =Fe(OH)3↓
红褐色固体、不溶于水
Fe(OH)3+3H+=Fe3++3H2O
Fe(OH)2+2H+=Fe2++2H2O
4Fe(OH)2+O2+2H2O=4Fe(OH)3
2Fe(OH)3==Fe2O3+3H2O
△
白色固体、不溶于水
meiyangyang8602
meiyangyang8602
练习
1, 下列各图示中,能较长时间观察到Fe(OH)2白色沉淀的是( )
①②④
meiyangyang8602
练习
2,某同学欲利用如图装置制取能较长时间存在的 Fe(OH)2,其中实验所用溶液现配现用且蒸馏水先加热煮沸。下列分析正确的是( )
A.蒸馏烧瓶中反应的离子方程式是
2Fe+6H+===3Fe2++3H2↑
B.实验开始时应先关闭止水夹a、
打开 b,再向烧瓶中加入稀盐酸
C.反应一段时间后可在烧瓶中观察到白色沉淀
D.反应结束后若关闭 b 及分液漏斗活塞,则 Fe(OH)2可较长时间存在
D
meiyangyang8602
练习
3,已知A为常见的金属单质,根据如图所示的关系,下列叙述中正确的是( )
A.A为Fe,B为FeO
B.C→D溶液的颜色变化:浅绿色→棕黄色
C.④的离子方程式:
D.⑤的离子方程式:
B
