第四章 第三节 金属的腐蚀与防护 学案 (含答案)—2023-2024学年(人教版2019)高中化学选择性必修1
文档属性
| 名称 | 第四章 第三节 金属的腐蚀与防护 学案 (含答案)—2023-2024学年(人教版2019)高中化学选择性必修1 |

|
|
| 格式 | docx | ||
| 文件大小 | 614.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-30 00:00:00 | ||
图片预览


文档简介
第三节 金属的腐蚀与防护
[核心素养发展目标] 1.通过实验科学探究金属腐蚀的本质及原因,认识金属腐蚀的主要类型,能正确书写析氢腐蚀和吸氧腐蚀的电极反应式。2.认识金属腐蚀产生的危害和影响,树立防止金属腐蚀的意识,熟知金属腐蚀常用的防护方法。
一、金属的腐蚀
1.金属的腐蚀
(1)概念:金属或合金与周围的__________发生____________反应而引起损耗的现象。其实质是金属原子________电子变为阳离子,金属发生________反应。
(2)根据与金属接触的______________不同,金属腐蚀可分为两类:
①化学腐蚀:金属与其表面接触的一些物质(如O2、Cl2、SO2等)直接反应而引起的腐蚀。腐蚀的速率随温度升高而________。
②电化学腐蚀:当________的金属与__________溶液接触时会发生________反应,____________的金属发生氧化反应而被腐蚀。
特别提醒 金属腐蚀过程中,电化学腐蚀和化学腐蚀同时发生,但绝大多数属于电化学腐蚀,且比化学腐蚀的速率大得多。
2.钢铁的电化学腐蚀
类别 项目 析氢腐蚀 吸氧腐蚀
示意图
条件 水膜酸性较强 水膜酸性很弱或呈中性
负极反应式
正极反应式
总反应
联系 通常两种腐蚀同时存在,但后者更普遍
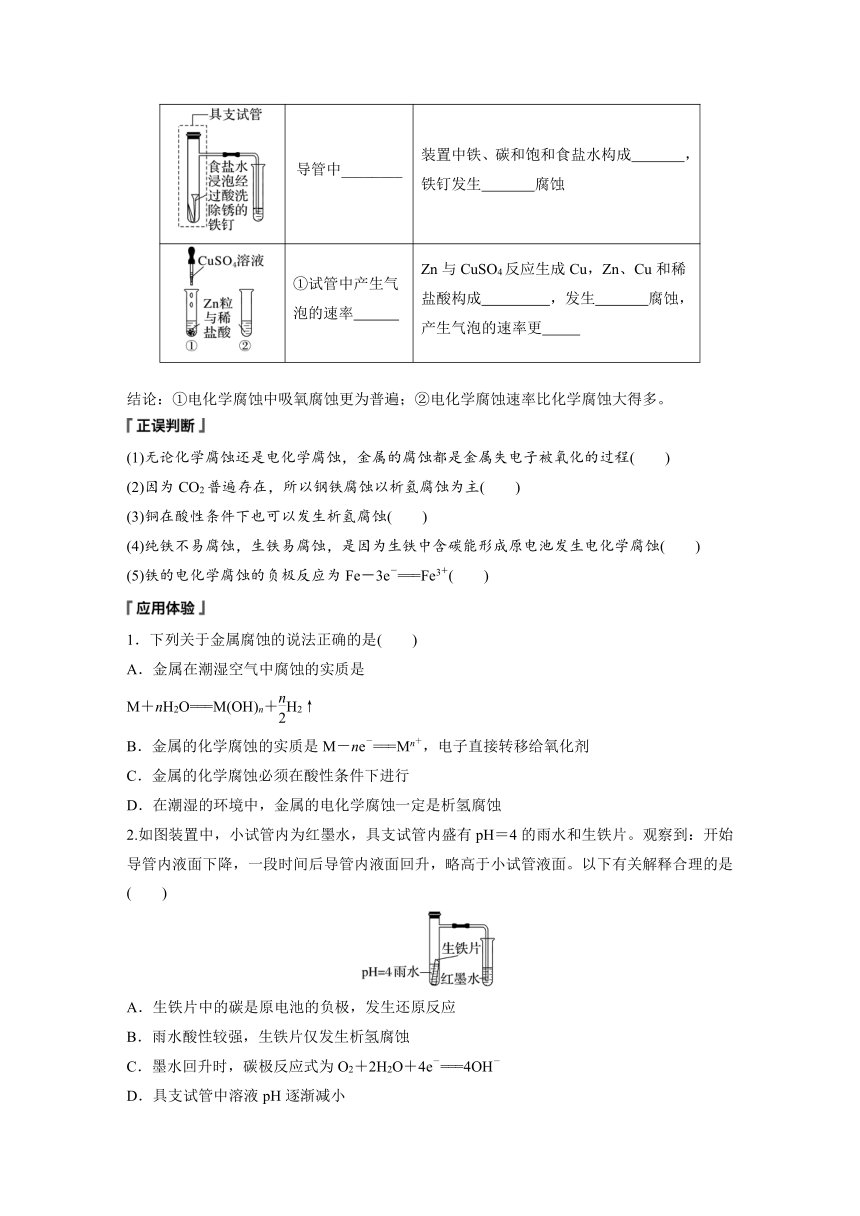
3.实验探究
实验操作 实验现象 实验解释
导管中________ 装置中铁、碳和饱和食盐水构成 ,铁钉发生 腐蚀
①试管中产生气泡的速率 Zn与CuSO4反应生成Cu,Zn、Cu和稀盐酸构成 ,发生 腐蚀,产生气泡的速率更
结论:①电化学腐蚀中吸氧腐蚀更为普遍;②电化学腐蚀速率比化学腐蚀大得多。
(1)无论化学腐蚀还是电化学腐蚀,金属的腐蚀都是金属失电子被氧化的过程( )
(2)因为CO2普遍存在,所以钢铁腐蚀以析氢腐蚀为主( )
(3)铜在酸性条件下也可以发生析氢腐蚀( )
(4)纯铁不易腐蚀,生铁易腐蚀,是因为生铁中含碳能形成原电池发生电化学腐蚀( )
(5)铁的电化学腐蚀的负极反应为Fe-3e-===Fe3+( )
1.下列关于金属腐蚀的说法正确的是( )
A.金属在潮湿空气中腐蚀的实质是
M+nH2O===M(OH)n+H2↑
B.金属的化学腐蚀的实质是M-ne-===Mn+,电子直接转移给氧化剂
C.金属的化学腐蚀必须在酸性条件下进行
D.在潮湿的环境中,金属的电化学腐蚀一定是析氢腐蚀
2.如图装置中,小试管内为红墨水,具支试管内盛有pH=4的雨水和生铁片。观察到:开始导管内液面下降,一段时间后导管内液面回升,略高于小试管液面。以下有关解释合理的是( )
A.生铁片中的碳是原电池的负极,发生还原反应
B.雨水酸性较强,生铁片仅发生析氢腐蚀
C.墨水回升时,碳极反应式为O2+2H2O+4e-===4OH-
D.具支试管中溶液pH逐渐减小
二、金属的防护
1.改变金属材料的组成
如普通钢中加入________等制成不锈钢产品,________不仅具有优异的抗腐蚀性,还具有良好的生物相容性。
2.在金属表面覆盖保护层
(1)在钢铁制品的表面喷涂油漆、矿物性油脂或覆盖搪瓷、塑料等。
(2)用电镀等方法在钢铁表面镀上一层锌、锡、铬、镍等金属。
(3)用化学方法在钢铁部件表面进行发蓝处理(生成一层致密的四氧化三铁薄膜)。
(4)利用阳极氧化处理铝制品的表面,使之形成致密的氧化膜而钝化。
(5)采用离子注入、表面渗镀等方式在金属表面形成稳定的钝化膜。
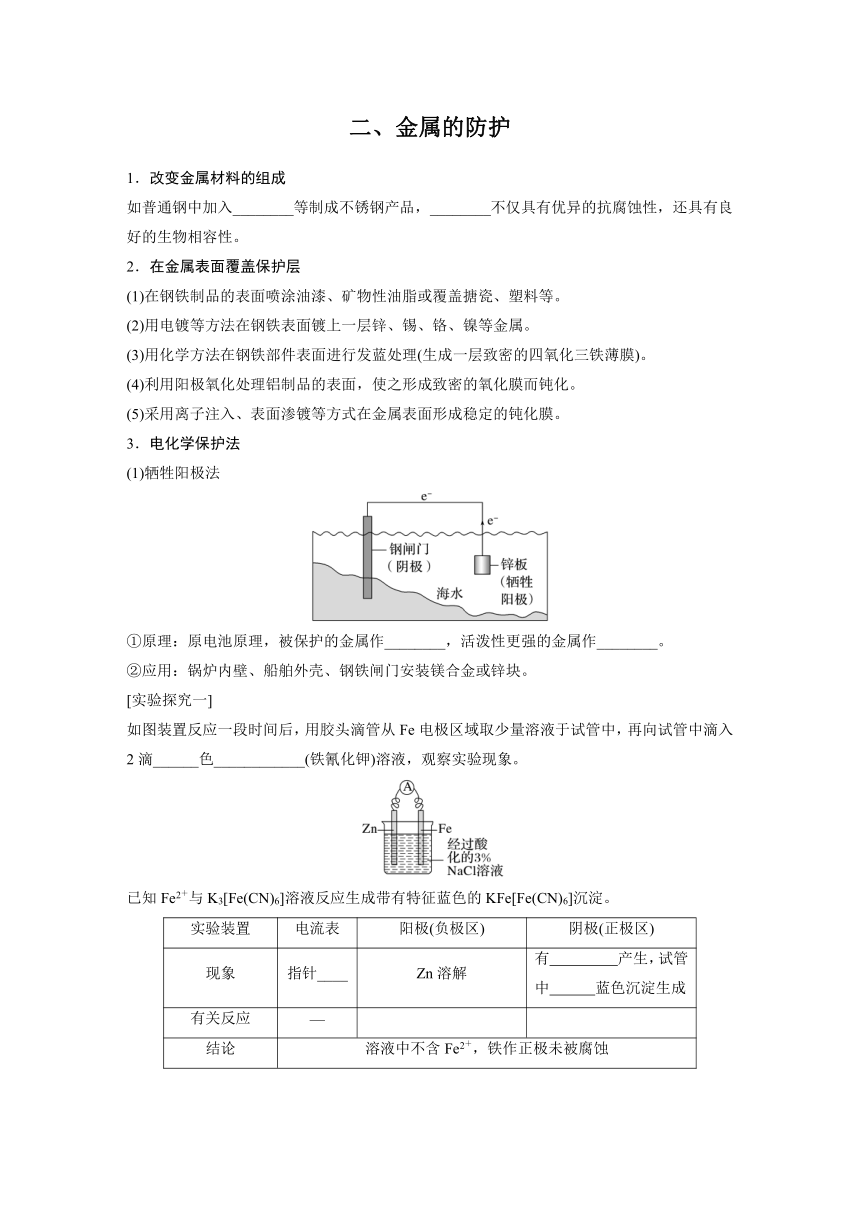
3.电化学保护法
(1)牺牲阳极法
①原理:原电池原理,被保护的金属作________,活泼性更强的金属作________。
②应用:锅炉内壁、船舶外壳、钢铁闸门安装镁合金或锌块。
[实验探究一]
如图装置反应一段时间后,用胶头滴管从Fe电极区域取少量溶液于试管中,再向试管中滴入2滴______色____________(铁氰化钾)溶液,观察实验现象。
已知Fe2+与K3[Fe(CN)6]溶液反应生成带有特征蓝色的KFe[Fe(CN)6]沉淀。
实验装置 电流表 阳极(负极区) 阴极(正极区)
现象 指针____ Zn溶解 有 产生,试管中 蓝色沉淀生成
有关反应 —
结论 溶液中不含Fe2+,铁作正极未被腐蚀
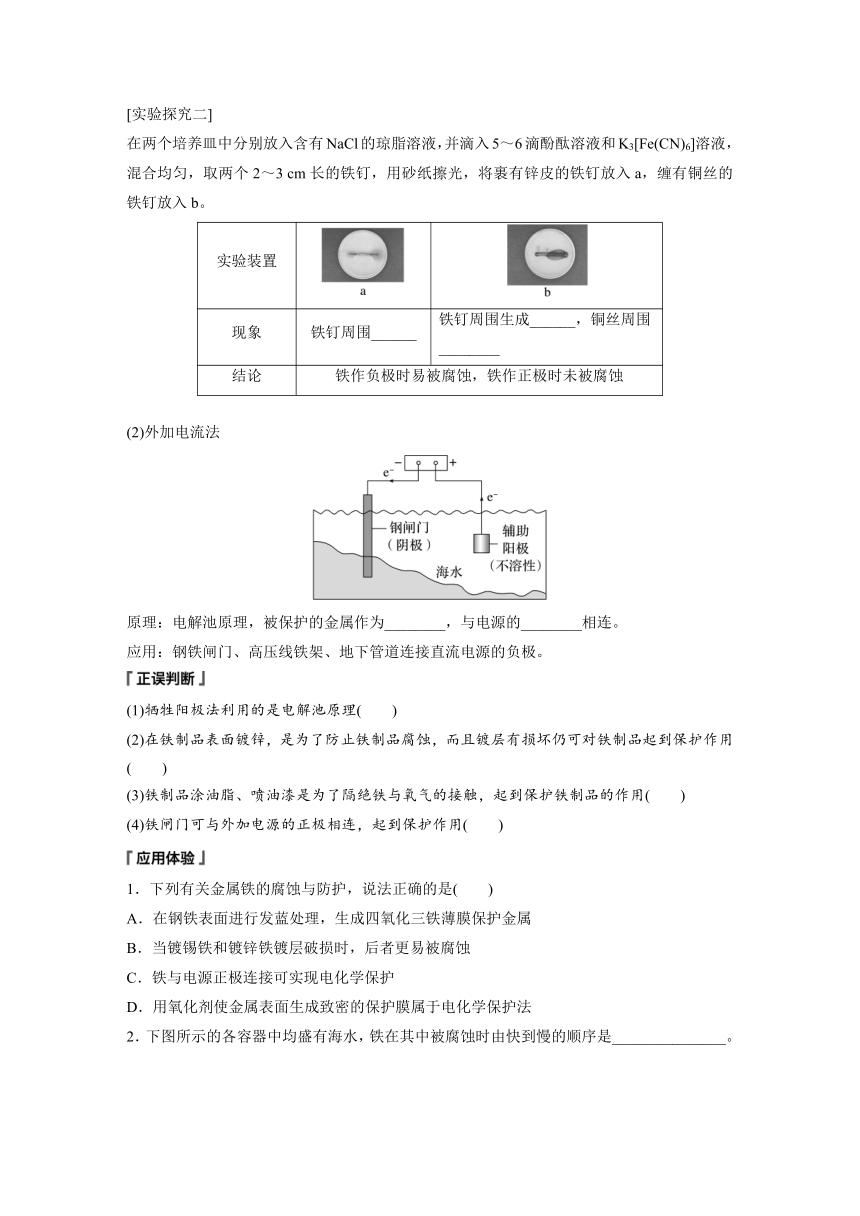
[实验探究二]
在两个培养皿中分别放入含有NaCl的琼脂溶液,并滴入5~6滴酚酞溶液和K3[Fe(CN)6]溶液,混合均匀,取两个2~3 cm长的铁钉,用砂纸擦光,将裹有锌皮的铁钉放入a,缠有铜丝的铁钉放入b。
实验装置
现象 铁钉周围______ 铁钉周围生成______,铜丝周围________
结论 铁作负极时易被腐蚀,铁作正极时未被腐蚀
(2)外加电流法
原理:电解池原理,被保护的金属作为________,与电源的________相连。
应用:钢铁闸门、高压线铁架、地下管道连接直流电源的负极。
(1)牺牲阳极法利用的是电解池原理( )
(2)在铁制品表面镀锌,是为了防止铁制品腐蚀,而且镀层有损坏仍可对铁制品起到保护作用( )
(3)铁制品涂油脂、喷油漆是为了隔绝铁与氧气的接触,起到保护铁制品的作用( )
(4)铁闸门可与外加电源的正极相连,起到保护作用( )
1.下列有关金属铁的腐蚀与防护,说法正确的是( )
A.在钢铁表面进行发蓝处理,生成四氧化三铁薄膜保护金属
B.当镀锡铁和镀锌铁镀层破损时,后者更易被腐蚀
C.铁与电源正极连接可实现电化学保护
D.用氧化剂使金属表面生成致密的保护膜属于电化学保护法
2.下图所示的各容器中均盛有海水,铁在其中被腐蚀时由快到慢的顺序是_______________。
3.某城市为了减少钢管因锈蚀而造成的损失,拟用如图所示方法保护埋在酸性土壤中的钢管。下列有关说法正确的是( )
A.在潮湿的酸性土壤中钢管主要发生吸氧腐蚀
B.在潮湿的酸性土壤中金属棒M中的电子通过导线流向钢管
C.在潮湿的酸性土壤中H+向金属棒M移动,抑制H+与铁的反应
D.钢管与金属棒M也可用导线分别连接直流电源的正、负极
金属腐蚀快慢的判断方法
(1)在同一电解质溶液中,同一种金属腐蚀由快到慢的顺序为电解池的阳极>原电池的负极>化学腐蚀>原电池的正极>电解池的阴极。
(2)同一种金属在不同介质中腐蚀由快到慢的顺序为强电解质溶液>弱电解质溶液>非电解质溶液。
(3)对同一种电解质溶液来说,电解质溶液浓度越大,金属腐蚀越快。
(4)金属活动性差别越大,活泼性强的金属腐蚀越快。
第三节 金属的腐蚀与防护
[核心素养发展目标] 1.通过实验科学探究金属腐蚀的本质及原因,认识金属腐蚀的主要类型,能正确书写析氢腐蚀和吸氧腐蚀的电极反应式。2.认识金属腐蚀产生的危害和影响,树立防止金属腐蚀的意识,熟知金属腐蚀常用的防护方法。
一、金属的腐蚀
1.金属的腐蚀
(1)概念:金属或合金与周围的气体或液体发生氧化还原反应而引起损耗的现象。其实质是金属原子失去电子变为阳离子,金属发生氧化反应。
(2)根据与金属接触的气体或液体不同,金属腐蚀可分为两类:
①化学腐蚀:金属与其表面接触的一些物质(如O2、Cl2、SO2等)直接反应而引起的腐蚀。腐蚀的速率随温度升高而加快。
②电化学腐蚀:当不纯的金属与电解质溶液接触时会发生原电池反应,比较活泼的金属发生氧化反应而被腐蚀。
特别提醒 金属腐蚀过程中,电化学腐蚀和化学腐蚀同时发生,但绝大多数属于电化学腐蚀,且比化学腐蚀的速率大得多。
2.钢铁的电化学腐蚀
类别 项目 析氢腐蚀 吸氧腐蚀
示意图
条件 水膜酸性较强 水膜酸性很弱或呈中性
负极反应式 Fe-2e-===Fe2+
正极反应式 2H++2e-===H2↑ O2+4e-+2H2O===4OH-
总反应 Fe+2H+===Fe2++H2↑ 2Fe+O2+2H2O===2Fe(OH)2
联系 通常两种腐蚀同时存在,但后者更普遍
3.实验探究
实验操作 实验现象 实验解释
导管中液面上升 装置中铁、碳和饱和食盐水构成原电池,铁钉发生吸氧腐蚀
①试管中产生气泡的速率快 Zn与CuSO4反应生成Cu,Zn、Cu和稀盐酸构成原电池,发生电化学腐蚀,产生气泡的速率更快
结论:①电化学腐蚀中吸氧腐蚀更为普遍;②电化学腐蚀速率比化学腐蚀大得多。
(1)无论化学腐蚀还是电化学腐蚀,金属的腐蚀都是金属失电子被氧化的过程( )
(2)因为CO2普遍存在,所以钢铁腐蚀以析氢腐蚀为主( )
(3)铜在酸性条件下也可以发生析氢腐蚀( )
(4)纯铁不易腐蚀,生铁易腐蚀,是因为生铁中含碳能形成原电池发生电化学腐蚀( )
(5)铁的电化学腐蚀的负极反应为Fe-3e-===Fe3+( )
答案 (1)√ (2)× (3)× (4)√ (5)×
1.下列关于金属腐蚀的说法正确的是( )
A.金属在潮湿空气中腐蚀的实质是
M+nH2O===M(OH)n+H2↑
B.金属的化学腐蚀的实质是M-ne-===Mn+,电子直接转移给氧化剂
C.金属的化学腐蚀必须在酸性条件下进行
D.在潮湿的环境中,金属的电化学腐蚀一定是析氢腐蚀
答案 B
2.如图装置中,小试管内为红墨水,具支试管内盛有pH=4的雨水和生铁片。观察到:开始导管内液面下降,一段时间后导管内液面回升,略高于小试管液面。以下有关解释合理的是( )
A.生铁片中的碳是原电池的负极,发生还原反应
B.雨水酸性较强,生铁片仅发生析氢腐蚀
C.墨水回升时,碳极反应式为O2+2H2O+4e-===4OH-
D.具支试管中溶液pH逐渐减小
答案 C
解析 生铁片中的碳是原电池的正极,A错误;雨水酸性较强,开始时铁片发生析氢腐蚀,产生氢气,导管内液面下降,一段时间后铁片发生吸氧腐蚀,吸收氧气,导管内液面回升,B错误;墨水回升时,铁片发生吸氧腐蚀,碳极为正极,电极反应式为O2+2H2O+4e-===4OH-,C正确;铁片无论是发生析氢腐蚀还是吸氧腐蚀,具支试管中溶液pH都增大,D错误。
二、金属的防护
1.改变金属材料的组成
如普通钢中加入镍、铬等制成不锈钢产品,钛合金不仅具有优异的抗腐蚀性,还具有良好的生物相容性。
2.在金属表面覆盖保护层
(1)在钢铁制品的表面喷涂油漆、矿物性油脂或覆盖搪瓷、塑料等。
(2)用电镀等方法在钢铁表面镀上一层锌、锡、铬、镍等金属。
(3)用化学方法在钢铁部件表面进行发蓝处理(生成一层致密的四氧化三铁薄膜)。
(4)利用阳极氧化处理铝制品的表面,使之形成致密的氧化膜而钝化。
(5)采用离子注入、表面渗镀等方式在金属表面形成稳定的钝化膜。
3.电化学保护法
(1)牺牲阳极法
①原理:原电池原理,被保护的金属作正极,活泼性更强的金属作负极。
②应用:锅炉内壁、船舶外壳、钢铁闸门安装镁合金或锌块。
[实验探究一]
如图装置反应一段时间后,用胶头滴管从Fe电极区域取少量溶液于试管中,再向试管中滴入2滴黄色K3[Fe(CN)6](铁氰化钾)溶液,观察实验现象。
已知Fe2+与K3[Fe(CN)6]溶液反应生成带有特征蓝色的KFe[Fe(CN)6]沉淀。
实验装置 电流表 阳极(负极区) 阴极(正极区)
现象 指针偏转 Zn溶解 有气泡产生,试管中无蓝色沉淀生成
有关反应 — Zn-2e-===Zn2+ 2H++2e-===H2↑
结论 溶液中不含Fe2+,铁作正极未被腐蚀
[实验探究二]
在两个培养皿中分别放入含有NaCl的琼脂溶液,并滴入5~6滴酚酞溶液和K3[Fe(CN)6]溶液,混合均匀,取两个2~3 cm长的铁钉,用砂纸擦光,将裹有锌皮的铁钉放入a,缠有铜丝的铁钉放入b。
实验装置
现象 铁钉周围变红 铁钉周围生成蓝色沉淀,铜丝周围变红
结论 铁作负极时易被腐蚀,铁作正极时未被腐蚀
(2)外加电流法
原理:电解池原理,被保护的金属作为阴极,与电源的负极相连。
应用:钢铁闸门、高压线铁架、地下管道连接直流电源的负极。
(1)牺牲阳极法利用的是电解池原理( )
(2)在铁制品表面镀锌,是为了防止铁制品腐蚀,而且镀层有损坏仍可对铁制品起到保护作用( )
(3)铁制品涂油脂、喷油漆是为了隔绝铁与氧气的接触,起到保护铁制品的作用( )
(4)铁闸门可与外加电源的正极相连,起到保护作用( )
答案 (1)× (2)√ (3)√ (4)×
1.下列有关金属铁的腐蚀与防护,说法正确的是( )
A.在钢铁表面进行发蓝处理,生成四氧化三铁薄膜保护金属
B.当镀锡铁和镀锌铁镀层破损时,后者更易被腐蚀
C.铁与电源正极连接可实现电化学保护
D.用氧化剂使金属表面生成致密的保护膜属于电化学保护法
答案 A
解析 A项,四氧化三铁的致密保护膜可防止金属腐蚀,正确;B项,由于金属活动性:Zn>Fe>Sn,所以镀锡铁镀层破损时,Fe作原电池的负极首先被腐蚀,而镀锌铁镀层破损时,由于Fe作正极,被腐蚀的是活动性强的Zn,Fe被保护起来,因此当镀锡铁和镀锌铁镀层破损时,前者更易被腐蚀,错误;C项,铁与电源负极连接可实现电化学保护,错误。
2.下图所示的各容器中均盛有海水,铁在其中被腐蚀时由快到慢的顺序是_______________。
答案 ④>②>①>③
解析 当电解质溶液相同时,同一金属腐蚀的快慢顺序是电解池的阳极>原电池的负极>化学腐蚀>原电池的正极>电解池的阴极。本题中,铁腐蚀由快到慢的顺序为④>②>①>③。
3.某城市为了减少钢管因锈蚀而造成的损失,拟用如图所示方法保护埋在酸性土壤中的钢管。下列有关说法正确的是( )
A.在潮湿的酸性土壤中钢管主要发生吸氧腐蚀
B.在潮湿的酸性土壤中金属棒M中的电子通过导线流向钢管
C.在潮湿的酸性土壤中H+向金属棒M移动,抑制H+与铁的反应
D.钢管与金属棒M也可用导线分别连接直流电源的正、负极
答案 B
解析 在酸性环境下,钢铁主要发生析氢腐蚀,A项错误;金属棒M、钢管在酸性土壤中形成原电池,其中金属棒M作负极,失去电子,失去的电子通过导线流向钢管,钢管作正极被保护,B项正确;在潮湿的酸性土壤中,存在大量H+,H+移动到正极上得电子被还原,即移动到钢管上得电子,抑制H+与铁的反应,C项错误;若钢管与金属棒M用导线分别连接直流电源的正、负极,则钢管作阳极,腐蚀速率加快,D项错误。
金属腐蚀快慢的判断方法
(1)在同一电解质溶液中,同一种金属腐蚀由快到慢的顺序为电解池的阳极>原电池的负极>化学腐蚀>原电池的正极>电解池的阴极。
(2)同一种金属在不同介质中腐蚀由快到慢的顺序为强电解质溶液>弱电解质溶液>非电解质溶液。
(3)对同一种电解质溶液来说,电解质溶液浓度越大,金属腐蚀越快。
(4)金属活动性差别越大,活泼性强的金属腐蚀越快。
[核心素养发展目标] 1.通过实验科学探究金属腐蚀的本质及原因,认识金属腐蚀的主要类型,能正确书写析氢腐蚀和吸氧腐蚀的电极反应式。2.认识金属腐蚀产生的危害和影响,树立防止金属腐蚀的意识,熟知金属腐蚀常用的防护方法。
一、金属的腐蚀
1.金属的腐蚀
(1)概念:金属或合金与周围的__________发生____________反应而引起损耗的现象。其实质是金属原子________电子变为阳离子,金属发生________反应。
(2)根据与金属接触的______________不同,金属腐蚀可分为两类:
①化学腐蚀:金属与其表面接触的一些物质(如O2、Cl2、SO2等)直接反应而引起的腐蚀。腐蚀的速率随温度升高而________。
②电化学腐蚀:当________的金属与__________溶液接触时会发生________反应,____________的金属发生氧化反应而被腐蚀。
特别提醒 金属腐蚀过程中,电化学腐蚀和化学腐蚀同时发生,但绝大多数属于电化学腐蚀,且比化学腐蚀的速率大得多。
2.钢铁的电化学腐蚀
类别 项目 析氢腐蚀 吸氧腐蚀
示意图
条件 水膜酸性较强 水膜酸性很弱或呈中性
负极反应式
正极反应式
总反应
联系 通常两种腐蚀同时存在,但后者更普遍
3.实验探究
实验操作 实验现象 实验解释
导管中________ 装置中铁、碳和饱和食盐水构成 ,铁钉发生 腐蚀
①试管中产生气泡的速率 Zn与CuSO4反应生成Cu,Zn、Cu和稀盐酸构成 ,发生 腐蚀,产生气泡的速率更
结论:①电化学腐蚀中吸氧腐蚀更为普遍;②电化学腐蚀速率比化学腐蚀大得多。
(1)无论化学腐蚀还是电化学腐蚀,金属的腐蚀都是金属失电子被氧化的过程( )
(2)因为CO2普遍存在,所以钢铁腐蚀以析氢腐蚀为主( )
(3)铜在酸性条件下也可以发生析氢腐蚀( )
(4)纯铁不易腐蚀,生铁易腐蚀,是因为生铁中含碳能形成原电池发生电化学腐蚀( )
(5)铁的电化学腐蚀的负极反应为Fe-3e-===Fe3+( )
1.下列关于金属腐蚀的说法正确的是( )
A.金属在潮湿空气中腐蚀的实质是
M+nH2O===M(OH)n+H2↑
B.金属的化学腐蚀的实质是M-ne-===Mn+,电子直接转移给氧化剂
C.金属的化学腐蚀必须在酸性条件下进行
D.在潮湿的环境中,金属的电化学腐蚀一定是析氢腐蚀
2.如图装置中,小试管内为红墨水,具支试管内盛有pH=4的雨水和生铁片。观察到:开始导管内液面下降,一段时间后导管内液面回升,略高于小试管液面。以下有关解释合理的是( )
A.生铁片中的碳是原电池的负极,发生还原反应
B.雨水酸性较强,生铁片仅发生析氢腐蚀
C.墨水回升时,碳极反应式为O2+2H2O+4e-===4OH-
D.具支试管中溶液pH逐渐减小
二、金属的防护
1.改变金属材料的组成
如普通钢中加入________等制成不锈钢产品,________不仅具有优异的抗腐蚀性,还具有良好的生物相容性。
2.在金属表面覆盖保护层
(1)在钢铁制品的表面喷涂油漆、矿物性油脂或覆盖搪瓷、塑料等。
(2)用电镀等方法在钢铁表面镀上一层锌、锡、铬、镍等金属。
(3)用化学方法在钢铁部件表面进行发蓝处理(生成一层致密的四氧化三铁薄膜)。
(4)利用阳极氧化处理铝制品的表面,使之形成致密的氧化膜而钝化。
(5)采用离子注入、表面渗镀等方式在金属表面形成稳定的钝化膜。
3.电化学保护法
(1)牺牲阳极法
①原理:原电池原理,被保护的金属作________,活泼性更强的金属作________。
②应用:锅炉内壁、船舶外壳、钢铁闸门安装镁合金或锌块。
[实验探究一]
如图装置反应一段时间后,用胶头滴管从Fe电极区域取少量溶液于试管中,再向试管中滴入2滴______色____________(铁氰化钾)溶液,观察实验现象。
已知Fe2+与K3[Fe(CN)6]溶液反应生成带有特征蓝色的KFe[Fe(CN)6]沉淀。
实验装置 电流表 阳极(负极区) 阴极(正极区)
现象 指针____ Zn溶解 有 产生,试管中 蓝色沉淀生成
有关反应 —
结论 溶液中不含Fe2+,铁作正极未被腐蚀
[实验探究二]
在两个培养皿中分别放入含有NaCl的琼脂溶液,并滴入5~6滴酚酞溶液和K3[Fe(CN)6]溶液,混合均匀,取两个2~3 cm长的铁钉,用砂纸擦光,将裹有锌皮的铁钉放入a,缠有铜丝的铁钉放入b。
实验装置
现象 铁钉周围______ 铁钉周围生成______,铜丝周围________
结论 铁作负极时易被腐蚀,铁作正极时未被腐蚀
(2)外加电流法
原理:电解池原理,被保护的金属作为________,与电源的________相连。
应用:钢铁闸门、高压线铁架、地下管道连接直流电源的负极。
(1)牺牲阳极法利用的是电解池原理( )
(2)在铁制品表面镀锌,是为了防止铁制品腐蚀,而且镀层有损坏仍可对铁制品起到保护作用( )
(3)铁制品涂油脂、喷油漆是为了隔绝铁与氧气的接触,起到保护铁制品的作用( )
(4)铁闸门可与外加电源的正极相连,起到保护作用( )
1.下列有关金属铁的腐蚀与防护,说法正确的是( )
A.在钢铁表面进行发蓝处理,生成四氧化三铁薄膜保护金属
B.当镀锡铁和镀锌铁镀层破损时,后者更易被腐蚀
C.铁与电源正极连接可实现电化学保护
D.用氧化剂使金属表面生成致密的保护膜属于电化学保护法
2.下图所示的各容器中均盛有海水,铁在其中被腐蚀时由快到慢的顺序是_______________。
3.某城市为了减少钢管因锈蚀而造成的损失,拟用如图所示方法保护埋在酸性土壤中的钢管。下列有关说法正确的是( )
A.在潮湿的酸性土壤中钢管主要发生吸氧腐蚀
B.在潮湿的酸性土壤中金属棒M中的电子通过导线流向钢管
C.在潮湿的酸性土壤中H+向金属棒M移动,抑制H+与铁的反应
D.钢管与金属棒M也可用导线分别连接直流电源的正、负极
金属腐蚀快慢的判断方法
(1)在同一电解质溶液中,同一种金属腐蚀由快到慢的顺序为电解池的阳极>原电池的负极>化学腐蚀>原电池的正极>电解池的阴极。
(2)同一种金属在不同介质中腐蚀由快到慢的顺序为强电解质溶液>弱电解质溶液>非电解质溶液。
(3)对同一种电解质溶液来说,电解质溶液浓度越大,金属腐蚀越快。
(4)金属活动性差别越大,活泼性强的金属腐蚀越快。
第三节 金属的腐蚀与防护
[核心素养发展目标] 1.通过实验科学探究金属腐蚀的本质及原因,认识金属腐蚀的主要类型,能正确书写析氢腐蚀和吸氧腐蚀的电极反应式。2.认识金属腐蚀产生的危害和影响,树立防止金属腐蚀的意识,熟知金属腐蚀常用的防护方法。
一、金属的腐蚀
1.金属的腐蚀
(1)概念:金属或合金与周围的气体或液体发生氧化还原反应而引起损耗的现象。其实质是金属原子失去电子变为阳离子,金属发生氧化反应。
(2)根据与金属接触的气体或液体不同,金属腐蚀可分为两类:
①化学腐蚀:金属与其表面接触的一些物质(如O2、Cl2、SO2等)直接反应而引起的腐蚀。腐蚀的速率随温度升高而加快。
②电化学腐蚀:当不纯的金属与电解质溶液接触时会发生原电池反应,比较活泼的金属发生氧化反应而被腐蚀。
特别提醒 金属腐蚀过程中,电化学腐蚀和化学腐蚀同时发生,但绝大多数属于电化学腐蚀,且比化学腐蚀的速率大得多。
2.钢铁的电化学腐蚀
类别 项目 析氢腐蚀 吸氧腐蚀
示意图
条件 水膜酸性较强 水膜酸性很弱或呈中性
负极反应式 Fe-2e-===Fe2+
正极反应式 2H++2e-===H2↑ O2+4e-+2H2O===4OH-
总反应 Fe+2H+===Fe2++H2↑ 2Fe+O2+2H2O===2Fe(OH)2
联系 通常两种腐蚀同时存在,但后者更普遍
3.实验探究
实验操作 实验现象 实验解释
导管中液面上升 装置中铁、碳和饱和食盐水构成原电池,铁钉发生吸氧腐蚀
①试管中产生气泡的速率快 Zn与CuSO4反应生成Cu,Zn、Cu和稀盐酸构成原电池,发生电化学腐蚀,产生气泡的速率更快
结论:①电化学腐蚀中吸氧腐蚀更为普遍;②电化学腐蚀速率比化学腐蚀大得多。
(1)无论化学腐蚀还是电化学腐蚀,金属的腐蚀都是金属失电子被氧化的过程( )
(2)因为CO2普遍存在,所以钢铁腐蚀以析氢腐蚀为主( )
(3)铜在酸性条件下也可以发生析氢腐蚀( )
(4)纯铁不易腐蚀,生铁易腐蚀,是因为生铁中含碳能形成原电池发生电化学腐蚀( )
(5)铁的电化学腐蚀的负极反应为Fe-3e-===Fe3+( )
答案 (1)√ (2)× (3)× (4)√ (5)×
1.下列关于金属腐蚀的说法正确的是( )
A.金属在潮湿空气中腐蚀的实质是
M+nH2O===M(OH)n+H2↑
B.金属的化学腐蚀的实质是M-ne-===Mn+,电子直接转移给氧化剂
C.金属的化学腐蚀必须在酸性条件下进行
D.在潮湿的环境中,金属的电化学腐蚀一定是析氢腐蚀
答案 B
2.如图装置中,小试管内为红墨水,具支试管内盛有pH=4的雨水和生铁片。观察到:开始导管内液面下降,一段时间后导管内液面回升,略高于小试管液面。以下有关解释合理的是( )
A.生铁片中的碳是原电池的负极,发生还原反应
B.雨水酸性较强,生铁片仅发生析氢腐蚀
C.墨水回升时,碳极反应式为O2+2H2O+4e-===4OH-
D.具支试管中溶液pH逐渐减小
答案 C
解析 生铁片中的碳是原电池的正极,A错误;雨水酸性较强,开始时铁片发生析氢腐蚀,产生氢气,导管内液面下降,一段时间后铁片发生吸氧腐蚀,吸收氧气,导管内液面回升,B错误;墨水回升时,铁片发生吸氧腐蚀,碳极为正极,电极反应式为O2+2H2O+4e-===4OH-,C正确;铁片无论是发生析氢腐蚀还是吸氧腐蚀,具支试管中溶液pH都增大,D错误。
二、金属的防护
1.改变金属材料的组成
如普通钢中加入镍、铬等制成不锈钢产品,钛合金不仅具有优异的抗腐蚀性,还具有良好的生物相容性。
2.在金属表面覆盖保护层
(1)在钢铁制品的表面喷涂油漆、矿物性油脂或覆盖搪瓷、塑料等。
(2)用电镀等方法在钢铁表面镀上一层锌、锡、铬、镍等金属。
(3)用化学方法在钢铁部件表面进行发蓝处理(生成一层致密的四氧化三铁薄膜)。
(4)利用阳极氧化处理铝制品的表面,使之形成致密的氧化膜而钝化。
(5)采用离子注入、表面渗镀等方式在金属表面形成稳定的钝化膜。
3.电化学保护法
(1)牺牲阳极法
①原理:原电池原理,被保护的金属作正极,活泼性更强的金属作负极。
②应用:锅炉内壁、船舶外壳、钢铁闸门安装镁合金或锌块。
[实验探究一]
如图装置反应一段时间后,用胶头滴管从Fe电极区域取少量溶液于试管中,再向试管中滴入2滴黄色K3[Fe(CN)6](铁氰化钾)溶液,观察实验现象。
已知Fe2+与K3[Fe(CN)6]溶液反应生成带有特征蓝色的KFe[Fe(CN)6]沉淀。
实验装置 电流表 阳极(负极区) 阴极(正极区)
现象 指针偏转 Zn溶解 有气泡产生,试管中无蓝色沉淀生成
有关反应 — Zn-2e-===Zn2+ 2H++2e-===H2↑
结论 溶液中不含Fe2+,铁作正极未被腐蚀
[实验探究二]
在两个培养皿中分别放入含有NaCl的琼脂溶液,并滴入5~6滴酚酞溶液和K3[Fe(CN)6]溶液,混合均匀,取两个2~3 cm长的铁钉,用砂纸擦光,将裹有锌皮的铁钉放入a,缠有铜丝的铁钉放入b。
实验装置
现象 铁钉周围变红 铁钉周围生成蓝色沉淀,铜丝周围变红
结论 铁作负极时易被腐蚀,铁作正极时未被腐蚀
(2)外加电流法
原理:电解池原理,被保护的金属作为阴极,与电源的负极相连。
应用:钢铁闸门、高压线铁架、地下管道连接直流电源的负极。
(1)牺牲阳极法利用的是电解池原理( )
(2)在铁制品表面镀锌,是为了防止铁制品腐蚀,而且镀层有损坏仍可对铁制品起到保护作用( )
(3)铁制品涂油脂、喷油漆是为了隔绝铁与氧气的接触,起到保护铁制品的作用( )
(4)铁闸门可与外加电源的正极相连,起到保护作用( )
答案 (1)× (2)√ (3)√ (4)×
1.下列有关金属铁的腐蚀与防护,说法正确的是( )
A.在钢铁表面进行发蓝处理,生成四氧化三铁薄膜保护金属
B.当镀锡铁和镀锌铁镀层破损时,后者更易被腐蚀
C.铁与电源正极连接可实现电化学保护
D.用氧化剂使金属表面生成致密的保护膜属于电化学保护法
答案 A
解析 A项,四氧化三铁的致密保护膜可防止金属腐蚀,正确;B项,由于金属活动性:Zn>Fe>Sn,所以镀锡铁镀层破损时,Fe作原电池的负极首先被腐蚀,而镀锌铁镀层破损时,由于Fe作正极,被腐蚀的是活动性强的Zn,Fe被保护起来,因此当镀锡铁和镀锌铁镀层破损时,前者更易被腐蚀,错误;C项,铁与电源负极连接可实现电化学保护,错误。
2.下图所示的各容器中均盛有海水,铁在其中被腐蚀时由快到慢的顺序是_______________。
答案 ④>②>①>③
解析 当电解质溶液相同时,同一金属腐蚀的快慢顺序是电解池的阳极>原电池的负极>化学腐蚀>原电池的正极>电解池的阴极。本题中,铁腐蚀由快到慢的顺序为④>②>①>③。
3.某城市为了减少钢管因锈蚀而造成的损失,拟用如图所示方法保护埋在酸性土壤中的钢管。下列有关说法正确的是( )
A.在潮湿的酸性土壤中钢管主要发生吸氧腐蚀
B.在潮湿的酸性土壤中金属棒M中的电子通过导线流向钢管
C.在潮湿的酸性土壤中H+向金属棒M移动,抑制H+与铁的反应
D.钢管与金属棒M也可用导线分别连接直流电源的正、负极
答案 B
解析 在酸性环境下,钢铁主要发生析氢腐蚀,A项错误;金属棒M、钢管在酸性土壤中形成原电池,其中金属棒M作负极,失去电子,失去的电子通过导线流向钢管,钢管作正极被保护,B项正确;在潮湿的酸性土壤中,存在大量H+,H+移动到正极上得电子被还原,即移动到钢管上得电子,抑制H+与铁的反应,C项错误;若钢管与金属棒M用导线分别连接直流电源的正、负极,则钢管作阳极,腐蚀速率加快,D项错误。
金属腐蚀快慢的判断方法
(1)在同一电解质溶液中,同一种金属腐蚀由快到慢的顺序为电解池的阳极>原电池的负极>化学腐蚀>原电池的正极>电解池的阴极。
(2)同一种金属在不同介质中腐蚀由快到慢的顺序为强电解质溶液>弱电解质溶液>非电解质溶液。
(3)对同一种电解质溶液来说,电解质溶液浓度越大,金属腐蚀越快。
(4)金属活动性差别越大,活泼性强的金属腐蚀越快。
