【人教版】高中化学 选择性必修一 第二章 第四节 化学反应的调控 课件(共16张PPT)
文档属性
| 名称 | 【人教版】高中化学 选择性必修一 第二章 第四节 化学反应的调控 课件(共16张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 31.7MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-31 00:00:00 | ||
图片预览





文档简介
(共16张PPT)
吴 彦
化学反应的调控
第二章 化学反应速率与化学平衡
第4节 化学反应的调控
一、创设情境,任务驱动
有人想创建一座合成氨工厂,如何根据所学提出建议?
从哪些方面考虑合成氨工厂生产技术的可行性?
原料的获得、反应原理的选择、设备的要求、工业副产品的处理、环境保护......
二、合成氨反应的原料
如何获得合成氨的原料?
方法 评价
分离液态空气法将空气液化、蒸发分离出N2 非常便宜、纯净、规模大、产率高
将空气中的O2与碳作用生成CO2,除去CO2后得到N2 产生温室气体
天然气制氢气 清洁环保、价格较低、技术成熟、可作为燃料
电解法制氢气 成本高
电解饱和盐水 与氯碱工业联合建厂,互惠互利
煤气化获得氢气:煤在高温下和水反应生成CO和H2 成本低、易获得
三、合成氨反应的限度
工业合成氨的反应为:N2(g)+3H2(g) 2NH3(g)。
1. 已知在 298 K 时:ΔH = -92.2 kJ·mol-1 ΔS = -198.2 J·K-1·mol-1
分析在 298 K 时合成氨反应能否正向自发进行。
2. 利用化学平衡移动的知识分析什么条件有利于氨的合成。
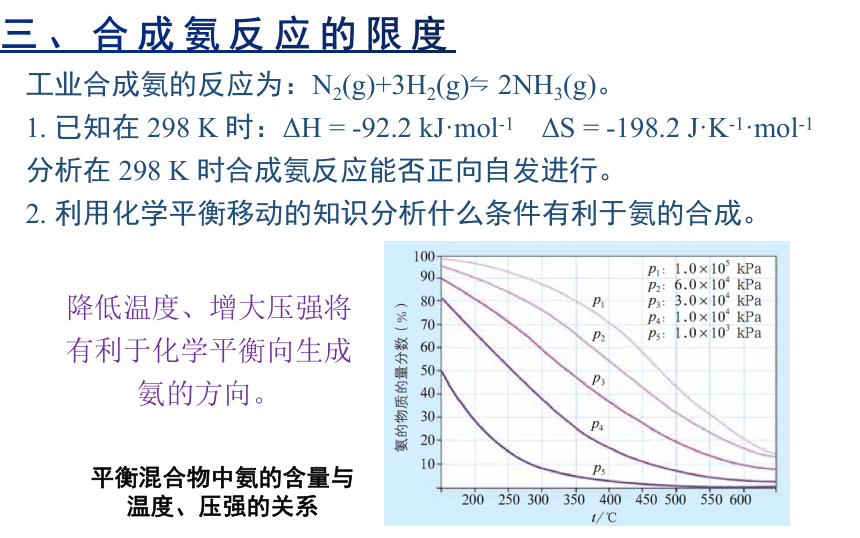
降低温度、增大压强将有利于化学平衡向生成氨的方向。
平衡混合物中氨的含量与温度、压强的关系
四、合成氨反应的速率
1. 可以通过控制哪些反应条件来提高合成氨反应的速率?
2.实验研究表明,在特定条件下,合成氨反应的速率与参与反应的物质浓度的关系式为:
υ = kc (N2)·c1.5(H2)·c-1(NH3)
式中各物质的浓度对反应速率有哪些影响?可以采取哪些措施来提高反应速率?
3. 根据表 2-4-1 所给数据分析催化剂对合成氨反应的速率的影响。
条件 Ea/(kJ ·mol )
无催化剂 335 3.4×1012(700K)
使用铁催化剂 167 四、合成氨反应的速率
研究投料比
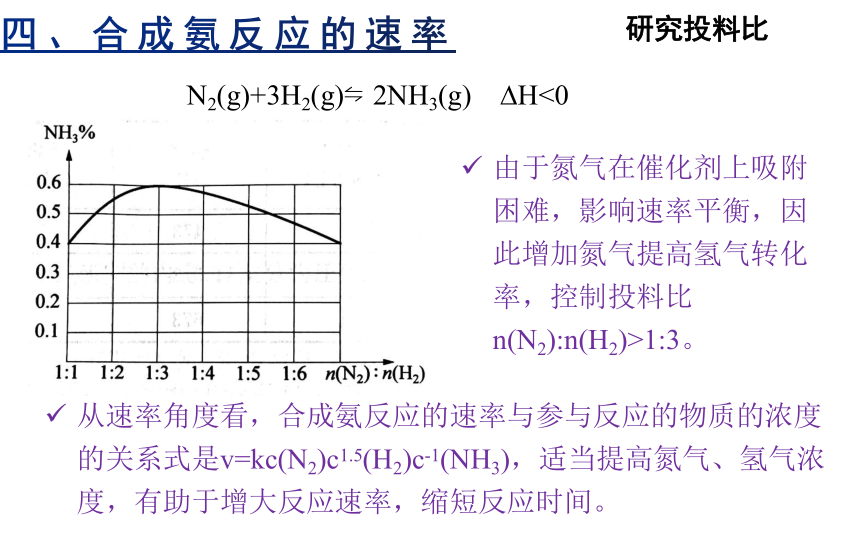
N2(g)+3H2(g) 2NH3(g) H<0
由于氮气在催化剂上吸附困难,影响速率平衡,因此增加氮气提高氢气转化率,控制投料比n(N2):n(H2)>1:3。
从速率角度看,合成氨反应的速率与参与反应的物质的浓度的关系式是v=kc(N2)c1.5(H2)c-1(NH3),适当提高氮气、氢气浓度,有助于增大反应速率,缩短反应时间。
四、合成氨反应的速率
催化剂资料
锇是哈伯使用的催化剂,在700℃时活性最大。
铁是合成氨工业中广泛使用的催化剂,具有价格低廉、稳定性好等特点。制备方法:以磁铁矿和铁为主要原料,添加各类助剂化合物,经电阻炉熔炼后再冷却、破碎筛分成不同颗粒的铁催化剂,最好的熔铁催化剂应该只有一种铁氧化物(单相性原理),任何两种铁氧化物的混杂都会降低催化活性。
钌催化剂:由于在低温、低压等温和的条件下具有较高的活性,被誉为第二代氨合成催化剂,但在合成氨过程中,钌和助剂会使催化炭载体发生甲烷化反应,影响钌催化剂的稳定性,从而对钌催化剂的工业化应用产生不利影响。此外,钌较高的价格也是催化剂工业化应用的一大障碍。
合金型催化剂被认为是最有希望成为继熔铁催化剂和钌催化剂之后的新一代氨合成催化剂。
复合型氢化物材料在催化合成氨研究方面取得重要进展,提出了“双活性中心”催化剂设计理论,开发了过渡金属-氢化锂复合催化剂体系,实现了氨的低温催化合成。
对于合成氨反应中的铁催化剂,O2、CO、CO2和水蒸气等都能使催化剂中毒,但利用纯净的氢、氮混合气体通过中毒的催化剂时,催化剂的活性又能恢复,因此这种中毒是暂时性中毒。工业上为了防止催化剂中毒,要把反应物原料加以净化,以除去毒物,这样就要增加设备,提高成本。因此,研制具有较强抗毒能量的新型催化剂,是未来的发展方向。
合成氨常用铁触媒(以铁为主,混合催化剂),铁触媒在500℃时活性最大,结合温度组和压强组讨论的结果,确定合成氨温度在400-500℃。
四、合成氨反应的速率
工业合成氨的催化历程
工业上,氮气与氢气合成氨的反应是在催化剂表面上进行的。这是一个复杂的过程,一般要经历反应物扩散至催化剂表面、吸附在催化剂表面、发生表面反应、产物从催化剂表面脱附、产物扩散离开反应区等五个步骤。
四、合成氨反应的速率
1. 第一步(氮的吸附分解)所需活化能最高,是控制总反应速率的关键步骤。为保证氮气占有一定份额的催化剂活性中心并提高吸附速率,应适当提高氮气的比例,即不是达到最大平衡转化率要求的 n(N2)∶n(H2) = 1∶3,而是 n(N2)∶n(H2) = 1∶2.8。
2. 为了提高氨的脱附速率,以空出活性中心供继续合成氨使用,必须降低反应后混合气体中氨的比例,适时地将氨从反应后的混合气体中分离出来。
五、合成氨生产的适宜条件
1. 根据合成氨反应的特点,应分别采取什么措施提高该反应的平衡转化率和反应速率?将有关建议填入下表中。
提高反应的平衡转化率 提高反应的速率 反应特点 措施 反应特点 措施
放热 活化能高
正向反应分子数减小 低温时反应速率低
反应可逆 原料气浓度增大能提高反应速率
氨气浓度增大能降低反应速率
五、合成氨生产的适宜条件
温度 25℃ 350℃ 400℃ 450℃ 600℃ 700℃
K 4×106 1.847 0.507 0.152 0.009 2.6×10-3
温度/℃ NH3含量——压强/Mpa 0.1 10 20 30 60 100
200 15.3 81.5 86.4 89.9 95.4 98.8
300 2.2 52.0 64.2 71.0 84.2 92.6
400 0.4 25.1 38.2 47.0 65.2 79.8
500 0.1 10.6 19.1 26.4 42.2 57.5
600 0.05 4.5 9.1 13.8 23.1 31.4
c(N2)/ (mol/L) 温度/℃ 活化能/(kJ/mol) 平衡时各组分浓度/(mol/L) 到达平衡的时间/s
N2 H2 NH3 1 200 50 0.160 0.480 1.680 29040
1 300 50 0.195 0.585 1.610 5783
1 400 50 0.224 0.672 1.552 2408
<
<
五、合成氨生产的适宜条件
压强资料
压强大有利于提高转化率和速率,但是对设备和能耗有要求。有研究表明,压强超过200Mpa时,不使用催化剂,氨便可以顺利合成。但缺点是太大的压强需要的动力就大,对设备材料的要求也会增高。根据合成氨双层塔的构造和抗压抗温原理,高压条件下小分子H2与设备钢中碳反应,使钢瓶破裂,因此工业生产中压强不能超过30Mpa。过去追求产率,合成氨压力由低压向高压发展,现在从降低能耗的角度又向低压发展,目前已经成功运用15Mpa,10Mpa正在试验中,这样既可以做到电耗最低,又能确保合成的效率。
根据反应器可使用钢材的质量及综合指标来选择压强,大致分为低压(1×107Pa)、中压(2×107~3×107Pa)和高(8.5×107~1×108Pa)三种类型;通常采用氮气与氢气物质的量之比为 1∶2.8 的投料比。在中压工艺条件下,合成氨厂出口气中的氨含量一般为 13% ~ 14%。
五、合成氨生产的适宜条件
合成氨的条件:
压强:10-30MPa;催化剂:铁;温度:400-500℃
N2:H2物质的量之比为1:2.8;液氨加压或降温及时分离
合成氨工业生产流程示意图
五、合成氨生产的适宜条件
未来的合成氨工厂是什么形式的?
新型催化剂(生物固氮催化剂);创建一些副产品工厂——CO2
常温常压合成氨气;进行根瘤菌的提取。
合成氨工业生产流程示意图
课堂小结
化学反应的调控
合成氨
N2(g)+3H2(g) 2NH3(g) H<0
反应原料
生产条件
绿色化学
副产品工厂三废处理
N2:分离液态空气
H2:碳和水
甲烷和水
氯碱工业
压强:10-30MPa
温度:400-400℃
催化剂:Fe
投料比(n):1:2.8
今日作业
1.梳理课堂笔记。
吴 彦
化学反应的调控
第二章 化学反应速率与化学平衡
第4节 化学反应的调控
一、创设情境,任务驱动
有人想创建一座合成氨工厂,如何根据所学提出建议?
从哪些方面考虑合成氨工厂生产技术的可行性?
原料的获得、反应原理的选择、设备的要求、工业副产品的处理、环境保护......
二、合成氨反应的原料
如何获得合成氨的原料?
方法 评价
分离液态空气法将空气液化、蒸发分离出N2 非常便宜、纯净、规模大、产率高
将空气中的O2与碳作用生成CO2,除去CO2后得到N2 产生温室气体
天然气制氢气 清洁环保、价格较低、技术成熟、可作为燃料
电解法制氢气 成本高
电解饱和盐水 与氯碱工业联合建厂,互惠互利
煤气化获得氢气:煤在高温下和水反应生成CO和H2 成本低、易获得
三、合成氨反应的限度
工业合成氨的反应为:N2(g)+3H2(g) 2NH3(g)。
1. 已知在 298 K 时:ΔH = -92.2 kJ·mol-1 ΔS = -198.2 J·K-1·mol-1
分析在 298 K 时合成氨反应能否正向自发进行。
2. 利用化学平衡移动的知识分析什么条件有利于氨的合成。
降低温度、增大压强将有利于化学平衡向生成氨的方向。
平衡混合物中氨的含量与温度、压强的关系
四、合成氨反应的速率
1. 可以通过控制哪些反应条件来提高合成氨反应的速率?
2.实验研究表明,在特定条件下,合成氨反应的速率与参与反应的物质浓度的关系式为:
υ = kc (N2)·c1.5(H2)·c-1(NH3)
式中各物质的浓度对反应速率有哪些影响?可以采取哪些措施来提高反应速率?
3. 根据表 2-4-1 所给数据分析催化剂对合成氨反应的速率的影响。
条件 Ea/(kJ ·mol )
无催化剂 335 3.4×1012(700K)
使用铁催化剂 167 四、合成氨反应的速率
研究投料比
N2(g)+3H2(g) 2NH3(g) H<0
由于氮气在催化剂上吸附困难,影响速率平衡,因此增加氮气提高氢气转化率,控制投料比n(N2):n(H2)>1:3。
从速率角度看,合成氨反应的速率与参与反应的物质的浓度的关系式是v=kc(N2)c1.5(H2)c-1(NH3),适当提高氮气、氢气浓度,有助于增大反应速率,缩短反应时间。
四、合成氨反应的速率
催化剂资料
锇是哈伯使用的催化剂,在700℃时活性最大。
铁是合成氨工业中广泛使用的催化剂,具有价格低廉、稳定性好等特点。制备方法:以磁铁矿和铁为主要原料,添加各类助剂化合物,经电阻炉熔炼后再冷却、破碎筛分成不同颗粒的铁催化剂,最好的熔铁催化剂应该只有一种铁氧化物(单相性原理),任何两种铁氧化物的混杂都会降低催化活性。
钌催化剂:由于在低温、低压等温和的条件下具有较高的活性,被誉为第二代氨合成催化剂,但在合成氨过程中,钌和助剂会使催化炭载体发生甲烷化反应,影响钌催化剂的稳定性,从而对钌催化剂的工业化应用产生不利影响。此外,钌较高的价格也是催化剂工业化应用的一大障碍。
合金型催化剂被认为是最有希望成为继熔铁催化剂和钌催化剂之后的新一代氨合成催化剂。
复合型氢化物材料在催化合成氨研究方面取得重要进展,提出了“双活性中心”催化剂设计理论,开发了过渡金属-氢化锂复合催化剂体系,实现了氨的低温催化合成。
对于合成氨反应中的铁催化剂,O2、CO、CO2和水蒸气等都能使催化剂中毒,但利用纯净的氢、氮混合气体通过中毒的催化剂时,催化剂的活性又能恢复,因此这种中毒是暂时性中毒。工业上为了防止催化剂中毒,要把反应物原料加以净化,以除去毒物,这样就要增加设备,提高成本。因此,研制具有较强抗毒能量的新型催化剂,是未来的发展方向。
合成氨常用铁触媒(以铁为主,混合催化剂),铁触媒在500℃时活性最大,结合温度组和压强组讨论的结果,确定合成氨温度在400-500℃。
四、合成氨反应的速率
工业合成氨的催化历程
工业上,氮气与氢气合成氨的反应是在催化剂表面上进行的。这是一个复杂的过程,一般要经历反应物扩散至催化剂表面、吸附在催化剂表面、发生表面反应、产物从催化剂表面脱附、产物扩散离开反应区等五个步骤。
四、合成氨反应的速率
1. 第一步(氮的吸附分解)所需活化能最高,是控制总反应速率的关键步骤。为保证氮气占有一定份额的催化剂活性中心并提高吸附速率,应适当提高氮气的比例,即不是达到最大平衡转化率要求的 n(N2)∶n(H2) = 1∶3,而是 n(N2)∶n(H2) = 1∶2.8。
2. 为了提高氨的脱附速率,以空出活性中心供继续合成氨使用,必须降低反应后混合气体中氨的比例,适时地将氨从反应后的混合气体中分离出来。
五、合成氨生产的适宜条件
1. 根据合成氨反应的特点,应分别采取什么措施提高该反应的平衡转化率和反应速率?将有关建议填入下表中。
提高反应的平衡转化率 提高反应的速率 反应特点 措施 反应特点 措施
放热 活化能高
正向反应分子数减小 低温时反应速率低
反应可逆 原料气浓度增大能提高反应速率
氨气浓度增大能降低反应速率
五、合成氨生产的适宜条件
温度 25℃ 350℃ 400℃ 450℃ 600℃ 700℃
K 4×106 1.847 0.507 0.152 0.009 2.6×10-3
温度/℃ NH3含量——压强/Mpa 0.1 10 20 30 60 100
200 15.3 81.5 86.4 89.9 95.4 98.8
300 2.2 52.0 64.2 71.0 84.2 92.6
400 0.4 25.1 38.2 47.0 65.2 79.8
500 0.1 10.6 19.1 26.4 42.2 57.5
600 0.05 4.5 9.1 13.8 23.1 31.4
c(N2)/ (mol/L) 温度/℃ 活化能/(kJ/mol) 平衡时各组分浓度/(mol/L) 到达平衡的时间/s
N2 H2 NH3 1 200 50 0.160 0.480 1.680 29040
1 300 50 0.195 0.585 1.610 5783
1 400 50 0.224 0.672 1.552 2408
<
<
五、合成氨生产的适宜条件
压强资料
压强大有利于提高转化率和速率,但是对设备和能耗有要求。有研究表明,压强超过200Mpa时,不使用催化剂,氨便可以顺利合成。但缺点是太大的压强需要的动力就大,对设备材料的要求也会增高。根据合成氨双层塔的构造和抗压抗温原理,高压条件下小分子H2与设备钢中碳反应,使钢瓶破裂,因此工业生产中压强不能超过30Mpa。过去追求产率,合成氨压力由低压向高压发展,现在从降低能耗的角度又向低压发展,目前已经成功运用15Mpa,10Mpa正在试验中,这样既可以做到电耗最低,又能确保合成的效率。
根据反应器可使用钢材的质量及综合指标来选择压强,大致分为低压(1×107Pa)、中压(2×107~3×107Pa)和高(8.5×107~1×108Pa)三种类型;通常采用氮气与氢气物质的量之比为 1∶2.8 的投料比。在中压工艺条件下,合成氨厂出口气中的氨含量一般为 13% ~ 14%。
五、合成氨生产的适宜条件
合成氨的条件:
压强:10-30MPa;催化剂:铁;温度:400-500℃
N2:H2物质的量之比为1:2.8;液氨加压或降温及时分离
合成氨工业生产流程示意图
五、合成氨生产的适宜条件
未来的合成氨工厂是什么形式的?
新型催化剂(生物固氮催化剂);创建一些副产品工厂——CO2
常温常压合成氨气;进行根瘤菌的提取。
合成氨工业生产流程示意图
课堂小结
化学反应的调控
合成氨
N2(g)+3H2(g) 2NH3(g) H<0
反应原料
生产条件
绿色化学
副产品工厂三废处理
N2:分离液态空气
H2:碳和水
甲烷和水
氯碱工业
压强:10-30MPa
温度:400-400℃
催化剂:Fe
投料比(n):1:2.8
今日作业
1.梳理课堂笔记。
