化学苏教版(2019)必修第一册 4.3防治二氧化硫对环境的污染课件(共18张PPT)
文档属性
| 名称 | 化学苏教版(2019)必修第一册 4.3防治二氧化硫对环境的污染课件(共18张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 2.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-08-31 00:00:00 | ||
图片预览






文档简介
(共18张PPT)
专题四 硫及环境保护
第三单元 防止二氧化硫对环境的污染
森林受到酸雨破坏
二氧化硫对环境造成的污染
如何利用SO2的性质和含硫物质的转化规律,防治SO2对环境的污染?
自然界中的硫循环
思考:学生阅读课本内容,了解硫元素在自然界的循环过程,回答下列问题:
1、SO2的来源有哪些?
2、SO2的主要危害是什么
化石矿物的风化分解、燃烧、火山爆发等
造成土壤酸化、酸雨等
(3)硫酸、磷酸、纸浆等工业排放的废气
(2)含硫矿石的冶炼
(1)主要来自化石燃料的燃烧
SO2主要来源
“空中死神”——酸雨
思考:
1、酸雨的危害有哪些?
2、酸雨是怎么形成的?
3、如何防治酸雨?
1、影响水生物的繁殖;
2、使土壤肥力下降,逐渐酸化;
3、加快了桥梁、雕塑等建筑物的腐蚀速度。
酸雨的危害
结论:
SO2中的 S为+4价,处于中间价态, 所以可能既有氧化性,也可能有还原性。
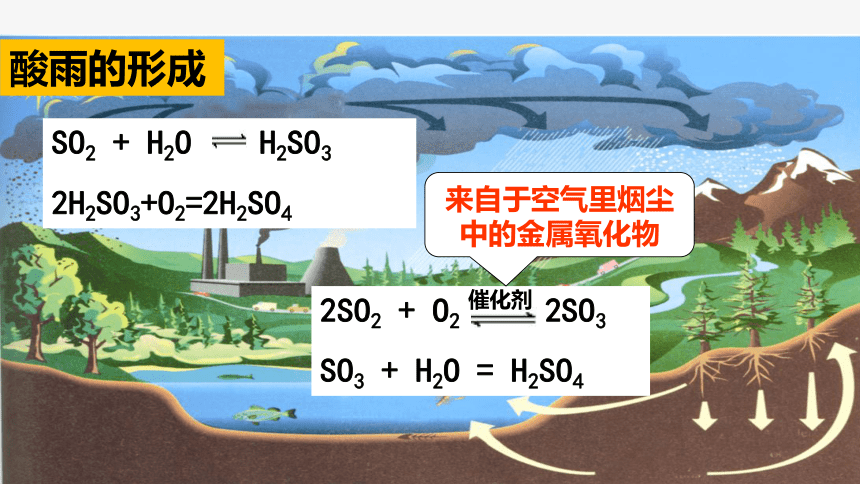
SO2 + H2O H2SO3
2H2SO3+O2=2H2SO4
SO2 + H2O H2SO3
2H2SO3+O2=2H2SO4
酸雨的形成
2SO2 + O2 2SO3
SO3 + H2O = H2SO4
催化剂
来自于空气里烟尘中的金属氧化物
引起酸雨的物质是:
减少SO2 的排放
(1)开发新能源,减少化石燃料的燃烧
(2)对燃煤烟气进行脱硫处理
酸雨的防治
SOx(SO2和SO3)
酸雨的防治:
减少SO2 排放的方法:
酸雨的防治
思考:实验室用哪种碱液吸收尾气SO2?
工业上选用哪种碱液吸收尾气SO2?
NaOH
Ca(OH)2 成本低
工业上需同时考虑:环保、成本、工艺流程简单等因素
2NaOH + SO2 = H2O + Na2SO3
原理:
Ca(OH)2 + SO2 = H2O + CaSO3
氨水法
石灰石-石膏法
SO2 + CaCO3 = CaSO3+CO2↑
△
2CaSO3 +O2 = 2 CaSO4
△
SO2+2NH3+H2O = (NH4)2SO3
2(NH4)2SO3+O2 = (NH4)2SO4
上述处理法既可以消除污染,同时可以得到石膏(CaSO4·2H2O)和硫酸铵(化肥)。
燃煤烟气脱硫
氨脱硫法
拓展视野
氨水法
空气质量评价
思考:阅读课本,分析空气质量指数的标准是什么?
空气质量指数与空气质量的关系?
空气质量指数(AQI):是根据空气中的细颗粒物(PM2.5)、可吸入颗粒物(PM10)、SO2、NO2、O3、CO的浓度计算出来的数值。
空气质量指数越小,空气质量越好。
颗粒物直径为2.5μm
1μm=1x10-6m
μm:微米
氨水法
跨学科链接
思考:每天都更新的和发布的空气质量指数是如何确定的?空气质量等级如何确定?
首先测定细颗粒物(PM2.5)、可吸入颗粒物(PM10)、SO2、NO2、O3、CO的浓度,再换算成对应的质量指数,其中指数最大的污染物会被确定为首要污染物,其指数即为该地区的空气质量指数。
空气质量指数越大,空气质量等级污染程度越高。
氨水法
跨学科链接
思考:每天都更新的和发布的空气质量指数是如何确定的?空气质量等级如何确定?
首先测定细颗粒物(PM2.5)、可吸入颗粒物(PM10)、SO2、NO2、O3、CO的浓度,再换算成对应的质量指数,其中指数最大的污染物会被确定为首要污染物,其指数即为该地区的空气质量指数。
空气质量指数越大,空气质量等级污染程度越高。
雾霾
雾霾:大量极细微的颗粒物均匀地悬浮在空中,这些颗粒物吸附空气中的水蒸气形成雾滴,是空气水平能见度小于10km,这种空气混浊的现象叫作雾霾。
思考:近年来,我国许多地区受到了雾霾天气的干扰。那么,什么是雾霾?
颗粒物分类依据:
颗粒物分类:细颗粒物(PM2.5直径<2.5μm)
可吸入颗粒物(PM10直径<10μm)
颗粒物直径大小
雾霾的形成
思考:分析图4-13、图4-14,了解、分析含硫物质的排放,与雾霾的形成有什么关系?
常见细颗粒物(PM2.5):燃烧颗粒、有机物、金属颗粒等,均可导致雾霾天气的形成,被人体吸收后,对人体健康造成极大危害。
SO2形成的硫酸盐物质(如CaSO4)在空气中可形成细微颗粒物,导致雾霾天气。
从源头上解决大气污染问题,依靠绿色发展, 实现零排放,保护环境,刻不容缓。
保护环境,刻不容缓
专题四 硫及环境保护
第三单元 防止二氧化硫对环境的污染
森林受到酸雨破坏
二氧化硫对环境造成的污染
如何利用SO2的性质和含硫物质的转化规律,防治SO2对环境的污染?
自然界中的硫循环
思考:学生阅读课本内容,了解硫元素在自然界的循环过程,回答下列问题:
1、SO2的来源有哪些?
2、SO2的主要危害是什么
化石矿物的风化分解、燃烧、火山爆发等
造成土壤酸化、酸雨等
(3)硫酸、磷酸、纸浆等工业排放的废气
(2)含硫矿石的冶炼
(1)主要来自化石燃料的燃烧
SO2主要来源
“空中死神”——酸雨
思考:
1、酸雨的危害有哪些?
2、酸雨是怎么形成的?
3、如何防治酸雨?
1、影响水生物的繁殖;
2、使土壤肥力下降,逐渐酸化;
3、加快了桥梁、雕塑等建筑物的腐蚀速度。
酸雨的危害
结论:
SO2中的 S为+4价,处于中间价态, 所以可能既有氧化性,也可能有还原性。
SO2 + H2O H2SO3
2H2SO3+O2=2H2SO4
SO2 + H2O H2SO3
2H2SO3+O2=2H2SO4
酸雨的形成
2SO2 + O2 2SO3
SO3 + H2O = H2SO4
催化剂
来自于空气里烟尘中的金属氧化物
引起酸雨的物质是:
减少SO2 的排放
(1)开发新能源,减少化石燃料的燃烧
(2)对燃煤烟气进行脱硫处理
酸雨的防治
SOx(SO2和SO3)
酸雨的防治:
减少SO2 排放的方法:
酸雨的防治
思考:实验室用哪种碱液吸收尾气SO2?
工业上选用哪种碱液吸收尾气SO2?
NaOH
Ca(OH)2 成本低
工业上需同时考虑:环保、成本、工艺流程简单等因素
2NaOH + SO2 = H2O + Na2SO3
原理:
Ca(OH)2 + SO2 = H2O + CaSO3
氨水法
石灰石-石膏法
SO2 + CaCO3 = CaSO3+CO2↑
△
2CaSO3 +O2 = 2 CaSO4
△
SO2+2NH3+H2O = (NH4)2SO3
2(NH4)2SO3+O2 = (NH4)2SO4
上述处理法既可以消除污染,同时可以得到石膏(CaSO4·2H2O)和硫酸铵(化肥)。
燃煤烟气脱硫
氨脱硫法
拓展视野
氨水法
空气质量评价
思考:阅读课本,分析空气质量指数的标准是什么?
空气质量指数与空气质量的关系?
空气质量指数(AQI):是根据空气中的细颗粒物(PM2.5)、可吸入颗粒物(PM10)、SO2、NO2、O3、CO的浓度计算出来的数值。
空气质量指数越小,空气质量越好。
颗粒物直径为2.5μm
1μm=1x10-6m
μm:微米
氨水法
跨学科链接
思考:每天都更新的和发布的空气质量指数是如何确定的?空气质量等级如何确定?
首先测定细颗粒物(PM2.5)、可吸入颗粒物(PM10)、SO2、NO2、O3、CO的浓度,再换算成对应的质量指数,其中指数最大的污染物会被确定为首要污染物,其指数即为该地区的空气质量指数。
空气质量指数越大,空气质量等级污染程度越高。
氨水法
跨学科链接
思考:每天都更新的和发布的空气质量指数是如何确定的?空气质量等级如何确定?
首先测定细颗粒物(PM2.5)、可吸入颗粒物(PM10)、SO2、NO2、O3、CO的浓度,再换算成对应的质量指数,其中指数最大的污染物会被确定为首要污染物,其指数即为该地区的空气质量指数。
空气质量指数越大,空气质量等级污染程度越高。
雾霾
雾霾:大量极细微的颗粒物均匀地悬浮在空中,这些颗粒物吸附空气中的水蒸气形成雾滴,是空气水平能见度小于10km,这种空气混浊的现象叫作雾霾。
思考:近年来,我国许多地区受到了雾霾天气的干扰。那么,什么是雾霾?
颗粒物分类依据:
颗粒物分类:细颗粒物(PM2.5直径<2.5μm)
可吸入颗粒物(PM10直径<10μm)
颗粒物直径大小
雾霾的形成
思考:分析图4-13、图4-14,了解、分析含硫物质的排放,与雾霾的形成有什么关系?
常见细颗粒物(PM2.5):燃烧颗粒、有机物、金属颗粒等,均可导致雾霾天气的形成,被人体吸收后,对人体健康造成极大危害。
SO2形成的硫酸盐物质(如CaSO4)在空气中可形成细微颗粒物,导致雾霾天气。
从源头上解决大气污染问题,依靠绿色发展, 实现零排放,保护环境,刻不容缓。
保护环境,刻不容缓
