2023-2024学年沪教版(全国)化学九上同步教学 1.2化学研究些什么 课件(共20张PPT)
文档属性
| 名称 | 2023-2024学年沪教版(全国)化学九上同步教学 1.2化学研究些什么 课件(共20张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-05 00:00:00 | ||
图片预览





文档简介
(共20张PPT)
1.2化学研究些什么
1 氢 H
5 硼 B
2 氦 He
3 锂 Li
4 铍 Be
15 磷 P
14 硅 Si
13 铝 Al
12 镁 Mg
10 氖 Ne
11 钠 Na
9 氟 F
8 氧 O
7 氮 N
6 碳 C
19 钾 K
20 钙 Ca
18 氩 Ar
17 氯 Cl
16 硫 P
化学研究物质的性质与变化
蜡烛燃烧的现象?
一起动动手!
物理变化
(1) 石蜡的“三态”变化是什么变化?
化学变化
石蜡
+
氧气
点燃
水
+
二氧化碳
——变化中没有新的物质生成
——变化中有新的物质生成
(2) 石蜡燃烧生成二氧化碳和水是什么变化?
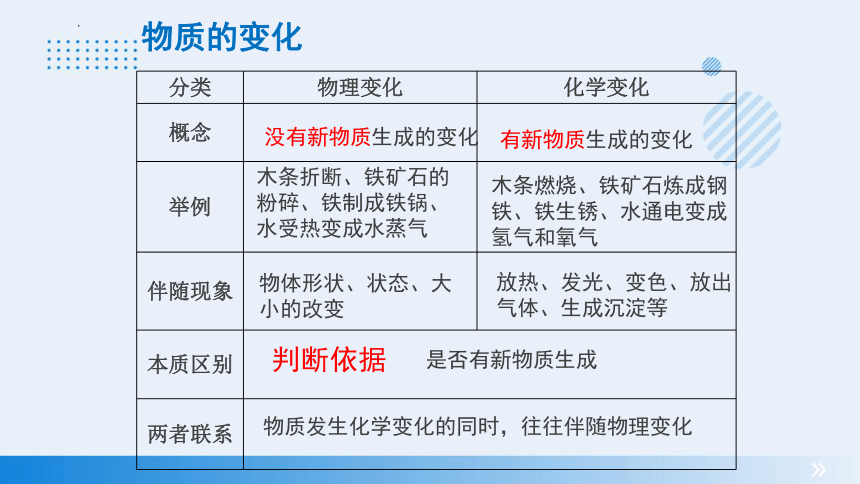
分类 物理变化 化学变化
概念
举例
伴随现象
本质区别
两者联系
物质的变化
木条折断、铁矿石的
粉碎、铁制成铁锅、
水受热变成水蒸气
有新物质生成的变化
没有新物质生成的变化
物体形状、状态、大
小的改变
放热、发光、变色、放出
气体、生成沉淀等
是否有新物质生成
物质发生化学变化的同时,往往伴随物理变化
木条燃烧、铁矿石炼成钢
铁、铁生锈、水通电变成
氢气和氧气
判断依据
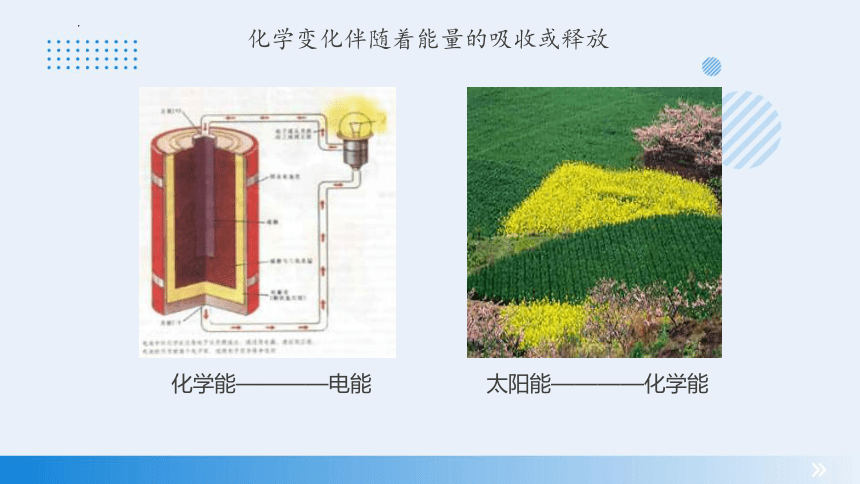
化学变化伴随着能量的吸收或释放
化学能————电能
太阳能————化学能
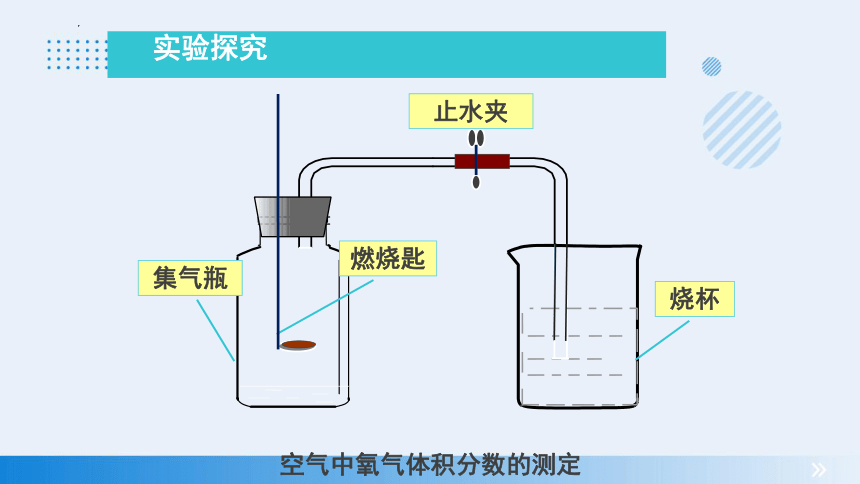
止水夹
燃烧匙
烧杯
实验探究
集气瓶
空气中氧气体积分数的测定
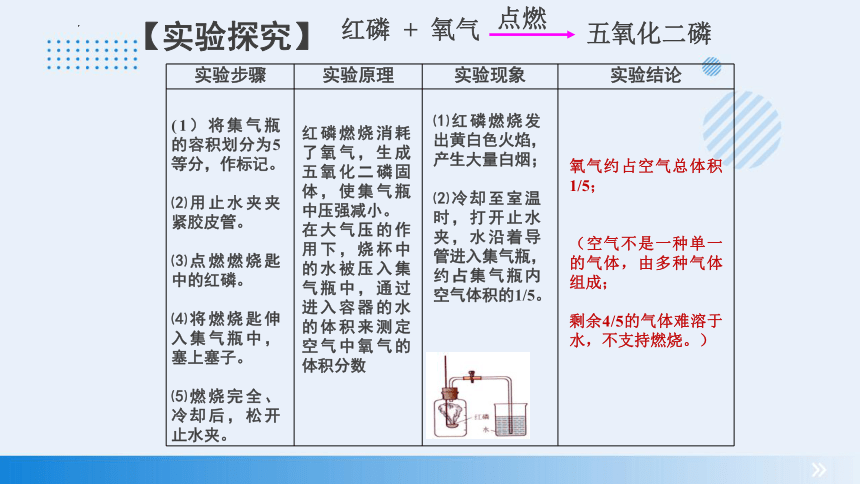
实验步骤 实验原理 实验现象 实验结论
红磷燃烧消耗了氧气,生成五氧化二磷固体,使集气瓶中压强减小。
在大气压的作用下,烧杯中的水被压入集气瓶中,通过进入容器的水的体积来测定空气中氧气的体积分数
(1)将集气瓶的容积划分为5等分,作标记。
⑵用止水夹夹紧胶皮管。
⑶点燃燃烧匙中的红磷。
⑷将燃烧匙伸入集气瓶中,塞上塞子。
⑸燃烧完全、冷却后,松开止水夹。
⑴红磷燃烧发出黄白色火焰,产生大量白烟;
⑵冷却至室温时,打开止水夹,水沿着导管进入集气瓶,约占集气瓶内空气体积的1/5。
氧气约占空气总体积1/5;
(空气不是一种单一的气体,由多种气体组成;
剩余4/5的气体难溶于水,不支持燃烧。)
【实验探究】
红磷 + 氧气
五氧化二磷
点燃
小试牛刀
下列变化属于化学变化的是( )
A. 蜡烛燃烧 B. 冰雪融化
C. 酒精挥发 D. 试管破裂
A
空气的组成?
如何测定?
化学研究物质的组成和结构
因素 影响
测定结果小于
五分之一 装置漏气 反应结束后外界空气进入
红磷量不足 氧气不能完全被消耗
未待装置冷却到室温就打
开止水夹 温度较高,气体膨胀,剩余气体
占有较大的体积
测定结果大于
五分之一 点燃的红磷插入瓶中后未
立即塞上塞子 瓶内空气受热膨胀,部分逸出
最初止水夹未夹紧 瓶内部分空气受热膨胀逸出
空气中氧气含量测定的误差分析
【交流讨论】
1、燃烧后剩余气体 (填“支持”或“不支持”)燃烧且难溶于水,主要是 。
2、空气中氧气含量的测定药品选择红磷依据:红磷燃烧只消耗了氧气,生成了五氧化二磷固体。
3、已知蜡烛燃烧产生二氧化碳(气体),木炭燃烧产生二氧化碳,硫燃烧产生二氧化硫(气体)。铁在纯氧当中燃烧产生黑色固体。镁与氧气反应又与氮气、二氧化碳反应,请判断蜡烛、木炭、硫、金属铁、金属镁是否可以代替磷进行该试并写原因。
蜡烛 (木炭、硫)
铁丝
镁
支持
氮气
实验过程中是否存在误差,若存在,请分析存在误差的原因。
思考
①若装置气密性差,外界空气会进入集气瓶,使得进入水的体积减小,导致测量结果偏低;
②若红磷的量不足,则不能将集气瓶内空气中的氧气完全反应掉,导致测量结果偏低;
③若未冷却就打开止水夹,集气瓶中的气体会因为温度升高,体积增大,使得进入水的体积偏小,导致测量结果偏低。
化学研究物质的组成与结构
实验过程中是否存在误差,若存在,请分析存在误差的原因。
思考
④实验前没有将止水夹夹紧,红磷燃烧时温度升高,集气瓶内气体受热膨胀,顺着导管排出,使得集气瓶内减少的气体多于空气的1/5,导致测量结果偏高;
⑤点燃红磷后塞入胶塞过慢,燃烧产生的热量会使集气瓶中的空气受热膨胀而排出,集气瓶中减少的气体就等于因膨胀排出的空气加上消耗的氧气,导致测量结果偏高。
化学研究物质的组成与结构
物质的初步分类
⑴纯净物
概念:只由一种物质组成
实例:氧气、二氧化碳、二氧化碳、水、碳酸氢铵等
⑵混合物
概念:是由两种或两种以上物质混合而成的
实例:空气、食盐水、糖水、海水、自来水、医用酒精等
纯净物可以用专门的化学式表示
空气中各组成成分及所占体积分数
阅读课本内容,了解人类对空气成分的发现
空气成分的发现
空气的成分(按体积分数计算)
氮气
78% 主要成分(99%)
氧气
21%
稀有气体
0.94%
其他成分
二氧化碳
0.03%
其他气体和杂质
0.03%
化学研究物质的用途和制法
金刚石:无色透明晶体,具有特殊光学性质;是自然界中天然存在的最坚硬的物质;不导电,化学性质稳定,耐酸耐碱。
石墨:灰黑色不透明固体;质软,导电,导热;化学性质稳定,耐腐蚀,同酸、碱等物质不易发生反应。
制作钻石
作为电池的电极
制作铅笔的笔芯
切割玻璃
金刚石(无色透明晶体,有特殊光学性质)
石墨(能导电)
石墨(质软)
金刚石(硬度大)
化学研究物质的用途和制法
化学研究物质的用途和制法
请指出下列用途中,哪些是金刚石的用途,哪些是石墨的用途,并说明该用途分别利用了金刚石或石墨的哪些性质。
1、制作钻石
2、作为电池的电极
3、制作铅笔的笔芯
4、切割玻璃
性质 用途
决定
体现
1.2化学研究些什么
1 氢 H
5 硼 B
2 氦 He
3 锂 Li
4 铍 Be
15 磷 P
14 硅 Si
13 铝 Al
12 镁 Mg
10 氖 Ne
11 钠 Na
9 氟 F
8 氧 O
7 氮 N
6 碳 C
19 钾 K
20 钙 Ca
18 氩 Ar
17 氯 Cl
16 硫 P
化学研究物质的性质与变化
蜡烛燃烧的现象?
一起动动手!
物理变化
(1) 石蜡的“三态”变化是什么变化?
化学变化
石蜡
+
氧气
点燃
水
+
二氧化碳
——变化中没有新的物质生成
——变化中有新的物质生成
(2) 石蜡燃烧生成二氧化碳和水是什么变化?
分类 物理变化 化学变化
概念
举例
伴随现象
本质区别
两者联系
物质的变化
木条折断、铁矿石的
粉碎、铁制成铁锅、
水受热变成水蒸气
有新物质生成的变化
没有新物质生成的变化
物体形状、状态、大
小的改变
放热、发光、变色、放出
气体、生成沉淀等
是否有新物质生成
物质发生化学变化的同时,往往伴随物理变化
木条燃烧、铁矿石炼成钢
铁、铁生锈、水通电变成
氢气和氧气
判断依据
化学变化伴随着能量的吸收或释放
化学能————电能
太阳能————化学能
止水夹
燃烧匙
烧杯
实验探究
集气瓶
空气中氧气体积分数的测定
实验步骤 实验原理 实验现象 实验结论
红磷燃烧消耗了氧气,生成五氧化二磷固体,使集气瓶中压强减小。
在大气压的作用下,烧杯中的水被压入集气瓶中,通过进入容器的水的体积来测定空气中氧气的体积分数
(1)将集气瓶的容积划分为5等分,作标记。
⑵用止水夹夹紧胶皮管。
⑶点燃燃烧匙中的红磷。
⑷将燃烧匙伸入集气瓶中,塞上塞子。
⑸燃烧完全、冷却后,松开止水夹。
⑴红磷燃烧发出黄白色火焰,产生大量白烟;
⑵冷却至室温时,打开止水夹,水沿着导管进入集气瓶,约占集气瓶内空气体积的1/5。
氧气约占空气总体积1/5;
(空气不是一种单一的气体,由多种气体组成;
剩余4/5的气体难溶于水,不支持燃烧。)
【实验探究】
红磷 + 氧气
五氧化二磷
点燃
小试牛刀
下列变化属于化学变化的是( )
A. 蜡烛燃烧 B. 冰雪融化
C. 酒精挥发 D. 试管破裂
A
空气的组成?
如何测定?
化学研究物质的组成和结构
因素 影响
测定结果小于
五分之一 装置漏气 反应结束后外界空气进入
红磷量不足 氧气不能完全被消耗
未待装置冷却到室温就打
开止水夹 温度较高,气体膨胀,剩余气体
占有较大的体积
测定结果大于
五分之一 点燃的红磷插入瓶中后未
立即塞上塞子 瓶内空气受热膨胀,部分逸出
最初止水夹未夹紧 瓶内部分空气受热膨胀逸出
空气中氧气含量测定的误差分析
【交流讨论】
1、燃烧后剩余气体 (填“支持”或“不支持”)燃烧且难溶于水,主要是 。
2、空气中氧气含量的测定药品选择红磷依据:红磷燃烧只消耗了氧气,生成了五氧化二磷固体。
3、已知蜡烛燃烧产生二氧化碳(气体),木炭燃烧产生二氧化碳,硫燃烧产生二氧化硫(气体)。铁在纯氧当中燃烧产生黑色固体。镁与氧气反应又与氮气、二氧化碳反应,请判断蜡烛、木炭、硫、金属铁、金属镁是否可以代替磷进行该试并写原因。
蜡烛 (木炭、硫)
铁丝
镁
支持
氮气
实验过程中是否存在误差,若存在,请分析存在误差的原因。
思考
①若装置气密性差,外界空气会进入集气瓶,使得进入水的体积减小,导致测量结果偏低;
②若红磷的量不足,则不能将集气瓶内空气中的氧气完全反应掉,导致测量结果偏低;
③若未冷却就打开止水夹,集气瓶中的气体会因为温度升高,体积增大,使得进入水的体积偏小,导致测量结果偏低。
化学研究物质的组成与结构
实验过程中是否存在误差,若存在,请分析存在误差的原因。
思考
④实验前没有将止水夹夹紧,红磷燃烧时温度升高,集气瓶内气体受热膨胀,顺着导管排出,使得集气瓶内减少的气体多于空气的1/5,导致测量结果偏高;
⑤点燃红磷后塞入胶塞过慢,燃烧产生的热量会使集气瓶中的空气受热膨胀而排出,集气瓶中减少的气体就等于因膨胀排出的空气加上消耗的氧气,导致测量结果偏高。
化学研究物质的组成与结构
物质的初步分类
⑴纯净物
概念:只由一种物质组成
实例:氧气、二氧化碳、二氧化碳、水、碳酸氢铵等
⑵混合物
概念:是由两种或两种以上物质混合而成的
实例:空气、食盐水、糖水、海水、自来水、医用酒精等
纯净物可以用专门的化学式表示
空气中各组成成分及所占体积分数
阅读课本内容,了解人类对空气成分的发现
空气成分的发现
空气的成分(按体积分数计算)
氮气
78% 主要成分(99%)
氧气
21%
稀有气体
0.94%
其他成分
二氧化碳
0.03%
其他气体和杂质
0.03%
化学研究物质的用途和制法
金刚石:无色透明晶体,具有特殊光学性质;是自然界中天然存在的最坚硬的物质;不导电,化学性质稳定,耐酸耐碱。
石墨:灰黑色不透明固体;质软,导电,导热;化学性质稳定,耐腐蚀,同酸、碱等物质不易发生反应。
制作钻石
作为电池的电极
制作铅笔的笔芯
切割玻璃
金刚石(无色透明晶体,有特殊光学性质)
石墨(能导电)
石墨(质软)
金刚石(硬度大)
化学研究物质的用途和制法
化学研究物质的用途和制法
请指出下列用途中,哪些是金刚石的用途,哪些是石墨的用途,并说明该用途分别利用了金刚石或石墨的哪些性质。
1、制作钻石
2、作为电池的电极
3、制作铅笔的笔芯
4、切割玻璃
性质 用途
决定
体现
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
