2023-2024学年沪教版(上海)化学九年级第一学期同步教学 1.2走进化学实验室 课件(共18张PPT)
文档属性
| 名称 | 2023-2024学年沪教版(上海)化学九年级第一学期同步教学 1.2走进化学实验室 课件(共18张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 4.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-05 00:00:00 | ||
图片预览





文档简介
(共18张PPT)
新课导入
问1:日常生活中,我们经常能观察到一些变化,如秋天降的霜、冬天下的雪、春天起的雾、夏天落的冰雹其实是同一种物质。这一系列变化是什么物质在发生变化?属于什么变化?
问2:日常生活中,我们还经常能观察到另外一些变化,天然气、煤气、液化气等可燃物的燃烧,钢铁生锈,这些变化属于什么变化?
问3:单纯的观察能否获得关于物质组成、结构、性质和变化规律的足够的信息?
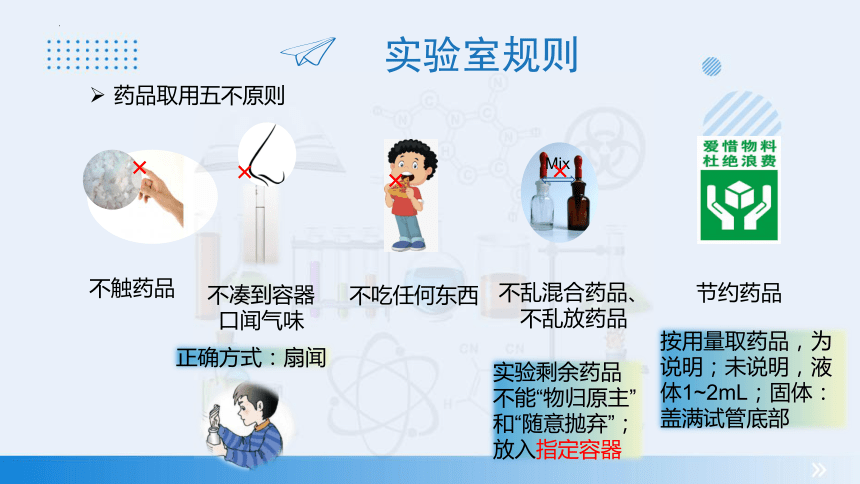
药品取用五不原则
Mix
不触药品
不凑到容器口闻气味
不吃任何东西
不乱混合药品、不乱放药品
节约药品
正确方式:扇闻
实验剩余药品不能“物归原主”和“随意抛弃”;放入指定容器
按用量取药品,为说明;未说明,液体1~2mL;固体:盖满试管底部
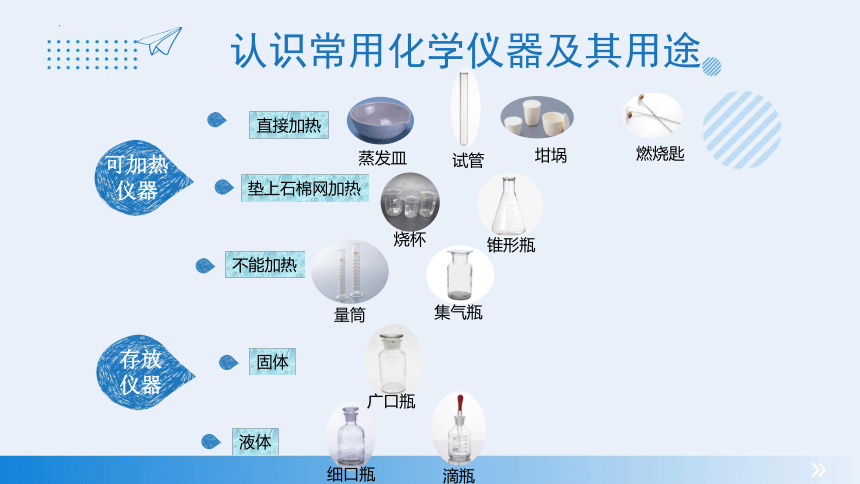
直接加热
垫上石棉网加热
不能加热
液体
固体
蒸发皿
试管
坩埚
燃烧匙
烧杯
锥形瓶
量筒
集气瓶
广口瓶
细口瓶
滴瓶
认识常见化学仪器
存放药品的仪器:广口瓶、细口瓶、滴瓶、集气瓶。
反应容器有:试管、蒸发皿、燃烧匙
烧杯、烧瓶、锥形瓶
加热仪器:酒精灯、酒精喷灯(加强热)
计量仪器:托盘天平、量筒
取用仪器:药匙(取用粉末或小晶粒状)、镊子(取用块状或较大颗粒)、胶头滴管(取用少量液体)。
夹持仪器:试管夹、铁架台(带铁夹、铁圈)、坩埚钳。
其他仪器:长颈漏斗、石棉网、玻璃棒、试管刷、试管架、水槽、表面皿、三角架、研钵。
遵守化学实验规则
目的:效果、安全
内容:课本p132
课前:预习——熟悉实验内容
课堂:(1)先查仪器、用品是否齐全、干净;
(2)再按规范要求进行实验 (且要安、静、守、节);
(3)观察记录实验现象;
(4)做好善后工作(尤其是两废的处理)。
课后:完成实验报告
液体药品取用
固体药品取用
定量:
非定量:
量筒+胶头滴管
少量:滴管滴加
多量:倾倒法
量筒读数:
先倾倒液体至接近刻度线
再用胶头滴管滴加至刻度线
竖直悬空
块状
粉末状
一横、二放、三慢竖
一横、二入、三直立
镊子
药匙或纸槽
瓶塞倒放、标签向心(手心)
用外焰加热:外焰温度最高
酒精量:酒精灯容量的1/4~2/3
加热源:酒精灯
构造
加热液体
加热固体
液体量不超过1/3;试管倾斜45°,试管口不对着自己或他人;热试管不能立即冷水冲洗;
加热前预热;试管口略向下倾斜。
PS:不论热固加热时容器外壁保持干燥!
试管夹
铁架台
灭火
[提问]实验时万一不小心失火怎么办?
知道消防用品(灭火器)的摆放位置;
一般的小火可用湿布或沙土扑盖扑灭火,不能用水冲,以免火势蔓延。
火势大时可使用泡沫灭火器或二氧化碳灭火器。
电器着火时,应先切断电源,再使用二氧化碳灭火器。
实验内容:向盛有2mL氢氧化钠溶液的试管中滴加1-2滴酚酞试液,观察现象;再逐滴滴加盐酸,边滴加边震荡,观察现象
实验用品:试管、酚酞试液、配制好的氢氧化钠溶液与盐酸溶液
实验演示(略)
酚酞试液
盐酸
氢氧化钠溶液
氢氧化钠呈碱性,遇到酚酞指示剂红
氢氧化钠 + 稀盐酸 →氯化钠 + 水
NaOH
HCl
NaCl
H2O
实验内容:在试管中加入2mL硫酸铜溶液,逐滴滴加约1mL氢氧化钠溶液,观察现象;再逐滴滴加稀硫酸,振荡试管,观察现象。
实验用品:试管、氢氧化钠溶液、硫酸铜溶液、稀硫酸溶液
实验演示(略)
氢氧化钠溶液
稀硫酸
氢氧化钠 + 硫酸铜 → 氢氧化铜 + 硫酸钠
NaOH CuSO4 Cu(OH)2 Na2SO4
硫酸铜溶液
氢氧化铜 + 稀硫酸 → 硫酸铜 + 水
Cu(OH)2 H2SO4 CuSO4 H2O
氢氧化铜:蓝色絮状沉淀
[提问]为什么用完酒精灯后,必须用灯帽盖灭,不可用嘴吹熄?
防止将火焰沿着灯颈吹入灯内
[提问]为什么用完后,立即盖上灯帽?
防止酒精挥发和灯芯吸水而不易点燃
灯体内的酒精不可超过灯容积的3/4,也不应少于1/4。
板书设计
1.2 走进化学实验室
参观化学实验室
一、化学实验室配备的化学实验药品和仪器
反应容器: ——可直接受热的:试管、蒸发皿、燃烧匙等, ——可间接受热的:烧杯、烧瓶、锥形瓶。
存放药品仪器:广口瓶、细口瓶、滴瓶、集气瓶。
加热仪器:酒精灯、酒精喷灯。
计量仪器:托盘天平、量筒。
取用仪器:药匙、镊子、胶头滴管。
实验内容:在试管中,加入少量高锰酸钾晶体,用酒精灯缓慢加热,把带有火星的木条放在试管口,观察发生的现象
实验用品:铁架台、酒精灯、药匙、试管、高锰酸钾。
搭建装置顺序:从左至右、从下至上
拆装置顺序则相反
实验报告
实验名称、实验目的、实验用品、实验内容(操作步骤、实验现象)、结论、实验小结
实验内容是核心
实验室仪器及用途
开展化学实验
撰写实验报告
走进化学实验室
实验室规则
新课导入
问1:日常生活中,我们经常能观察到一些变化,如秋天降的霜、冬天下的雪、春天起的雾、夏天落的冰雹其实是同一种物质。这一系列变化是什么物质在发生变化?属于什么变化?
问2:日常生活中,我们还经常能观察到另外一些变化,天然气、煤气、液化气等可燃物的燃烧,钢铁生锈,这些变化属于什么变化?
问3:单纯的观察能否获得关于物质组成、结构、性质和变化规律的足够的信息?
药品取用五不原则
Mix
不触药品
不凑到容器口闻气味
不吃任何东西
不乱混合药品、不乱放药品
节约药品
正确方式:扇闻
实验剩余药品不能“物归原主”和“随意抛弃”;放入指定容器
按用量取药品,为说明;未说明,液体1~2mL;固体:盖满试管底部
直接加热
垫上石棉网加热
不能加热
液体
固体
蒸发皿
试管
坩埚
燃烧匙
烧杯
锥形瓶
量筒
集气瓶
广口瓶
细口瓶
滴瓶
认识常见化学仪器
存放药品的仪器:广口瓶、细口瓶、滴瓶、集气瓶。
反应容器有:试管、蒸发皿、燃烧匙
烧杯、烧瓶、锥形瓶
加热仪器:酒精灯、酒精喷灯(加强热)
计量仪器:托盘天平、量筒
取用仪器:药匙(取用粉末或小晶粒状)、镊子(取用块状或较大颗粒)、胶头滴管(取用少量液体)。
夹持仪器:试管夹、铁架台(带铁夹、铁圈)、坩埚钳。
其他仪器:长颈漏斗、石棉网、玻璃棒、试管刷、试管架、水槽、表面皿、三角架、研钵。
遵守化学实验规则
目的:效果、安全
内容:课本p132
课前:预习——熟悉实验内容
课堂:(1)先查仪器、用品是否齐全、干净;
(2)再按规范要求进行实验 (且要安、静、守、节);
(3)观察记录实验现象;
(4)做好善后工作(尤其是两废的处理)。
课后:完成实验报告
液体药品取用
固体药品取用
定量:
非定量:
量筒+胶头滴管
少量:滴管滴加
多量:倾倒法
量筒读数:
先倾倒液体至接近刻度线
再用胶头滴管滴加至刻度线
竖直悬空
块状
粉末状
一横、二放、三慢竖
一横、二入、三直立
镊子
药匙或纸槽
瓶塞倒放、标签向心(手心)
用外焰加热:外焰温度最高
酒精量:酒精灯容量的1/4~2/3
加热源:酒精灯
构造
加热液体
加热固体
液体量不超过1/3;试管倾斜45°,试管口不对着自己或他人;热试管不能立即冷水冲洗;
加热前预热;试管口略向下倾斜。
PS:不论热固加热时容器外壁保持干燥!
试管夹
铁架台
灭火
[提问]实验时万一不小心失火怎么办?
知道消防用品(灭火器)的摆放位置;
一般的小火可用湿布或沙土扑盖扑灭火,不能用水冲,以免火势蔓延。
火势大时可使用泡沫灭火器或二氧化碳灭火器。
电器着火时,应先切断电源,再使用二氧化碳灭火器。
实验内容:向盛有2mL氢氧化钠溶液的试管中滴加1-2滴酚酞试液,观察现象;再逐滴滴加盐酸,边滴加边震荡,观察现象
实验用品:试管、酚酞试液、配制好的氢氧化钠溶液与盐酸溶液
实验演示(略)
酚酞试液
盐酸
氢氧化钠溶液
氢氧化钠呈碱性,遇到酚酞指示剂红
氢氧化钠 + 稀盐酸 →氯化钠 + 水
NaOH
HCl
NaCl
H2O
实验内容:在试管中加入2mL硫酸铜溶液,逐滴滴加约1mL氢氧化钠溶液,观察现象;再逐滴滴加稀硫酸,振荡试管,观察现象。
实验用品:试管、氢氧化钠溶液、硫酸铜溶液、稀硫酸溶液
实验演示(略)
氢氧化钠溶液
稀硫酸
氢氧化钠 + 硫酸铜 → 氢氧化铜 + 硫酸钠
NaOH CuSO4 Cu(OH)2 Na2SO4
硫酸铜溶液
氢氧化铜 + 稀硫酸 → 硫酸铜 + 水
Cu(OH)2 H2SO4 CuSO4 H2O
氢氧化铜:蓝色絮状沉淀
[提问]为什么用完酒精灯后,必须用灯帽盖灭,不可用嘴吹熄?
防止将火焰沿着灯颈吹入灯内
[提问]为什么用完后,立即盖上灯帽?
防止酒精挥发和灯芯吸水而不易点燃
灯体内的酒精不可超过灯容积的3/4,也不应少于1/4。
板书设计
1.2 走进化学实验室
参观化学实验室
一、化学实验室配备的化学实验药品和仪器
反应容器: ——可直接受热的:试管、蒸发皿、燃烧匙等, ——可间接受热的:烧杯、烧瓶、锥形瓶。
存放药品仪器:广口瓶、细口瓶、滴瓶、集气瓶。
加热仪器:酒精灯、酒精喷灯。
计量仪器:托盘天平、量筒。
取用仪器:药匙、镊子、胶头滴管。
实验内容:在试管中,加入少量高锰酸钾晶体,用酒精灯缓慢加热,把带有火星的木条放在试管口,观察发生的现象
实验用品:铁架台、酒精灯、药匙、试管、高锰酸钾。
搭建装置顺序:从左至右、从下至上
拆装置顺序则相反
实验报告
实验名称、实验目的、实验用品、实验内容(操作步骤、实验现象)、结论、实验小结
实验内容是核心
实验室仪器及用途
开展化学实验
撰写实验报告
走进化学实验室
实验室规则
