2023-2024学年鲁教版(五四制)化学九年级全册同步教学 1.4 到实验室去:配制一定溶质质量分数的溶液 课件(共21张PPT)
文档属性
| 名称 | 2023-2024学年鲁教版(五四制)化学九年级全册同步教学 1.4 到实验室去:配制一定溶质质量分数的溶液 课件(共21张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-05 00:00:00 | ||
图片预览







文档简介
(共21张PPT)
1.4 到实验室去:配制一定溶质质
量分数的溶液
1.与同学合作配制一定溶质质量分数的溶液。
2.初步学会配制一定溶质质量分数溶液的方法。
3.进一步规范药品的取用、称量、量取、溶解、搅拌等基本操作。
1、利用溶质质量分数的计算,了解溶液配制的方法
2、用化学计算来解决生产生活中有关溶液的实际问题
在医院里,我们经常会看到病人输液,许多就是氯化钠生理盐水(即溶质质量分数为0.9%的食盐水)那么你知道怎样配制一定溶质质量分数的溶液吗?
氯化钠溶液的配制
配制80g溶质质量分数为10%的氯化钠溶液
1、计算
氯化钠的质量=氯化钠溶液的质量×氯化钠的质量分数=80g×10%=8g
水的质量=氯化钠溶液的质量-氯化钠的质量=80g-8g=72g
水的体积=
水的质量
水的密度
=
72g
1.0g/cm3
=
72cm3
=72mL
2、称量
用托盘天平进行称量
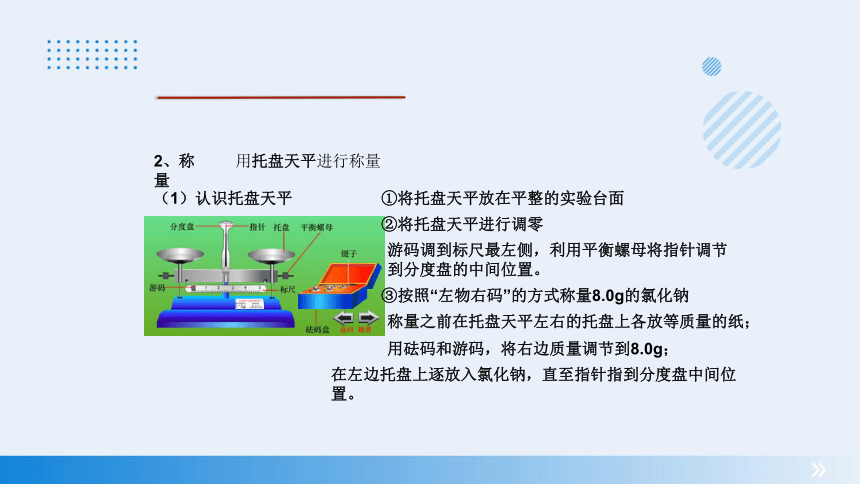
(1)认识托盘天平
①将托盘天平放在平整的实验台面
②将托盘天平进行调零
游码调到标尺最左侧,利用平衡螺母将指针调节
到分度盘的中间位置。
③按照“左物右码”的方式称量8.0g的氯化钠
称量之前在托盘天平左右的托盘上各放等质量的纸;
用砝码和游码,将右边质量调节到8.0g;
在左边托盘上逐放入氯化钠,直至指针指到分度盘中间位置。
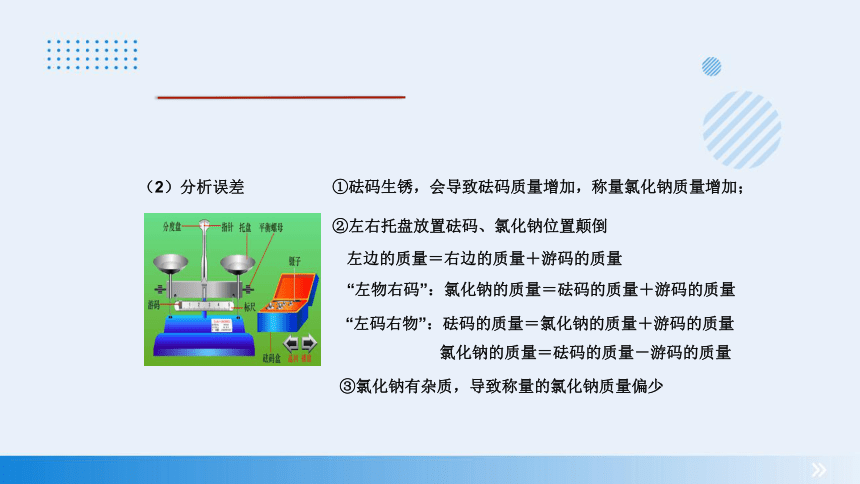
(2)分析误差
①砝码生锈,会导致砝码质量增加,称量氯化钠质量增加;
②左右托盘放置砝码、氯化钠位置颠倒
左边的质量=右边的质量+游码的质量
“左物右码”:氯化钠的质量=砝码的质量+游码的质量
“左码右物”:砝码的质量=氯化钠的质量+游码的质量
氯化钠的质量=砝码的质量-游码的质量
③氯化钠有杂质,导致称量的氯化钠质量偏少
3、量取
用量筒量取72.0mL的水
误差分析:
量筒的构造是特殊的,在量筒内,液面是凹液面的
视线通过了凹液面最低处,
但视线最先接触量筒的红
点处,所以,读数偏大。
视线通过了凹液面最低处,
但视线最先接触量筒的红
点处,所以读数偏小。
视线通过了凹液面最低处,
视线为平视,读数正好。
4、溶解
将称量好的8.0g的食盐放入烧杯中,
再倒入量取好的72.0mL的水,
搅拌玻璃棒,加快溶解速度。
5、装瓶,贴标签
将配置好的80g溶质质量分数为10%的
氯化钠溶液倒入试剂瓶中,并贴好标签。
配制一定溶质质量分数的溶液
如何配制50克6%的NaCl溶液
配制溶质质量分数一定的氯化钠溶液
方法一:溶质+水 食盐加水
方法二:浓溶液+水 20%的食盐水加水
方法三:稀溶液+溶质 10%的食盐水加食盐
方法四:浓溶液+稀溶液 20%的和10%的食盐水混合
配制 50g 6% 的氯化钠溶液
⑴.计算: NaCl g H2O g
⑵.称量、量取:用____称量3g食盐,用 量取47mL水
⑶.溶解:将溶质和溶剂在烧杯中混合,搅拌至溶质完全溶解。
⑷.装瓶:(盖好瓶塞贴上标签)
1、实验步骤:
3
47
托盘天平
量筒
2、实验中用到了哪些仪器?
托盘天平、烧杯、量筒、玻璃棒、药匙、胶头滴管
3、在实验操作中应该注意哪些问题?
注意药品的名称
左“物”右“码”
选用适合量程的量筒
4、讨论造成误差的原因有哪些?
实验误差分析
1.称量时左物右码放反了
2.药品中有杂质
3.量取体积时仰视读数或俯视读数
4.倾倒溶剂水时,洒出烧杯外
若俯视则读数偏高,液
体的实际体积<读数
仰视,读数偏低,液
体的实际体积>读数
1.【中考·天水】实验室配制氯化钠溶液的操作中,正确的是( )
D
2.【中考·自贡】某同学配制50 g 9%的氯化钠溶液,整个操作过程如图所示,回答下列问题:
(1)配制溶液的正确操作顺序为_____________(填序号),其中操作错误的是________(填序号)。
②①⑤③④
①
(2)图②中盛放氯化钠固体的仪器名称是__________,需称取氯化钠________g。
(3)量取水时选用的量筒的量程最合适的是________(填字母),读数时视线要与量筒内__________________ 保持水平。
A.10 mL B.25 mL C.50 mL D.100 mL
广口瓶
C
4.5
凹液面的最低处
3.要配制100 g溶质质量分数为5%的氢氧化钠溶液,下列说法正确的是( )
A.实验中要用到的玻璃仪器只有烧杯和玻璃棒
B.称量氢氧化钠固体时应该将砝码放在左盘,药品放在右盘
C.配制好的氢氧化钠溶液中溶质和溶剂的质量之比为1 : 20
D.称量时,必须将氢氧化钠固体放在玻璃器皿中称量
一、溶质的质量分数
1、溶质的质量分数
溶质质量(g)
溶液质量(g)
100%
二、配制溶质质量分数一定的溶液
实验步骤:
实验仪器:
⑴计算 ⑵称量,量取 ⑶溶解 ⑷装瓶
药匙 托盘天平 量筒 滴管 烧杯 玻璃棒
2、溶液稀释前后,溶质的质量不变
溶质质量 = 溶液质量×溶质的质量分数
1.4 到实验室去:配制一定溶质质
量分数的溶液
1.与同学合作配制一定溶质质量分数的溶液。
2.初步学会配制一定溶质质量分数溶液的方法。
3.进一步规范药品的取用、称量、量取、溶解、搅拌等基本操作。
1、利用溶质质量分数的计算,了解溶液配制的方法
2、用化学计算来解决生产生活中有关溶液的实际问题
在医院里,我们经常会看到病人输液,许多就是氯化钠生理盐水(即溶质质量分数为0.9%的食盐水)那么你知道怎样配制一定溶质质量分数的溶液吗?
氯化钠溶液的配制
配制80g溶质质量分数为10%的氯化钠溶液
1、计算
氯化钠的质量=氯化钠溶液的质量×氯化钠的质量分数=80g×10%=8g
水的质量=氯化钠溶液的质量-氯化钠的质量=80g-8g=72g
水的体积=
水的质量
水的密度
=
72g
1.0g/cm3
=
72cm3
=72mL
2、称量
用托盘天平进行称量
(1)认识托盘天平
①将托盘天平放在平整的实验台面
②将托盘天平进行调零
游码调到标尺最左侧,利用平衡螺母将指针调节
到分度盘的中间位置。
③按照“左物右码”的方式称量8.0g的氯化钠
称量之前在托盘天平左右的托盘上各放等质量的纸;
用砝码和游码,将右边质量调节到8.0g;
在左边托盘上逐放入氯化钠,直至指针指到分度盘中间位置。
(2)分析误差
①砝码生锈,会导致砝码质量增加,称量氯化钠质量增加;
②左右托盘放置砝码、氯化钠位置颠倒
左边的质量=右边的质量+游码的质量
“左物右码”:氯化钠的质量=砝码的质量+游码的质量
“左码右物”:砝码的质量=氯化钠的质量+游码的质量
氯化钠的质量=砝码的质量-游码的质量
③氯化钠有杂质,导致称量的氯化钠质量偏少
3、量取
用量筒量取72.0mL的水
误差分析:
量筒的构造是特殊的,在量筒内,液面是凹液面的
视线通过了凹液面最低处,
但视线最先接触量筒的红
点处,所以,读数偏大。
视线通过了凹液面最低处,
但视线最先接触量筒的红
点处,所以读数偏小。
视线通过了凹液面最低处,
视线为平视,读数正好。
4、溶解
将称量好的8.0g的食盐放入烧杯中,
再倒入量取好的72.0mL的水,
搅拌玻璃棒,加快溶解速度。
5、装瓶,贴标签
将配置好的80g溶质质量分数为10%的
氯化钠溶液倒入试剂瓶中,并贴好标签。
配制一定溶质质量分数的溶液
如何配制50克6%的NaCl溶液
配制溶质质量分数一定的氯化钠溶液
方法一:溶质+水 食盐加水
方法二:浓溶液+水 20%的食盐水加水
方法三:稀溶液+溶质 10%的食盐水加食盐
方法四:浓溶液+稀溶液 20%的和10%的食盐水混合
配制 50g 6% 的氯化钠溶液
⑴.计算: NaCl g H2O g
⑵.称量、量取:用____称量3g食盐,用 量取47mL水
⑶.溶解:将溶质和溶剂在烧杯中混合,搅拌至溶质完全溶解。
⑷.装瓶:(盖好瓶塞贴上标签)
1、实验步骤:
3
47
托盘天平
量筒
2、实验中用到了哪些仪器?
托盘天平、烧杯、量筒、玻璃棒、药匙、胶头滴管
3、在实验操作中应该注意哪些问题?
注意药品的名称
左“物”右“码”
选用适合量程的量筒
4、讨论造成误差的原因有哪些?
实验误差分析
1.称量时左物右码放反了
2.药品中有杂质
3.量取体积时仰视读数或俯视读数
4.倾倒溶剂水时,洒出烧杯外
若俯视则读数偏高,液
体的实际体积<读数
仰视,读数偏低,液
体的实际体积>读数
1.【中考·天水】实验室配制氯化钠溶液的操作中,正确的是( )
D
2.【中考·自贡】某同学配制50 g 9%的氯化钠溶液,整个操作过程如图所示,回答下列问题:
(1)配制溶液的正确操作顺序为_____________(填序号),其中操作错误的是________(填序号)。
②①⑤③④
①
(2)图②中盛放氯化钠固体的仪器名称是__________,需称取氯化钠________g。
(3)量取水时选用的量筒的量程最合适的是________(填字母),读数时视线要与量筒内__________________ 保持水平。
A.10 mL B.25 mL C.50 mL D.100 mL
广口瓶
C
4.5
凹液面的最低处
3.要配制100 g溶质质量分数为5%的氢氧化钠溶液,下列说法正确的是( )
A.实验中要用到的玻璃仪器只有烧杯和玻璃棒
B.称量氢氧化钠固体时应该将砝码放在左盘,药品放在右盘
C.配制好的氢氧化钠溶液中溶质和溶剂的质量之比为1 : 20
D.称量时,必须将氢氧化钠固体放在玻璃器皿中称量
一、溶质的质量分数
1、溶质的质量分数
溶质质量(g)
溶液质量(g)
100%
二、配制溶质质量分数一定的溶液
实验步骤:
实验仪器:
⑴计算 ⑵称量,量取 ⑶溶解 ⑷装瓶
药匙 托盘天平 量筒 滴管 烧杯 玻璃棒
2、溶液稀释前后,溶质的质量不变
溶质质量 = 溶液质量×溶质的质量分数
同课章节目录
- 第一单元 溶液
- 1 溶液的形成
- 2 溶液组成的定量表示
- 3物质的溶解性
- 到实验室去:配制一定溶质质量分数的溶液
- 第二单元 常见的酸和碱
- 1 酸及其性质
- 2 碱及其性质
- 3 溶液的酸碱性
- 4 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 到图书馆去:分子变成离子
- 第三单元 海水中的化学
- 1 海洋化学资源
- 2 海水“晒盐”
- 3 海水“制碱”
- 到实验室去:粗盐中难溶性杂质的去除
- 第四单元 金属
- 1 常见的金属材料
- 2 金属的化学性质
- 3 钢铁的锈蚀与防护
- 到实验室去:探究金属的性质
- 第五单元 化学与健康
- 1 食物中的有机物
- 2 化学元素与人体健康
- 3 远离有毒物质
- 第六单元 化学与社会发展
- 1 化学与能源开发
- 2 化学与材料研制
- 3 化学与农业生产
- 4 化学与环境保护
