3.2原子的结构导学案-2023-2024学年九年级化学人教版上册(word 无答案)
文档属性
| 名称 | 3.2原子的结构导学案-2023-2024学年九年级化学人教版上册(word 无答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 322.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-05 00:00:00 | ||
图片预览


文档简介
九年级上册 化学 导学案
班级: 姓名:
课题: 第三章 第2节 原子的结构 第二课时
学习过程(定向导学:教材55 页)---先学后教,当堂训练
流程及学习内容:
一、学习目标
1、知道离子也是构成物质的一种微粒,了解离子的概念。
2、掌握离子的形成过程以及离子的表示方法。
3、掌握离子的分类并会判断原子、阳离子和阴离子。
二、自主学习
1、离子的形成和分类
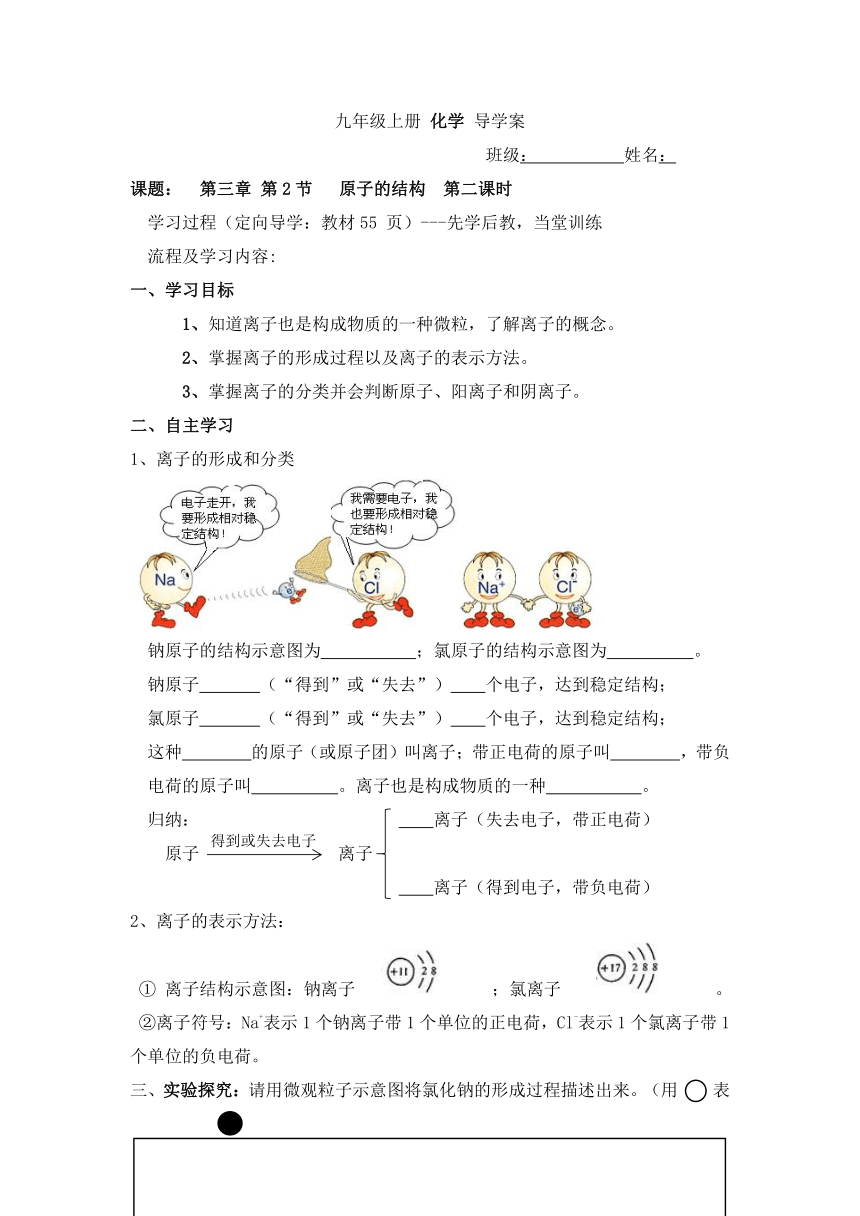
钠原子的结构示意图为 ;氯原子的结构示意图为 。
钠原子 (“得到”或“失去”) 个电子,达到稳定结构;
氯原子 (“得到”或“失去”) 个电子,达到稳定结构;
这种 的原子(或原子团)叫离子;带正电荷的原子叫 ,带负电荷的原子叫 。离子也是构成物质的一种 。
归纳: 离子(失去电子,带正电荷)
原子 离子
离子(得到电子,带负电荷)
离子的表示方法:
① 离子结构示意图:钠离子 ;氯离子 。
②离子符号:Na+表示1个钠离子带1个单位的正电荷,Cl-表示1个氯离子带1个单位的负电荷。
三、实验探究:请用微观粒子示意图将氯化钠的形成过程描述出来。(用 表示原子核, 表示核外电子)
结论: 的原子叫离子;带正电荷的原子叫 ,带负电荷的原子叫 。氯化钠这种物质由 构成。
交流反思:寻找原子的最外层电子数与元素化学性质的关系
示例元素 最外层电子数 在化学反应中易得(或失)电子 形成离子类型及结构示意图 与之相同的稀有气体元素稳定结构
1 易失 个电子 阳离子:
易 2个电子 离子:
3 易 个电子 离子:
6 易 个电子 离子:
易 个电子 离子:
易 个电子 离子:
结论:元素的化学性质由 决定。最外层电子数<4,易失去电子,形成 离子;最外层电子数>4,易得到电子,形成 离子。最外层电子为 时,元素为稳定结构。
当堂训练:
1、下面是4位同学对分子、原子、离子的描述,其中正确的是( )
A.B.C.D.
2.下列是几种粒子的结构示意图,有关说法正确的是( )。
A. ①和②两种粒子的化学性质相似 B. ③和④均属于离子结构示意图
C. 粒子②在化学反应中容易失去电子 D. ①②③④共表示四种元素的粒子
3.下列各组是元素的原子结构示意图,其中具有相似化学性质的一对元素是( )
A.B.C. D.
4.下列关于四种粒子的结构示意图的说法中正确的是
A.①③属于不同种元素 B.④属于离子,离子符号为Mg2+
C.②③的化学性质相似 D.①表示的氯原子
5.如图是元素X的一种粒子结构示意图,下列说法正确的是( )。
A. X是非金属元素
B. X的原子最外层电子数为8
C. 该粒子最外电子层已达到相对稳定结构
D. 该粒子可表示为X-
堂堂清:
6.如图中,A、B、C是三种粒子的结构示意图。试回答:
(1)A、B、C中属于同种元素的粒子是_________(写字母编号)
(2)A和B两种粒子的_________________相同,所以它们具有相似的化学性质;在化学反应中它们容易________(填“得到”或“失去”)电子;属于__________(填“金属”或“非金属”)元素。(3)C所表示的粒子是_________(填“原子”或“离子”)。
(4)由于原子核外电子层数与元素所在周期表中的周期数相同,可知B图所表示的元素在元素周期表中应该排在笫_______周期。
班级: 姓名:
课题: 第三章 第2节 原子的结构 第二课时
学习过程(定向导学:教材55 页)---先学后教,当堂训练
流程及学习内容:
一、学习目标
1、知道离子也是构成物质的一种微粒,了解离子的概念。
2、掌握离子的形成过程以及离子的表示方法。
3、掌握离子的分类并会判断原子、阳离子和阴离子。
二、自主学习
1、离子的形成和分类
钠原子的结构示意图为 ;氯原子的结构示意图为 。
钠原子 (“得到”或“失去”) 个电子,达到稳定结构;
氯原子 (“得到”或“失去”) 个电子,达到稳定结构;
这种 的原子(或原子团)叫离子;带正电荷的原子叫 ,带负电荷的原子叫 。离子也是构成物质的一种 。
归纳: 离子(失去电子,带正电荷)
原子 离子
离子(得到电子,带负电荷)
离子的表示方法:
① 离子结构示意图:钠离子 ;氯离子 。
②离子符号:Na+表示1个钠离子带1个单位的正电荷,Cl-表示1个氯离子带1个单位的负电荷。
三、实验探究:请用微观粒子示意图将氯化钠的形成过程描述出来。(用 表示原子核, 表示核外电子)
结论: 的原子叫离子;带正电荷的原子叫 ,带负电荷的原子叫 。氯化钠这种物质由 构成。
交流反思:寻找原子的最外层电子数与元素化学性质的关系
示例元素 最外层电子数 在化学反应中易得(或失)电子 形成离子类型及结构示意图 与之相同的稀有气体元素稳定结构
1 易失 个电子 阳离子:
易 2个电子 离子:
3 易 个电子 离子:
6 易 个电子 离子:
易 个电子 离子:
易 个电子 离子:
结论:元素的化学性质由 决定。最外层电子数<4,易失去电子,形成 离子;最外层电子数>4,易得到电子,形成 离子。最外层电子为 时,元素为稳定结构。
当堂训练:
1、下面是4位同学对分子、原子、离子的描述,其中正确的是( )
A.B.C.D.
2.下列是几种粒子的结构示意图,有关说法正确的是( )。
A. ①和②两种粒子的化学性质相似 B. ③和④均属于离子结构示意图
C. 粒子②在化学反应中容易失去电子 D. ①②③④共表示四种元素的粒子
3.下列各组是元素的原子结构示意图,其中具有相似化学性质的一对元素是( )
A.B.C. D.
4.下列关于四种粒子的结构示意图的说法中正确的是
A.①③属于不同种元素 B.④属于离子,离子符号为Mg2+
C.②③的化学性质相似 D.①表示的氯原子
5.如图是元素X的一种粒子结构示意图,下列说法正确的是( )。
A. X是非金属元素
B. X的原子最外层电子数为8
C. 该粒子最外电子层已达到相对稳定结构
D. 该粒子可表示为X-
堂堂清:
6.如图中,A、B、C是三种粒子的结构示意图。试回答:
(1)A、B、C中属于同种元素的粒子是_________(写字母编号)
(2)A和B两种粒子的_________________相同,所以它们具有相似的化学性质;在化学反应中它们容易________(填“得到”或“失去”)电子;属于__________(填“金属”或“非金属”)元素。(3)C所表示的粒子是_________(填“原子”或“离子”)。
(4)由于原子核外电子层数与元素所在周期表中的周期数相同,可知B图所表示的元素在元素周期表中应该排在笫_______周期。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
