4.1.1人类对原子结构的认识 课件(共65张PPT)2023-2024学年高一化学课件(人教版2019必修第一册)
文档属性
| 名称 | 4.1.1人类对原子结构的认识 课件(共65张PPT)2023-2024学年高一化学课件(人教版2019必修第一册) |

|
|
| 格式 | pptx | ||
| 文件大小 | 58.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-05 00:00:00 | ||
图片预览








文档简介
(共65张PPT)
现代原子物理学的奠基者卢瑟福对思考极为推崇。
一天深夜,他偶然发现一位学生还在埋头实验,便好奇地问:“上午你在干什么?”学生回答:“在做实验。”,“下午呢?”,“做实验。”卢瑟福不禁皱起了眉头,继续追问:“那晚上呢?”,也在做实验。
勤奋的学生以为能够得到导师的一番夸奖,没想到卢瑟福居然大为光火,厉声斥责:“你一天到晚都在做实验,什么时间用于思考呢?”。
被训斥的勤奋
历史上第一个控制和移动单个原子的人——Donald Mark Eigler
原子书法
1989年11月11日,Eigler和他的团队用自制的显微镜用了22小时,将35个氙原子拼写出了“I、B、M”三个字母。
人类对原子结构的认识
原子结构的探索之路
质量数
核素
同位素
4
1
2
3
学
习
目
标
原子结构的探索之路
1
化学史话
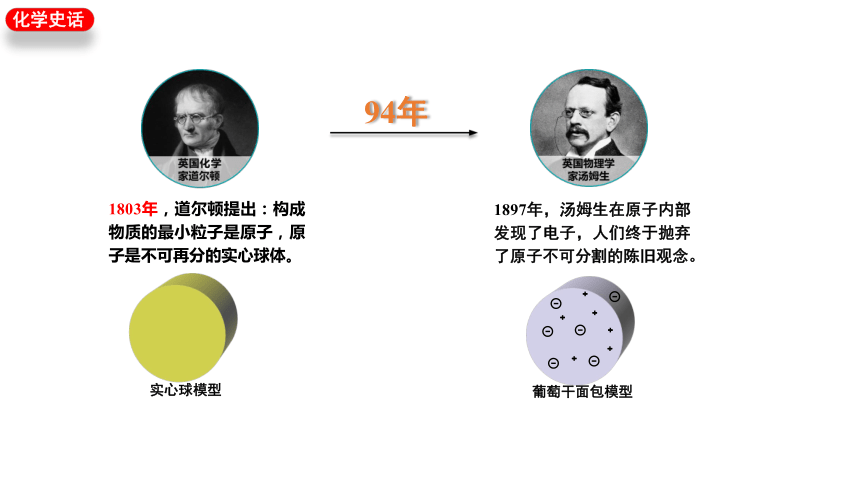
1803年,道尔顿提出:构成物质的最小粒子是原子,原子是不可再分的实心球体。
实心球模型
1897年,汤姆生在原子内部发现了电子,人们终于抛弃了原子不可分割的陈旧观念。
葡萄干面包模型
94年
化学史话
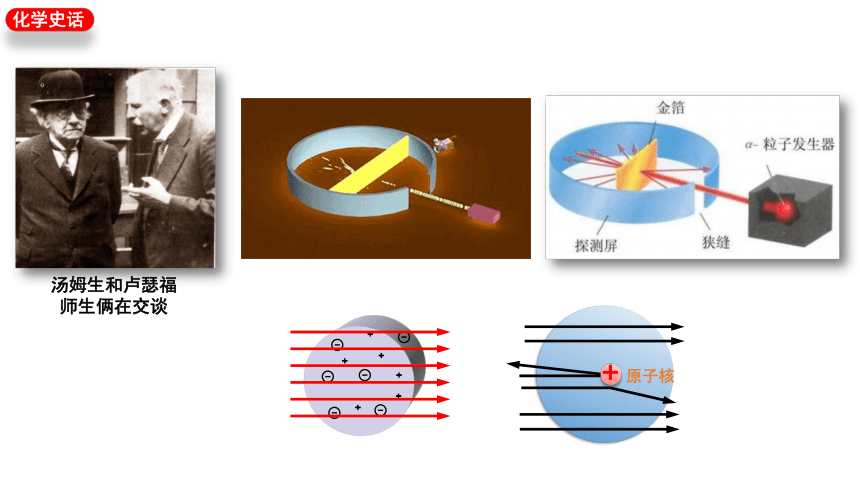
汤姆生和卢瑟福
师生俩在交谈
+
原子核
实验室中的卢瑟福
1908年诺贝尔化学奖
卢瑟福发牢骚说,他搞了一辈子物理学,却在几天之内变成一个化学家了,这是我一生中绝妙的一次玩笑!
化学史话
1911年,卢瑟福通过精密的实验证明在原子中心有一个极小的核,电子绕核做高速旋转。
行星有核模型
丹麦科学家
玻尔
1911年,在卢瑟福模型的基础上,提出了电子在核外的量子化轨道,解决了原子结构的稳定性问题。
玻尔原子模型
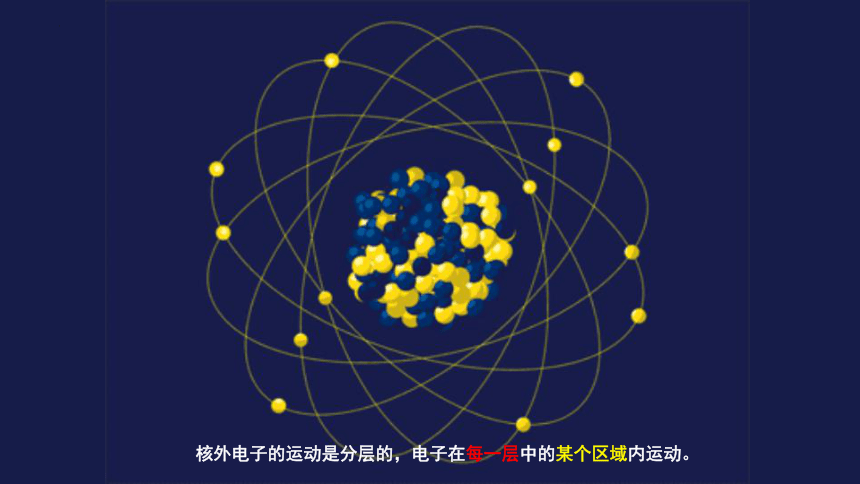
核外电子的运动是分层的,电子在每一层中的某个区域内运动。
核外电子的运动是分层的,电子在每一层中的某个区域内运动。
原子核
电子层
电子在固定的轨道上分层运动
原子结构模型的演变
1
1803
道尔顿
原子学说
1904
汤姆生
葡萄干面包
1911
卢瑟福
核式原子
1913
玻 尔
电子分层排布
1926
电子云
历史的脚步 铭记这一刻
原子结构模型的演变
1
道尔顿
核式原子结构模型
玻尔
量子力学
01
02
03
中学时代的查德威克并未显现出过人天赋。他沉默寡言,成绩平平,但坚持自己的信条:会做则必须做对,一丝不苟;不会做又没弄懂,绝不下笔。因此他有时不能按期完成物理作业。而正是他这种不骛虚荣、实事求是、“驽马十驾,功在不舍”的精神,使他在科学研究事业中受益一生。
学习
一些科学家在研究中发现,原子核的正电荷数与它的质量居然不相等!也就是说,原子核除去含有带正电荷的质子外,还应该含有其他的粒子。那么,那种“其他的粒子”是什么呢?他解决了这一物理难题,发现那种“其他的粒子”是“中子”。
成就
1935年诺贝尔物理学奖。
荣誉
化学趣史
查得维克
电子在核外做无规则的高速运转
现代原子结构
电子
中子
质子
原子核
1.6726×10-27kg
9.109×10-31kg
1.6749×10-27kg
质量很小,可忽略不计
原子的质量主要集中在原子核上
原子质量≈原子核质量=质子的质量+中子的质量
原子
原子核
电子
质子
中子
带一个单位正电荷
带一个单位负电荷
不带电
原子中含有带电的粒子,为何原子不显电性?
质子数(Z)=核电荷数=核外电子数
对原子而言
战争狂人美梦灭
1942年2月的一天清晨,当纳粹德国满载重水的“开特罗”号火轮渡船正准备横渡挪威的廷斯佐湖的时候,突然一声低沉的爆炸声自甲板下传出来,船身立即倾斜,5分钟后便沉入湖底。
船上装载的被战争狂人希特勒视为无价之宝的重水顷刻间也溶入茫茫湖水。
使希特勒梦想制造第一枚原子弹的计划彻底破灭。
重水与普通水看起来十分相像,是无臭无味的液体。
重水与普通水有何不同?
普通水能够滋养生命,培育万物,而重水则不能使种子发芽。人和动物若是喝了重水,还会引起死亡。
重水的特殊价值体现在原子能技术应用中。制造威力巨大的核武器,就需要重水来作为原子核裂变反应中的减速剂,作中子的减速剂。
重水趣史
密度
重水与普通水有何不同?
1.056 g/cm3
3.8℃
重水趣史
1.000 g/cm3
101.42℃
0℃
100℃
沸点
冰点
认识质量数
2
原子质量很小,使用不方便,人们采取了什么方式来表示?
知识回顾
构成原子微粒 电子 原子核
质子 中子
电量 1.6×10-19C 1.6×10-19C 0
质量/kg 9.109×10-31 1.673×10-27 1.675×10-27
相对质量
=1/1 836
=1.007
1.008
资料在线
Ar=
=
=
=
=
Z×1.007
+
N×1.008
=
Z+N
质量数
2
概念
将原子核内所有的质子和中子的相对质量取整数,
加起来所得的数值
符号
A
原子组成
X
Z
A
X
A
Z
——元素符号
质量数 ——
核电荷数 ——
(核内质子数)
含义:代表一个质量数为A、质子数为Z的原子。
质量数
2
概念
将原子核内所有的质子和中子的相对质量取整数,
加起来所得的数值
符号
A
原子组成
数量关系
X
Z
A
A.所含质子数为A-n
B.所含中子数为A+n
C.所含电子数为Z-n
D.质量数为A+Z
某微粒用 表示,下列关于该微粒的叙述正确的是
考考你自己
原子
原子核
核外电子
质子
中子
Z 个
(A-Z)个
Z 个
组成原子的粒子间关系
1.质子数为35、中子数为45的溴原子:
2.中子数为146、质子数为92的铀(U)原子:
3.中子数为20的氯原子:
4.质子数为53、中子数为78的碘原子:
请判断以下说法是否正确?
5.中子数为18的氯原子:
考考你自己
请完成下表:
核符号 质子数(Z) 中子数(N) 电子数(e-) 质量数(A)
11 23
12
35
17
12
11
23
18
17
请你试一试
11
10
17
20
18
37
阳离子:核外电子数=质子数-电荷数
阴离子:核外电子数=质子数+电荷数
核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学诊断等高科技领域。已知只有质子数或中子数为奇数的原子核有NMR现象。试判断下列哪种原子不能产生NMR现象
A.
B.
C.
D.
学以致用
同一元素的原子,其质子数相同,那么其中子数是否也相同?
认识核素
3
都是中子惹的祸
氢元素的三种原子
原子
名称
——
符号
1H
1
1H
2
1H
3
氕(pie)
氘(dao)
氚(chuan)
重氢
超重氢
H
D
T
氢元素的三种原子
重水
碳元素的三种原子
氧元素的三种原子
问题解决
每种原子都有:
具有一定数目质子和一定数目中子
核素
3
概念
具有一定数目质子和一定数目中子的一种原子
每种原子就是一核素
三种核素间是何关系
氢元素的三种原子
原子的“孪生兄弟”—同位素
3
原子
名称
——
符号
氕(pie)
氘(dao)
氚(chuan)
重氢
超重氢
H
D
T
核素
1 1 1
0 1 2
问题解决
1H
1
1H
2
1H
3
氢元素的三种核素
相同
不同
同位素
3
3.1 概念
质子数相同
而中子数不同的
核素
互称同位素
O
8
16
O
8
17
O
8
18
并非所有的元素都有同位素
Na、Al、F等没有
01
02
03
少年时就立志将来作一位有成就的科学家,为此,从小学到大学他都努力学习,学习成绩年年优秀,还曾多次获得奖学金,1898年,他以荣获一级荣誉学位的优异成绩毕业于牛津大学。
学习
索迪刚出校门不久,就很幸运地成为卢瑟福的助手。 1910年提出了一个著名的概念——同位素。由于他对现代化学和物理学发展的卓越贡献,他的名字将永远和同位素联系在一起。
成就
1921年诺贝尔化学奖。
荣誉
化学趣史
查得维克
英国科学家
索迪
1910年提出了一个著名的概念。
1921年获得了诺贝尔化学奖
化学趣史
19世纪、20世纪之交发生的物理因此而生长出一批富有活力的新学科,促成了一系列新技术和新的实验手段的出现,揭开了现代自然科学的序幕,在这场伟大的科技革命中,一些化学家也建立了永载史册的业绩,卢瑟福、居里夫人、索迪就是其中的代表。
1913年发现了放射性元素的位移规律,为放射化学、核物理学这两门新学科的建立奠定了重要基础。
同位素
同位素
氢元素
核素1
……
核素n
同位素
元素
概念辨析
同位素
两特征
同一元素的各同位素的化学性质几乎相同
天然存在的元素里,不论是游离态还是化合态,各同位素原子所占原子的百分比一般是不变的。
如下是四位同学学习原子结构知识后,对这节内容的认识,你认为不正确的是
你学会了吗?
“玉兔”号月球车用 作为热源材料。下列关于Pu的说法正确的是
A. 与 互为同位素
B. 与 为两种元素
C. 与 具有完全相同的化学性质
D. 与 具有相同的最外层电子数
成功体验
同位素分离器
1934年尤里因发现重氢而获得1934年诺贝尔化学奖
吉奥克首先发现了自然界的氧有16O、17O、18O三种同位素
化学史话
3.2 应用
同位素
3
利用放射性
医学诊断、检查金属有无沙眼或裂纹
利用核反应能量
原子弹、核潜艇
利用示踪性
古董鉴定、测定年代、化学分析
中国这具尸体
日本只求一根头发丝,美国用月球土壤换,都遭拒绝
1972年马王堆古尸
化学趣史
这节课我学到了什么?
(用一句话表示)
还有什么疑问?
课堂小结
道尔顿原子实模型
葡萄干面包式原子模型
核式原子模型
电子分层排布模型
原子四种模型
原子的组成和质量数
元素、核素、同位素
元素
核素1
……
核素n
具有一定数目的质子和一定数目的中子的一种原子
质子数相同,中子数不同的同一元素的不同核素的互称
具有相同的核电荷数的同一类原子的总称
一种元素可能有多种不同的核素
三关系
数量关系
质量关系
电性关系
<
Rm+:e-=Z-m
Rn-:e-=Z+n
原子、元素、核素、同位素等都是重要的化学基本概念。下列八种化学符号:
、 、 、 、 、 、 、 。
(1)涉及到的核素共有____种。
(2)互为同位素的是______和______。
(3)质量数相等,但不能互称为同位素的是______和_____。
(4)中子数相等,但质子数不相等的是_____和_____。
8
看我七十二变
以下说法中,正确的是_____
⑤
①标准状况下,22.4 L DT含中子数为2NA
②20 g重水(D2O)中的中子数为8NA
③常温常压下,18.0 g 重水(D2O)所含的电子数约为10×6.02×1023
④12 g 13C含有的中子数为7NA
⑤9 g水含质子数为5NA
⑥1 mol 核素,含有235NA个中子
看谁做得既准又快
孙先辉制作
学好原子结构,更好理解物质性质
现代原子物理学的奠基者卢瑟福对思考极为推崇。
一天深夜,他偶然发现一位学生还在埋头实验,便好奇地问:“上午你在干什么?”学生回答:“在做实验。”,“下午呢?”,“做实验。”卢瑟福不禁皱起了眉头,继续追问:“那晚上呢?”,也在做实验。
勤奋的学生以为能够得到导师的一番夸奖,没想到卢瑟福居然大为光火,厉声斥责:“你一天到晚都在做实验,什么时间用于思考呢?”。
被训斥的勤奋
历史上第一个控制和移动单个原子的人——Donald Mark Eigler
原子书法
1989年11月11日,Eigler和他的团队用自制的显微镜用了22小时,将35个氙原子拼写出了“I、B、M”三个字母。
人类对原子结构的认识
原子结构的探索之路
质量数
核素
同位素
4
1
2
3
学
习
目
标
原子结构的探索之路
1
化学史话
1803年,道尔顿提出:构成物质的最小粒子是原子,原子是不可再分的实心球体。
实心球模型
1897年,汤姆生在原子内部发现了电子,人们终于抛弃了原子不可分割的陈旧观念。
葡萄干面包模型
94年
化学史话
汤姆生和卢瑟福
师生俩在交谈
+
原子核
实验室中的卢瑟福
1908年诺贝尔化学奖
卢瑟福发牢骚说,他搞了一辈子物理学,却在几天之内变成一个化学家了,这是我一生中绝妙的一次玩笑!
化学史话
1911年,卢瑟福通过精密的实验证明在原子中心有一个极小的核,电子绕核做高速旋转。
行星有核模型
丹麦科学家
玻尔
1911年,在卢瑟福模型的基础上,提出了电子在核外的量子化轨道,解决了原子结构的稳定性问题。
玻尔原子模型
核外电子的运动是分层的,电子在每一层中的某个区域内运动。
核外电子的运动是分层的,电子在每一层中的某个区域内运动。
原子核
电子层
电子在固定的轨道上分层运动
原子结构模型的演变
1
1803
道尔顿
原子学说
1904
汤姆生
葡萄干面包
1911
卢瑟福
核式原子
1913
玻 尔
电子分层排布
1926
电子云
历史的脚步 铭记这一刻
原子结构模型的演变
1
道尔顿
核式原子结构模型
玻尔
量子力学
01
02
03
中学时代的查德威克并未显现出过人天赋。他沉默寡言,成绩平平,但坚持自己的信条:会做则必须做对,一丝不苟;不会做又没弄懂,绝不下笔。因此他有时不能按期完成物理作业。而正是他这种不骛虚荣、实事求是、“驽马十驾,功在不舍”的精神,使他在科学研究事业中受益一生。
学习
一些科学家在研究中发现,原子核的正电荷数与它的质量居然不相等!也就是说,原子核除去含有带正电荷的质子外,还应该含有其他的粒子。那么,那种“其他的粒子”是什么呢?他解决了这一物理难题,发现那种“其他的粒子”是“中子”。
成就
1935年诺贝尔物理学奖。
荣誉
化学趣史
查得维克
电子在核外做无规则的高速运转
现代原子结构
电子
中子
质子
原子核
1.6726×10-27kg
9.109×10-31kg
1.6749×10-27kg
质量很小,可忽略不计
原子的质量主要集中在原子核上
原子质量≈原子核质量=质子的质量+中子的质量
原子
原子核
电子
质子
中子
带一个单位正电荷
带一个单位负电荷
不带电
原子中含有带电的粒子,为何原子不显电性?
质子数(Z)=核电荷数=核外电子数
对原子而言
战争狂人美梦灭
1942年2月的一天清晨,当纳粹德国满载重水的“开特罗”号火轮渡船正准备横渡挪威的廷斯佐湖的时候,突然一声低沉的爆炸声自甲板下传出来,船身立即倾斜,5分钟后便沉入湖底。
船上装载的被战争狂人希特勒视为无价之宝的重水顷刻间也溶入茫茫湖水。
使希特勒梦想制造第一枚原子弹的计划彻底破灭。
重水与普通水看起来十分相像,是无臭无味的液体。
重水与普通水有何不同?
普通水能够滋养生命,培育万物,而重水则不能使种子发芽。人和动物若是喝了重水,还会引起死亡。
重水的特殊价值体现在原子能技术应用中。制造威力巨大的核武器,就需要重水来作为原子核裂变反应中的减速剂,作中子的减速剂。
重水趣史
密度
重水与普通水有何不同?
1.056 g/cm3
3.8℃
重水趣史
1.000 g/cm3
101.42℃
0℃
100℃
沸点
冰点
认识质量数
2
原子质量很小,使用不方便,人们采取了什么方式来表示?
知识回顾
构成原子微粒 电子 原子核
质子 中子
电量 1.6×10-19C 1.6×10-19C 0
质量/kg 9.109×10-31 1.673×10-27 1.675×10-27
相对质量
=1/1 836
=1.007
1.008
资料在线
Ar=
=
=
=
=
Z×1.007
+
N×1.008
=
Z+N
质量数
2
概念
将原子核内所有的质子和中子的相对质量取整数,
加起来所得的数值
符号
A
原子组成
X
Z
A
X
A
Z
——元素符号
质量数 ——
核电荷数 ——
(核内质子数)
含义:代表一个质量数为A、质子数为Z的原子。
质量数
2
概念
将原子核内所有的质子和中子的相对质量取整数,
加起来所得的数值
符号
A
原子组成
数量关系
X
Z
A
A.所含质子数为A-n
B.所含中子数为A+n
C.所含电子数为Z-n
D.质量数为A+Z
某微粒用 表示,下列关于该微粒的叙述正确的是
考考你自己
原子
原子核
核外电子
质子
中子
Z 个
(A-Z)个
Z 个
组成原子的粒子间关系
1.质子数为35、中子数为45的溴原子:
2.中子数为146、质子数为92的铀(U)原子:
3.中子数为20的氯原子:
4.质子数为53、中子数为78的碘原子:
请判断以下说法是否正确?
5.中子数为18的氯原子:
考考你自己
请完成下表:
核符号 质子数(Z) 中子数(N) 电子数(e-) 质量数(A)
11 23
12
35
17
12
11
23
18
17
请你试一试
11
10
17
20
18
37
阳离子:核外电子数=质子数-电荷数
阴离子:核外电子数=质子数+电荷数
核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学诊断等高科技领域。已知只有质子数或中子数为奇数的原子核有NMR现象。试判断下列哪种原子不能产生NMR现象
A.
B.
C.
D.
学以致用
同一元素的原子,其质子数相同,那么其中子数是否也相同?
认识核素
3
都是中子惹的祸
氢元素的三种原子
原子
名称
——
符号
1H
1
1H
2
1H
3
氕(pie)
氘(dao)
氚(chuan)
重氢
超重氢
H
D
T
氢元素的三种原子
重水
碳元素的三种原子
氧元素的三种原子
问题解决
每种原子都有:
具有一定数目质子和一定数目中子
核素
3
概念
具有一定数目质子和一定数目中子的一种原子
每种原子就是一核素
三种核素间是何关系
氢元素的三种原子
原子的“孪生兄弟”—同位素
3
原子
名称
——
符号
氕(pie)
氘(dao)
氚(chuan)
重氢
超重氢
H
D
T
核素
1 1 1
0 1 2
问题解决
1H
1
1H
2
1H
3
氢元素的三种核素
相同
不同
同位素
3
3.1 概念
质子数相同
而中子数不同的
核素
互称同位素
O
8
16
O
8
17
O
8
18
并非所有的元素都有同位素
Na、Al、F等没有
01
02
03
少年时就立志将来作一位有成就的科学家,为此,从小学到大学他都努力学习,学习成绩年年优秀,还曾多次获得奖学金,1898年,他以荣获一级荣誉学位的优异成绩毕业于牛津大学。
学习
索迪刚出校门不久,就很幸运地成为卢瑟福的助手。 1910年提出了一个著名的概念——同位素。由于他对现代化学和物理学发展的卓越贡献,他的名字将永远和同位素联系在一起。
成就
1921年诺贝尔化学奖。
荣誉
化学趣史
查得维克
英国科学家
索迪
1910年提出了一个著名的概念。
1921年获得了诺贝尔化学奖
化学趣史
19世纪、20世纪之交发生的物理因此而生长出一批富有活力的新学科,促成了一系列新技术和新的实验手段的出现,揭开了现代自然科学的序幕,在这场伟大的科技革命中,一些化学家也建立了永载史册的业绩,卢瑟福、居里夫人、索迪就是其中的代表。
1913年发现了放射性元素的位移规律,为放射化学、核物理学这两门新学科的建立奠定了重要基础。
同位素
同位素
氢元素
核素1
……
核素n
同位素
元素
概念辨析
同位素
两特征
同一元素的各同位素的化学性质几乎相同
天然存在的元素里,不论是游离态还是化合态,各同位素原子所占原子的百分比一般是不变的。
如下是四位同学学习原子结构知识后,对这节内容的认识,你认为不正确的是
你学会了吗?
“玉兔”号月球车用 作为热源材料。下列关于Pu的说法正确的是
A. 与 互为同位素
B. 与 为两种元素
C. 与 具有完全相同的化学性质
D. 与 具有相同的最外层电子数
成功体验
同位素分离器
1934年尤里因发现重氢而获得1934年诺贝尔化学奖
吉奥克首先发现了自然界的氧有16O、17O、18O三种同位素
化学史话
3.2 应用
同位素
3
利用放射性
医学诊断、检查金属有无沙眼或裂纹
利用核反应能量
原子弹、核潜艇
利用示踪性
古董鉴定、测定年代、化学分析
中国这具尸体
日本只求一根头发丝,美国用月球土壤换,都遭拒绝
1972年马王堆古尸
化学趣史
这节课我学到了什么?
(用一句话表示)
还有什么疑问?
课堂小结
道尔顿原子实模型
葡萄干面包式原子模型
核式原子模型
电子分层排布模型
原子四种模型
原子的组成和质量数
元素、核素、同位素
元素
核素1
……
核素n
具有一定数目的质子和一定数目的中子的一种原子
质子数相同,中子数不同的同一元素的不同核素的互称
具有相同的核电荷数的同一类原子的总称
一种元素可能有多种不同的核素
三关系
数量关系
质量关系
电性关系
<
Rm+:e-=Z-m
Rn-:e-=Z+n
原子、元素、核素、同位素等都是重要的化学基本概念。下列八种化学符号:
、 、 、 、 、 、 、 。
(1)涉及到的核素共有____种。
(2)互为同位素的是______和______。
(3)质量数相等,但不能互称为同位素的是______和_____。
(4)中子数相等,但质子数不相等的是_____和_____。
8
看我七十二变
以下说法中,正确的是_____
⑤
①标准状况下,22.4 L DT含中子数为2NA
②20 g重水(D2O)中的中子数为8NA
③常温常压下,18.0 g 重水(D2O)所含的电子数约为10×6.02×1023
④12 g 13C含有的中子数为7NA
⑤9 g水含质子数为5NA
⑥1 mol 核素,含有235NA个中子
看谁做得既准又快
孙先辉制作
学好原子结构,更好理解物质性质
