【核心素养目标】人教版(2019)高一化学必修第一册1.1 物质的分类及转化(第3课时 物质的转化)
文档属性
| 名称 | 【核心素养目标】人教版(2019)高一化学必修第一册1.1 物质的分类及转化(第3课时 物质的转化) |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.7MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-06 00:00:00 | ||
图片预览




文档简介
(共21张PPT)
第一节 物质的分类及转化
第3课时 物质的转化
人教版必修第一册
学习目标
1.通过物质的宏观特征入手理解物质的性质及其转化。
2.熟悉酸、碱、盐、氧化物间的转化关系。
学习目标
1.通过典型物质的性质,能对酸、碱、盐、氧化物及它们之间反应进行描述和符号表征,培养“宏观辨识与微观探析”的核心素养。
2.通过归纳相关物质间的化学反应关系,建立物质转化模型,认识物质的变化规律,培养“变化观念与模型认知”的核心素养。
素养目标
情境引入
在丰富多彩的化学物质中,为了获得生活和发展需要的新物质,并更好地利用这些物质为人类服务, 化学家们需要将众多的物质进行分类研究,需要探索物质转化的条件和转化时所遵循的规律。
教学过程
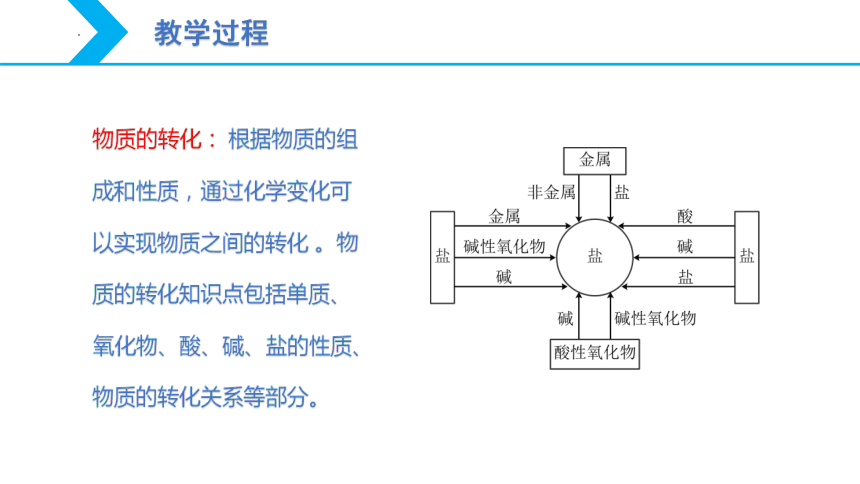
物质的转化: 根据物质的组成和性质,通过化学变化可以实现物质之间的转化 。物质的转化知识点包括单质、氧化物、酸、碱、盐的性质、物质的转化关系等部分。
教学过程
一、酸、碱、盐的性质
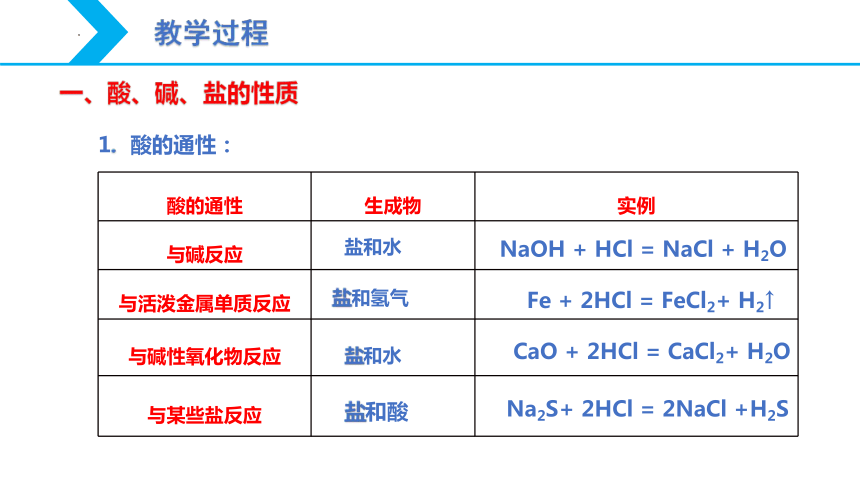
酸的通性 生成物 实例
与碱反应
与活泼金属单质反应
与碱性氧化物反应
与某些盐反应
盐和水
盐和氢气
盐和水
盐和酸
NaOH + HCl = NaCl + H2O
Fe + 2HCl = FeCl2+ H2↑
CaO + 2HCl = CaCl2+ H2O
Na2S+ 2HCl = 2NaCl +H2S
1. 酸的通性:
教学过程
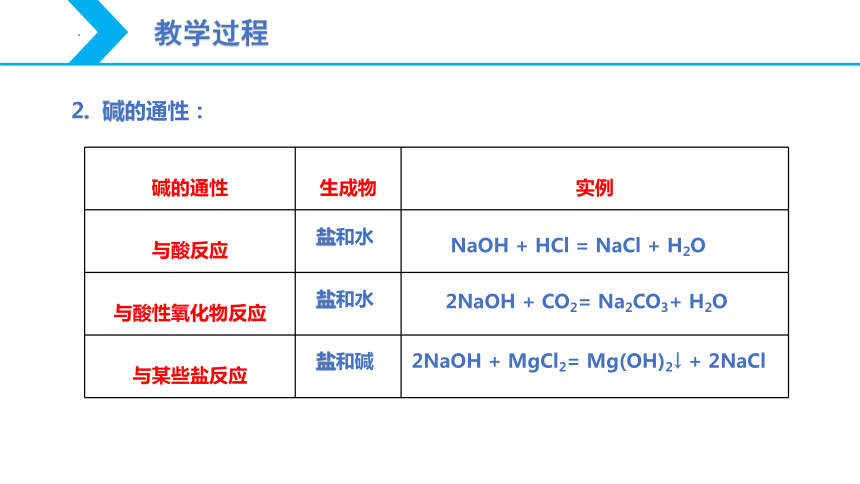
碱的通性 生成物 实例
与酸反应
与酸性氧化物反应
与某些盐反应
盐和水
盐和水
盐和碱
NaOH + HCl = NaCl + H2O
2NaOH + CO2= Na2CO3+ H2O
2NaOH + MgCl2= Mg(OH)2↓ + 2NaCl
2. 碱的通性:
教学过程
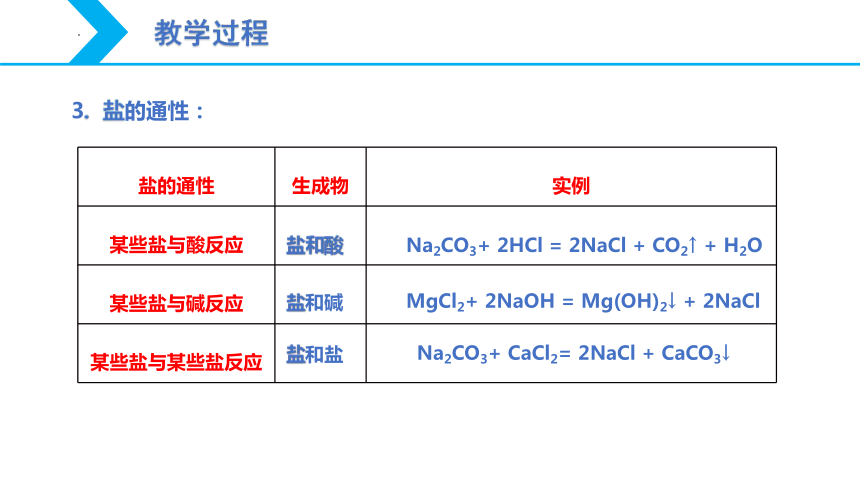
盐的通性 生成物 实例
某些盐与酸反应
某些盐与碱反应
某些盐与某些盐反应
盐和碱
盐和酸
盐和盐
Na2CO3+ 2HCl = 2NaCl + CO2↑ + H2O
MgCl2+ 2NaOH = Mg(OH)2↓ + 2NaCl
Na2CO3+ CaCl2= 2NaCl + CaCO3↓
3. 盐的通性:
教学过程
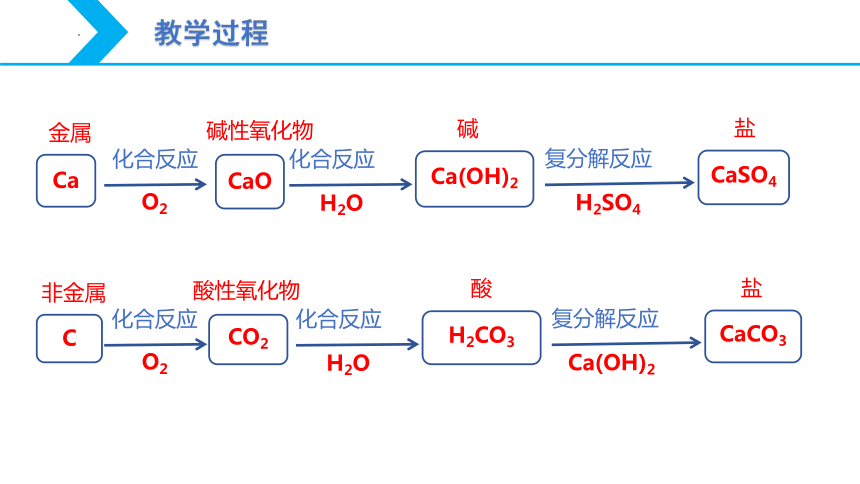
二、物质的转化
教学过程
Ca
CaO
Ca(OH)2
CaSO4
金属
碱性氧化物
碱
盐
H2O
化合反应
化合反应
O2
H2SO4
复分解反应
C
CO2
H2CO3
CaCO3
非金属
酸性氧化物
酸
盐
H2O
化合反应
化合反应
O2
Ca(OH)2
复分解反应
教学过程
物质转化的一般流程
思维模型
教学过程
物质转化模型可以直观而简明地表达不同类型物质间的转化关系。通过转化关系,可以确定制取某类物质的可能方法。
物质转化模型
“两条主线通到底 四条横线相联系 六条交叉成网络”
教学过程
三、物质的转化的应用
在工业生产中,除了要考虑反应进行的可能性,还要考虑原料来源、成本和设备要求等因素,以选取最恰当的方法。
氢氧化钠的制备
途径(方法)
选择因素
①氧化钠与水反应
②碳酸钠与氢氧化钙反应
③电解饱和食盐水等
④盐 (如 Na2CO3)与 碱 [如 Ca(OH)2]反应
考虑成本
电解饱和食盐水
反应的可能性、原料来源、成本高低、设备要求等方面来选择物质制备的适宜方法。
课堂练习
典例1.
奥运五环代表着全世界五大洲的人民团结在一起。下列各项中的物质,能满足如图所示中阴影部分关系的是( )
① ② ③ ④
A NaCl K2SO4 KCl (NH4)2SO4
B Na2SO4 K2SO4 KCl NH4Cl
C NaCl K2SO4 KCl NH4Cl
D Na2SO4 K2SO4 KCl (NH4)2SO4
【答案】B
【解析】①中此盐既属于钠盐又属于硫酸盐。则可排除A、C两选项,④中此盐既属于铵盐又属于盐酸盐,则B项中的NH4Cl正确,排除了D项。
课堂练习
典例2.
下图中,“——”表示相连的物质间在一定条件下可以反应,“―→”表示丁在一定条件下通过置换反应可以转化为乙。下列四组选项中,符合图示要求的是( )
选项 甲 乙 丙 丁
A H2SO4 Na2SO4 NaOH NaCl
B BaCl2 K2CO3 HCl KOH
C O2 CO CuO C
D Fe CuCl2 Zn HCl
【答案】C
典例3.
甘肃马家窑遗址出土的青铜刀是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,该“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO2、O2作用产生的,化学式为[Cu2(OH)2CO3],“铜绿”能跟酸反应生成铜盐、CO2和H2O。某同学利用以下反应实现了“铜→铜绿→……→铜”的转化。
(1)从物质分类标准看,“铜绿”属于________(填字母)。
A.酸 B.碱 C.盐 D.氧化物
(2)写出B的化学式:________。
(3)请写出铜绿与盐酸反应的化学方程式:_____________________________。
(4)上述转化过程中属于化合反应的是________,属于氧化还原反应的是________。
课堂练习
课堂练习
课堂练习
“探险队员”——盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质),盐酸必须避开它们,否则就无法通过。
(1)请你帮助盐酸走出迷宫(请用“→”把图中物质前的序号连接起来表示所走的路线): 。
(2)在能“吃掉”盐酸的化学反应中,属于酸碱中和反应的有 个,其中能“吃掉”盐酸的盐是 (写化学式),写出该反应的化学方程式: 。
(3)在不能与盐酸反应的物质中,属于氧化物的是 (填写物质序号,下同),属于单质的是 。
(4)如果将盐酸换成氧气,它能沿着盐酸所走的路线“走出”这个迷宫吗?为什么?
。
典例4.
课堂练习
【答案】(1)③→⑥→⑩→⑦→ →
(2) 2 Na2CO3 Na2CO3+2HCl=2NaCl+H2O+CO2↑
(3) ③⑩ ⑦
(4)不能。因为氧气遇到CO等物质会被“吃掉”
【解析】该题考查盐酸的化学性质。盐酸能与①②④⑤⑧⑨发生反应,与③⑥⑦⑩ 不能反应。(1)图中物质③⑥⑩⑦ 均不与盐酸反应,沿该路线可走出迷宫。(2)盐酸与NaOH、Ca(OH)2的反应属于酸碱中和反应;能“吃掉”盐酸的盐是Na2CO3,该反应的化学方程式为Na2CO3+2HCl===CO2↑+H2O+2NaCl。(3)在不能与盐酸反应的物质中,属于氧化物的是CO2、CO,属于单质的是Cu、Ag。(4)如果将盐酸换成氧气,它不能沿着盐酸所走的路线“走出”这个迷宫,因为氧气遇到一氧化碳、铜、银等物质时会发生反应而被“吃掉”。
课堂小结
课后小任务
认真阅读材料,了解学习与化学相关职业的特点、工作内容、知识背景和就业方向等,立志成为化学专业人才。
感 谢 倾 听
第一节 物质的分类及转化
第3课时 物质的转化
人教版必修第一册
学习目标
1.通过物质的宏观特征入手理解物质的性质及其转化。
2.熟悉酸、碱、盐、氧化物间的转化关系。
学习目标
1.通过典型物质的性质,能对酸、碱、盐、氧化物及它们之间反应进行描述和符号表征,培养“宏观辨识与微观探析”的核心素养。
2.通过归纳相关物质间的化学反应关系,建立物质转化模型,认识物质的变化规律,培养“变化观念与模型认知”的核心素养。
素养目标
情境引入
在丰富多彩的化学物质中,为了获得生活和发展需要的新物质,并更好地利用这些物质为人类服务, 化学家们需要将众多的物质进行分类研究,需要探索物质转化的条件和转化时所遵循的规律。
教学过程
物质的转化: 根据物质的组成和性质,通过化学变化可以实现物质之间的转化 。物质的转化知识点包括单质、氧化物、酸、碱、盐的性质、物质的转化关系等部分。
教学过程
一、酸、碱、盐的性质
酸的通性 生成物 实例
与碱反应
与活泼金属单质反应
与碱性氧化物反应
与某些盐反应
盐和水
盐和氢气
盐和水
盐和酸
NaOH + HCl = NaCl + H2O
Fe + 2HCl = FeCl2+ H2↑
CaO + 2HCl = CaCl2+ H2O
Na2S+ 2HCl = 2NaCl +H2S
1. 酸的通性:
教学过程
碱的通性 生成物 实例
与酸反应
与酸性氧化物反应
与某些盐反应
盐和水
盐和水
盐和碱
NaOH + HCl = NaCl + H2O
2NaOH + CO2= Na2CO3+ H2O
2NaOH + MgCl2= Mg(OH)2↓ + 2NaCl
2. 碱的通性:
教学过程
盐的通性 生成物 实例
某些盐与酸反应
某些盐与碱反应
某些盐与某些盐反应
盐和碱
盐和酸
盐和盐
Na2CO3+ 2HCl = 2NaCl + CO2↑ + H2O
MgCl2+ 2NaOH = Mg(OH)2↓ + 2NaCl
Na2CO3+ CaCl2= 2NaCl + CaCO3↓
3. 盐的通性:
教学过程
二、物质的转化
教学过程
Ca
CaO
Ca(OH)2
CaSO4
金属
碱性氧化物
碱
盐
H2O
化合反应
化合反应
O2
H2SO4
复分解反应
C
CO2
H2CO3
CaCO3
非金属
酸性氧化物
酸
盐
H2O
化合反应
化合反应
O2
Ca(OH)2
复分解反应
教学过程
物质转化的一般流程
思维模型
教学过程
物质转化模型可以直观而简明地表达不同类型物质间的转化关系。通过转化关系,可以确定制取某类物质的可能方法。
物质转化模型
“两条主线通到底 四条横线相联系 六条交叉成网络”
教学过程
三、物质的转化的应用
在工业生产中,除了要考虑反应进行的可能性,还要考虑原料来源、成本和设备要求等因素,以选取最恰当的方法。
氢氧化钠的制备
途径(方法)
选择因素
①氧化钠与水反应
②碳酸钠与氢氧化钙反应
③电解饱和食盐水等
④盐 (如 Na2CO3)与 碱 [如 Ca(OH)2]反应
考虑成本
电解饱和食盐水
反应的可能性、原料来源、成本高低、设备要求等方面来选择物质制备的适宜方法。
课堂练习
典例1.
奥运五环代表着全世界五大洲的人民团结在一起。下列各项中的物质,能满足如图所示中阴影部分关系的是( )
① ② ③ ④
A NaCl K2SO4 KCl (NH4)2SO4
B Na2SO4 K2SO4 KCl NH4Cl
C NaCl K2SO4 KCl NH4Cl
D Na2SO4 K2SO4 KCl (NH4)2SO4
【答案】B
【解析】①中此盐既属于钠盐又属于硫酸盐。则可排除A、C两选项,④中此盐既属于铵盐又属于盐酸盐,则B项中的NH4Cl正确,排除了D项。
课堂练习
典例2.
下图中,“——”表示相连的物质间在一定条件下可以反应,“―→”表示丁在一定条件下通过置换反应可以转化为乙。下列四组选项中,符合图示要求的是( )
选项 甲 乙 丙 丁
A H2SO4 Na2SO4 NaOH NaCl
B BaCl2 K2CO3 HCl KOH
C O2 CO CuO C
D Fe CuCl2 Zn HCl
【答案】C
典例3.
甘肃马家窑遗址出土的青铜刀是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,该“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO2、O2作用产生的,化学式为[Cu2(OH)2CO3],“铜绿”能跟酸反应生成铜盐、CO2和H2O。某同学利用以下反应实现了“铜→铜绿→……→铜”的转化。
(1)从物质分类标准看,“铜绿”属于________(填字母)。
A.酸 B.碱 C.盐 D.氧化物
(2)写出B的化学式:________。
(3)请写出铜绿与盐酸反应的化学方程式:_____________________________。
(4)上述转化过程中属于化合反应的是________,属于氧化还原反应的是________。
课堂练习
课堂练习
课堂练习
“探险队员”——盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质),盐酸必须避开它们,否则就无法通过。
(1)请你帮助盐酸走出迷宫(请用“→”把图中物质前的序号连接起来表示所走的路线): 。
(2)在能“吃掉”盐酸的化学反应中,属于酸碱中和反应的有 个,其中能“吃掉”盐酸的盐是 (写化学式),写出该反应的化学方程式: 。
(3)在不能与盐酸反应的物质中,属于氧化物的是 (填写物质序号,下同),属于单质的是 。
(4)如果将盐酸换成氧气,它能沿着盐酸所走的路线“走出”这个迷宫吗?为什么?
。
典例4.
课堂练习
【答案】(1)③→⑥→⑩→⑦→ →
(2) 2 Na2CO3 Na2CO3+2HCl=2NaCl+H2O+CO2↑
(3) ③⑩ ⑦
(4)不能。因为氧气遇到CO等物质会被“吃掉”
【解析】该题考查盐酸的化学性质。盐酸能与①②④⑤⑧⑨发生反应,与③⑥⑦⑩ 不能反应。(1)图中物质③⑥⑩⑦ 均不与盐酸反应,沿该路线可走出迷宫。(2)盐酸与NaOH、Ca(OH)2的反应属于酸碱中和反应;能“吃掉”盐酸的盐是Na2CO3,该反应的化学方程式为Na2CO3+2HCl===CO2↑+H2O+2NaCl。(3)在不能与盐酸反应的物质中,属于氧化物的是CO2、CO,属于单质的是Cu、Ag。(4)如果将盐酸换成氧气,它不能沿着盐酸所走的路线“走出”这个迷宫,因为氧气遇到一氧化碳、铜、银等物质时会发生反应而被“吃掉”。
课堂小结
课后小任务
认真阅读材料,了解学习与化学相关职业的特点、工作内容、知识背景和就业方向等,立志成为化学专业人才。
感 谢 倾 听
