第二章空气、物质的构成预习自测卷(含答案) ---2023-2024学年九年级化学科粤版(2012)上册
文档属性
| 名称 | 第二章空气、物质的构成预习自测卷(含答案) ---2023-2024学年九年级化学科粤版(2012)上册 |  | |
| 格式 | docx | ||
| 文件大小 | 145.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-06 16:23:57 | ||
图片预览




文档简介
第二章空气、物质的构成 预习自测卷
一、单选题
1.科学家利用“基因剪刀”技术降低了水稻中砷的含量。下图是砷在元素周期表中的部分信息和原子结构示意图,下列关于砷的说法正确的是
A.属于金属元素 B.位于第五周期
C.核内质子数为33 D.相对原子质量为74.92g
2.一种有趣的钟表式元素周期表如图所示,关于时针所对应的元素说法中正确的是( )
A.12:00 对应的元素为非金属元素
B.10:00 对应的元素易形成化合物
C.9:00 对应元素的离子符号为 F+
D.该钟表的整点时间与该元素的质子数相等
3.对下列一些事实的解释不正确的是
事 实 解 释
A 墙内开花墙外香 分子在不断地运动
B 固体酒精和液体酒精都可做燃料 同种分子,性质相同
C 温度计中的水银热胀冷缩 原子的大小发生改变
D 50mL水与50mL酒精混合后总体积小于100mL 分子间有间隔
A.A B.B C.C D.D
4.分子与原子的本质区别在于( )
A.分子是构成物质的一种微粒,而原子构成分子
B.分子比原子大
C.分子能保持物质的化学性质,而原子不能
D.在化学变化中分子可再分,原子不能再分
5.如图是水分解的微观过程,下列叙述正确的一组是
①化学变化中,分子可分,而原子不能再分;化学反应的实质是分子分裂成原子,原子重新组合成新的分子
②分子是构成物质的一种基本微粒;分子是由原子构成的
③水通电分解是化学变化;水分子是保持水化学性质的微粒
④化学反应前后原子的种类和个数不变
A.①②③④ B.①②④ C.①② D.③④
6.下列有关粒子结构示意图的说法正确的是( )
A.③和④的元素在元素周期表中属于同一周期
B.②和⑥形成化合物的化学式为MgO
C.①和②、⑤和⑥的最外层电子数相同,化学性质相似
D.①③④是具有稳定结构的原子
7.保持氧气化学性质的最小微粒是
A.O
B.O2
C.O3
D.CO2
8.过氧化钠(Na2O2)因能与CO2反应生成氧气,故可作为呼吸面具中氧气的来源,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2。以下说法不正确的是( )
A.过氧化钠属于氧化物 B.该反应可用于实验室制取纯净的氧气
C.该反应可用于潜水艇 D.Na2O2应密封保存
9.下图是元素周期表中的一格,依据图中的信息得到的下列认识错误的是
A.该元素原子的质子数为14
B.该元素属于非金属元素
C.该元素一个原子的原子核有14个中子
D.该元素的相对原子质量为28.09g
10.镍在元素周期表中的信息如图所示,下列有关镍元素的说法不正确的是
A.原子序数是28 B.属于金属元素
C.元素符号是Ni D.一个原子的实际质量是58.69 g
11.以下微观粒子中带电荷的是
A.原子核 B.原子
C.分子 D.中子
12.下列关于空气的说法中,错误的是( )
A.氮气约占空气总体积的78%
B.氧气能助燃,可作燃料
C.稀有气体通电时能发出不同颜色的光,可制作电光源
D.空气中的二氧化碳可以用于灭火
13.下列物质属于纯净物的是
A.大理石 B.澄清石灰水 C.食盐水 D.干冰
二、填空题
14.构建模型又常常是我们认识微观世界的重要手段.看下列各组微观模型图回答问题:下列四幅图中用“”、“”、“”表示核电荷数不同的原子,其中能用来表示混合物的是① ;能表示3H2的是② (填图下字母,下同),能用来表示氧化物的是③ ,能用来表示铁这种物质的是④ 。
15.根据下列粒子结构示意图,回答问题:
(1)属于非金属原子的是 。
(2)若E中x=18,则该粒子的名称是 。
(3)若E是阳离子,则E在元素周期表中属于第 周期。
(4)A、B、C、D四种粒子中属于同种元素的是 。
16.下图中的①、②是钙元素、硒元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图。
请回答:
(1)钙元素的原子序数为 ,硒元素的相对原子质量为 。
(2)C所表示粒子的符号为 ,B所表示粒子的符号为 。
(3) A、B、C、D四种粒子中属于同种元素的是 (填序号,下同);原子的最外层电子数相等则元素的化学性质相似,化学性质相似的是 。
(4)从①、②、A、B、C、D中选择适当的元素组成物质,写出符合下列要求的物质的化学式:
①氧化物 ;②非金属单质 (只写一种)。
17.化学知识上存在很多数字,正确回答数字相关问题:
(1)没有说明用量时,液体取 。
(2)给液体加热时,液体体积不超过试管容积的 。
(3)拉瓦锡测定空气中氧气含量,氧气约占空气体积的 。
18.如图中A、B、C、D是四种粒子的结构示意图,E是钙元素在元素周期表中的信息.
请回答下列问题:(填序号)
(1)A.B.C. D四种粒子结构示意图中,属于同种元素的粒子是 ;
(2)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似 ;
(3)D原子中X= ;
(4)从E图中你获得的信息钙元素的相对原子质量为: .
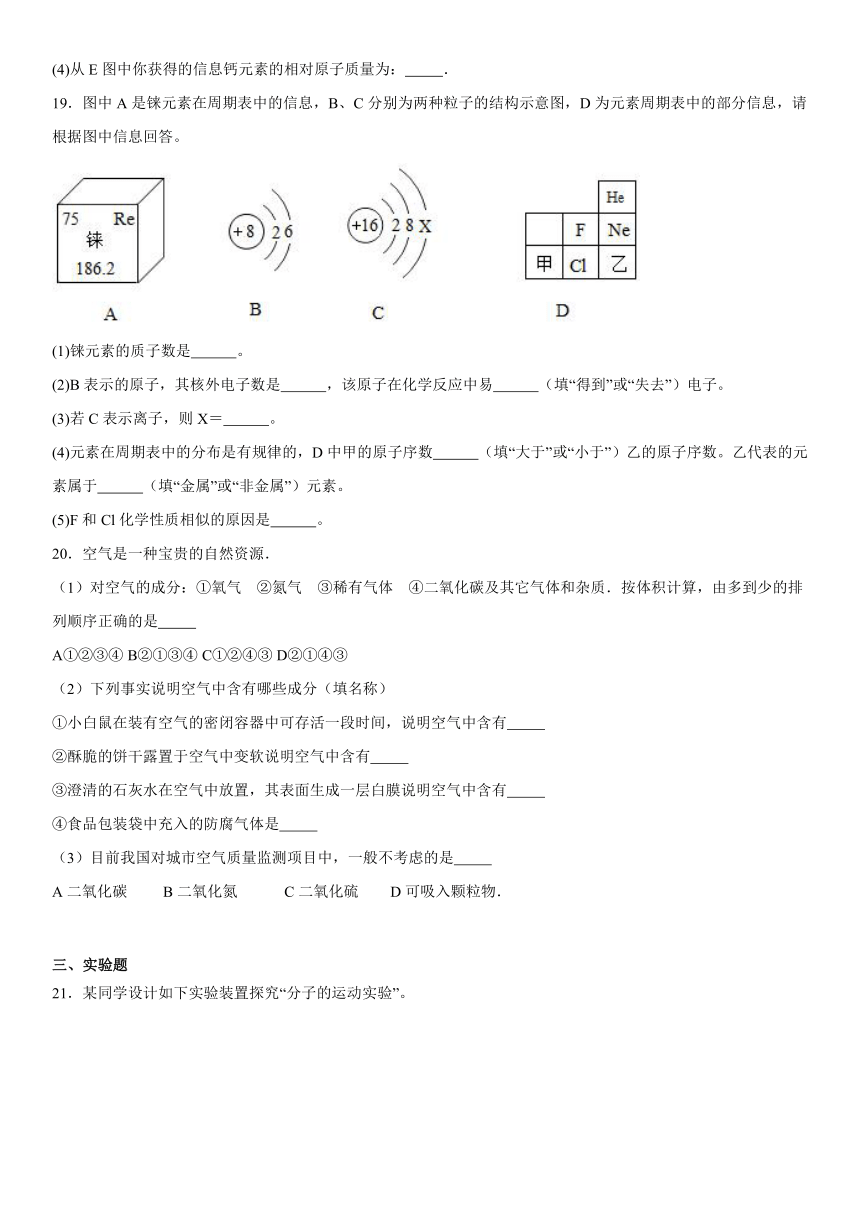
19.图中A是铼元素在周期表中的信息,B、C分别为两种粒子的结构示意图,D为元素周期表中的部分信息,请根据图中信息回答。
(1)铼元素的质子数是 。
(2)B表示的原子,其核外电子数是 ,该原子在化学反应中易 (填“得到”或“失去”)电子。
(3)若C表示离子,则X= 。
(4)元素在周期表中的分布是有规律的,D中甲的原子序数 (填“大于”或“小于”)乙的原子序数。乙代表的元素属于 (填“金属”或“非金属”)元素。
(5)F和Cl化学性质相似的原因是 。
20.空气是一种宝贵的自然资源.
(1)对空气的成分:①氧气 ②氮气 ③稀有气体 ④二氧化碳及其它气体和杂质.按体积计算,由多到少的排列顺序正确的是
A①②③④ B②①③④ C①②④③ D②①④③
(2)下列事实说明空气中含有哪些成分(填名称)
①小白鼠在装有空气的密闭容器中可存活一段时间,说明空气中含有
②酥脆的饼干露置于空气中变软说明空气中含有
③澄清的石灰水在空气中放置,其表面生成一层白膜说明空气中含有
④食品包装袋中充入的防腐气体是
(3)目前我国对城市空气质量监测项目中,一般不考虑的是
A二氧化碳 B二氧化氮 C二氧化硫 D可吸入颗粒物.
三、实验题
21.某同学设计如下实验装置探究“分子的运动实验”。
(1)图I是按老版课本进行的一个化学实验,大烧杯中的实验现象是 ,此实验说明分子 。但是在实验时同学们闻到了一股难闻的刺激性气味,于是小明对原实验装置进行了改进,装置如图Ⅱ,并进行如下操作:
a向B、C二支试管中分别加入5mL的蒸馏水,各滴入滴无色酚酞溶液,振荡,观察溶液颜色。
b在A、D试管中分别加入2mL浓氨水,立即用带橡皮塞的导管按实验图Ⅱ连接好,并将D试管放置在盛有热水的烧杯中,观察几分钟。
(2)【现象记录】BC两试管中的酚酞溶液变色情况是 。【分析讨论】由此可以得到温度与分子运动速率的关系是 。对比改进前的实验,改进后实验的优点是 。
(3)结合上述实验,实验室保存浓氨水等药品时,应注意的事项是 。
22.学习小组利用了数字化实验技术进行了“空气中氧气体积分数测定”再探究(如图1)。实验通过严谨的测定得到数据如下图2。请你根据实验及其数据分析回答下列问题。
(1)写出本实验红磷燃烧的反应化学方程式 。
(2)压强曲线点A表示红磷开始在集气瓶中燃烧。燃烧过程测得其曲线,A→B→C→D→变化呈现先上升后下降的原因是 。
(3)根据图表数据分析,用红磷燃烧的方法不能准确测定空气中氧气的含量。原因是 。
23.按要求回答下列问题。
(1) 向盛有蒸馏水的试管中加5滴酚酞水溶液,无明显现象,再加入浓氨水,会出现 色;
(2) 按图所示进行实验探究,用大烧杯罩住A、C两个小烧杯一段时间后,A烧杯中溶液变色。贝贝同学提出了以下几种假设:
假设1 空气中的氮气使酚酞溶液变色
假设2 空气中的氧气使酚酞溶液变色
假设3 浓氨水中的氨分子运动使酚酞溶液变色
假设4 浓氨水中的水分子运动使酚酞溶液变色
你认为假设 不能成立,理由是 ;
(3) 为了验证剩下几种假设的正确性,小马同学增加了烧杯B作对比实验,烧杯B能够否定假设 的合理性。
参考答案:
1.C
【详解】A. 砷属于非金属元素,此选项错误;
B. 砷原子核外有4个电子层,所以砷元素位于第四周期,此选项错误;
C. 由题中信息可知,砷原子核内质子数为33 ,此选项正确;
D. 相对原子质量是一个比值,单位是“1”,此选项错误。
故选C。
2.D
【详解】A.12:00对应的元素为镁元素,汉字偏旁是“金”的属于金属元素,此选项错误;
B.10:00对应的元素是氖元素,氖元素属于稀有气体元素,化学性质稳定,不易形成化合物,此选项错误;
C.9:00对应元素是氟元素,氟原子的最外层有7个电子,在化学反应中易得到1个电子而形成带有一个单位负电荷的氟离子,离子符号为F﹣,此选项错误;
D.由图示可知,该钟表的整点时间与原子结构中的质子数相等。此选项正确。故选D。
3.C
【详解】A、墙内开花墙外香,是因为花香中含有的分子是在不断运动的,向四周扩散,使人们闻到花香,故选项解释正确。
B、固体酒精和液体酒精都可做燃料,是因为分子构成相同,化学性质相同,故选项解释正确。
C、温度计中的水银热胀冷缩,是因为汞原子间的间隔(而不是大小)随着温度改变而改变,故选项解释错误。
D、50mL水与50mL酒精混合后总体积小于100mL,是因为分子之间有间隔,一部分水分子和酒精分子会互相占据分子之间的间隔,故选项解释正确。
故选:C。
4.D
【详解】化学变化中分子可以分为原子,原子重新组合成新分子;分子原子的本质区别是在化学变化中可否再分;
A、分子是构成物质的一种微粒,而原子可以构成分子,这不是分子与原子的本质区别;
B、分子比原子大,这不是分子与原子的本质区别;
C、分子能保持物质的化学性质,由原子构成的物质,保持物质的化学性质是原子,如铁原子能保持铁的化学性质,但这不是分子与原子的本质区别;
D、在化学变化中分子可再分,原子不能再分,是分子与原子的本质区别;
故选D。
5.A
【详解】①由微粒的变化可知,在化学变化中,分子可分,而原子不能再分;化学反应的实质是分子分裂成原子,原子重新组合成新的分子,叙述正确;
②由微粒的构成可知,分子是构成物质的一种基本微粒;分子是由原子构成的,叙述正确;
③由水分子的变化和水的构成可知,水通电分解是化学变化;水分子是保持水化学性质的微粒,叙述正确;
④由微粒的构成可知,化学反应前后原子的种类和个数不变,元素的种类也不变。故叙述正确;
由以上分析可知:A正确。
故选A。
6.B
【详解】A、③的元素属于第三周期,④的元素属于第二周期元素,故A选项错误;
B、②的元素是镁元素,⑥的元素是氧元素,故形成的化学式为MgO,故B选项正确;
C、①是稀有气体元素、②是金属元素,化学性质不相似,故C选项错误;
D、③是离子结构示意图,故D选项错误。故选B。
7.B
【详解】氧气是由氧分子构成的,保持氧气化学性质的最小微粒是氧分子。故选B。
8.B
【详解】A、过氧化钠(Na2O2)是由两种元素组成的且有一种是氧元素的化合物,属于氧化物,故A正确;
B、根据化学方程式2Na2O2+2CO2=2Na2CO3+O2可知,反应物二氧化碳气体,不能用于实验室制取纯净的氧气,故B错误;
C、在常温下过氧化钠固体与二氧化碳反应生碳酸钠和氧气,常温下即可发生反应,且可把空气中的二氧化碳转化为氧气,供给氧气的同时吸收了人呼出的二氧化碳,该反应用于潜艇供氧节能环保,故C正确;
D、二氧化碳能与过氧化钠反应,Na2O2应密封保存,故D正确。故选B。
【点睛】氧化物的概念可简记为:两元素、氧元素、化合物。
9.D
【详解】A、由信息可知,元素原子的质子数为14,故A正确;B、此元素为硅元素,属于非金属元素,故B正确;C、质子数等于核外电子数,则一个原子的原子核外有14个电子,故C正确;D、元素的相对原子质量为28.09,而不是原子质量,故D错误。故选D。
10.D
【详解】A、根据元素周期表中的一格可知,左上角的数字表示原子序数,该元素的原子序数为26,故选项说法正确;
B、根据元素周期表中的一格可知,中间的汉子表示元素名称,该元素带有“钅”字旁,属于金属元素,故选项说法正确。
C、根据元素周期表中的一格可知,字母表示该元素的元素符号,铁的元素符号是“Ni”,故选项说法正确;
D、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为55. 85,故选项说法错误。
故选:D。
11.A
【详解】A、原子核带正电,符合题意;B、原子不显电性,不符合题意;C、分子不显电性,不符合题意;D、中子不显电性,不符合题意;故选A。
12.B
【详解】A、空气中,氧气约占空气总体积的21%,故正确;
B、氧气可以支持燃烧,说明氧气具有助燃性,而不是可燃性,不能作燃料,故错误;
C、稀有气体通电时能发出不同颜色的光,可制成多种用途的电光源,故正确;
D、二氧化碳既不能燃烧也不支持燃烧,密度比空气大,常用来灭火,故正确。
故选B。
13.D
【详解】A、大理石主要成分碳酸钙,还含有其他杂质,是混合物。
B、澄清石灰水是氢氧化钙和水组成的混合物。
C、食盐水是水和氯化钠组成的混合物。
D、干冰是固态二氧化碳,是纯净物。
故选D。
14. C B A D
【详解】由微粒的构成可知:
①C物质是由不同种分子构成的,属于混合物;
②B图中有三个同种的分子,每个分子是由两个同种的原子的构成的,可以表示3H2;
③A图中的分子是同种的分子构成的,每个分子是由两个不同种的原子的构成的,若一种原子是氧原子,就属于氧化物;
④D物质是同种的原子直接构成的,能用来表示铁这种物质;
故答案为①C;②B;③A;④D.
【点睛】本题考查学生利用图形来分析物质的构成,明确两种不同的球代表两种不同的原子,然后利用只有一种分子的为纯净物,含有两种或两种以上分子的为混合物;根据变化微观示意图,根据分子由原子构成等特点,正确判断变化中的物质构成与粒子个数关系.
15. AD 氩原子 四 BC
【详解】(1)非金属元素的原子最外层电子数多于4个,所以属于非金属原子的是A(氧元素)、D(氯元素),故填:AD;
(2)若E中x=18,则该粒子的名称是氩原子,故填:氩原子;
(3)若E是阳离子,是E原子失去最外层电子形成的,则E原子核外电子层数是4,在元素周期表中属于第四周期,故填:四;
(4)质子数决定元素种类,A、B、C、D四种粒子中属于同种元素的是BC,是因为它们核内质子数相等,故填:BC。
16. 20 78.96 S O2- B和D C和D CaO或SO2或CO2等 O2(或S或C)(合理就可以)
【详解】(1)由钙元素周期表信息可知:钙元素名称左上角的数字表示钙原子原子序数,钙元素的原子序数为20;由硒元素周期表信息可知:硒元素正下方的数字表示硒原子相对原子质量,硒元素的相对原子质量为78.96;
(2)C核外电子数等于原子核内质子数,C表示原子,且原子序数为16是硫原子,C所表示粒子的符号为S,B原子核外由10个电子,原子核内由8个电子,表示阴离子,且原子序数为8,表示氧离子,B所表示粒子的符号为O2-;
(3)元素是具有相同质子数一类原子的总称,A、B、C、D四种粒子中属于同种元素的是B和D,最外层电子数相同的原子化学性质相似,化学性质相似的是C和D;
(4)①由两种元素组成的物质化合物,且一种元素是氧元素的物质叫做氧化物,氧化物:CaO或SO2或CO2;
②由同种元素组成的纯净物叫做单质,金属元素组成的单质叫做金属单质,非金属元素组成的单质叫做非金属单质,非金属单质:O2(或S或C)。
17.(1)1~2mL
(2)三分之一
(3)五分之一
【详解】(1)如果没有说明用量,一般应该取用最少量,固体药品只需盖满试管底部,液体药品取用1~2mL;
(2)给液体加热时,试管内液体的体积不超过试管容积的三分之一;
(3)拉瓦锡测定空气中氧气含量,氧气约占空气体积的五分之一。
18.(1)AB
(2)C
(3)8
(4)40.08
【详解】(1)A、B、C、D四种粒子中,AB的质子数相同,属于同种元素;
(2)A和C的最外层电子数相同,化学性质相似;
(3)D的核内质子数为18,原子中,质子数=核外电子数,则18=2+8+x,x=8;
(4)根据元素周期表中的一格可知,左上角的数字为20,表示原子序数为20;中间的汉字表示元素名称,该元素的名称是钙,属于金属元素;汉字下面的数字表示相对原子质量,元素的相对原子质量为40.08,故填40.08
19.(1)75
(2) 8 得到
(3)8
(4) 小于 非金属
(5)最外层电子数相等
【详解】(1)由铼元素在周期表中的信息可知,左上角的数字表示原子序数,原子序数=质子数,铼元素的质子数是75;
(2)B表示的原子,质子数=核外电子数,故其核外电子数是2+6=8;该原子的最外层电子数是6,大于4,该原子在化学反应中易得到电子;
(3)若C表示离子,硫原子最外层电子数是6,在化学反应中易得到2个电子形成硫离子,故X=8;
(4)元素在周期表中的分布是有规律的,同周期从左至右,原子序数逐渐增大,故D中甲的原子序数小于乙的原子序数;乙代表的氩元素,属于非金属元素;
(5)F和Cl化学性质相似的原因是最外层电子数相等。
20. B 氧气 水蒸气 二氧化碳 氮气 A
【详解】(1)空气的成分按体积计算,大约是:氮气占78%、氧气占21%、稀有气体占0.94%、二氧化碳占0.03%、其它气体和杂质占0.03%,故按体积分数由大到小的顺序排列正确的是②①③④.故填:B;
(2)① 氧气能供给呼吸,小白鼠在装有空气的密闭容器中可存活一段时间,说明空气中含有氧气,故填:氧气;② 酥脆的饼干露置于空气中变软说明空气中含有水蒸气,故填:水蒸气;③ 澄清石灰水是氢氧化钙溶液,能与二氧化碳反应生成白色沉淀碳酸钙,澄清石灰水在空气中放置,其表面生成一层白膜说明空气中含有二氧化碳,故填:二氧化碳;④食品包装袋中充入的防腐气体是氮气,因为氮气的化学性质稳定、无毒。故填:氮气;
(3)目前计入空气质量监测项目为:二氧化硫、二氧化氮、一氧化碳及可吸入颗粒物和臭氧等。A.二氧化碳是空气的成分之一,不是空气污染物,此选项符合题意;B.二氧化氮是空气污染物中的气体污染物,此选项不符合题意;C.二氧化硫是空气污染物中的气体污染物,此选项不符合题意;D.可吸入颗粒物是空气污染物中的固体污染物,此选项不符合题意。
故选A。
21. 甲中酚酞变红,丙和乙中不变 不断运动 C中酚酞溶液先变为红色,B中后变红 温度越高分子运动越快 防止氨气扩散到空气中,污染大气;能够得出在不同温度下分子运动的剧烈程度的差异(答案合理即可) 密封保存
【分析】因为氨水显碱性,遇到酚酞溶液可以使酚酞溶液变红。因分子的质量和体积都很小且总是在不断运动着,故氨分子虽看不见,但依然做运动,遇到酚酞溶液可以使酚酞溶液变红;而且分子运动的速率受温度影响,温度越高,分子运动速率越快。
【详解】(1)因为分子不断地做运动,所以丙中的氨分子运动到甲烧杯中,使甲烧杯中的酚酞溶液变红,故①为甲中的酚酞溶液变红,丙和乙中不变红;②做运动;
(2)因分子做运动,且运动速率受温度影响:温度越高,分子运动越快。故③为C中酚酞溶液先变为红色,B中后变红;④为温度越高分子运动越快;而改进后的装置是一套密闭装置,氨气不会泄露,且该套装置还能很好的测量出温度对分子运动的影响,故⑤为防止氨气扩散到空气中,污染大气;能够得出在不同温度下分子运动的剧烈程度的差异(合理即可);
(3)因氨水有挥发性,所以在保存时需密封保存。
22. 红磷燃烧放热,温度升高,气压变大,曲线上升;反应完全,氧气被消耗,同时温度降低,使装置中气压变小,曲线下降 氧气浓度下降至一定程度,红磷不燃烧,不能完全消耗氧气
【分析】红磷在氧气中燃烧生成五氧化二磷,红磷燃烧放热,温度升高,气压变大,同时红磷燃烧消耗氧气,反应完全,温度降低,气压变小。
【详解】(1)红磷燃烧生成五氧化二磷,反应的化学方程式为。
(2)红磷燃烧放热,温度升高,气体膨胀,气压变大;反应后红磷燃烧消耗氧气,温度降低,使气压变小,故燃烧过程测得其曲线,A→B→C→D→变化呈现先上升后下降的原因是红磷燃烧放热,温度升高,气压变大,曲线上升;反应完全,氧气被消耗,同时温度降低,使装置中气压变小,曲线下降。
(3)根据图表数据可知,反应最后氧气有剩余,故用红磷燃烧的方法不能准确测定空气中氧气的含量,原因是氧气浓度下降至一定程度,红磷不燃烧,氧气不能完全消耗。
【点睛】红磷燃烧时,氧气要达到一定程度,氧气浓度下降至一定程度,红磷不燃烧,不能准确测定空气中氧气的含量。
23. 红 4 酚酞溶液中含有水分子 1、2
【详解】(1)向盛有蒸馏水的试管中加5滴酚酞水溶液,无明显现象,再加入浓氨水时,由于浓氨水显碱性,因此会出现红色;
(2)假设4不能成立,理由是酚酞溶液中含有水分子,如果水分子能使酚酞溶液变红色,则酚酞试液应该是红色溶液;
(3)为了验证剩下几种假设的正确性,小马同学增加了烧杯B作对比实验,烧杯B能够否定假设1、2的合理性,这是因为空气中含有氮气、氧气,而B中酚酞溶液不变色,说明氮气、氧气不能使酚酞试液变色。
一、单选题
1.科学家利用“基因剪刀”技术降低了水稻中砷的含量。下图是砷在元素周期表中的部分信息和原子结构示意图,下列关于砷的说法正确的是
A.属于金属元素 B.位于第五周期
C.核内质子数为33 D.相对原子质量为74.92g
2.一种有趣的钟表式元素周期表如图所示,关于时针所对应的元素说法中正确的是( )
A.12:00 对应的元素为非金属元素
B.10:00 对应的元素易形成化合物
C.9:00 对应元素的离子符号为 F+
D.该钟表的整点时间与该元素的质子数相等
3.对下列一些事实的解释不正确的是
事 实 解 释
A 墙内开花墙外香 分子在不断地运动
B 固体酒精和液体酒精都可做燃料 同种分子,性质相同
C 温度计中的水银热胀冷缩 原子的大小发生改变
D 50mL水与50mL酒精混合后总体积小于100mL 分子间有间隔
A.A B.B C.C D.D
4.分子与原子的本质区别在于( )
A.分子是构成物质的一种微粒,而原子构成分子
B.分子比原子大
C.分子能保持物质的化学性质,而原子不能
D.在化学变化中分子可再分,原子不能再分
5.如图是水分解的微观过程,下列叙述正确的一组是
①化学变化中,分子可分,而原子不能再分;化学反应的实质是分子分裂成原子,原子重新组合成新的分子
②分子是构成物质的一种基本微粒;分子是由原子构成的
③水通电分解是化学变化;水分子是保持水化学性质的微粒
④化学反应前后原子的种类和个数不变
A.①②③④ B.①②④ C.①② D.③④
6.下列有关粒子结构示意图的说法正确的是( )
A.③和④的元素在元素周期表中属于同一周期
B.②和⑥形成化合物的化学式为MgO
C.①和②、⑤和⑥的最外层电子数相同,化学性质相似
D.①③④是具有稳定结构的原子
7.保持氧气化学性质的最小微粒是
A.O
B.O2
C.O3
D.CO2
8.过氧化钠(Na2O2)因能与CO2反应生成氧气,故可作为呼吸面具中氧气的来源,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2。以下说法不正确的是( )
A.过氧化钠属于氧化物 B.该反应可用于实验室制取纯净的氧气
C.该反应可用于潜水艇 D.Na2O2应密封保存
9.下图是元素周期表中的一格,依据图中的信息得到的下列认识错误的是
A.该元素原子的质子数为14
B.该元素属于非金属元素
C.该元素一个原子的原子核有14个中子
D.该元素的相对原子质量为28.09g
10.镍在元素周期表中的信息如图所示,下列有关镍元素的说法不正确的是
A.原子序数是28 B.属于金属元素
C.元素符号是Ni D.一个原子的实际质量是58.69 g
11.以下微观粒子中带电荷的是
A.原子核 B.原子
C.分子 D.中子
12.下列关于空气的说法中,错误的是( )
A.氮气约占空气总体积的78%
B.氧气能助燃,可作燃料
C.稀有气体通电时能发出不同颜色的光,可制作电光源
D.空气中的二氧化碳可以用于灭火
13.下列物质属于纯净物的是
A.大理石 B.澄清石灰水 C.食盐水 D.干冰
二、填空题
14.构建模型又常常是我们认识微观世界的重要手段.看下列各组微观模型图回答问题:下列四幅图中用“”、“”、“”表示核电荷数不同的原子,其中能用来表示混合物的是① ;能表示3H2的是② (填图下字母,下同),能用来表示氧化物的是③ ,能用来表示铁这种物质的是④ 。
15.根据下列粒子结构示意图,回答问题:
(1)属于非金属原子的是 。
(2)若E中x=18,则该粒子的名称是 。
(3)若E是阳离子,则E在元素周期表中属于第 周期。
(4)A、B、C、D四种粒子中属于同种元素的是 。
16.下图中的①、②是钙元素、硒元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图。
请回答:
(1)钙元素的原子序数为 ,硒元素的相对原子质量为 。
(2)C所表示粒子的符号为 ,B所表示粒子的符号为 。
(3) A、B、C、D四种粒子中属于同种元素的是 (填序号,下同);原子的最外层电子数相等则元素的化学性质相似,化学性质相似的是 。
(4)从①、②、A、B、C、D中选择适当的元素组成物质,写出符合下列要求的物质的化学式:
①氧化物 ;②非金属单质 (只写一种)。
17.化学知识上存在很多数字,正确回答数字相关问题:
(1)没有说明用量时,液体取 。
(2)给液体加热时,液体体积不超过试管容积的 。
(3)拉瓦锡测定空气中氧气含量,氧气约占空气体积的 。
18.如图中A、B、C、D是四种粒子的结构示意图,E是钙元素在元素周期表中的信息.
请回答下列问题:(填序号)
(1)A.B.C. D四种粒子结构示意图中,属于同种元素的粒子是 ;
(2)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似 ;
(3)D原子中X= ;
(4)从E图中你获得的信息钙元素的相对原子质量为: .
19.图中A是铼元素在周期表中的信息,B、C分别为两种粒子的结构示意图,D为元素周期表中的部分信息,请根据图中信息回答。
(1)铼元素的质子数是 。
(2)B表示的原子,其核外电子数是 ,该原子在化学反应中易 (填“得到”或“失去”)电子。
(3)若C表示离子,则X= 。
(4)元素在周期表中的分布是有规律的,D中甲的原子序数 (填“大于”或“小于”)乙的原子序数。乙代表的元素属于 (填“金属”或“非金属”)元素。
(5)F和Cl化学性质相似的原因是 。
20.空气是一种宝贵的自然资源.
(1)对空气的成分:①氧气 ②氮气 ③稀有气体 ④二氧化碳及其它气体和杂质.按体积计算,由多到少的排列顺序正确的是
A①②③④ B②①③④ C①②④③ D②①④③
(2)下列事实说明空气中含有哪些成分(填名称)
①小白鼠在装有空气的密闭容器中可存活一段时间,说明空气中含有
②酥脆的饼干露置于空气中变软说明空气中含有
③澄清的石灰水在空气中放置,其表面生成一层白膜说明空气中含有
④食品包装袋中充入的防腐气体是
(3)目前我国对城市空气质量监测项目中,一般不考虑的是
A二氧化碳 B二氧化氮 C二氧化硫 D可吸入颗粒物.
三、实验题
21.某同学设计如下实验装置探究“分子的运动实验”。
(1)图I是按老版课本进行的一个化学实验,大烧杯中的实验现象是 ,此实验说明分子 。但是在实验时同学们闻到了一股难闻的刺激性气味,于是小明对原实验装置进行了改进,装置如图Ⅱ,并进行如下操作:
a向B、C二支试管中分别加入5mL的蒸馏水,各滴入滴无色酚酞溶液,振荡,观察溶液颜色。
b在A、D试管中分别加入2mL浓氨水,立即用带橡皮塞的导管按实验图Ⅱ连接好,并将D试管放置在盛有热水的烧杯中,观察几分钟。
(2)【现象记录】BC两试管中的酚酞溶液变色情况是 。【分析讨论】由此可以得到温度与分子运动速率的关系是 。对比改进前的实验,改进后实验的优点是 。
(3)结合上述实验,实验室保存浓氨水等药品时,应注意的事项是 。
22.学习小组利用了数字化实验技术进行了“空气中氧气体积分数测定”再探究(如图1)。实验通过严谨的测定得到数据如下图2。请你根据实验及其数据分析回答下列问题。
(1)写出本实验红磷燃烧的反应化学方程式 。
(2)压强曲线点A表示红磷开始在集气瓶中燃烧。燃烧过程测得其曲线,A→B→C→D→变化呈现先上升后下降的原因是 。
(3)根据图表数据分析,用红磷燃烧的方法不能准确测定空气中氧气的含量。原因是 。
23.按要求回答下列问题。
(1) 向盛有蒸馏水的试管中加5滴酚酞水溶液,无明显现象,再加入浓氨水,会出现 色;
(2) 按图所示进行实验探究,用大烧杯罩住A、C两个小烧杯一段时间后,A烧杯中溶液变色。贝贝同学提出了以下几种假设:
假设1 空气中的氮气使酚酞溶液变色
假设2 空气中的氧气使酚酞溶液变色
假设3 浓氨水中的氨分子运动使酚酞溶液变色
假设4 浓氨水中的水分子运动使酚酞溶液变色
你认为假设 不能成立,理由是 ;
(3) 为了验证剩下几种假设的正确性,小马同学增加了烧杯B作对比实验,烧杯B能够否定假设 的合理性。
参考答案:
1.C
【详解】A. 砷属于非金属元素,此选项错误;
B. 砷原子核外有4个电子层,所以砷元素位于第四周期,此选项错误;
C. 由题中信息可知,砷原子核内质子数为33 ,此选项正确;
D. 相对原子质量是一个比值,单位是“1”,此选项错误。
故选C。
2.D
【详解】A.12:00对应的元素为镁元素,汉字偏旁是“金”的属于金属元素,此选项错误;
B.10:00对应的元素是氖元素,氖元素属于稀有气体元素,化学性质稳定,不易形成化合物,此选项错误;
C.9:00对应元素是氟元素,氟原子的最外层有7个电子,在化学反应中易得到1个电子而形成带有一个单位负电荷的氟离子,离子符号为F﹣,此选项错误;
D.由图示可知,该钟表的整点时间与原子结构中的质子数相等。此选项正确。故选D。
3.C
【详解】A、墙内开花墙外香,是因为花香中含有的分子是在不断运动的,向四周扩散,使人们闻到花香,故选项解释正确。
B、固体酒精和液体酒精都可做燃料,是因为分子构成相同,化学性质相同,故选项解释正确。
C、温度计中的水银热胀冷缩,是因为汞原子间的间隔(而不是大小)随着温度改变而改变,故选项解释错误。
D、50mL水与50mL酒精混合后总体积小于100mL,是因为分子之间有间隔,一部分水分子和酒精分子会互相占据分子之间的间隔,故选项解释正确。
故选:C。
4.D
【详解】化学变化中分子可以分为原子,原子重新组合成新分子;分子原子的本质区别是在化学变化中可否再分;
A、分子是构成物质的一种微粒,而原子可以构成分子,这不是分子与原子的本质区别;
B、分子比原子大,这不是分子与原子的本质区别;
C、分子能保持物质的化学性质,由原子构成的物质,保持物质的化学性质是原子,如铁原子能保持铁的化学性质,但这不是分子与原子的本质区别;
D、在化学变化中分子可再分,原子不能再分,是分子与原子的本质区别;
故选D。
5.A
【详解】①由微粒的变化可知,在化学变化中,分子可分,而原子不能再分;化学反应的实质是分子分裂成原子,原子重新组合成新的分子,叙述正确;
②由微粒的构成可知,分子是构成物质的一种基本微粒;分子是由原子构成的,叙述正确;
③由水分子的变化和水的构成可知,水通电分解是化学变化;水分子是保持水化学性质的微粒,叙述正确;
④由微粒的构成可知,化学反应前后原子的种类和个数不变,元素的种类也不变。故叙述正确;
由以上分析可知:A正确。
故选A。
6.B
【详解】A、③的元素属于第三周期,④的元素属于第二周期元素,故A选项错误;
B、②的元素是镁元素,⑥的元素是氧元素,故形成的化学式为MgO,故B选项正确;
C、①是稀有气体元素、②是金属元素,化学性质不相似,故C选项错误;
D、③是离子结构示意图,故D选项错误。故选B。
7.B
【详解】氧气是由氧分子构成的,保持氧气化学性质的最小微粒是氧分子。故选B。
8.B
【详解】A、过氧化钠(Na2O2)是由两种元素组成的且有一种是氧元素的化合物,属于氧化物,故A正确;
B、根据化学方程式2Na2O2+2CO2=2Na2CO3+O2可知,反应物二氧化碳气体,不能用于实验室制取纯净的氧气,故B错误;
C、在常温下过氧化钠固体与二氧化碳反应生碳酸钠和氧气,常温下即可发生反应,且可把空气中的二氧化碳转化为氧气,供给氧气的同时吸收了人呼出的二氧化碳,该反应用于潜艇供氧节能环保,故C正确;
D、二氧化碳能与过氧化钠反应,Na2O2应密封保存,故D正确。故选B。
【点睛】氧化物的概念可简记为:两元素、氧元素、化合物。
9.D
【详解】A、由信息可知,元素原子的质子数为14,故A正确;B、此元素为硅元素,属于非金属元素,故B正确;C、质子数等于核外电子数,则一个原子的原子核外有14个电子,故C正确;D、元素的相对原子质量为28.09,而不是原子质量,故D错误。故选D。
10.D
【详解】A、根据元素周期表中的一格可知,左上角的数字表示原子序数,该元素的原子序数为26,故选项说法正确;
B、根据元素周期表中的一格可知,中间的汉子表示元素名称,该元素带有“钅”字旁,属于金属元素,故选项说法正确。
C、根据元素周期表中的一格可知,字母表示该元素的元素符号,铁的元素符号是“Ni”,故选项说法正确;
D、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原子质量为55. 85,故选项说法错误。
故选:D。
11.A
【详解】A、原子核带正电,符合题意;B、原子不显电性,不符合题意;C、分子不显电性,不符合题意;D、中子不显电性,不符合题意;故选A。
12.B
【详解】A、空气中,氧气约占空气总体积的21%,故正确;
B、氧气可以支持燃烧,说明氧气具有助燃性,而不是可燃性,不能作燃料,故错误;
C、稀有气体通电时能发出不同颜色的光,可制成多种用途的电光源,故正确;
D、二氧化碳既不能燃烧也不支持燃烧,密度比空气大,常用来灭火,故正确。
故选B。
13.D
【详解】A、大理石主要成分碳酸钙,还含有其他杂质,是混合物。
B、澄清石灰水是氢氧化钙和水组成的混合物。
C、食盐水是水和氯化钠组成的混合物。
D、干冰是固态二氧化碳,是纯净物。
故选D。
14. C B A D
【详解】由微粒的构成可知:
①C物质是由不同种分子构成的,属于混合物;
②B图中有三个同种的分子,每个分子是由两个同种的原子的构成的,可以表示3H2;
③A图中的分子是同种的分子构成的,每个分子是由两个不同种的原子的构成的,若一种原子是氧原子,就属于氧化物;
④D物质是同种的原子直接构成的,能用来表示铁这种物质;
故答案为①C;②B;③A;④D.
【点睛】本题考查学生利用图形来分析物质的构成,明确两种不同的球代表两种不同的原子,然后利用只有一种分子的为纯净物,含有两种或两种以上分子的为混合物;根据变化微观示意图,根据分子由原子构成等特点,正确判断变化中的物质构成与粒子个数关系.
15. AD 氩原子 四 BC
【详解】(1)非金属元素的原子最外层电子数多于4个,所以属于非金属原子的是A(氧元素)、D(氯元素),故填:AD;
(2)若E中x=18,则该粒子的名称是氩原子,故填:氩原子;
(3)若E是阳离子,是E原子失去最外层电子形成的,则E原子核外电子层数是4,在元素周期表中属于第四周期,故填:四;
(4)质子数决定元素种类,A、B、C、D四种粒子中属于同种元素的是BC,是因为它们核内质子数相等,故填:BC。
16. 20 78.96 S O2- B和D C和D CaO或SO2或CO2等 O2(或S或C)(合理就可以)
【详解】(1)由钙元素周期表信息可知:钙元素名称左上角的数字表示钙原子原子序数,钙元素的原子序数为20;由硒元素周期表信息可知:硒元素正下方的数字表示硒原子相对原子质量,硒元素的相对原子质量为78.96;
(2)C核外电子数等于原子核内质子数,C表示原子,且原子序数为16是硫原子,C所表示粒子的符号为S,B原子核外由10个电子,原子核内由8个电子,表示阴离子,且原子序数为8,表示氧离子,B所表示粒子的符号为O2-;
(3)元素是具有相同质子数一类原子的总称,A、B、C、D四种粒子中属于同种元素的是B和D,最外层电子数相同的原子化学性质相似,化学性质相似的是C和D;
(4)①由两种元素组成的物质化合物,且一种元素是氧元素的物质叫做氧化物,氧化物:CaO或SO2或CO2;
②由同种元素组成的纯净物叫做单质,金属元素组成的单质叫做金属单质,非金属元素组成的单质叫做非金属单质,非金属单质:O2(或S或C)。
17.(1)1~2mL
(2)三分之一
(3)五分之一
【详解】(1)如果没有说明用量,一般应该取用最少量,固体药品只需盖满试管底部,液体药品取用1~2mL;
(2)给液体加热时,试管内液体的体积不超过试管容积的三分之一;
(3)拉瓦锡测定空气中氧气含量,氧气约占空气体积的五分之一。
18.(1)AB
(2)C
(3)8
(4)40.08
【详解】(1)A、B、C、D四种粒子中,AB的质子数相同,属于同种元素;
(2)A和C的最外层电子数相同,化学性质相似;
(3)D的核内质子数为18,原子中,质子数=核外电子数,则18=2+8+x,x=8;
(4)根据元素周期表中的一格可知,左上角的数字为20,表示原子序数为20;中间的汉字表示元素名称,该元素的名称是钙,属于金属元素;汉字下面的数字表示相对原子质量,元素的相对原子质量为40.08,故填40.08
19.(1)75
(2) 8 得到
(3)8
(4) 小于 非金属
(5)最外层电子数相等
【详解】(1)由铼元素在周期表中的信息可知,左上角的数字表示原子序数,原子序数=质子数,铼元素的质子数是75;
(2)B表示的原子,质子数=核外电子数,故其核外电子数是2+6=8;该原子的最外层电子数是6,大于4,该原子在化学反应中易得到电子;
(3)若C表示离子,硫原子最外层电子数是6,在化学反应中易得到2个电子形成硫离子,故X=8;
(4)元素在周期表中的分布是有规律的,同周期从左至右,原子序数逐渐增大,故D中甲的原子序数小于乙的原子序数;乙代表的氩元素,属于非金属元素;
(5)F和Cl化学性质相似的原因是最外层电子数相等。
20. B 氧气 水蒸气 二氧化碳 氮气 A
【详解】(1)空气的成分按体积计算,大约是:氮气占78%、氧气占21%、稀有气体占0.94%、二氧化碳占0.03%、其它气体和杂质占0.03%,故按体积分数由大到小的顺序排列正确的是②①③④.故填:B;
(2)① 氧气能供给呼吸,小白鼠在装有空气的密闭容器中可存活一段时间,说明空气中含有氧气,故填:氧气;② 酥脆的饼干露置于空气中变软说明空气中含有水蒸气,故填:水蒸气;③ 澄清石灰水是氢氧化钙溶液,能与二氧化碳反应生成白色沉淀碳酸钙,澄清石灰水在空气中放置,其表面生成一层白膜说明空气中含有二氧化碳,故填:二氧化碳;④食品包装袋中充入的防腐气体是氮气,因为氮气的化学性质稳定、无毒。故填:氮气;
(3)目前计入空气质量监测项目为:二氧化硫、二氧化氮、一氧化碳及可吸入颗粒物和臭氧等。A.二氧化碳是空气的成分之一,不是空气污染物,此选项符合题意;B.二氧化氮是空气污染物中的气体污染物,此选项不符合题意;C.二氧化硫是空气污染物中的气体污染物,此选项不符合题意;D.可吸入颗粒物是空气污染物中的固体污染物,此选项不符合题意。
故选A。
21. 甲中酚酞变红,丙和乙中不变 不断运动 C中酚酞溶液先变为红色,B中后变红 温度越高分子运动越快 防止氨气扩散到空气中,污染大气;能够得出在不同温度下分子运动的剧烈程度的差异(答案合理即可) 密封保存
【分析】因为氨水显碱性,遇到酚酞溶液可以使酚酞溶液变红。因分子的质量和体积都很小且总是在不断运动着,故氨分子虽看不见,但依然做运动,遇到酚酞溶液可以使酚酞溶液变红;而且分子运动的速率受温度影响,温度越高,分子运动速率越快。
【详解】(1)因为分子不断地做运动,所以丙中的氨分子运动到甲烧杯中,使甲烧杯中的酚酞溶液变红,故①为甲中的酚酞溶液变红,丙和乙中不变红;②做运动;
(2)因分子做运动,且运动速率受温度影响:温度越高,分子运动越快。故③为C中酚酞溶液先变为红色,B中后变红;④为温度越高分子运动越快;而改进后的装置是一套密闭装置,氨气不会泄露,且该套装置还能很好的测量出温度对分子运动的影响,故⑤为防止氨气扩散到空气中,污染大气;能够得出在不同温度下分子运动的剧烈程度的差异(合理即可);
(3)因氨水有挥发性,所以在保存时需密封保存。
22. 红磷燃烧放热,温度升高,气压变大,曲线上升;反应完全,氧气被消耗,同时温度降低,使装置中气压变小,曲线下降 氧气浓度下降至一定程度,红磷不燃烧,不能完全消耗氧气
【分析】红磷在氧气中燃烧生成五氧化二磷,红磷燃烧放热,温度升高,气压变大,同时红磷燃烧消耗氧气,反应完全,温度降低,气压变小。
【详解】(1)红磷燃烧生成五氧化二磷,反应的化学方程式为。
(2)红磷燃烧放热,温度升高,气体膨胀,气压变大;反应后红磷燃烧消耗氧气,温度降低,使气压变小,故燃烧过程测得其曲线,A→B→C→D→变化呈现先上升后下降的原因是红磷燃烧放热,温度升高,气压变大,曲线上升;反应完全,氧气被消耗,同时温度降低,使装置中气压变小,曲线下降。
(3)根据图表数据可知,反应最后氧气有剩余,故用红磷燃烧的方法不能准确测定空气中氧气的含量,原因是氧气浓度下降至一定程度,红磷不燃烧,氧气不能完全消耗。
【点睛】红磷燃烧时,氧气要达到一定程度,氧气浓度下降至一定程度,红磷不燃烧,不能准确测定空气中氧气的含量。
23. 红 4 酚酞溶液中含有水分子 1、2
【详解】(1)向盛有蒸馏水的试管中加5滴酚酞水溶液,无明显现象,再加入浓氨水时,由于浓氨水显碱性,因此会出现红色;
(2)假设4不能成立,理由是酚酞溶液中含有水分子,如果水分子能使酚酞溶液变红色,则酚酞试液应该是红色溶液;
(3)为了验证剩下几种假设的正确性,小马同学增加了烧杯B作对比实验,烧杯B能够否定假设1、2的合理性,这是因为空气中含有氮气、氧气,而B中酚酞溶液不变色,说明氮气、氧气不能使酚酞试液变色。
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
