2023-2024学年鲁科版高中化学选择性必修一 3.4.1离子反应 第一课时 课件 (共20张PPT)
文档属性
| 名称 | 2023-2024学年鲁科版高中化学选择性必修一 3.4.1离子反应 第一课时 课件 (共20张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 2.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-07 00:00:00 | ||
图片预览







文档简介
(共20张PPT)
离子反应
第一课时
【前置作业】
1、回忆你所知道的物质的分类方法及分类依据?
分类因需而定,
无固定依据。
概括归理一
2、设计“家庭实验”来验证:家庭常见物质中哪些能导电?哪些不能导电?并做好实验记录。
实验探究与创新意识
概括归理二
很多物质固态时不导电,在水溶液中导电
水
【每课一题】
举例说明溶液导电的原因?
概括归理三
溶液导电的本质:
离子的自由移动
思维模型
物质导电的本质:
带电粒子的定向移动
【主题一】 NaCl导电性探究
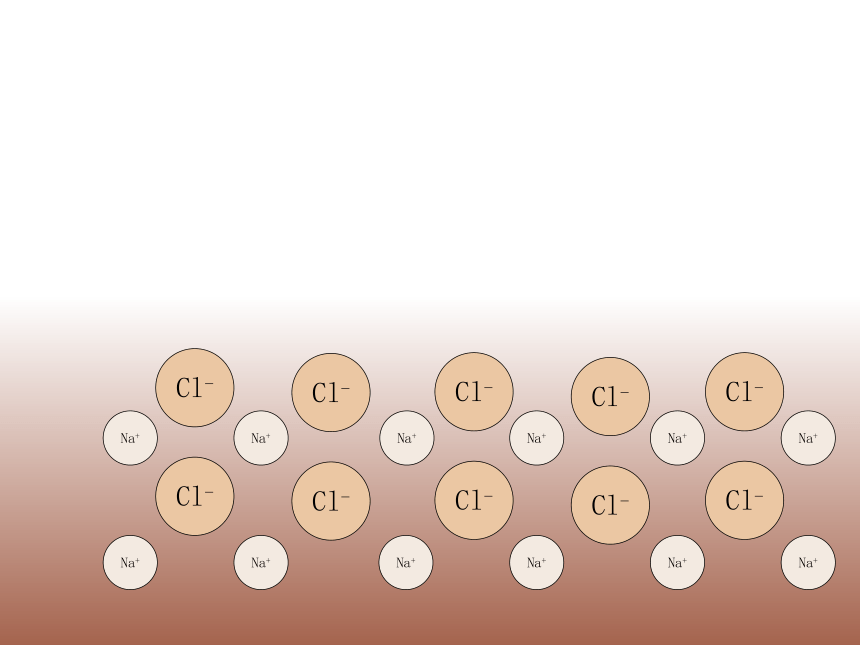
问题(1)为什么NaCl固体不导电?
因为正负电荷相互吸引,虽有离子,但不自由移动
(2)融化的NaCl是否导电?为什么?
Na+
Na+
Na+
Na+
Na+
Na+
Na+
Na+
Na+
Na+
Na+
Na+
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
【主题一】 NaCl导电性探究
问题(1)为什么NaCl固体不导电?
(2)融化的NaCl是否导电?为什么?
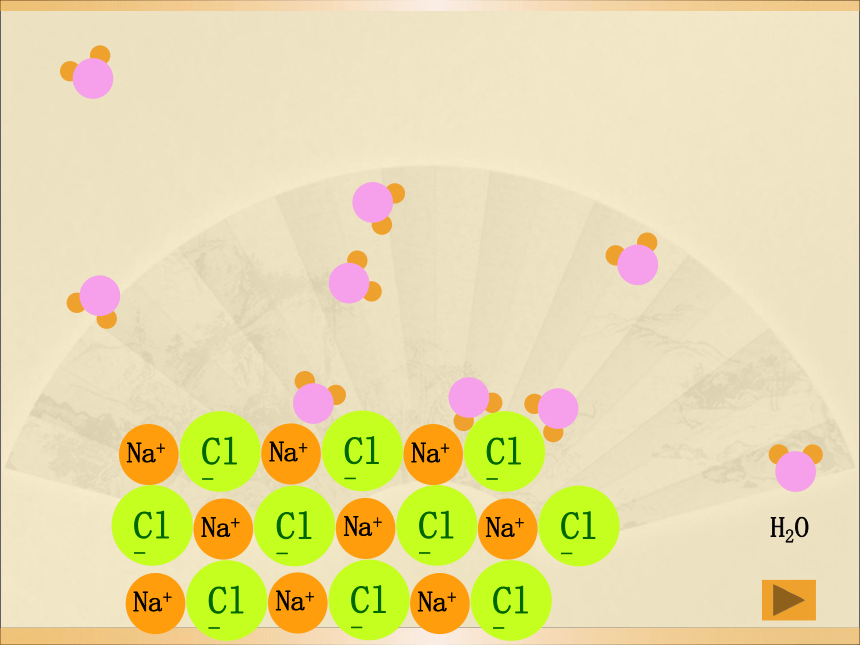
(3) NaCl溶液导电的原因?
有自由移动的离子
思考: 溶液中自由移动的离子是因为什么原因产生的呢?
Cl-
Na+
Cl-
Na+
Cl-
Na+
Cl-
Na+
Cl-
Na+
Cl-
Na+
Cl-
Na+
Cl-
Na+
Cl-
Na+
Cl-
H2O
1、电离: 像氯化钠这样溶于水或受热熔化时,离解成能够自由移动的离子的过程称为电离。
【主题二】 电离及电离方程式
问题(3):NaCl作为一种可溶于水的盐,固体不导电而在溶液中因为电离而导电,是不是这一类盐的普遍现象呢?
问题(1):电离的本质是什么?
概括归理四:电离是结果,是正负电荷的分离
问题(2):电离的条件是什么?
溶于水或受热熔化
实验探究1:CaCl2固体、 CaCl2溶液的导电情况
实验探究2:如何证明CaCl2在水溶液中电离为Ca2+ 和Cl-?
概括归理五:酸碱盐在水溶液中都能电离
化学上有个别到一般的学科思想
微粒观
宏观辨识与微观探析
定义:用化学式和离子符号表示电解质电离的式子叫做电离方程式
问题(1)电离前后原子的种类和数目变化吗?
(2) 电离后,产生的阴阳离子之间存在什么
关系?
概括归理六
电离方程式的书写要遵循:
原子守恒和电中性原则
第一组: HCl HNO3 H2SO4
第二组:KOH NaOH Ba(OH)2
第三组:Na2CO3 (NH4)2SO4 KNO3
比一比:
书写电离方程式
思考:每一组电离出的微粒有什么样的共同点?
酸
碱
盐
电离时生成的阳离子全部是氢离子的化合物叫做酸
电离时生成的阴离子全部是氢氧根离子的化合物叫做碱
电离时生成的阳离子是金属阳离子(或铵根离子),阴离子是酸根阴离子的化合物叫做盐
电解质:在水溶液里或熔融状态下能够导电
的化合物
非电解质:在水溶液里和熔融状态下均不导
电的化合物
【主题三】 电解质与非电解质
问题组:请判断对错,并解释原因。
2、 电解质自身一定导电
1、不是电解质的物质就是非电解质
概括归理七
(1)、电解质和非电解质必须是化合物
(2)、必须是电解质自身电离出的离子导电
下列物质中:
1、CH3COOH 2、熔融NaCl 3、NaOH 4、HNO3
5、石墨 6、AgCl 7、CuSO4溶液 8、Na2CO3
9、C2H5OH 10、盐酸 11、 Fe 12、SO2
属于电解质的是_______________
属于非电解质的是______________
1 2 3 4 6 8
9 12
酸、碱、绝大多数盐、水、金属氧化物等
大部分有机物,非金属氧化物、非酸性气态氢化物等
归纳
常见的电解质:
常见的非电解质:
物质
纯净物
混合物
单质
化合物
酸、碱、盐
氧化物
溶液
浊液
胶体
再回首:对物质分类的再认识
不是电解质
也不是非电解质
有机物
无机物
分类依据:
在水溶液或熔融状态下是否导电
电解质
非电解质
组成
性质
是否含碳
课堂总结
表达方式
概念
物质分类方法
理论
知识
电离理论
电离方程式
电解质
非电解质
水溶液或熔融状态能否导电
课堂总结
化学核心素养
实验探究与创新意识
宏观辨识与微观探析
证据推理与模型认知
科学精神与社会责任
作业:
1 完善笔记,巩固基本知识
2 完成学案课后跟踪练习
离子反应
第一课时
【前置作业】
1、回忆你所知道的物质的分类方法及分类依据?
分类因需而定,
无固定依据。
概括归理一
2、设计“家庭实验”来验证:家庭常见物质中哪些能导电?哪些不能导电?并做好实验记录。
实验探究与创新意识
概括归理二
很多物质固态时不导电,在水溶液中导电
水
【每课一题】
举例说明溶液导电的原因?
概括归理三
溶液导电的本质:
离子的自由移动
思维模型
物质导电的本质:
带电粒子的定向移动
【主题一】 NaCl导电性探究
问题(1)为什么NaCl固体不导电?
因为正负电荷相互吸引,虽有离子,但不自由移动
(2)融化的NaCl是否导电?为什么?
Na+
Na+
Na+
Na+
Na+
Na+
Na+
Na+
Na+
Na+
Na+
Na+
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
Cl-
【主题一】 NaCl导电性探究
问题(1)为什么NaCl固体不导电?
(2)融化的NaCl是否导电?为什么?
(3) NaCl溶液导电的原因?
有自由移动的离子
思考: 溶液中自由移动的离子是因为什么原因产生的呢?
Cl-
Na+
Cl-
Na+
Cl-
Na+
Cl-
Na+
Cl-
Na+
Cl-
Na+
Cl-
Na+
Cl-
Na+
Cl-
Na+
Cl-
H2O
1、电离: 像氯化钠这样溶于水或受热熔化时,离解成能够自由移动的离子的过程称为电离。
【主题二】 电离及电离方程式
问题(3):NaCl作为一种可溶于水的盐,固体不导电而在溶液中因为电离而导电,是不是这一类盐的普遍现象呢?
问题(1):电离的本质是什么?
概括归理四:电离是结果,是正负电荷的分离
问题(2):电离的条件是什么?
溶于水或受热熔化
实验探究1:CaCl2固体、 CaCl2溶液的导电情况
实验探究2:如何证明CaCl2在水溶液中电离为Ca2+ 和Cl-?
概括归理五:酸碱盐在水溶液中都能电离
化学上有个别到一般的学科思想
微粒观
宏观辨识与微观探析
定义:用化学式和离子符号表示电解质电离的式子叫做电离方程式
问题(1)电离前后原子的种类和数目变化吗?
(2) 电离后,产生的阴阳离子之间存在什么
关系?
概括归理六
电离方程式的书写要遵循:
原子守恒和电中性原则
第一组: HCl HNO3 H2SO4
第二组:KOH NaOH Ba(OH)2
第三组:Na2CO3 (NH4)2SO4 KNO3
比一比:
书写电离方程式
思考:每一组电离出的微粒有什么样的共同点?
酸
碱
盐
电离时生成的阳离子全部是氢离子的化合物叫做酸
电离时生成的阴离子全部是氢氧根离子的化合物叫做碱
电离时生成的阳离子是金属阳离子(或铵根离子),阴离子是酸根阴离子的化合物叫做盐
电解质:在水溶液里或熔融状态下能够导电
的化合物
非电解质:在水溶液里和熔融状态下均不导
电的化合物
【主题三】 电解质与非电解质
问题组:请判断对错,并解释原因。
2、 电解质自身一定导电
1、不是电解质的物质就是非电解质
概括归理七
(1)、电解质和非电解质必须是化合物
(2)、必须是电解质自身电离出的离子导电
下列物质中:
1、CH3COOH 2、熔融NaCl 3、NaOH 4、HNO3
5、石墨 6、AgCl 7、CuSO4溶液 8、Na2CO3
9、C2H5OH 10、盐酸 11、 Fe 12、SO2
属于电解质的是_______________
属于非电解质的是______________
1 2 3 4 6 8
9 12
酸、碱、绝大多数盐、水、金属氧化物等
大部分有机物,非金属氧化物、非酸性气态氢化物等
归纳
常见的电解质:
常见的非电解质:
物质
纯净物
混合物
单质
化合物
酸、碱、盐
氧化物
溶液
浊液
胶体
再回首:对物质分类的再认识
不是电解质
也不是非电解质
有机物
无机物
分类依据:
在水溶液或熔融状态下是否导电
电解质
非电解质
组成
性质
是否含碳
课堂总结
表达方式
概念
物质分类方法
理论
知识
电离理论
电离方程式
电解质
非电解质
水溶液或熔融状态能否导电
课堂总结
化学核心素养
实验探究与创新意识
宏观辨识与微观探析
证据推理与模型认知
科学精神与社会责任
作业:
1 完善笔记,巩固基本知识
2 完成学案课后跟踪练习
同课章节目录
- 第1章 化学反应与能量转化
- 第1节 化学反应的热效应
- 第2节 化学能转化为电能——电池
- 第3节 电能转化为化学能——电解
- 第4节 金属的腐蚀与防护
- 微项目 设计载人航天器用化学电池与氧气再生方案——化学反应中能量及物质的转化利用
- 第2章 化学反应的方向、 限度与速率
- 第1节 化学反应的方向
- 第2节 化学反应的限度
- 第3节 化学反应的速率
- 第4节 化学反应条件的优化——工业合成氨
- 微项目 探讨如何利用工业废气中的二氧化碳合成甲醇——化学反应选择与反应条件优化
- 第3章 物质在水溶液中的行为
- 第1节 水与水溶液
- 第2节 弱电解质的电离 盐类的水解
- 第3节 沉淀溶解平衡
- 第4节 离子反应
- 微项目 揭秘索尔维制碱法和侯氏制碱法——化学平衡思想的创造性应用
