化学苏教版(2019)必修第一册 3.1.1氯气的发现与制备 课件(共21张PPT)
文档属性
| 名称 | 化学苏教版(2019)必修第一册 3.1.1氯气的发现与制备 课件(共21张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 16.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-09 00:00:00 | ||
图片预览







文档简介
(共21张PPT)
3.1.1 氯气的发现与制备
浩瀚、美丽的海洋
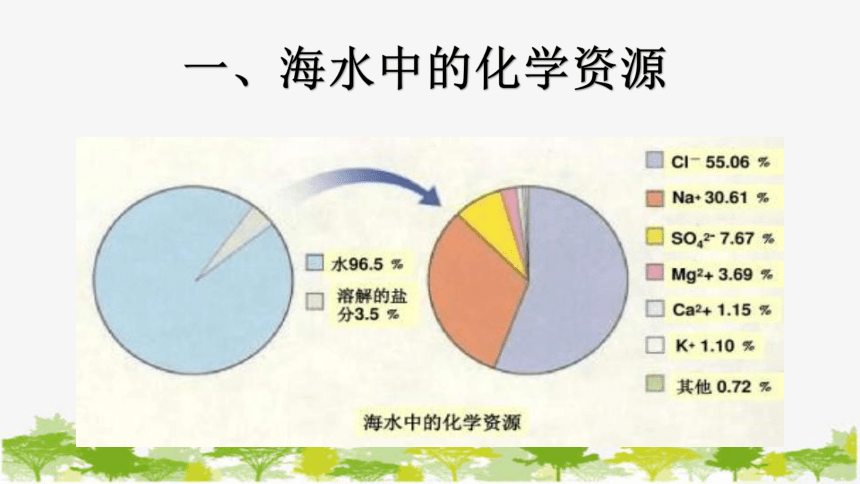
一、海水中的化学资源
事实上海水中蕴含的元素有80多种,它是一个巨大的宝藏库,期待着人们去开放利用。
食盐的作用
从海水中获得氯化钠
把海水引到盐滩上,利用日光和风力使水分蒸发,得到食盐。
海水晒盐
19世纪,科学家发明了电解饱和食盐水制取氯气的方法,但粗食盐(泥沙、Ca2+、Mg2+、SO42-)不符合电解要求,必须精制。请设计实验方案。
设计实验方案
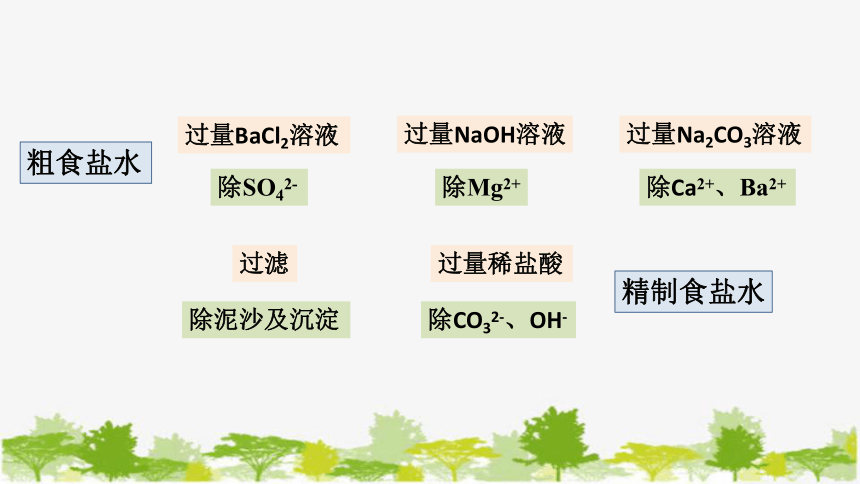
粗食盐水
过量BaCl2溶液
过量NaOH溶液
过量Na2CO3溶液
除SO42-
除Mg2+
除Ca2+、Ba2+
过滤
除泥沙及沉淀
过量稀盐酸
除CO32-、OH-
精制食盐水
注意点:
①在除杂时所加试剂的顺序要求是:Na2CO3必须在BaCl2之后加入,过滤后要加入稀盐酸。
②试剂加入的顺序有多种选择,如:
BaCl2、NaOH、Na2CO3、过滤、盐酸;
BaCl2、Na2CO3、NaOH、过滤、盐酸;
NaOH、BaCl2、Na2CO3、过滤、盐酸。
回忆初中电解水
二、电解饱和食盐水
通电后铁棒和碳棒上都有气泡产生
铁棒收集到的气体靠近火焰,有爆鸣声
有气体物质生成
有氢气生成
碳棒上收集到黄绿色气体,且能使湿润的淀粉碘化钾试纸变蓝
铁棒周围溶液变红
有氯气生成
有碱性物质生成
根据实验现象推断电解饱和食盐水
(1)阳极产生什么物质?
(2)阴极产生什么物质?
(3)写出发生的化学方程式。
(4)碳棒端为什么产生的气体要通入到氢氧化钠溶液中?
阳极产生Cl2
阴极产生H2和NaOH
氯气有毒,防止氯气扩散到空气中造成污染
三、氯气的工业制法----电解饱和食盐水:
化学方程式:2NaCl+2H2O====2NaOH+H2↑+Cl2↑
阳极产生Cl2;
阴极产生H2和NaOH
电解食盐水的方法工业上称为“氯碱工业”。
通电
四、氯气的实验室制法
1.原理:MnO2+4HCl(浓)===MnCl2+Cl2↑+2H2O
2.发生装置类型:
△
“固 +液”加热型制气体
发生装置选择
思考,以上3种装置分别使用于什么气体的制备?
装置(1)“固+固”加热型制气体。可制取O2。
装置(2)“(块状)固+液”不加热型制气体。可制取H2、CO2。
装置(3)“固 +液”或“液 +液”加热型制气体。可制取Cl2
3.收集装置:
氯气的密度比空气大,向上排空气法
氯气不溶于饱和食盐水,排饱和食盐水法。
4.尾气装置:
氢氧化钠溶液
那利用上述原理制取的氯气是纯净的氯气吗?若不是可能含有哪些杂质呢?
因为浓盐酸易挥发,产生的杂质气体有氯化氢气体和水蒸气,需要选择净化装置除去这些杂质。
根据以上的选择和制取氯气的反应原理,请设计制取干燥、纯净的氯气的实验装置。请同学们进行分组讨论。画出制取氯气的整套装置图。
思考
1、装有饱和食盐水装置和装有浓硫酸装置位置能否调换?为什么?
2、使用浓盐酸与足量的MnO2共热制Cl2,实际产生的Cl2总比理论值低,其主要原因是什么?
小结:氯气的实验室制法
1.原理:MnO2+4HCl(浓)===MnCl2+Cl2↑+2H2O
2.发生装置:“固 +液”加热型制气体
3.净化装置:饱和食盐水——除氯化氢气体
浓硫酸——除水蒸气
4.收集装置:向上排空气法/排饱和食盐水
5.尾气处理:NaOH溶液
△
3.1.1 氯气的发现与制备
浩瀚、美丽的海洋
一、海水中的化学资源
事实上海水中蕴含的元素有80多种,它是一个巨大的宝藏库,期待着人们去开放利用。
食盐的作用
从海水中获得氯化钠
把海水引到盐滩上,利用日光和风力使水分蒸发,得到食盐。
海水晒盐
19世纪,科学家发明了电解饱和食盐水制取氯气的方法,但粗食盐(泥沙、Ca2+、Mg2+、SO42-)不符合电解要求,必须精制。请设计实验方案。
设计实验方案
粗食盐水
过量BaCl2溶液
过量NaOH溶液
过量Na2CO3溶液
除SO42-
除Mg2+
除Ca2+、Ba2+
过滤
除泥沙及沉淀
过量稀盐酸
除CO32-、OH-
精制食盐水
注意点:
①在除杂时所加试剂的顺序要求是:Na2CO3必须在BaCl2之后加入,过滤后要加入稀盐酸。
②试剂加入的顺序有多种选择,如:
BaCl2、NaOH、Na2CO3、过滤、盐酸;
BaCl2、Na2CO3、NaOH、过滤、盐酸;
NaOH、BaCl2、Na2CO3、过滤、盐酸。
回忆初中电解水
二、电解饱和食盐水
通电后铁棒和碳棒上都有气泡产生
铁棒收集到的气体靠近火焰,有爆鸣声
有气体物质生成
有氢气生成
碳棒上收集到黄绿色气体,且能使湿润的淀粉碘化钾试纸变蓝
铁棒周围溶液变红
有氯气生成
有碱性物质生成
根据实验现象推断电解饱和食盐水
(1)阳极产生什么物质?
(2)阴极产生什么物质?
(3)写出发生的化学方程式。
(4)碳棒端为什么产生的气体要通入到氢氧化钠溶液中?
阳极产生Cl2
阴极产生H2和NaOH
氯气有毒,防止氯气扩散到空气中造成污染
三、氯气的工业制法----电解饱和食盐水:
化学方程式:2NaCl+2H2O====2NaOH+H2↑+Cl2↑
阳极产生Cl2;
阴极产生H2和NaOH
电解食盐水的方法工业上称为“氯碱工业”。
通电
四、氯气的实验室制法
1.原理:MnO2+4HCl(浓)===MnCl2+Cl2↑+2H2O
2.发生装置类型:
△
“固 +液”加热型制气体
发生装置选择
思考,以上3种装置分别使用于什么气体的制备?
装置(1)“固+固”加热型制气体。可制取O2。
装置(2)“(块状)固+液”不加热型制气体。可制取H2、CO2。
装置(3)“固 +液”或“液 +液”加热型制气体。可制取Cl2
3.收集装置:
氯气的密度比空气大,向上排空气法
氯气不溶于饱和食盐水,排饱和食盐水法。
4.尾气装置:
氢氧化钠溶液
那利用上述原理制取的氯气是纯净的氯气吗?若不是可能含有哪些杂质呢?
因为浓盐酸易挥发,产生的杂质气体有氯化氢气体和水蒸气,需要选择净化装置除去这些杂质。
根据以上的选择和制取氯气的反应原理,请设计制取干燥、纯净的氯气的实验装置。请同学们进行分组讨论。画出制取氯气的整套装置图。
思考
1、装有饱和食盐水装置和装有浓硫酸装置位置能否调换?为什么?
2、使用浓盐酸与足量的MnO2共热制Cl2,实际产生的Cl2总比理论值低,其主要原因是什么?
小结:氯气的实验室制法
1.原理:MnO2+4HCl(浓)===MnCl2+Cl2↑+2H2O
2.发生装置:“固 +液”加热型制气体
3.净化装置:饱和食盐水——除氯化氢气体
浓硫酸——除水蒸气
4.收集装置:向上排空气法/排饱和食盐水
5.尾气处理:NaOH溶液
△
