化学人教版(2019)必修第一册1.1.3物质的转化 课件(共20张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第一册1.1.3物质的转化 课件(共20张ppt) |  | |
| 格式 | pptx | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-11 17:22:47 | ||
图片预览




文档简介
(共20张PPT)
第一节 物质的分类
第三课时
物质的转化
美丽的化学——
化学实验中物质的转化
元素
同一类物质在组成及性能方面往往具有一定的相似性,一定条件下,不同类别的物质可以相互转化。研究物质的转化,不仅可以揭示物质转化所遵循的规律,更重要的是可以利用物质的转化制备人类生活和生产所需要的新物质。
二、物质的转化
1.酸、碱、盐的性质
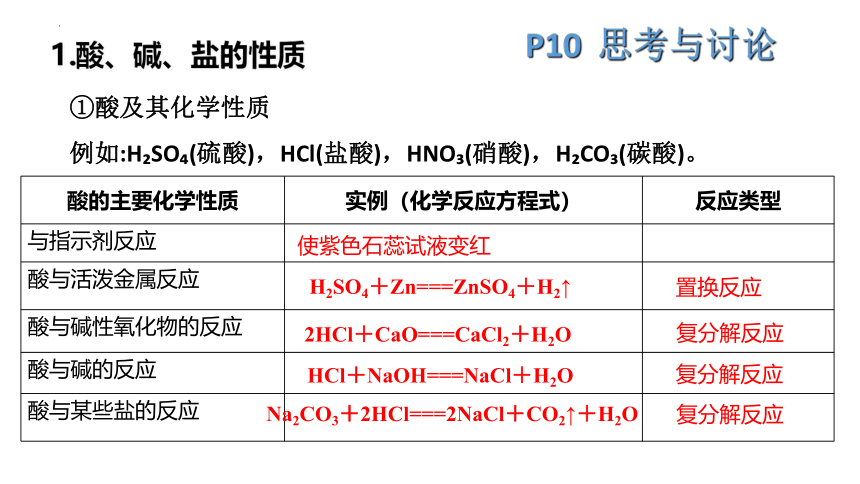
①酸及其化学性质
例如:H SO (硫酸),HCl(盐酸),HNO (硝酸),H CO (碳酸)。
酸的主要化学性质 实例(化学反应方程式) 反应类型
与指示剂反应
酸与活泼金属反应
酸与碱性氧化物的反应
酸与碱的反应
酸与某些盐的反应
使紫色石蕊试液变红
H2SO4+Zn===ZnSO4+H2↑
HCl+NaOH===NaCl+H2O
2HCl+CaO===CaCl2+H2O
Na2CO3+2HCl===2NaCl+CO2↑+H2O
置换反应
复分解反应
复分解反应
复分解反应
P10 思考与讨论
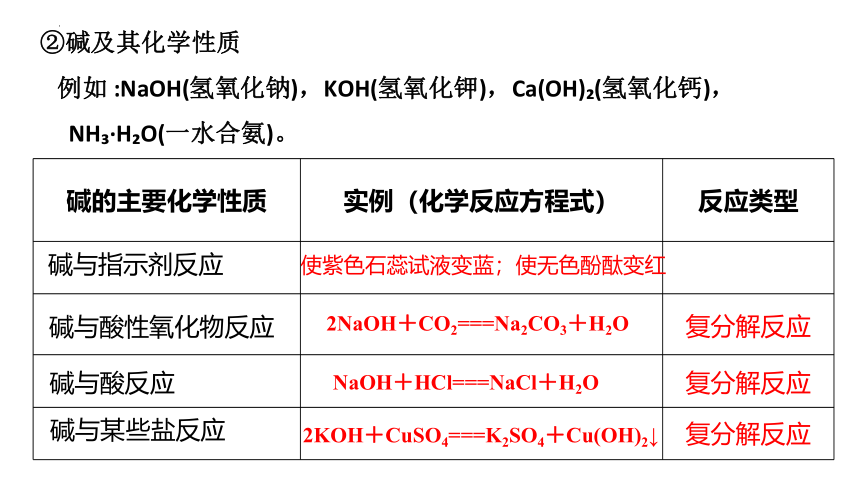
②碱及其化学性质
例如 :NaOH(氢氧化钠),KOH(氢氧化钾),Ca(OH) (氢氧化钙),
NH ·H O(一水合氨)。
碱的主要化学性质 实例(化学反应方程式) 反应类型
使紫色石蕊试液变蓝;使无色酚酞变红
NaOH+HCl===NaCl+H2O
2NaOH+CO2===Na2CO3+H2O
2KOH+CuSO4===K2SO4+Cu(OH)2↓
复分解反应
复分解反应
复分解反应
碱与指示剂反应
碱与酸性氧化物反应
碱与酸反应
碱与某些盐反应
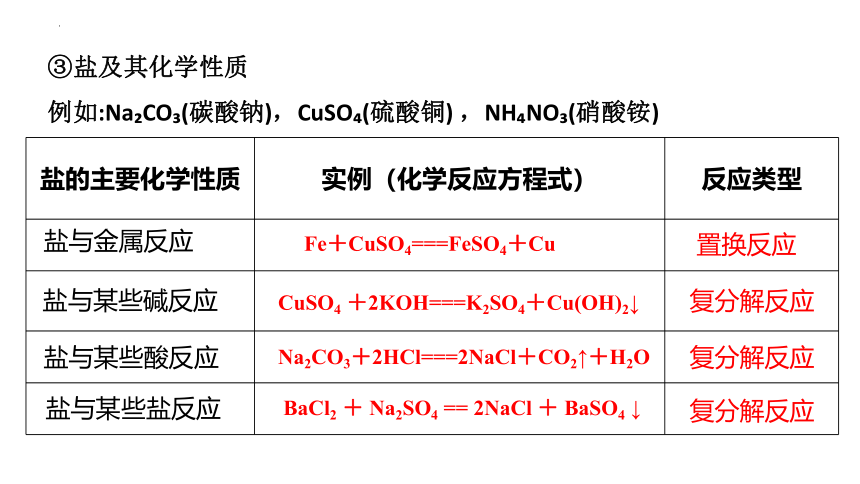
③盐及其化学性质
例如:Na CO (碳酸钠),CuSO (硫酸铜) ,NH NO (硝酸铵)
盐的主要化学性质 实例(化学反应方程式) 反应类型
Na2CO3+2HCl===2NaCl+CO2↑+H2O
CuSO4 +2KOH===K2SO4+Cu(OH)2↓
BaCl2 + Na2SO4 == 2NaCl + BaSO4 ↓
Fe+CuSO4===FeSO4+Cu
置换反应
复分解反应
复分解反应
复分解反应
盐与金属反应
盐与某些碱反应
盐与某些酸反应
盐与某些盐反应
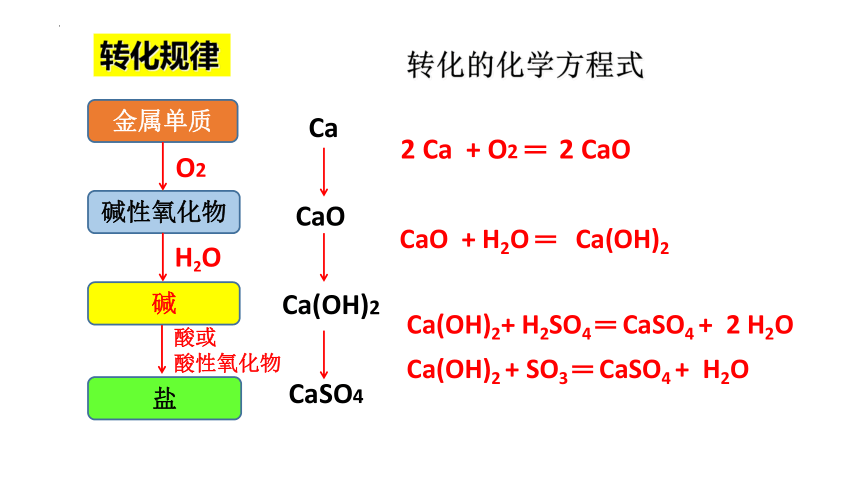
2. 物质的转化
Ca
CaO
Ca(OH)2
CaSO4
2 Ca + O2 ═ 2 CaO
Ca(OH)2+ H2SO4 ═ CaSO4 + 2 H2O
CaO + H2O ═ Ca(OH)2
转化的化学方程式
Ca(OH)2 + SO3 ═ CaSO4 + H2O
金属单质
碱性氧化物
碱
盐
H2O
酸或
酸性氧化物
O2
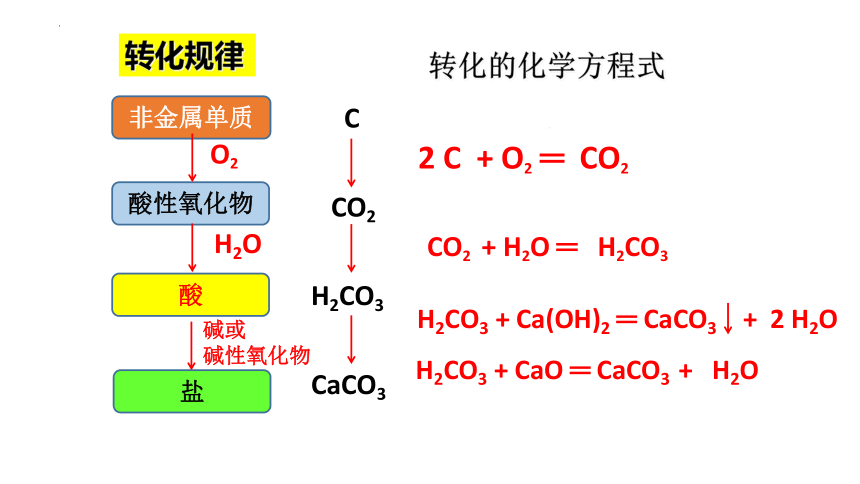
转化规律
C
CO2
H2CO3
CaCO3
CO2 + H2O ═ H2CO3
H2CO3 + Ca(OH)2 ═ CaCO3 + 2 H2O
转化的化学方程式
H2CO3 + CaO ═ CaCO3 + H2O
2 C + O2 ═ CO2
点燃
非金属单质
酸性氧化物
酸
盐
O2
H2O
碱或
碱性氧化物
转化规律
对于上述转化关系,从物质分类的角度,由单质转化成盐的规律为:
金属单质
碱性
氧化物
碱
盐
O2
H2O
酸性
氧化物
酸
非金属单质
酸性
氧化物
酸
盐
O2
H2O
碱性
氧化物
碱
单质到盐的转化
1.确定依据:根据物质的组成和性质,以及物质之间的转化关系,我们可以确定制取某物质的可能方法。例如制取NaOH有下列三种方法:
⑴ 用Na2O与H2O化合:
Na2O+H2O=2NaOH
⑵ 用Na2CO3与Ca(OH)2反应:
Na2CO3+ Ca(OH)2 = 2NaOH + CaCO3↓
⑶ 工业上电解饱和食盐水
三、确定制备物质的方法
2.工业生产方法的选择
(1)最适当方法的选择
(2)实例——工业上制取NaOH
①不采用Na2O与H2O反应的原因:Na2O作为原料 ,来源少,成本高
②过去曾采用:用盐(如Na2CO3)与碱[如Ca(OH)2]反应
③主要采用:电解饱和食盐水
1.判断正误,正确的打“√”,错误的打“×”
(1)酸、碱、盐都易溶于水,且水溶液为无色溶液。( )
(2)金属都能与酸反应产生氢气。( )
(3)酸和碱发生反应都有盐和水生成。( )
(4)有酸味的物质都是酸,有咸味的物质都是盐。( )
×
×
×
√
(5)物质的变化是复杂的,物质之间的转化可能有多种途径。( )
(6)物质转化的过程一定发生了化学反应。 ( )
(7)Cu、CuO均可与盐酸反应生成CuCl2。 ( )
(8)物质间的转化是可认识的、有规律的,转化是有条件的,在研究陌生物质的性质时,要特别关注反应条件和环境。 ( )
√
√
√
×
3.按一定特点或规律对物质进行分类,给化学学习和研究带来很大的方便。下列各组物质中,按“氧化物—酸—碱—盐”顺序排列的一组是( )
A.HClO HCl Mg(OH)2 MgCl2
B.CO2 H2CO3 CaCO3 Ca(HCO3)2
C.H2O HNO2 NH3·H2O NH4NO3
D.SO3 NaHSO4 NaOH Na2SO4
C
解析 A中HClO属于酸,B中CaCO3属于盐,D中NaHSO4是一种盐。
4.下列关于化合物的分类正确的是( )
A
解析 纯碱属于盐,不是碱;氮化镁不属于氧化物;醋酸溶液属于混合物,不属于化合物。
5.铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见的物质,四种物质间的反应关系如图所示,图中两圆相交部分(①、②、③、④)表示物质间的反应,其中对应的四种反应类型正确的是( )
A.复分解反应、复分解反应、化合反应、置换反应
B.复分解反应、置换反应、复分解反应、置换反应
C.复分解反应、复分解反应、置换反应、置换反应
D.分解反应、复分解反应、置换反应、置换反应
C
解析 本题图形中物质间的反应分别为①Ca(OH)2+2HCl===CaCl2+2H2O(复分解反应);②Ca(OH)2+CuCl2===CaCl2+Cu(OH)2↓(复分解反应);③Fe+CuCl2===FeCl2+Cu(置换反应);④Fe+2HCl===FeCl2+H2↑(置换反应)。
6.将下列各组物质按酸、碱、盐的分类依次排列,正确的是( )
A.硫酸、纯碱、石膏 B.硫酸、烧碱、胆矾
C.硫酸氢钠、生石灰、醋酸钠 D.磷酸、熟石灰、苛性钠
B
解析 硫酸属于酸,纯碱是Na2CO3,属于盐,石膏属于盐,A错误;硫酸属于酸,烧碱是NaOH,属于碱,胆矾是五水硫酸铜,属于盐,B正确;硫酸氢钠属于盐,生石灰属于氧化物,醋酸钠属于盐,C错误;磷酸属于酸,熟石灰属于碱,苛性钠是NaOH,属于碱,D错误。
总结
单质、氧化物、酸、碱、盐之间的转化关系
第一节 物质的分类
第三课时
物质的转化
美丽的化学——
化学实验中物质的转化
元素
同一类物质在组成及性能方面往往具有一定的相似性,一定条件下,不同类别的物质可以相互转化。研究物质的转化,不仅可以揭示物质转化所遵循的规律,更重要的是可以利用物质的转化制备人类生活和生产所需要的新物质。
二、物质的转化
1.酸、碱、盐的性质
①酸及其化学性质
例如:H SO (硫酸),HCl(盐酸),HNO (硝酸),H CO (碳酸)。
酸的主要化学性质 实例(化学反应方程式) 反应类型
与指示剂反应
酸与活泼金属反应
酸与碱性氧化物的反应
酸与碱的反应
酸与某些盐的反应
使紫色石蕊试液变红
H2SO4+Zn===ZnSO4+H2↑
HCl+NaOH===NaCl+H2O
2HCl+CaO===CaCl2+H2O
Na2CO3+2HCl===2NaCl+CO2↑+H2O
置换反应
复分解反应
复分解反应
复分解反应
P10 思考与讨论
②碱及其化学性质
例如 :NaOH(氢氧化钠),KOH(氢氧化钾),Ca(OH) (氢氧化钙),
NH ·H O(一水合氨)。
碱的主要化学性质 实例(化学反应方程式) 反应类型
使紫色石蕊试液变蓝;使无色酚酞变红
NaOH+HCl===NaCl+H2O
2NaOH+CO2===Na2CO3+H2O
2KOH+CuSO4===K2SO4+Cu(OH)2↓
复分解反应
复分解反应
复分解反应
碱与指示剂反应
碱与酸性氧化物反应
碱与酸反应
碱与某些盐反应
③盐及其化学性质
例如:Na CO (碳酸钠),CuSO (硫酸铜) ,NH NO (硝酸铵)
盐的主要化学性质 实例(化学反应方程式) 反应类型
Na2CO3+2HCl===2NaCl+CO2↑+H2O
CuSO4 +2KOH===K2SO4+Cu(OH)2↓
BaCl2 + Na2SO4 == 2NaCl + BaSO4 ↓
Fe+CuSO4===FeSO4+Cu
置换反应
复分解反应
复分解反应
复分解反应
盐与金属反应
盐与某些碱反应
盐与某些酸反应
盐与某些盐反应
2. 物质的转化
Ca
CaO
Ca(OH)2
CaSO4
2 Ca + O2 ═ 2 CaO
Ca(OH)2+ H2SO4 ═ CaSO4 + 2 H2O
CaO + H2O ═ Ca(OH)2
转化的化学方程式
Ca(OH)2 + SO3 ═ CaSO4 + H2O
金属单质
碱性氧化物
碱
盐
H2O
酸或
酸性氧化物
O2
转化规律
C
CO2
H2CO3
CaCO3
CO2 + H2O ═ H2CO3
H2CO3 + Ca(OH)2 ═ CaCO3 + 2 H2O
转化的化学方程式
H2CO3 + CaO ═ CaCO3 + H2O
2 C + O2 ═ CO2
点燃
非金属单质
酸性氧化物
酸
盐
O2
H2O
碱或
碱性氧化物
转化规律
对于上述转化关系,从物质分类的角度,由单质转化成盐的规律为:
金属单质
碱性
氧化物
碱
盐
O2
H2O
酸性
氧化物
酸
非金属单质
酸性
氧化物
酸
盐
O2
H2O
碱性
氧化物
碱
单质到盐的转化
1.确定依据:根据物质的组成和性质,以及物质之间的转化关系,我们可以确定制取某物质的可能方法。例如制取NaOH有下列三种方法:
⑴ 用Na2O与H2O化合:
Na2O+H2O=2NaOH
⑵ 用Na2CO3与Ca(OH)2反应:
Na2CO3+ Ca(OH)2 = 2NaOH + CaCO3↓
⑶ 工业上电解饱和食盐水
三、确定制备物质的方法
2.工业生产方法的选择
(1)最适当方法的选择
(2)实例——工业上制取NaOH
①不采用Na2O与H2O反应的原因:Na2O作为原料 ,来源少,成本高
②过去曾采用:用盐(如Na2CO3)与碱[如Ca(OH)2]反应
③主要采用:电解饱和食盐水
1.判断正误,正确的打“√”,错误的打“×”
(1)酸、碱、盐都易溶于水,且水溶液为无色溶液。( )
(2)金属都能与酸反应产生氢气。( )
(3)酸和碱发生反应都有盐和水生成。( )
(4)有酸味的物质都是酸,有咸味的物质都是盐。( )
×
×
×
√
(5)物质的变化是复杂的,物质之间的转化可能有多种途径。( )
(6)物质转化的过程一定发生了化学反应。 ( )
(7)Cu、CuO均可与盐酸反应生成CuCl2。 ( )
(8)物质间的转化是可认识的、有规律的,转化是有条件的,在研究陌生物质的性质时,要特别关注反应条件和环境。 ( )
√
√
√
×
3.按一定特点或规律对物质进行分类,给化学学习和研究带来很大的方便。下列各组物质中,按“氧化物—酸—碱—盐”顺序排列的一组是( )
A.HClO HCl Mg(OH)2 MgCl2
B.CO2 H2CO3 CaCO3 Ca(HCO3)2
C.H2O HNO2 NH3·H2O NH4NO3
D.SO3 NaHSO4 NaOH Na2SO4
C
解析 A中HClO属于酸,B中CaCO3属于盐,D中NaHSO4是一种盐。
4.下列关于化合物的分类正确的是( )
A
解析 纯碱属于盐,不是碱;氮化镁不属于氧化物;醋酸溶液属于混合物,不属于化合物。
5.铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见的物质,四种物质间的反应关系如图所示,图中两圆相交部分(①、②、③、④)表示物质间的反应,其中对应的四种反应类型正确的是( )
A.复分解反应、复分解反应、化合反应、置换反应
B.复分解反应、置换反应、复分解反应、置换反应
C.复分解反应、复分解反应、置换反应、置换反应
D.分解反应、复分解反应、置换反应、置换反应
C
解析 本题图形中物质间的反应分别为①Ca(OH)2+2HCl===CaCl2+2H2O(复分解反应);②Ca(OH)2+CuCl2===CaCl2+Cu(OH)2↓(复分解反应);③Fe+CuCl2===FeCl2+Cu(置换反应);④Fe+2HCl===FeCl2+H2↑(置换反应)。
6.将下列各组物质按酸、碱、盐的分类依次排列,正确的是( )
A.硫酸、纯碱、石膏 B.硫酸、烧碱、胆矾
C.硫酸氢钠、生石灰、醋酸钠 D.磷酸、熟石灰、苛性钠
B
解析 硫酸属于酸,纯碱是Na2CO3,属于盐,石膏属于盐,A错误;硫酸属于酸,烧碱是NaOH,属于碱,胆矾是五水硫酸铜,属于盐,B正确;硫酸氢钠属于盐,生石灰属于氧化物,醋酸钠属于盐,C错误;磷酸属于酸,熟石灰属于碱,苛性钠是NaOH,属于碱,D错误。
总结
单质、氧化物、酸、碱、盐之间的转化关系
