【核心素养目标】人教版高中化学 选择性必修1 2.2 化学平衡(第1课时 化学平衡状态)课件
文档属性
| 名称 | 【核心素养目标】人教版高中化学 选择性必修1 2.2 化学平衡(第1课时 化学平衡状态)课件 |  | |
| 格式 | pptx | ||
| 文件大小 | 8.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-13 08:51:12 | ||
图片预览






文档简介
(共18张PPT)
第二节 化学平衡
第1课时 化学平衡状态
人教版选择性必修1
学习目标
1.通过溶解和结晶过程的分析,认识化学反应的可逆性。
2.通过化学平衡状态的建立过程,知道化学平衡是一种动态平衡,理解并会判断化学平衡状态的标志。
学习目标
1.可逆反应都有一定的限度,是可调控的,条件改变,限度被破坏, 达到新的平衡状态。能从多角度、动态地分析化学平衡状态的各种表现。培养学生“变化观念与平衡思想”的学科素养。
2.能建立“逆、等、动、定、变”的认知模型,并利用模型解决化学平衡的实际问题,培养学生“证据推理与模型认知”的学科素养。
素养目标
情境引入
合成氨是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,原理如下:
2NH3
N2 + 3H2
催化剂
高温、高压
为了提高生产效率,我们除了考虑提高化学反应速率问题,还应该考虑转化程度问题。
一、化学平衡状态
某温度下,在容积不变的密闭容器中N2与H2反应足够长时间后各物质的量不再改变,数据如下:
2NH3
N2 + 3H2
催化剂
高温、高压
各物质的起始量/mol 充分反应后各物质的量/mol N2 H2 NH3 N2 H2 NH3
10 15 0 8 9 4
教学过程
化学平衡状态
合成氨反应中有关物质的浓度随时间变化示意图
浓度
时间(t)
NH3
N2
H2
随着反应的进行,体系中NH3的浓度逐渐增大,而N2与H2的浓度逐渐减小。从某一时刻开始,它们的浓度均不再改变
正向: N2 + 3H2 2NH3
教学过程
化学平衡状态
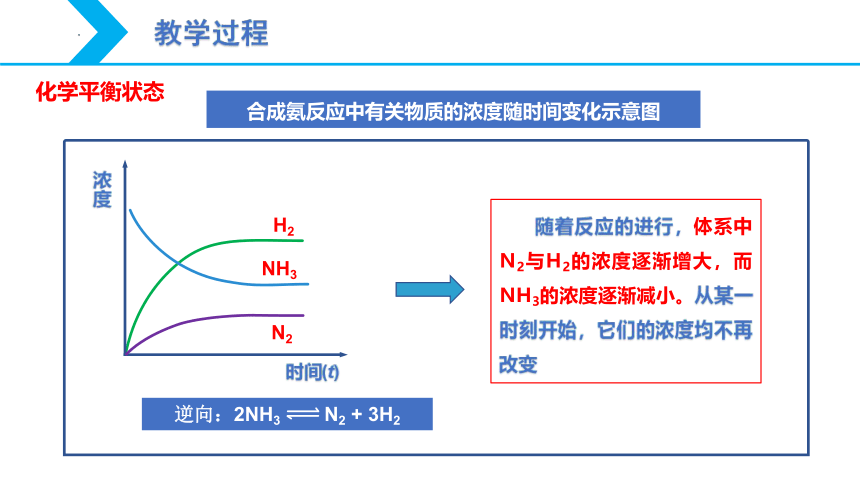
合成氨反应中有关物质的浓度随时间变化示意图
随着反应的进行,体系中N2与H2的浓度逐渐增大,而NH3的浓度逐渐减小。从某一时刻开始,它们的浓度均不再改变
逆向:2NH3 N2 + 3H2
教学过程
H2
浓度
时间(t)
NH3
N2
教学过程
2.转化率:化学反应的限度决定了反应物在一定条件下的最大转化率。
1. 定义: 在一定条件下,在可逆反应体系中,正反应速率与逆反应速率相等,反应物的浓度与生成物的浓度均保持不变,即体系的组成不随时间而改变,这表明该反应中物质的转化达到了“限度”,这时的状态我们称之为化学平衡状态,简称化学平衡。
一、化学平衡状态
转化率
(α)
=
转化的量
起始的量
×100%
教学过程
化学平衡的特征:“逆”、“等”、“动”、“定”、“变”
(1)“逆”:
化学平衡只存在于可逆反应中;
(2)“等”:
达到化学平衡状态时,v正=v逆≠0
(4)“定”:
(3)“动”:
化学平衡是一个动态平衡;
(5)“变”:
当条件变化时,原平衡被破坏,在新的条件下会重新建立新的平衡。
平衡时反应物和生成物的浓度保持不变
3.化学平衡状态的特征
教学过程
你觉得这些特征中,哪些可以说明一个可逆反应达到了一定条件下的反应限度(化学平衡状态)?
“等”
“定”
--标志
教学过程
如何理解 v(正)=v(逆)?
核心:1、有正有逆的描述;2、转化为同一物质速率相等
例如,一定条件下,对于可逆反应N2+3H2 2NH3,表示正、逆反应速率可以用N2或H2或NH3来表示:下列能表示反应达到化学平衡状态的是
(1)单位时间内,有1molN2消耗,同时有1molN2生成
(2)单位时间内,有3molH2消耗,同时有2molNH3生成
(3)单位时间内,有1molN2消耗,同时有3molH2消耗
(4)1moN三N键断裂的同时有2moN-H键断裂
(5)
(1) (5)
有正有逆
符合比例
教学过程
如何理解“定”
核心:一个量随反应一直变,突然不变
例如,一定条件下,对于可逆反应N2+3H2 2NH3,表示正、逆反应速率可以用N2或H2或NH3来表示,下列能表示反应达到化学平衡状态的是
(1)容器内氮气的物质的量不再改变
(2)容器内颜色不再改变
(3)固定容器恒容条件下,容器内压强不再改变
(4)固定容器恒容条件下,容器内气体密度不再改变
(5)恒容或恒压条件,容器内平均相对分子质量不再改变
变量不变 即平衡
(1) (3) (5)
教学过程
总结整理
教学过程
总结整理
下列说法中可以证明2HI(g) H2(g)+I2(g)(紫色)已达到平衡状态的是___________。
①单位时间内生成 n mol H2的同时生成 n molHI
②一个H-H键断裂的同时有两个H-I键断裂
③ 反应速率 v(H2) = v(I2) 时
④c(HI):c(H2):c(I2) = 2:1:1时
⑤温度和体积一定,容器内压强不再变化时
⑥温度和体积一定,混合气体的颜色不再变化时
⑦条件一定,混合气体的平均相对分子质量不再变化时
⑧温度和压强一定,混合气体的密度不再变化时
②⑥
课堂练习
典例1.
可逆反应2NO2(红棕色) N2O4(无色)在一固定密闭容器中反应,达到化学平衡状 态的是( )
A.单位时间内生成n mol N2O4 同时生成2n mol NO2
B.单位时间内生成n mol N2O4 同时消耗2n mol NO2
C.c(NO2):c(N2O4)= 2: 1
D.混合气体的颜色不再改变
E.混合气体的密度不再改变
F.混合气体的平均相对分子质量不再改变
H.混合气体各组分的体积分数不再改变
A D F H
课堂练习
典例2.
在一定条件下,向2 L密闭容器中通入2 mol N2和6 mol H2,发生反应:N2(g)+3H2(g) 2NH3(g),以下选项能够说明反应已达到平衡状态的是( )
A.c(NH3)∶c(H2)∶c(N2)=2∶3∶1
B.单位时间内1个 键断裂的同时,有6个N—H键形成
C.混合气体的平均相对分子质量不再改变
D.单位时间内有6个N—H键形成的同时,有3个H—H键断裂
典例3.
【答案】C
课堂练习
课堂小结
直接标志——“正逆反应速率相等”
间接标志——“变量不变”
化学平衡的状态
化学平衡状态的判定
定义
特征
化学平衡
感 谢 倾 听
第二节 化学平衡
第1课时 化学平衡状态
人教版选择性必修1
学习目标
1.通过溶解和结晶过程的分析,认识化学反应的可逆性。
2.通过化学平衡状态的建立过程,知道化学平衡是一种动态平衡,理解并会判断化学平衡状态的标志。
学习目标
1.可逆反应都有一定的限度,是可调控的,条件改变,限度被破坏, 达到新的平衡状态。能从多角度、动态地分析化学平衡状态的各种表现。培养学生“变化观念与平衡思想”的学科素养。
2.能建立“逆、等、动、定、变”的认知模型,并利用模型解决化学平衡的实际问题,培养学生“证据推理与模型认知”的学科素养。
素养目标
情境引入
合成氨是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,原理如下:
2NH3
N2 + 3H2
催化剂
高温、高压
为了提高生产效率,我们除了考虑提高化学反应速率问题,还应该考虑转化程度问题。
一、化学平衡状态
某温度下,在容积不变的密闭容器中N2与H2反应足够长时间后各物质的量不再改变,数据如下:
2NH3
N2 + 3H2
催化剂
高温、高压
各物质的起始量/mol 充分反应后各物质的量/mol N2 H2 NH3 N2 H2 NH3
10 15 0 8 9 4
教学过程
化学平衡状态
合成氨反应中有关物质的浓度随时间变化示意图
浓度
时间(t)
NH3
N2
H2
随着反应的进行,体系中NH3的浓度逐渐增大,而N2与H2的浓度逐渐减小。从某一时刻开始,它们的浓度均不再改变
正向: N2 + 3H2 2NH3
教学过程
化学平衡状态
合成氨反应中有关物质的浓度随时间变化示意图
随着反应的进行,体系中N2与H2的浓度逐渐增大,而NH3的浓度逐渐减小。从某一时刻开始,它们的浓度均不再改变
逆向:2NH3 N2 + 3H2
教学过程
H2
浓度
时间(t)
NH3
N2
教学过程
2.转化率:化学反应的限度决定了反应物在一定条件下的最大转化率。
1. 定义: 在一定条件下,在可逆反应体系中,正反应速率与逆反应速率相等,反应物的浓度与生成物的浓度均保持不变,即体系的组成不随时间而改变,这表明该反应中物质的转化达到了“限度”,这时的状态我们称之为化学平衡状态,简称化学平衡。
一、化学平衡状态
转化率
(α)
=
转化的量
起始的量
×100%
教学过程
化学平衡的特征:“逆”、“等”、“动”、“定”、“变”
(1)“逆”:
化学平衡只存在于可逆反应中;
(2)“等”:
达到化学平衡状态时,v正=v逆≠0
(4)“定”:
(3)“动”:
化学平衡是一个动态平衡;
(5)“变”:
当条件变化时,原平衡被破坏,在新的条件下会重新建立新的平衡。
平衡时反应物和生成物的浓度保持不变
3.化学平衡状态的特征
教学过程
你觉得这些特征中,哪些可以说明一个可逆反应达到了一定条件下的反应限度(化学平衡状态)?
“等”
“定”
--标志
教学过程
如何理解 v(正)=v(逆)?
核心:1、有正有逆的描述;2、转化为同一物质速率相等
例如,一定条件下,对于可逆反应N2+3H2 2NH3,表示正、逆反应速率可以用N2或H2或NH3来表示:下列能表示反应达到化学平衡状态的是
(1)单位时间内,有1molN2消耗,同时有1molN2生成
(2)单位时间内,有3molH2消耗,同时有2molNH3生成
(3)单位时间内,有1molN2消耗,同时有3molH2消耗
(4)1moN三N键断裂的同时有2moN-H键断裂
(5)
(1) (5)
有正有逆
符合比例
教学过程
如何理解“定”
核心:一个量随反应一直变,突然不变
例如,一定条件下,对于可逆反应N2+3H2 2NH3,表示正、逆反应速率可以用N2或H2或NH3来表示,下列能表示反应达到化学平衡状态的是
(1)容器内氮气的物质的量不再改变
(2)容器内颜色不再改变
(3)固定容器恒容条件下,容器内压强不再改变
(4)固定容器恒容条件下,容器内气体密度不再改变
(5)恒容或恒压条件,容器内平均相对分子质量不再改变
变量不变 即平衡
(1) (3) (5)
教学过程
总结整理
教学过程
总结整理
下列说法中可以证明2HI(g) H2(g)+I2(g)(紫色)已达到平衡状态的是___________。
①单位时间内生成 n mol H2的同时生成 n molHI
②一个H-H键断裂的同时有两个H-I键断裂
③ 反应速率 v(H2) = v(I2) 时
④c(HI):c(H2):c(I2) = 2:1:1时
⑤温度和体积一定,容器内压强不再变化时
⑥温度和体积一定,混合气体的颜色不再变化时
⑦条件一定,混合气体的平均相对分子质量不再变化时
⑧温度和压强一定,混合气体的密度不再变化时
②⑥
课堂练习
典例1.
可逆反应2NO2(红棕色) N2O4(无色)在一固定密闭容器中反应,达到化学平衡状 态的是( )
A.单位时间内生成n mol N2O4 同时生成2n mol NO2
B.单位时间内生成n mol N2O4 同时消耗2n mol NO2
C.c(NO2):c(N2O4)= 2: 1
D.混合气体的颜色不再改变
E.混合气体的密度不再改变
F.混合气体的平均相对分子质量不再改变
H.混合气体各组分的体积分数不再改变
A D F H
课堂练习
典例2.
在一定条件下,向2 L密闭容器中通入2 mol N2和6 mol H2,发生反应:N2(g)+3H2(g) 2NH3(g),以下选项能够说明反应已达到平衡状态的是( )
A.c(NH3)∶c(H2)∶c(N2)=2∶3∶1
B.单位时间内1个 键断裂的同时,有6个N—H键形成
C.混合气体的平均相对分子质量不再改变
D.单位时间内有6个N—H键形成的同时,有3个H—H键断裂
典例3.
【答案】C
课堂练习
课堂小结
直接标志——“正逆反应速率相等”
间接标志——“变量不变”
化学平衡的状态
化学平衡状态的判定
定义
特征
化学平衡
感 谢 倾 听
