2023秋高中化学人教版2019必修1 第二章 海水中的重要元素—钠和氯 第1节 第2课时 钠的几种化合物—氧化钠和过氧化钠 课时同步练(含答案)
文档属性
| 名称 | 2023秋高中化学人教版2019必修1 第二章 海水中的重要元素—钠和氯 第1节 第2课时 钠的几种化合物—氧化钠和过氧化钠 课时同步练(含答案) |

|
|
| 格式 | DOC | ||
| 文件大小 | 175.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-12 00:00:00 | ||
图片预览

文档简介
第2课时 钠的几种化合物——氧化钠和过氧化钠
1. Na2O属于下列分类标准中的( )
A. 酸性氧化物 B. 碱性氧化物
C. 两性氧化物 D. 盐
2. 关于金属钠在足量氧气中燃烧的现象,下列说法中错误的是( )
A. 生成白色固体 B. 产生黄色火焰
C. 生成淡黄色固体 D. 钠熔化后表面显银白色
3. 下列关于Na2O和Na2O2的叙述中,正确的是( )
A. 都是白色的固体 B. 与水反应都属于化合反应
C. 都能与水反应形成强碱溶液 D. 都是强氧化剂
4. 下列各组物质间反应,不能生成NaOH的是( )
A. Na与H2O B. Na2O2与H2O
C. Ca(OH)2溶液与Na2CO3溶液 D. Ca(OH)2溶液与NaCl溶液
5. 能与CO2反应放出氧气的物质是( )
A. Na2O2 B. Na2O
C. NaOH D. NaCl
6. 一团棉花包裹少量过氧化钠放在石棉网上,将CO2气体缓缓通入棉花中的过氧化钠上,棉花很快燃烧起来,根据实验分析,下列表达错误的是( )
A. 反应生成的O2有利于棉花燃烧 B. 过氧化钠与CO2反应放热
C. CO2对棉花燃烧起助燃作用 D. 过氧化钠与CO2的反应属于氧化还原反应
7. 适宜用于呼吸面具中作供氧剂的是( )
A. KMnO4 B. H2O2
C. KClO3 D. Na2O2
8. 在下列反应中,Na2O2只表现出强氧化性的是( )
A. 2Na2O2+2CO2===2Na2CO3+O2
B. Na2O2+MnO2===Na2MnO4
C. 2Na2O2+2H2SO4===2Na2SO4+2H2O+O2↑
D. 5Na2O2+2MnO+16H+===10Na++2Mn2++5O2↑+8H2O
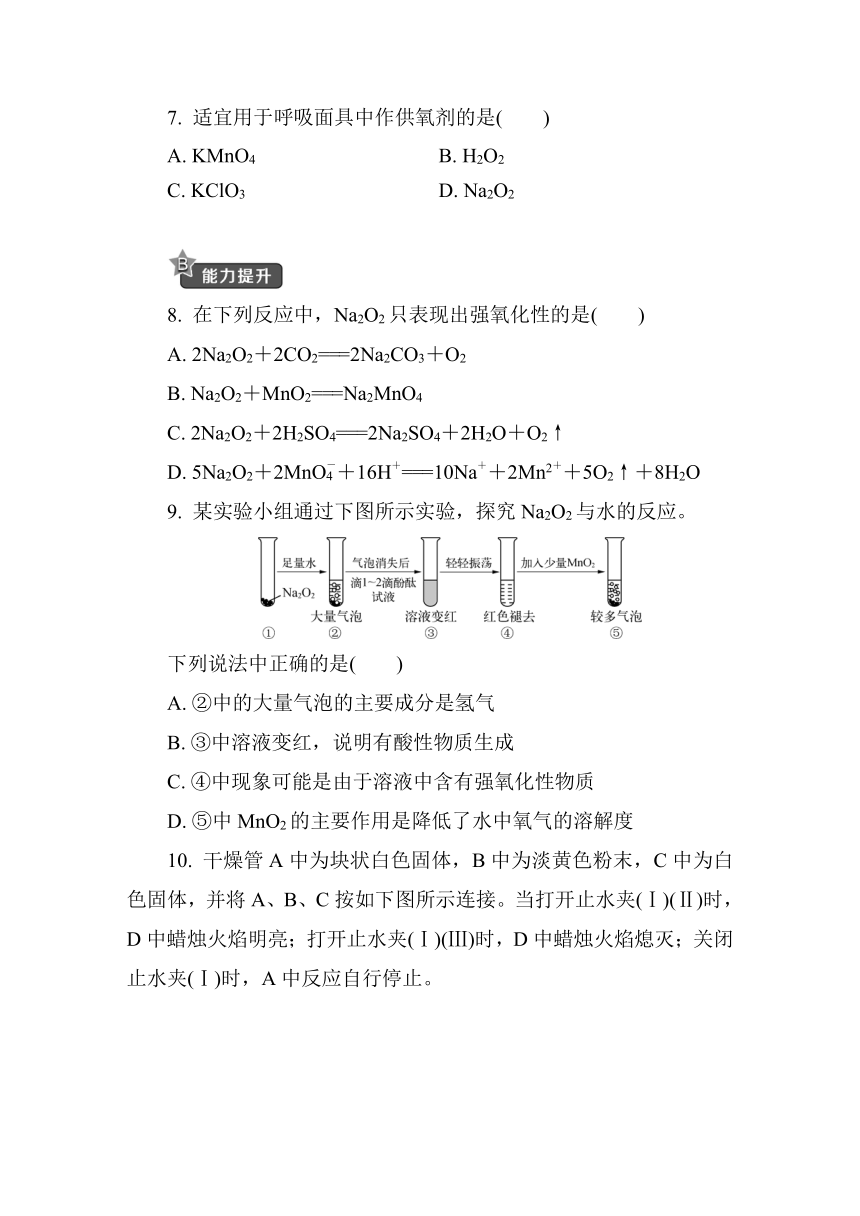
9. 某实验小组通过下图所示实验,探究Na2O2与水的反应。
下列说法中正确的是( )
A. ②中的大量气泡的主要成分是氢气
B. ③中溶液变红,说明有酸性物质生成
C. ④中现象可能是由于溶液中含有强氧化性物质
D. ⑤中MnO2的主要作用是降低了水中氧气的溶解度
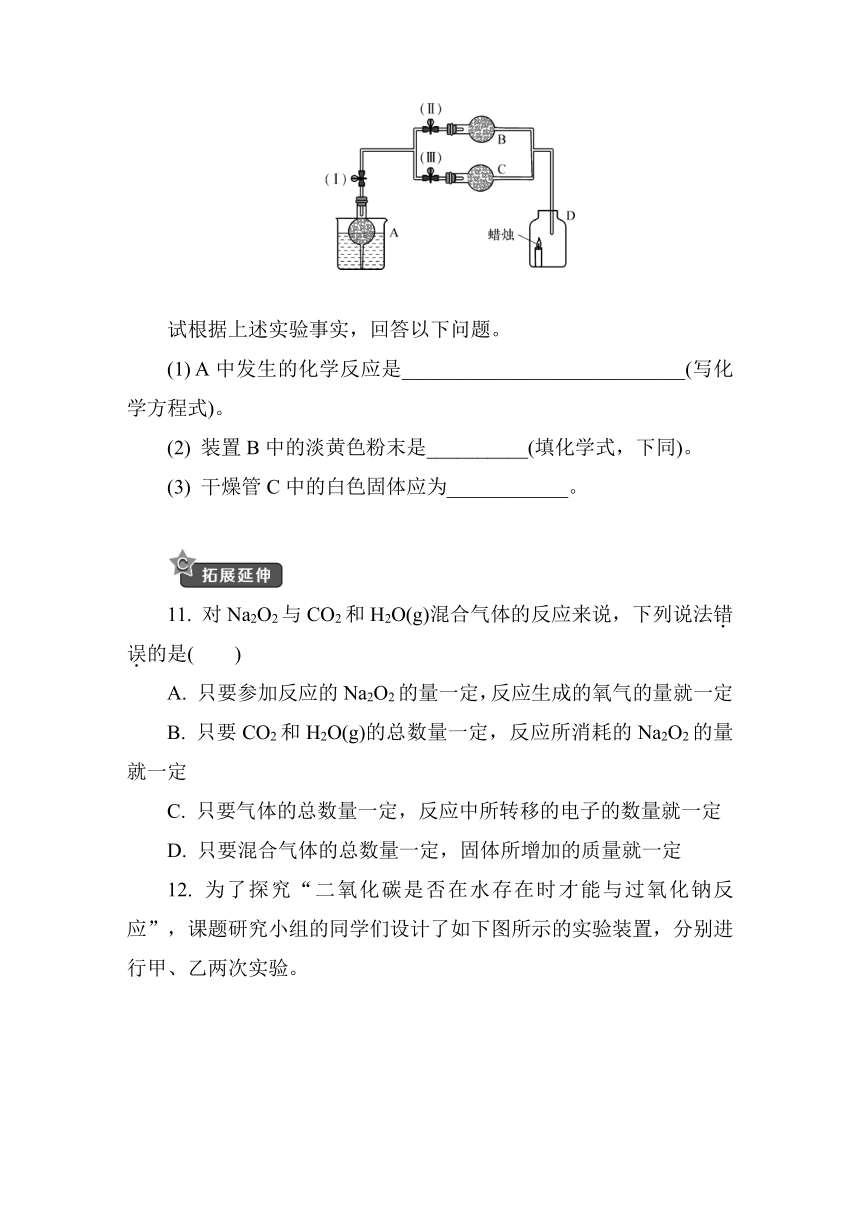
10. 干燥管A中为块状白色固体,B中为淡黄色粉末,C中为白色固体,并将A、B、C按如下图所示连接。当打开止水夹(Ⅰ)(Ⅱ)时,D中蜡烛火焰明亮;打开止水夹(Ⅰ)(Ⅲ)时,D中蜡烛火焰熄灭;关闭止水夹(Ⅰ)时,A中反应自行停止。
试根据上述实验事实,回答以下问题。
(1) A中发生的化学反应是____________________________(写化学方程式)。
(2) 装置B中的淡黄色粉末是__________(填化学式,下同)。
(3) 干燥管C中的白色固体应为____________。
11. 对Na2O2与CO2和H2O(g)混合气体的反应来说,下列说法错误的是( )
A. 只要参加反应的Na2O2的量一定,反应生成的氧气的量就一定
B. 只要CO2和H2O(g)的总数量一定,反应所消耗的Na2O2的量就一定
C. 只要气体的总数量一定,反应中所转移的电子的数量就一定
D. 只要混合气体的总数量一定,固体所增加的质量就一定
12. 为了探究“二氧化碳是否在水存在时才能与过氧化钠反应”,课题研究小组的同学们设计了如下图所示的实验装置,分别进行甲、乙两次实验。
实验甲: 干燥的二氧化碳与过氧化钠反应。在干燥的试管Ⅱ中装入Na2O2,在通入CO2之前,关闭K1和K2。在试管Ⅰ内装入试剂X后,打开K1和K2,通入CO2,几分钟后,将带火星的木条插入试管Ⅲ的液面上,观察到木条不复燃,且Ⅱ中的淡黄色没有变化。
实验乙: 潮湿的二氧化碳与过氧化钠反应。在试管Ⅰ内装入试剂Y,其他操作同实验甲,观察到木条复燃,且Ⅱ中的淡黄色变为白色。试回答下列问题:
(1) 在装入Na2O2后,通入CO2前,关闭K1和K2的目的是__________________。
(2) 在实验甲中,试剂X是____________,其作用是______________。
在实验乙中,试剂Y是________________。
(3) 根据上述两个实验现象,得到的结论是____________________________________。
(4) 试管Ⅲ中NaOH溶液的作用是____________________________________。
(5) 为了确保实验现象的准确性,制备CO2所用的反应物最好选用______________(填字母)。
A. 大理石 B. 小苏打 C. 烧碱 D. 盐酸 E. 稀硫酸 F. 稀硝酸
答案与解析
第2课时 钠的几种化合物——氧化钠和过氧化钠
1. B [解析] 碱性氧化物是指能与酸反应生成盐和水的化合物。
2. A [解析] 金属钠在足量氧气中燃烧生成Na2O2,为淡黄色固体。
3. C [解析] Na2O是白色固体,Na2O2是淡黄色固体;Na2O与水反应是化合反应,Na2O2与水反应生成NaOH和O2,不是化合反应;Na2O2是强氧化剂,Na2O不是。C项正确。
4. D [解析] A项中Na与H2O反应生成NaOH和H2;B项中Na2O2与H2O反应生成NaOH和O2;C项中Ca(OH)2溶液与Na2CO3溶液反应生成NaOH和CaCO3;D项中两种物质不反应。
5. A [解析] 过氧化钠与二氧化碳反应生成碳酸钠和氧气,氧化钠与二氧化碳反应生成碳酸钠,氢氧化钠与二氧化碳反应生成碳酸钠和水,氯化钠与二氧化碳之间不会发生反应,故选A。
6. C [解析] 棉花燃烧说明棉花已达着火点,说明过氧化钠与CO2反应放热,生成的O2助燃。
7. D [解析] KMnO4加热才能分解生成氧气,不适合在呼吸面具中使用;过氧化氢能分解生成氧气,一般需要催化剂来加快反应速率,且过氧化氢为液体,不方便携带;氯酸钾能分解生成氧气,但需要加热、需要催化剂,不适合在呼吸面具中使用;因过氧化钠为固体,携带方便,且能与人呼吸产生的二氧化碳反应生成氧气,不需要催化剂、不需要加热,则最适宜用于呼吸面具中作供氧剂,故D项正确。
8. B [解析] B选项中,Na2O2中-1价的氧化合价只降低,只表现出强氧化性,该反应中Mn的化合价由+4→+6。
9. C [解析] 过氧化钠与水反应生成NaOH和O2,则②中大量气泡的主要成分是氧气,A项错误;酚酞遇到碱显红色,③中溶液变红,说明有碱性物质生成,B项错误;④中红色褪去,应该是溶液中的强氧化性物质氧化酚酞导致酚酞变质,C项正确;⑤中加入MnO2产生较多气泡,说明溶液中存在H2O2,MnO2的主要作用是作催化剂,D项错误。
10. (1) CaCO3+2HCl===CaCl2+CO2↑+H2O (2) Na2O2 (3) CaCl2(或P2O5) [解析] 此题以蜡烛火焰的明亮和熄灭为突破口。明亮一定是通入了O2,而熄灭一般是CO2。由此可确定B中是Na2O2(淡黄色粉末)和CO2的反应;从而可知A是产生CO2的简易发生器,C中是一个不与CO2反应的白色固体,即是中性或酸性的固体干燥剂。
11. D [解析] Na2O2与H2O(g)、CO2反应的化学方程式分别为2Na2O2+2H2O(g)===4NaOH+O2、2Na2O2+2CO2===2Na2CO3+O2。由于两个反应中Na2O2与O2的数量之比都为2∶1,所以A项正确;两个反应中,2Na2O2~2H2O(g),2Na2O2~2CO2,所以B项正确;根据上面化学方程式中的电子转移情况知,C项正确;根据化学方程式知,CO2、H2O与Na2O2反应时,固体增加的质量为“CO2”中“CO”的质量和“H2O”中“H2”的质量,所以当数量固定的混合气体中CO2气体所占的比例大时,固体增加的质量较大,当H2O所占的比例大时,固体所增加的质量较小,则D项错误。
12. (1) 防止Na2O2受潮 (2) 浓硫酸 除去CO2中的水 CO2的饱和溶液(或水) (3) 二氧化碳只有在水存在时才能与过氧化钠反应 (4) 除去混在氧气中的过量二氧化碳 (5) B、E [解析] 因为实验要求确保现象的准确性,所以酸应该选择不会挥发的硫酸,选择了硫酸,就不能选择大理石,只能选择小苏打。
1. Na2O属于下列分类标准中的( )
A. 酸性氧化物 B. 碱性氧化物
C. 两性氧化物 D. 盐
2. 关于金属钠在足量氧气中燃烧的现象,下列说法中错误的是( )
A. 生成白色固体 B. 产生黄色火焰
C. 生成淡黄色固体 D. 钠熔化后表面显银白色
3. 下列关于Na2O和Na2O2的叙述中,正确的是( )
A. 都是白色的固体 B. 与水反应都属于化合反应
C. 都能与水反应形成强碱溶液 D. 都是强氧化剂
4. 下列各组物质间反应,不能生成NaOH的是( )
A. Na与H2O B. Na2O2与H2O
C. Ca(OH)2溶液与Na2CO3溶液 D. Ca(OH)2溶液与NaCl溶液
5. 能与CO2反应放出氧气的物质是( )
A. Na2O2 B. Na2O
C. NaOH D. NaCl
6. 一团棉花包裹少量过氧化钠放在石棉网上,将CO2气体缓缓通入棉花中的过氧化钠上,棉花很快燃烧起来,根据实验分析,下列表达错误的是( )
A. 反应生成的O2有利于棉花燃烧 B. 过氧化钠与CO2反应放热
C. CO2对棉花燃烧起助燃作用 D. 过氧化钠与CO2的反应属于氧化还原反应
7. 适宜用于呼吸面具中作供氧剂的是( )
A. KMnO4 B. H2O2
C. KClO3 D. Na2O2
8. 在下列反应中,Na2O2只表现出强氧化性的是( )
A. 2Na2O2+2CO2===2Na2CO3+O2
B. Na2O2+MnO2===Na2MnO4
C. 2Na2O2+2H2SO4===2Na2SO4+2H2O+O2↑
D. 5Na2O2+2MnO+16H+===10Na++2Mn2++5O2↑+8H2O
9. 某实验小组通过下图所示实验,探究Na2O2与水的反应。
下列说法中正确的是( )
A. ②中的大量气泡的主要成分是氢气
B. ③中溶液变红,说明有酸性物质生成
C. ④中现象可能是由于溶液中含有强氧化性物质
D. ⑤中MnO2的主要作用是降低了水中氧气的溶解度
10. 干燥管A中为块状白色固体,B中为淡黄色粉末,C中为白色固体,并将A、B、C按如下图所示连接。当打开止水夹(Ⅰ)(Ⅱ)时,D中蜡烛火焰明亮;打开止水夹(Ⅰ)(Ⅲ)时,D中蜡烛火焰熄灭;关闭止水夹(Ⅰ)时,A中反应自行停止。
试根据上述实验事实,回答以下问题。
(1) A中发生的化学反应是____________________________(写化学方程式)。
(2) 装置B中的淡黄色粉末是__________(填化学式,下同)。
(3) 干燥管C中的白色固体应为____________。
11. 对Na2O2与CO2和H2O(g)混合气体的反应来说,下列说法错误的是( )
A. 只要参加反应的Na2O2的量一定,反应生成的氧气的量就一定
B. 只要CO2和H2O(g)的总数量一定,反应所消耗的Na2O2的量就一定
C. 只要气体的总数量一定,反应中所转移的电子的数量就一定
D. 只要混合气体的总数量一定,固体所增加的质量就一定
12. 为了探究“二氧化碳是否在水存在时才能与过氧化钠反应”,课题研究小组的同学们设计了如下图所示的实验装置,分别进行甲、乙两次实验。
实验甲: 干燥的二氧化碳与过氧化钠反应。在干燥的试管Ⅱ中装入Na2O2,在通入CO2之前,关闭K1和K2。在试管Ⅰ内装入试剂X后,打开K1和K2,通入CO2,几分钟后,将带火星的木条插入试管Ⅲ的液面上,观察到木条不复燃,且Ⅱ中的淡黄色没有变化。
实验乙: 潮湿的二氧化碳与过氧化钠反应。在试管Ⅰ内装入试剂Y,其他操作同实验甲,观察到木条复燃,且Ⅱ中的淡黄色变为白色。试回答下列问题:
(1) 在装入Na2O2后,通入CO2前,关闭K1和K2的目的是__________________。
(2) 在实验甲中,试剂X是____________,其作用是______________。
在实验乙中,试剂Y是________________。
(3) 根据上述两个实验现象,得到的结论是____________________________________。
(4) 试管Ⅲ中NaOH溶液的作用是____________________________________。
(5) 为了确保实验现象的准确性,制备CO2所用的反应物最好选用______________(填字母)。
A. 大理石 B. 小苏打 C. 烧碱 D. 盐酸 E. 稀硫酸 F. 稀硝酸
答案与解析
第2课时 钠的几种化合物——氧化钠和过氧化钠
1. B [解析] 碱性氧化物是指能与酸反应生成盐和水的化合物。
2. A [解析] 金属钠在足量氧气中燃烧生成Na2O2,为淡黄色固体。
3. C [解析] Na2O是白色固体,Na2O2是淡黄色固体;Na2O与水反应是化合反应,Na2O2与水反应生成NaOH和O2,不是化合反应;Na2O2是强氧化剂,Na2O不是。C项正确。
4. D [解析] A项中Na与H2O反应生成NaOH和H2;B项中Na2O2与H2O反应生成NaOH和O2;C项中Ca(OH)2溶液与Na2CO3溶液反应生成NaOH和CaCO3;D项中两种物质不反应。
5. A [解析] 过氧化钠与二氧化碳反应生成碳酸钠和氧气,氧化钠与二氧化碳反应生成碳酸钠,氢氧化钠与二氧化碳反应生成碳酸钠和水,氯化钠与二氧化碳之间不会发生反应,故选A。
6. C [解析] 棉花燃烧说明棉花已达着火点,说明过氧化钠与CO2反应放热,生成的O2助燃。
7. D [解析] KMnO4加热才能分解生成氧气,不适合在呼吸面具中使用;过氧化氢能分解生成氧气,一般需要催化剂来加快反应速率,且过氧化氢为液体,不方便携带;氯酸钾能分解生成氧气,但需要加热、需要催化剂,不适合在呼吸面具中使用;因过氧化钠为固体,携带方便,且能与人呼吸产生的二氧化碳反应生成氧气,不需要催化剂、不需要加热,则最适宜用于呼吸面具中作供氧剂,故D项正确。
8. B [解析] B选项中,Na2O2中-1价的氧化合价只降低,只表现出强氧化性,该反应中Mn的化合价由+4→+6。
9. C [解析] 过氧化钠与水反应生成NaOH和O2,则②中大量气泡的主要成分是氧气,A项错误;酚酞遇到碱显红色,③中溶液变红,说明有碱性物质生成,B项错误;④中红色褪去,应该是溶液中的强氧化性物质氧化酚酞导致酚酞变质,C项正确;⑤中加入MnO2产生较多气泡,说明溶液中存在H2O2,MnO2的主要作用是作催化剂,D项错误。
10. (1) CaCO3+2HCl===CaCl2+CO2↑+H2O (2) Na2O2 (3) CaCl2(或P2O5) [解析] 此题以蜡烛火焰的明亮和熄灭为突破口。明亮一定是通入了O2,而熄灭一般是CO2。由此可确定B中是Na2O2(淡黄色粉末)和CO2的反应;从而可知A是产生CO2的简易发生器,C中是一个不与CO2反应的白色固体,即是中性或酸性的固体干燥剂。
11. D [解析] Na2O2与H2O(g)、CO2反应的化学方程式分别为2Na2O2+2H2O(g)===4NaOH+O2、2Na2O2+2CO2===2Na2CO3+O2。由于两个反应中Na2O2与O2的数量之比都为2∶1,所以A项正确;两个反应中,2Na2O2~2H2O(g),2Na2O2~2CO2,所以B项正确;根据上面化学方程式中的电子转移情况知,C项正确;根据化学方程式知,CO2、H2O与Na2O2反应时,固体增加的质量为“CO2”中“CO”的质量和“H2O”中“H2”的质量,所以当数量固定的混合气体中CO2气体所占的比例大时,固体增加的质量较大,当H2O所占的比例大时,固体所增加的质量较小,则D项错误。
12. (1) 防止Na2O2受潮 (2) 浓硫酸 除去CO2中的水 CO2的饱和溶液(或水) (3) 二氧化碳只有在水存在时才能与过氧化钠反应 (4) 除去混在氧气中的过量二氧化碳 (5) B、E [解析] 因为实验要求确保现象的准确性,所以酸应该选择不会挥发的硫酸,选择了硫酸,就不能选择大理石,只能选择小苏打。
