2023秋高中化学人教版2019必修1 第三章 铁 金属材料 第1节 第1课时 铁的单质 课时同步练(含答案)
文档属性
| 名称 | 2023秋高中化学人教版2019必修1 第三章 铁 金属材料 第1节 第1课时 铁的单质 课时同步练(含答案) |

|
|
| 格式 | DOC | ||
| 文件大小 | 172.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-12 00:00:00 | ||
图片预览


文档简介
第三章 铁 金属材料
第一节 铁及其化合物
第1课时 铁的单质
1. 下列关于铁的说法中,正确的是( )
A. 纯净的铁单质是具有磁性的黑色固体
B. 铁是地壳中含量最多的金属元素
C. 铁及其合金是使用量最大的金属材料
D. 铁在氧气中燃烧生成三氧化二铁
2. 下列反应能通过置换反应生成铁的是( )
A. Cu+FeCl2(溶液) B. Na+FeSO4(溶液)
C. Fe2O3+CO(高温) D. Fe3O4+H2(加热)
3. 下列反应中,没有氢气生成的是( )
A. 单质钠投入水中 B. 镁投入稀盐酸中
C. 铜块放入稀硫酸中 D. 往铁粉中通入水蒸气,并高温加热
4. 铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中的常见物质,四种物质间的反应关系如图所示。图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应的离子方程式书写正确的是( )
A. OH-+HCl===H2O+Cl-
B. Ca(OH)2+Cu2+===Ca2++Cu(OH)2
C. Fe+Cu2+===Cu+Fe2+
D. Fe+2H+===Fe3++H2↑
5. 下列物质中,在一定条件下能将铁元素从0价转变为+3价的是( )
A. 氯气 B. 盐酸
C. 稀硫酸 D. 硫酸铜溶液
6. 下列说法不正确的是( )
A. 铁在高温下与水蒸气的反应是置换反应
B. 铁与纯氧气和水蒸气反应都能生成四氧化三铁
C. 铁与盐酸反应生成氯化铁和氢气
D. 铁与盐酸或水蒸气反应,铁都作还原剂
7. 等量的铁分别与足量的盐酸、水蒸气在一定的条件下充分反应,则在相同的条件下,产生氢气的体积比是( )
A. 1∶1 B. 3∶4
C. 2∶3 D. 4∶3
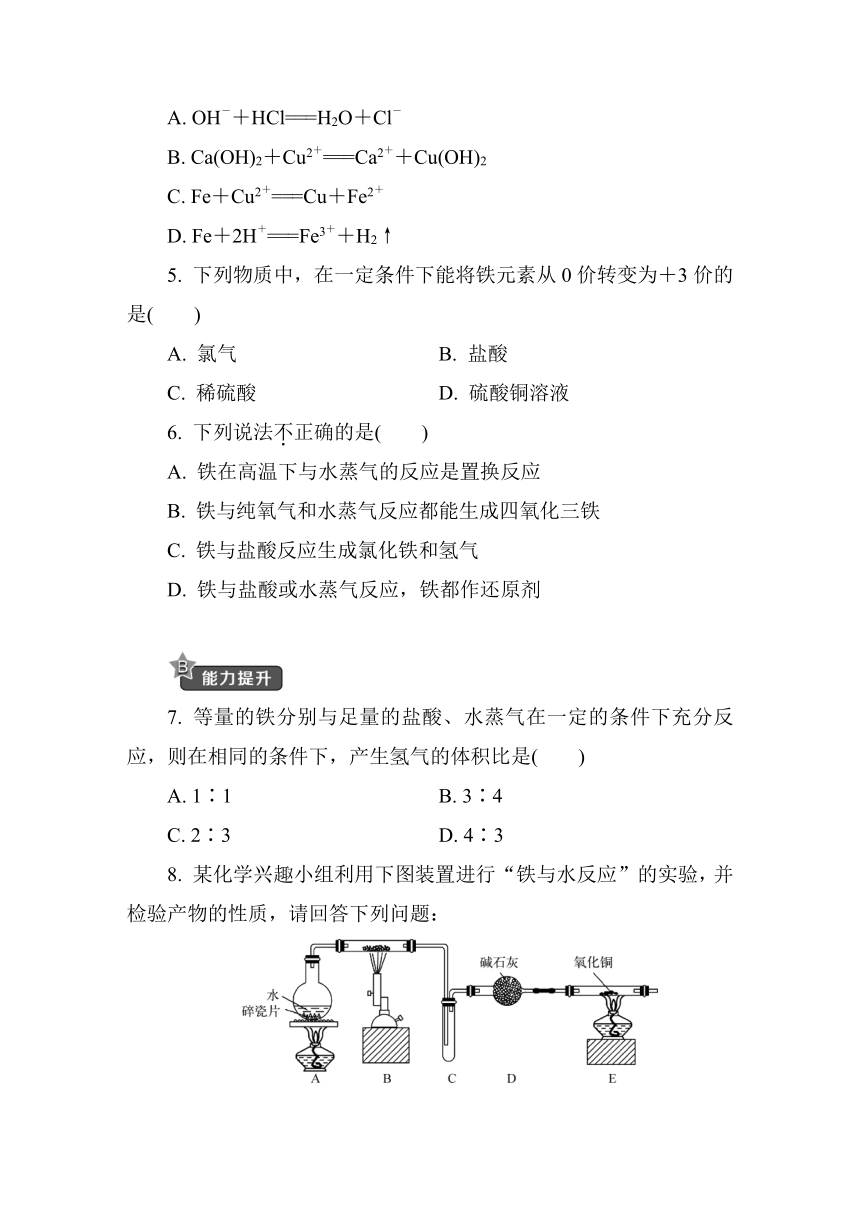
8. 某化学兴趣小组利用下图装置进行“铁与水反应”的实验,并检验产物的性质,请回答下列问题:
(1) A装置的作用是_______________________________________________________,
B中反应的化学方程式为__________________________________________________。
(2) D的作用是__________________________________________________。
(3) E中的现象是________________________________________________________。
(4) A、B两个装置中应先点燃________处的酒精灯,点燃E处酒精灯之前应进行的操作是________________________________________________________________________________________________________。
9. 在高温下用一氧化碳还原mg四氧化三铁得到ng铁。已知氧的相对原子质量为16,则铁的相对原子质量可表示为( )
A. B.
C. D.
10. 某同学利用下图所示实验装置进行铁与水蒸气反应的实验,并对反应后硬质试管中固体物质的组成进行了探究。
请回答下列问题:
(1) 硬质试管中湿棉花的作用是__________________________________________。
(2) 铁与水蒸气的反应中,氧化剂是____________(填化学式,下同),还原剂是________________。
(3) 该同学对反应后硬质试管中固体物质的组成提出了如下假设。
假设1: 只有Fe;
假设2: 只有____________(填化学式);
假设3: 既有Fe也有Fe3O4。
(4) 为了验证反应后硬质试管中固体物质的组成,该同学进行了定量研究: 反应前固体物质的质量为5.6g,反应后固体物质的质量为6.6g。从数据分析,反应后硬质试管中固体物质的组成为____________。
答案与解析
第一节 铁及其化合物
第1课时 铁的单质
1. C [解析] A项,具有磁性的黑色固体是Fe3O4;B项,地壳中含量最多的金属元素是Al;C项正确;D项,铁在氧气中燃烧生成Fe3O4。
2. D [解析] A项,Cu的活泼性弱于Fe,不能置换;B项,钠先与水反应生成氢氧化钠,不能置换出铁;C项,不是置换反应。
3. C [解析] A项,发生反应2Na+2H2O===2NaOH+H2↑;B项,发生反应Mg+2HCl===MgCl2+H2↑;C项,铜与稀硫酸不反应,不会生成氢气;D项,发生反应3Fe+4H2O(g)Fe3O4+4H2。
4. C [解析] 稀盐酸与石灰水发生中和反应,反应的离子方程式应为H++OH-===H2O,A项错误;氯化铜与石灰水反应生成氢氧化铜沉淀,反应的离子方程式为Cu2++2OH-===Cu(OH)2↓,B项错误;铁与氯化铜溶液发生置换反应,生成氯化亚铁和铜,反应的离子方程式为Fe+Cu2+===Fe2++Cu,C项正确;铁为活泼金属,与稀盐酸发生置换反应生成氢气,离子方程式为Fe+2H+===Fe2++H2↑,D项错误。
5. A [解析] 氯气与铁在点燃的条件下反应生成氯化铁和氢气,A项正确;盐酸与铁反应生成氯化亚铁和氢气,得到的是+2价铁,B项错误;稀硫酸与铁反应生成硫酸亚铁和氢气,得到的是+2价铁,C项错误;硫酸铜溶液与铁反应生成硫酸亚铁和铜,得到的是+2价铁,D项错误。
6. C [解析] 铁与盐酸反应生成氯化亚铁和氢气。
7. B [解析] 铁与足量的盐酸和水蒸气反应的化学方程式分别是Fe+2HCl===FeCl2+H2↑、 3Fe+4H2O(g)Fe3O4+4H2,则相同的条件下,等量的铁产生氢气的体积比为3∶4。
8. (1) 产生水蒸气 3Fe+4H2O(g)Fe3O4+4H2 (2) 吸收未反应的水蒸气 (3) 黑色固体变为红色,右端管壁有水珠生成 (4) A 收集H2,并检验其纯度 [解析] (1) B中进行的反应是3Fe+4H2O(g)Fe3O4+4H2,故A为提供水蒸气的装置。(2) D的作用是除去未反应的水蒸气,干燥H2。(3) E中反应为H2+CuOCu+H2O,故黑色固体变红,同时硬质玻璃管右端会有水珠生成。(4) 应先点燃A处,若先点燃B处,B中的Fe会与空气中的O2反应生成Fe3O4,点燃E处酒精灯前要收集H2,检验纯度。
9. B [解析] 设Fe的相对原子质量为x,则:
4CO+Fe3O44CO2+3Fe
3x+64 3x
mg ng
= x=
10. (1) 提供反应需要的水蒸气 (2) H2O Fe (3) Fe3O4 (4) Fe和Fe3O4 [解析] (1) 硬质试管中的湿棉花受热时可产生水蒸气,故硬质试管中湿棉花的作用是提供反应需要的水蒸气。(2) 根据化学方程式3Fe+4H2O(g)Fe3O4+4H2,Fe在反应中失去电子作还原剂,H2O在反应中得到电子作氧化剂。(3) 若Fe没有反应,则固体物质为Fe;若Fe部分反应,则固体物质为Fe与Fe3O4的混合物;若Fe全部反应,则固体物质为Fe3O4。(4) 根据化学方程式计算,若5.6g Fe完全反应,应得到约7.7g Fe3O4,而实验测得反应后固体物质的质量为6.6g,说明Fe部分反应,故反应后硬质试管中的固体物质为Fe和Fe3O4的混合物。
第一节 铁及其化合物
第1课时 铁的单质
1. 下列关于铁的说法中,正确的是( )
A. 纯净的铁单质是具有磁性的黑色固体
B. 铁是地壳中含量最多的金属元素
C. 铁及其合金是使用量最大的金属材料
D. 铁在氧气中燃烧生成三氧化二铁
2. 下列反应能通过置换反应生成铁的是( )
A. Cu+FeCl2(溶液) B. Na+FeSO4(溶液)
C. Fe2O3+CO(高温) D. Fe3O4+H2(加热)
3. 下列反应中,没有氢气生成的是( )
A. 单质钠投入水中 B. 镁投入稀盐酸中
C. 铜块放入稀硫酸中 D. 往铁粉中通入水蒸气,并高温加热
4. 铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中的常见物质,四种物质间的反应关系如图所示。图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应的离子方程式书写正确的是( )
A. OH-+HCl===H2O+Cl-
B. Ca(OH)2+Cu2+===Ca2++Cu(OH)2
C. Fe+Cu2+===Cu+Fe2+
D. Fe+2H+===Fe3++H2↑
5. 下列物质中,在一定条件下能将铁元素从0价转变为+3价的是( )
A. 氯气 B. 盐酸
C. 稀硫酸 D. 硫酸铜溶液
6. 下列说法不正确的是( )
A. 铁在高温下与水蒸气的反应是置换反应
B. 铁与纯氧气和水蒸气反应都能生成四氧化三铁
C. 铁与盐酸反应生成氯化铁和氢气
D. 铁与盐酸或水蒸气反应,铁都作还原剂
7. 等量的铁分别与足量的盐酸、水蒸气在一定的条件下充分反应,则在相同的条件下,产生氢气的体积比是( )
A. 1∶1 B. 3∶4
C. 2∶3 D. 4∶3
8. 某化学兴趣小组利用下图装置进行“铁与水反应”的实验,并检验产物的性质,请回答下列问题:
(1) A装置的作用是_______________________________________________________,
B中反应的化学方程式为__________________________________________________。
(2) D的作用是__________________________________________________。
(3) E中的现象是________________________________________________________。
(4) A、B两个装置中应先点燃________处的酒精灯,点燃E处酒精灯之前应进行的操作是________________________________________________________________________________________________________。
9. 在高温下用一氧化碳还原mg四氧化三铁得到ng铁。已知氧的相对原子质量为16,则铁的相对原子质量可表示为( )
A. B.
C. D.
10. 某同学利用下图所示实验装置进行铁与水蒸气反应的实验,并对反应后硬质试管中固体物质的组成进行了探究。
请回答下列问题:
(1) 硬质试管中湿棉花的作用是__________________________________________。
(2) 铁与水蒸气的反应中,氧化剂是____________(填化学式,下同),还原剂是________________。
(3) 该同学对反应后硬质试管中固体物质的组成提出了如下假设。
假设1: 只有Fe;
假设2: 只有____________(填化学式);
假设3: 既有Fe也有Fe3O4。
(4) 为了验证反应后硬质试管中固体物质的组成,该同学进行了定量研究: 反应前固体物质的质量为5.6g,反应后固体物质的质量为6.6g。从数据分析,反应后硬质试管中固体物质的组成为____________。
答案与解析
第一节 铁及其化合物
第1课时 铁的单质
1. C [解析] A项,具有磁性的黑色固体是Fe3O4;B项,地壳中含量最多的金属元素是Al;C项正确;D项,铁在氧气中燃烧生成Fe3O4。
2. D [解析] A项,Cu的活泼性弱于Fe,不能置换;B项,钠先与水反应生成氢氧化钠,不能置换出铁;C项,不是置换反应。
3. C [解析] A项,发生反应2Na+2H2O===2NaOH+H2↑;B项,发生反应Mg+2HCl===MgCl2+H2↑;C项,铜与稀硫酸不反应,不会生成氢气;D项,发生反应3Fe+4H2O(g)Fe3O4+4H2。
4. C [解析] 稀盐酸与石灰水发生中和反应,反应的离子方程式应为H++OH-===H2O,A项错误;氯化铜与石灰水反应生成氢氧化铜沉淀,反应的离子方程式为Cu2++2OH-===Cu(OH)2↓,B项错误;铁与氯化铜溶液发生置换反应,生成氯化亚铁和铜,反应的离子方程式为Fe+Cu2+===Fe2++Cu,C项正确;铁为活泼金属,与稀盐酸发生置换反应生成氢气,离子方程式为Fe+2H+===Fe2++H2↑,D项错误。
5. A [解析] 氯气与铁在点燃的条件下反应生成氯化铁和氢气,A项正确;盐酸与铁反应生成氯化亚铁和氢气,得到的是+2价铁,B项错误;稀硫酸与铁反应生成硫酸亚铁和氢气,得到的是+2价铁,C项错误;硫酸铜溶液与铁反应生成硫酸亚铁和铜,得到的是+2价铁,D项错误。
6. C [解析] 铁与盐酸反应生成氯化亚铁和氢气。
7. B [解析] 铁与足量的盐酸和水蒸气反应的化学方程式分别是Fe+2HCl===FeCl2+H2↑、 3Fe+4H2O(g)Fe3O4+4H2,则相同的条件下,等量的铁产生氢气的体积比为3∶4。
8. (1) 产生水蒸气 3Fe+4H2O(g)Fe3O4+4H2 (2) 吸收未反应的水蒸气 (3) 黑色固体变为红色,右端管壁有水珠生成 (4) A 收集H2,并检验其纯度 [解析] (1) B中进行的反应是3Fe+4H2O(g)Fe3O4+4H2,故A为提供水蒸气的装置。(2) D的作用是除去未反应的水蒸气,干燥H2。(3) E中反应为H2+CuOCu+H2O,故黑色固体变红,同时硬质玻璃管右端会有水珠生成。(4) 应先点燃A处,若先点燃B处,B中的Fe会与空气中的O2反应生成Fe3O4,点燃E处酒精灯前要收集H2,检验纯度。
9. B [解析] 设Fe的相对原子质量为x,则:
4CO+Fe3O44CO2+3Fe
3x+64 3x
mg ng
= x=
10. (1) 提供反应需要的水蒸气 (2) H2O Fe (3) Fe3O4 (4) Fe和Fe3O4 [解析] (1) 硬质试管中的湿棉花受热时可产生水蒸气,故硬质试管中湿棉花的作用是提供反应需要的水蒸气。(2) 根据化学方程式3Fe+4H2O(g)Fe3O4+4H2,Fe在反应中失去电子作还原剂,H2O在反应中得到电子作氧化剂。(3) 若Fe没有反应,则固体物质为Fe;若Fe部分反应,则固体物质为Fe与Fe3O4的混合物;若Fe全部反应,则固体物质为Fe3O4。(4) 根据化学方程式计算,若5.6g Fe完全反应,应得到约7.7g Fe3O4,而实验测得反应后固体物质的质量为6.6g,说明Fe部分反应,故反应后硬质试管中的固体物质为Fe和Fe3O4的混合物。
