5.1 质量守恒定律 同步练习 (含解析)2022-2023学年上学期广东省九年级化学期末试题选编
文档属性
| 名称 | 5.1 质量守恒定律 同步练习 (含解析)2022-2023学年上学期广东省九年级化学期末试题选编 |

|
|
| 格式 | docx | ||
| 文件大小 | 261.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-13 00:00:00 | ||
图片预览



文档简介
5.1 质量守恒定律
一、单选题
1.(2022秋·广东湛江·九年级统考期末)将一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下。下列说法不正确的是
A.a和b是反应物,d可能是催化剂
B.反应后a的质量为3.84g
C.c中元素种类一定等于a、b两种物质中元素的种类之和
D.该反应属于分解反应
2.(2022秋·广东揭阳·九年级统考期末)现取6.9g某可燃物在足量氧气中完全燃烧,生成了13.2gCO2和8.1gH2O,对该物质的组成有下列推断:
①一定含有C、H元素
②一定不含有O元素
③可能含有O元素
④一定含有O元素
⑤可燃物的分子中C、H的原子个数比为2:5
⑥可燃物中C、H元素的质量比为4:1
其中正确的是
A.①②⑤ B.①③⑥ C.①④⑤ D.①④⑥
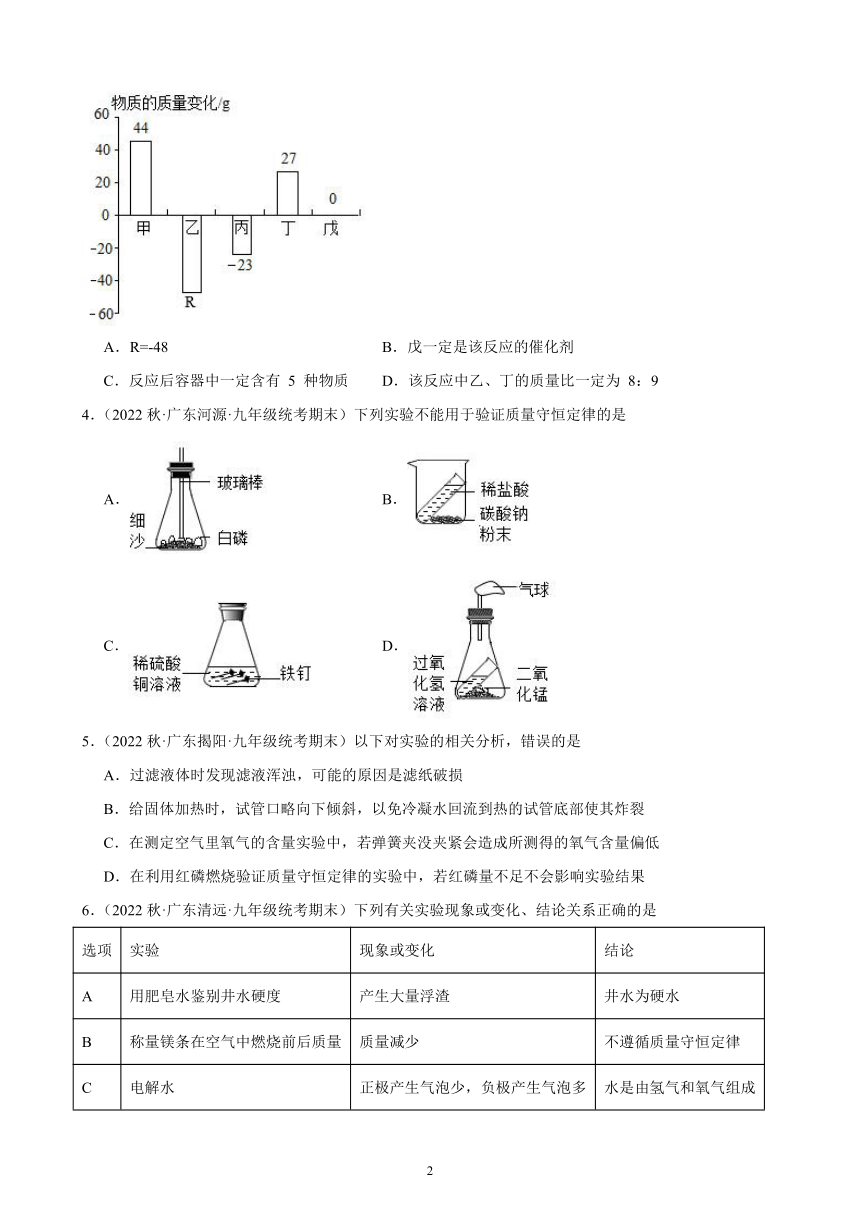
3.(2022秋·广东汕头·九年级统考期末)在一个密闭容器中,有甲、乙、丙、丁、戊五种物质,在一定条件下发生反应,测得反应前后各物质的质量变化量如图所示(图中正数表示物质质量的增加量,负数表示物质质量的减少量,0 表示物质质量不变),下列说法正确的是
A.R=-48 B.戊一定是该反应的催化剂
C.反应后容器中一定含有 5 种物质 D.该反应中乙、丁的质量比一定为 8:9
4.(2022秋·广东河源·九年级统考期末)下列实验不能用于验证质量守恒定律的是
A. B.
C. D.
5.(2022秋·广东揭阳·九年级统考期末)以下对实验的相关分析,错误的是
A.过滤液体时发现滤液浑浊,可能的原因是滤纸破损
B.给固体加热时,试管口略向下倾斜,以免冷凝水回流到热的试管底部使其炸裂
C.在测定空气里氧气的含量实验中,若弹簧夹没夹紧会造成所测得的氧气含量偏低
D.在利用红磷燃烧验证质量守恒定律的实验中,若红磷量不足不会影响实验结果
6.(2022秋·广东清远·九年级统考期末)下列有关实验现象或变化、结论关系正确的是
选项 实验 现象或变化 结论
A 用肥皂水鉴别井水硬度 产生大量浮渣 井水为硬水
B 称量镁条在空气中燃烧前后质量 质量减少 不遵循质量守恒定律
C 电解水 正极产生气泡少,负极产生气泡多 水是由氢气和氧气组成
D 测定空气中氧气成分 水流入集气瓶1/5 氧气质量分数约1/5
A.A B.B C.C D.D
7.(2022秋·广东东莞·九年级统考期末)下图是某化学反应的微观粒子图。反应后的方框内应再填入1个粒子
A. B. C. D.
8.(2022秋·广东韶关·九年级统考期末)下图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子。下列说法错误的是
A.此反应有单质生成
B.原子在化学变化中是不可分的
C.参加反应的两种分子的个数比为2∶2
D.图中生成物有三种
9.(2022秋·广东梅州·九年级统考期末)“宏观-微观-符号”三重表征是化学学科的基本特征。下图是某化学反应的微观示意图,下列说法错误的是
A.从定量研究看:该反应符合质量守恒定律
B.从微观构成看:该反应中涉及的物质均由分子构成
C.从反应类型看:该反应属于置换反应
D.从反应价值看:该反应能获取新物质
10.(2022秋·广东韶关·九年级统考期末)甲和乙在一定条件下反应生成丙和丁,微观示意图如下、有关说法正确的是
A.参加反应的甲和乙的分子个数比为5:4 B.反应前后各元素的化合价均不变
C.反应前后分子的种类不变 D.丙物质由2个氢原子和1个氧原子构成
11.(2022秋·广东韶关·九年级统考期末)在一个密闭容器中放入W、G、H、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表:
物质 W G H P
反应前质量/g 18 1 2 32
反应后质量/g 待测 26 2 12
对该反应的认识正确的是
A.该反应是分解反应 B.W待测值是13
C.P是生成物 D.物质H是该反应的催化剂
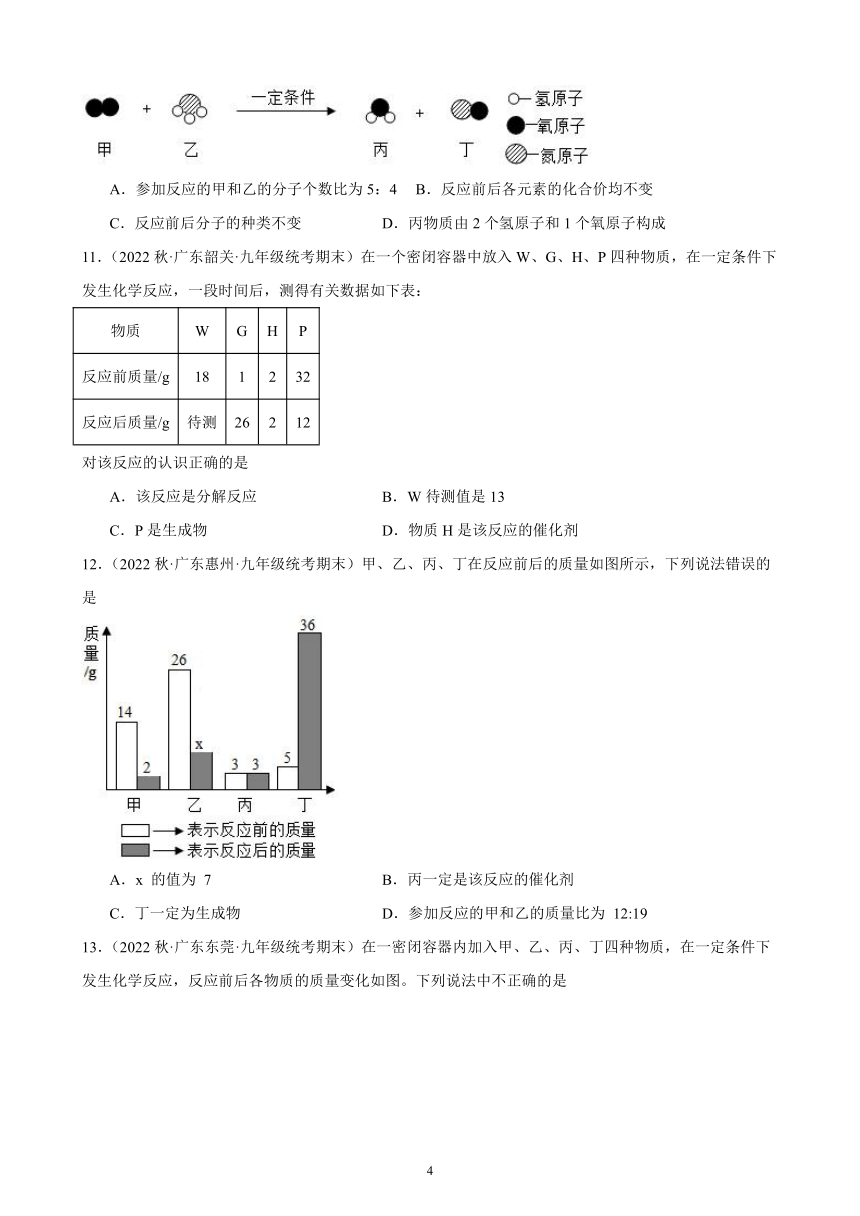
12.(2022秋·广东惠州·九年级统考期末)甲、乙、丙、丁在反应前后的质量如图所示,下列说法错误的是
A.x 的值为 7 B.丙一定是该反应的催化剂
C.丁一定为生成物 D.参加反应的甲和乙的质量比为 12:19
13.(2022秋·广东东莞·九年级统考期末)在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化如图。下列说法中不正确的是
A.X的数值为3 B.该反应为分解反应
C.丙一定是该反应的催化剂 D.参加反应的乙和丁质量比为3:2
14.(2022秋·广东深圳·九年级统考期末)在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应认识不正确的是
物质 M N Q P
反应前质量(g) 18 1 2 32
反应后质量(g) x 26 2 12
A.该变化的基本反应类型是分解反应
B.反应后物质x的值为13
C.反应中N、P的质量比为5:4
D.物质Q可能是该反应的催化剂
15.(2022秋·广东河源·九年级统考期末)在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如下表所示,下列说法不正确的是
物质 X Y Z W
反应前质量/g 10 3 90 0
反应后质量/g 3.2 3 待测 3.2
A.W可能是单质
B.Y可能是催化剂
C.该反应是分解反应
D.反应后Z物质的质量为86.4g
16.(2022秋·广东河源·九年级统考期末)下列图像能正确反映对应变化关系的是
A.①高温煅烧一定质量的碳酸钙 B.②测定空气中氧气的含量
C.③用两份等质量的氯酸钾固体制取氧气 D.④加热一定质量的高锰酸钾
17.(2022秋·广东东莞·九年级统考期末)看到千奇百怪的钟乳石,大家无不感叹大自然的鬼斧神工,其实里面蕴含了丰富的化学知识。其反应原理为X+CO2+H2O=Ca(HCO3)2(方程式已配平)则X的化学式是
A.CaO B.CaCO3 C.Ca(OH)2 D.CaO2
18.(2022秋·广东韶关·九年级统考期末)将一定质量的a,b,c,d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得各物质的质量如表:下列有关说法正确的是
物质 a b c d
反应前的质量/g 6.0 14.0 3.2 1.0
反应后的质量/g 10.0 7.2 x 1.0
A.x=3.2 B.该反应属于分解反应
C.反应中a与b的质量比为3:7 D.d一定是催化剂
二、选择题组
(2022秋·广东揭阳·九年级统考期末)在每小题给出的四个选项中,有一项或两项符合题目要求。
新鲜大蒜头中含蒜氨酸(C6H11NSO3),蒜氨酸受撞击后,会转化为大蒜素。大蒜素(C6H10S2O)有较强的抗菌作用,易挥发,遇热或碱立即失去抗菌活性,但不受酸的影响。根据以上材料,完成下面小题。
19.下列有关大蒜素和蒜氨酸的说法,正确的是
A.大蒜素和蒜氨酸组成元素相同
B.蒜氨酸中硫、氧元素的质量比为2:1
C.大蒜素完全燃烧时只生成二氧化碳和水
D.与蒜氨酸相比,大蒜素中碳元素的质量分数更高
20.下列有关大蒜性质与变化的说法,不正确的是
A.挥发性是大蒜素的物理性质 B.捣蒜过程中仅发生物理变化
C.大蒜煮熟食用比生食抗菌效果更好 D.捣好的蒜泥可以与醋一起食用
三、多选题
21.(2022秋·广东湛江·九年级统考期末)元素钠(Na)有多种化合价,将4.6gNa在氧气中充分燃烧,得到7.8g钠的氧化物,该氧化物的化学式是
A.Na2O B.NaO C.Na2O2 D.NaO2
四、填空题
22.(2022秋·广东广州·九年级统考期末)化学与生活、生产、科技发展息息相关。
(1)硅酸钠(Na2SiO3)可用作黏合剂和防火材料,其中Si元素的化合价为 。
(2)汽车是重要的交通工具,为了降低污染可以使用电动车,请完成铅酸电池充电反应的方程式:2PbSO4 + 2H2OPb + 2H2SO4 + 。
(3)2020年12月3日,我国“嫦娥五号”成功发射,显示我国科技实力的飞速发展。我国空间站“天宫”内的“空气”与地球上的空气组成基本一致,已知同温同压下,相同体积的气体含有相同数目的分子,“空气”中O2与N2的分子个数比约为 。
(4)Cu能与空气中的 、 (写出其中两种物质的化学式)发生化合反应生成“铜锈”[主要成分为Cu2(OH)2CO3]。
(5)一定条件下,CO2和H2反应生成CH4和H2O,见下图。
①该反应的化学方程式是 。
②从微观角度分析,A图中的物质属于混合物的原因是 。
③请在B图中将该反应的微观粒子补充完整 。
23.(2022秋·广东湛江·九年级统考期末)实验室制取氧气时,某同学取氯酸钾和二氧化锰的固体混合物共 15.0g 进行加热,固体的质量与加热时间的关系如图所示。
(1)解释固体质量不变的原因:t1时间前 ;t4后 ;
(2)t4时,制得氧气的质量是 g。
(3)t5时,固体混合物中 MnO2的质量为多少?
24.(2022秋·广东广州·九年级统考期末)洋溢着绿色与科技元素的2022北京冬奥会以中国式的传奇与浪漫惊艳了世界。
(1)衣:运动服中高科技材料石墨烯的使用,解决了超低温户外环境下运动员的取暖难题。石墨烯是由 元素组成的单质。
(2)住:奥运村实现了5G网络的全覆盖。制造5G芯片的氮化镓(GaN)材料可由氯化镓(GaCl3)制取,氮化镓中氮元素的化合价为 。
(3)行:冬奥会会务用车均使用氢能源汽车,基本实现了碳的零排放。相比于化石燃料,氢气作为燃料的优点是 (只写一点)。
(4)防:日常消杀也是必需的防疫措施。二氧化氯(ClO2)是一种常用消毒剂,其制取的一种原理是:Cl2+2NaClO2═2ClO2+2X,则X的化学式为 。
五、实验题
25.(2022秋·广东湛江·九年级统考期末)为验证质量守恒定律,某兴趣小组做了以下实验进行探究。
实验一:将 10g 水加入 10g 酒精中,一段时间后,称量混合液,质量仍为 20g。
(1)该实验 (填“能”或“不能”)验证质量守恒定律,原因是 。
实验二:如图 1,用细铜丝吊着一根长玻璃棒,两端分别绕上粗铜丝,并使玻璃棒保持水平,然后用酒精灯给 a 端铜丝加热 1~2 分钟。
(2)冷却后,观察到铜丝变黑、玻璃棒 (填“a”或“b”)端下沉。
实验三:称取镁条和石棉网的质量为 m1(如图 2 所示),然后在空气中点燃镁条;反应结束后将所得物质与石棉网一起再次称量,质量为 m2。
(3)写出镁条燃烧的化学方程式 ,该反应属于 反应(填基本反应类型)。
(4)根据质量守恒定律可知:生成氧化镁的质量大于参加反应的镁条的质量;而实验事实是 m2【分析与总结】
(5)根据以上实验可知,验证质量守恒定律时,对于有气体参加的反应,应在 容器中进行实验。
【拓展实验】兴趣小组按如图 3 装置改进实验,验证了质量守恒定律,却发现产物白色固体中还有少量黄色固体。查阅资料得知:镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体。
【反思与交流】
(6)空气中 N2的含量远大于 O2的含量,而镁条在空气中燃烧生成的 MgO 却远多于 Mg3N2,原因是 。
(7)图 3 实验中气球的作用除了使装置密闭之外,还可以防止 。
六、科学探究题
26.(2022秋·广东广州·九年级统考期末)2021年12月9日下午,小明观看完“天宫第一课”后,对王亚平老师的泡腾片实验非常感兴趣,想起自己在补充维生素C时也用过泡腾片,于是把一颗维生素C泡腾片药片丢入水中,发现药片表面产生大量的气泡。出于好奇他开展了如下探究:
【查阅资料】维C泡腾片是一种较新的药物剂型,主要成分有:维C(C6H8O6)、碳酸氢钠(NaHCO3)、柠檬酸(C6H8O7)。维C泡腾片利用柠檬酸和碳酸氢钠反应做泡腾崩解剂、置入水中,即刻发生泡腾反应,生成大量的气体,状如沸腾,故名泡腾片。
【提出猜想】假设产生的气体可能是CO2、N2、O2
(1)小明认真思考后认为产生的气体不可能是N2,因为 。
【进行实验】
(2)小明将气体通入 中,观察到 现象,证明该气体是CO2。
【反思评价】
(3)为了验证该反应是否遵循质量守恒定律,小明设计了如图所示的实验,实验前托盘天平的指针指向中间,反应结束后发现天平的指针偏 ,其原因是 。由此他得出凡是有气体参与或生成的化学反应,在验证质量守恒时,反应装置应该在 容器内进行。
小明继续查阅资料,得知:泡腾片在消毒剂上也有广泛的应用,其中二氧化氯泡腾片是其中一种消毒泡腾片。
(4)二氧化氯的化学式为 ,其中氯元素的化合价为 。
(5)我国研制出制取二氧化氯的新方法,其反应的微观过程如下图所示。(其中表示氯原子,表示钠原子,表示氧原子)请在丙方框虚线框内把微粒示意图补充完整 。
参考答案:
1.D
【详解】A、a反应后的质量比反应前的质量小,说明a是反应物;b反应后的质量比反应前的质量小,说明b是反应物;c反应后的质量比反应前的质量多,说明c是生成物;d反应前后质量不变,说明d可能不参加反应,也可能是该反应的催化剂;所以a和b是反应物,d可能是催化剂,此选项正确;
B、根据质量守恒定律反应前后物质的总质量相等,所以待测值=6.4g+3.2g+4.0g+0.5g-2.56g-7.2g-0.5g=3.84g,所以反应后a的质量为3.84g,此选项正确;
C、该反应是,根据质量守恒定律反应前后元素的种类不变,所以c中元素种类一定等于a、b两种物质中元素的种类之和,此选项正确;
D、该反应是,反应物是两种,生成物是一种,符合“多变一”的特点,属于化合反应,此选项错误;
故选D。
2.D
【详解】①该可燃物在足量氧气中燃烧生成二氧化碳和水,根据质量守恒定律,化学反应前后,元素的种类不变,生成物中含C、H、O元素,故该可燃物中一定含有C、H两种元素,则①正确;
②二氧化碳中碳元素的质量为:,水中氢元素的质量为:,3.6g+0.9g=4.5g小于6.9g,根据质量守恒定律,化学反应前后,元素的种类和质量不变,则该可燃物中一定有氧元素,则②错误;
③根据选项②分析可知,可燃物中一定有氧元素,故③错误;
④根据选项②分析可知,可燃物中一定有氧元素,故④正确;
⑤可燃物的分子中C、H的原子个数比为:,则⑤错误;
⑥C、H元素的质量比=3.6g:0.9g=4:1,则⑥正确。
正确的是①④⑥。
故选D。
3.A
【详解】A、根据质量守恒定律,参加反应的物质的总质量等于生成物的总质量,故44+27+R+(-23)=0,R=-48,符合题意;
B、化学反应前后,戊的质量不变,戊可能是催化剂,也可能是不参与反应的杂质,不符合题意;
C、在该反应中,甲、丁为生成物,乙、丙为反应物,戊的质量不变,故反应后容器中一定含甲、丁、戊,可能含乙、丙,不符合题意;
D、该反应中乙、丁的质量比一定为:48:27=16:9,不符合题意。
故选A。
4.B
【详解】A、本选项用的是密闭的容器,反应前后天平平衡,能用于验证质量守恒定律,故选项不符合题意;
B、碳酸钠与稀盐酸反应生成二氧化碳和水和氯化钙,二氧化碳和水都跑到空气中去了,因此不可以验证质量守恒定律,故选项符合题意;
C、铁钉和硫酸铜溶液反应生成铜和硫酸亚铁溶液,反应前后天平平衡,能用于验证质量守恒定律,故选项不符合题意;
D、过氧化氢溶液在二氧化锰催化作用下生成水和氧气,用密闭的容器,反应前后天平平衡,能用于验证质量守恒定律,故选项不符合题意。
故选B。
5.C
【详解】A、过滤液体时发现滤液浑浊,可能的原因是滤纸破损、液面高于滤纸边缘或底部的烧杯不干净,不符合题意;
B、给固体加热时,试管口略向下倾斜,以免冷凝水回流到热的试管底部使其炸裂,不符合题意;
C、 在测定空气里氧气的含量实验中,若弹簧夹没夹紧,红磷燃烧瓶内气压变大,会有大量的气体逸出,导致剩余的气体偏少,会造成所测得的氧气含量偏高,符合题意;
D、在利用红磷燃烧验证质量守恒定律的实验中,只要保证装置密闭并进行了化学反应即可,红磷量的多少不会影响实验结果,不符合题意;
故选C。
6.A
【详解】A、用肥皂水区别硬水和软水,振荡,泡沫多,浮渣少的是软水,泡沫少,浮渣多的是硬水,用肥皂水鉴别井水硬度,产生大量浮渣,说明井水为硬水,选项A正确;
B、镁条在空气中燃烧后固体质量变小,可能是因为产生的白烟逸散到空气中,有新物质生成,属于化学变化,能用质量守恒定律解释,选项B错误;
C、电解水实验,正极产生的气体是氧气,产生气泡少,负极产生的气体是氢气,产生气泡多,氢气由氢元素组成,氧气由氧元素组成,根据质量守恒定律,化学反应前后,元素的种类不变,可证明水是由氢元素和氧元素组成,选项C错误;
D、测定空气中氧气成分实验中,烧杯中的水倒吸进入集气瓶,进入的水的体积约占集气瓶内空气体积的五分之一,进入集气瓶中水的体积等于消耗氧气的体积,说明氧气约占空气体积的五分之一,不是质量分数,选项D错误。
故选A。
7.B
【详解】根据质量守恒定律可知,化学反应前后,原子数目和种类不变。根据图示,该反应中反应前 的个数为4, 的个数为为2,则反应后, 的个数为2, 的个数为1,说明生成物中还需1个 和2个 。
故选B。
8.D
【详解】A、由反应后的微观示意图可知,生成物分子中有由同种原子构成的分子,属于单质,所以反应中有单质生成,故不符合题意;
B、由微观示意图可知,化学变化的实质是分子裂分成原子,原子又重新结合成新分子,所以原子在化学变化中是不可分的,故不符合题意;
C、反应前后都有1个构成相同的化合物的分子,说明该分子在反应后有剩余,所以该分子参与反应的个数为3-1=2个,另一种参与反应的分子的个数为2个,因此,参加反应的两种分子的个数比为2:2,故不符合题意;
D、由反应后的微观示意图可知,有一个分子和反应物分子的构成相同,说明是同种物质,之所以出现在反应后的微观示意图中,是因为该分子在反应中没有完全参与反应,即该分子反应后剩余,不能看做是生成物,所以生成物有两种,故符合题意。
故选D。
9.C
【详解】A、该反应属于化学反应,则该反应符合质量守恒定律,故A正确;
B、该反应为氢气和氧气反应生成水,三者均由分子构成,故B正确;
C、该反应为氢气和氧气反应生成水,符合多变一特点,属于化合反应,故C错误;
D、化学反应中有新物质生成,该反应能获取新物质,故D正确。
故选C。
10.A
【分析】由微观反应示意图可知,该反应是由氨气和氧气在一定条件下反应生成水和一氧化氮,化学方程式为:。
【详解】A.由化学方程式可知,参加反应的甲和乙的分子个数比为5:4,选项A正确;
B.反应前氮元素为-2价,反应后为0价;反应前氧元素为0价,反应后为-2价,反应前后有元素的化合价变化,选项B错误;
C.由化学方程式可知,反应前后分子的种类、数目均发生改变,选项C错误;
D.由物质的构成可知,丙物质的一个分子是由2个氢原子和1个氧原子构成,选项D错误。
故选:A。
11.B
【分析】由表中信息可知,P物质的质量减少为反应物,参加反应的质量是20克;G物质的质量增加为生成物,生成的质量是25克;H物质的质量不变故H物质不参与反应。根据质量守恒定律可知,W是反应物,参加反应的质量是5克。
【详解】A、反应物是两种,生成物是一种,属于化合反应,故错误;
B、反应后物质W的质量为:18g-5g=13g,故正确;
C、P物质的质量减少故为反应物,故错误;
D、物质H的质量在反应前后不变,可能是该反应的催化剂,故错误。
故选B。
12.B
【分析】反应后质量增加的属于生成物,反应后质量减少的属于反应物,反应后质量不变可能属于催化剂。由表中数据分析可知,反应前后甲的质量减少了14g-2g=12g,故是反应物,参加反应的质量为12g;同理可以确定丙的质量不变,可能作该反应的催化剂,也可能没有参加反应;丁是生成物,生成的质量为36g-5g=31g;由质量守恒定律可知,乙是反应物,且参加反应的质量为31g-12g=19g,故x的数值为26-19=7。
【详解】A、x值为7,故选项说法正确;
B、丙可能是该反应的催化剂,故选项说法不正确;
C、丁是生成物,故选项说法正确;
D、参加反应的甲和乙的质量比为12g:19g=12:19,故选项说法正确。
故选B。
13.C
【分析】根据质量守恒定律,反应后丙的质量为:X=4g+10g+3g+4g-(6g+4g+8g)=3g,反应后质量减少的为反应物,质量增加的为生成物,故乙为反应物,甲、丁为生成物,丙质量不变,可能为催化剂,也可能为不参与反应的杂质。
【详解】A、根据分析,反应后丙的质量为:X=4g+10g+3g+4g-(6g+4g+8g)=3g,故A选项叙述正确;
B、乙为反应物,甲、丁为生成物,反应符合一变多的特点,为分解反应,故B选项叙述正确;
C、丙可能为该反应的催化剂,还可能是杂质,故C选项叙述不正确;
D、参加反应的乙、丁质量比为:(10g-4g):(8g-4g)=3:2,故D选项叙述正确;
故选C。
【点睛】化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础。
14.A
【详解】由表中数据分析可知,反应前后N的质量增加了26g-1g=25g,故是生成物,生成的质量为25g;同理可以确定P是反应物,参加反应的质量为32g-12g=20g;Q的质量反应前后不变,可能作该反应的催化剂,也可能没有参加反应;由质量守恒定律,M应是反应物,且参加反应的M的质量为25g-20g=5g,故X的数值为18g-5g=13g。
A、该反应的反应物为M和P,生成物是N,符合“多变一”的形式,属于化合反应,故选项说法错误;
B、参加反应的M的质量为25g-20g=5g,故X的数值为18g-5g=13g,故选项说法正确;
C、反应中N、P的质量比为25g:20g=5:4,故选项说法正确;
D、Q的质量不变,Q可能作该反应的催化剂,也可能没有参加反应,故选项说法正确。
故选:A。
15.D
【分析】由表中的数据可知,X的质量减少是反应物,参加反应的质量为:10g-3.2g=6.8g;W的质量增加是生成物,生成W的质量为3.2g。由于Y的质量不变,6.8g>3.2g,由质量守恒定律可知,Z是生成物,生成Z的质量为:6.8g-3.2g=3.6g。反应后Z的质量为90g+3.6g=93.6g。该反应由一种物质生成了两种物质,属于分解反应。
【详解】由以上分析可知:
A、W是由X分解的产物,可能是单质,故A正确;
B、由于Y的值不变,可能是催化剂,故B正确;
C、该反应是分解反应,故C正确;
D、反应后Z物质的质量93.6g,故D错误。
故选:D。
16.A
【详解】A、高温煅烧碳酸钙生成氧化钙和二氧化碳,固体质量会减少,当反应完固体质量不再改变,故图像正确;
B、因为氧气约占空气体积的五分之一,所以测定空气中氧气的含量时,最终装置内的气体体积剩余五分之四,故图像错误;
C、催化剂只改变化学反应速率,不改变生成物的质量,用两份等质量的氯酸钾固体制取氧气,最终生成氧气质量相等,故图像错误;
D、高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,随着反应进行,二氧化锰质量从零开始逐渐增大到不变,故图像错误。
故选A。
17.B
【详解】根据质量守恒定律可知,化学反应前后元素的种类不变,原子的种类和个数不变,该反应中反应后生成物含有Ca、H、C、O四种元素,且Ca原子个数为1,H原子的个数为2,C原子的个数为2,氧原子的个数为6,;反应前反应物中含C、H、O三种元素,则X中一定含有Ca元素,且Ca原子个数为1,反应前C原子个数为1,H原子个数为2,氧原子个数为3,由此可知X中含有1个Ca原子,1个C原子和3个O原子,则X化学式为CaCO3,故选B。
【点睛】本题主要考查质量守恒定律的应用,难度不大。根据化学反应中元素种类不变,原子的种类和个数不变解题。
18.B
【分析】由表格信息可知反应后a质量增加了10-6.0=4.0g,是生成物;b质量减少了14-7.2=6.8g,是反应物;d质量不变,做催化剂或者是杂质。反应后物质c的质量为6.0+14.0+3.2+1.0-10.0-7.2-1.0=6.0g,所以c是生成物;反应物是b,生成物是a、c,反应符合“一变多”的特点,属于分解反应;
【详解】A、反应后物质c的质量为6.0+14.0+3.2+1.0-10.0-7.2-1.0=6.0g,错误;
B、该反应属于分解反应,正确;
C、反应中a与b的质量比为4.0:6.8=10:17,错误;
D、d质量不变,做催化剂或者是杂质,错误。
故选B。
19.D 20.C
【解析】19.A、大蒜素(C6H10S2O)是由C、H、S、O四种元素组成,蒜氨酸(C6H11NSO3)是由C、H、N、S、O五种元素组成,故A错误;
B、蒜氨酸中硫、氧元素的质量比为:=2:3,故B错误;
C、大蒜素是由C、H、S、O四种元素组成,完全燃烧时生成二氧化碳、水、二氧化硫,故C错误;
D、大蒜素中碳元素的质量分数为:,蒜氨酸中碳元素的质量分数为:,所以大蒜素中碳元素的质量分数更高,故D正确;
故选D;
20.A、物理性质是不通过化学变化就能体现出来的性质,挥发性是大蒜素的物理性质,故A正确;
B、捣蒜过程中没有生成新的物质,发生的是物理变化,故B正确;
C、根据题中信息,大蒜素遇热或碱立即失去抗菌活性,所以大蒜生食抗菌效果更好,故C错误;
D、根据题中信息,大蒜素有较强的抗菌作用,易挥发,遇热或碱立即失去抗菌活性,不受酸的影响,所以捣好的蒜泥可以与醋一起食用,故D正确。
故选C。
21.BC
【详解】将4.6gNa在氧气中充分燃烧,得到7.8g钠的氧化物,所以氧元素质量=7.8g-4.6g=3.2g。
设该氧化物化学式为NaxOy,则23x:16y=4.6g:3.2g,x:y=1:1。
故选BC。
22.(1)+4
(2)PbO2
(3)1︰4
(4) H2O O2、CO2(三个中的任意两个)
(5) A中含有CO2和H2两种分子
【详解】(1)设硅元素化合价是,则:(+1)×2++(-2)×3=0解得=+4;
(2)根据反应的化学方程式,反应物中铅、硫、氧、氢原子个数分别为2、2、10、4,反应后的生成物中铅、硫、氧、氢原子个数分别为1、2、8、4,根据反应前后原子种类、数目不变,则横线上物质的1个分子中含有1个铅原子、2个氧原子,则物质的化学式为PbO2;
(3)已知同温同压下,相同体积的气体含有相同数目的分子,即体积比等于分子个数比,“空气”中O2与N2的体积比约为1:4,故“空气”中O2与N2的分子个数比约为1:4;
(4)根据“铜锈”[主要成分为Cu2(OH)2CO3]和质量守恒定律,Cu能和空气中的CO2、H2O和O2发生反应;
(5)一定条件下,CO2和H2反应生成CH4和H2O,反应的方程式为:;
从微观角度分析,A图中的物质属于混合物的原因是:A中含有CO2和H2两种分子;
根据化学方程式及质量守恒定律,一个二氧化碳分子和四个氢分子反应生成一个甲烷分子和两个水分子,故反应后剩余一个二氧化碳分子和两个氢分子,图示如下:
23.(1) 还未达到氯酸钾分解的温度 氯酸钾已经反应完
(2)4.8
(3)解:设原固体混合物中氯酸钾的质量为。
二氧化锰的质量为
答:固体混合物中的质量为2.75g。
【详解】(1)t1时间前固体质量不变是因为还未达到氯酸钾分解的温度,t4后固体质量不变是因为氯酸钾已经反应完,故填:还未达到氯酸钾分解的温度;氯酸钾已经反应完;
(2)根据质量守恒定律,化学反应前后质量不变,因此氧气质量为,故填:4.8;
(3)见答案。
24.(1)碳/C
(2)-3
(3)以水为原料制取氢气,原料来源广/燃烧的热值高/燃烧产物是水,无污染
(4)NaCl
【详解】(1)石墨烯是由碳元素组成的纯净物,属于单质,故填:碳或C;
(2)GaCl3中Cl元素的化合价是-1价,根据化合物中元素的化合价之和为0可知,Ga元素的化合价为+3价,故GaN中N元素的化合价为-3价;
(3)氢气作为燃料与广泛采用的化石燃料相比的优点:以水为原料制取氢气,原料来源广;燃烧的热值高;燃烧产物是水,无污染;
(4)在中,根据质量守恒定律中化学反应前后原子的种类和数目不变,反应前有4个Cl、2个Na、4个O,反应后有2个Cl、4个O,所以2X中含有2个Cl、2个Na,1个X中含有1个Cl、1个Na,故X的化学式为NaCl。
25.(1) 不能 水和酒精没有发生化学变化(答案合理即可)
(2)a
(3) 化合
(4)一部分镁燃烧产生的白烟逸散到空气中
(5)密闭
(6)相同条件下 O2比 N2活泼
(7)橡皮塞冲出
【详解】(1)质量守恒定律是指化学反应前后物质总质量不变,而水和酒精混合没有发生化学变化,故填:不能;水和酒精没有发生化学变化(答案合理即可);
(2)铜和氧气反应生成氧化铜,则左侧质量偏大,因此玻璃棒a端下沉;
(3)镁和氧气点燃生成氧化镁,化学方程式为:;该反应属于一变多,是化合反应;
(4)由于镁燃烧时,一部分镁燃烧产生的白烟逸散到空气中,而白烟即生成的氧化镁,因此造成反应后固体质量m2(5)根据以上实验可知,验证质量守恒定律时,对于有气体参加的反应,应在密闭的容器内进行;
(6)空气中 N2的含量远大于 O2的含量,而镁条在空气中燃烧生成的 MgO 却远多于 Mg3N2,原因是相同条件下 O2比 N2活泼,更容易与镁反应;
(7)图 3 实验中气球的作用除了使装置密闭之外,由于反应放热会使气体膨胀,因此气球还可以防止橡皮塞冲出
26. 根据质量守恒定律,反应前后元素种类不变,反应物没有氮元素 澄清石灰水 澄清石灰水变浑浊 右 反应生成气体逸出,带走了一部分质量 密闭 ClO2 +4
【详解】(1)根据质量守恒定律,化学反应前后元素的质量和种类均不变,维C泡腾片中不含有氮元素,则生成物中不含氮元素,故产生的气体不可能是N2,因为根据质量守恒定律,反应前后元素种类不变,反应物没有氮元素。
(2)二氧化碳能使澄清石灰水变浑浊,则将气体通入澄清石灰水中,观察到澄清石灰水变浑浊现象,证明该气体是CO2。
(3)维C泡腾片利用柠檬酸和碳酸氢钠反应做泡腾崩解剂、置入水中,即刻发生泡腾反应,生成大量的气体,气体逸散进空气中,左边烧杯中质量减少,则反应结束后发现天平的指针偏右,原因是反应生成气体逸出,带走了一部分质量,由此他得出凡是有气体参与或生成的化学反应,在验证质量守恒时,反应装置应该在密闭容器内进行。
(4)1个二氧化氯分子含有2个氧原子,1个氯原子,则二氧化氯的化学式为ClO2,氧元素的化合价为-2价,设氯元素的化合价为x,化合物中各元素的正负化合价代数和为0,,,则氯元素的化合价为+4。
(5)由反应的微观示意图可知,反应前含有4个氯原子,4个氧原子,2个钠原子,反应后有3个氯原子,4个氧原子,1个钠原子,还有1个氯原子,1个钠原子,则丙方框内的微粒示意图为。
一、单选题
1.(2022秋·广东湛江·九年级统考期末)将一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下。下列说法不正确的是
A.a和b是反应物,d可能是催化剂
B.反应后a的质量为3.84g
C.c中元素种类一定等于a、b两种物质中元素的种类之和
D.该反应属于分解反应
2.(2022秋·广东揭阳·九年级统考期末)现取6.9g某可燃物在足量氧气中完全燃烧,生成了13.2gCO2和8.1gH2O,对该物质的组成有下列推断:
①一定含有C、H元素
②一定不含有O元素
③可能含有O元素
④一定含有O元素
⑤可燃物的分子中C、H的原子个数比为2:5
⑥可燃物中C、H元素的质量比为4:1
其中正确的是
A.①②⑤ B.①③⑥ C.①④⑤ D.①④⑥
3.(2022秋·广东汕头·九年级统考期末)在一个密闭容器中,有甲、乙、丙、丁、戊五种物质,在一定条件下发生反应,测得反应前后各物质的质量变化量如图所示(图中正数表示物质质量的增加量,负数表示物质质量的减少量,0 表示物质质量不变),下列说法正确的是
A.R=-48 B.戊一定是该反应的催化剂
C.反应后容器中一定含有 5 种物质 D.该反应中乙、丁的质量比一定为 8:9
4.(2022秋·广东河源·九年级统考期末)下列实验不能用于验证质量守恒定律的是
A. B.
C. D.
5.(2022秋·广东揭阳·九年级统考期末)以下对实验的相关分析,错误的是
A.过滤液体时发现滤液浑浊,可能的原因是滤纸破损
B.给固体加热时,试管口略向下倾斜,以免冷凝水回流到热的试管底部使其炸裂
C.在测定空气里氧气的含量实验中,若弹簧夹没夹紧会造成所测得的氧气含量偏低
D.在利用红磷燃烧验证质量守恒定律的实验中,若红磷量不足不会影响实验结果
6.(2022秋·广东清远·九年级统考期末)下列有关实验现象或变化、结论关系正确的是
选项 实验 现象或变化 结论
A 用肥皂水鉴别井水硬度 产生大量浮渣 井水为硬水
B 称量镁条在空气中燃烧前后质量 质量减少 不遵循质量守恒定律
C 电解水 正极产生气泡少,负极产生气泡多 水是由氢气和氧气组成
D 测定空气中氧气成分 水流入集气瓶1/5 氧气质量分数约1/5
A.A B.B C.C D.D
7.(2022秋·广东东莞·九年级统考期末)下图是某化学反应的微观粒子图。反应后的方框内应再填入1个粒子
A. B. C. D.
8.(2022秋·广东韶关·九年级统考期末)下图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子。下列说法错误的是
A.此反应有单质生成
B.原子在化学变化中是不可分的
C.参加反应的两种分子的个数比为2∶2
D.图中生成物有三种
9.(2022秋·广东梅州·九年级统考期末)“宏观-微观-符号”三重表征是化学学科的基本特征。下图是某化学反应的微观示意图,下列说法错误的是
A.从定量研究看:该反应符合质量守恒定律
B.从微观构成看:该反应中涉及的物质均由分子构成
C.从反应类型看:该反应属于置换反应
D.从反应价值看:该反应能获取新物质
10.(2022秋·广东韶关·九年级统考期末)甲和乙在一定条件下反应生成丙和丁,微观示意图如下、有关说法正确的是
A.参加反应的甲和乙的分子个数比为5:4 B.反应前后各元素的化合价均不变
C.反应前后分子的种类不变 D.丙物质由2个氢原子和1个氧原子构成
11.(2022秋·广东韶关·九年级统考期末)在一个密闭容器中放入W、G、H、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表:
物质 W G H P
反应前质量/g 18 1 2 32
反应后质量/g 待测 26 2 12
对该反应的认识正确的是
A.该反应是分解反应 B.W待测值是13
C.P是生成物 D.物质H是该反应的催化剂
12.(2022秋·广东惠州·九年级统考期末)甲、乙、丙、丁在反应前后的质量如图所示,下列说法错误的是
A.x 的值为 7 B.丙一定是该反应的催化剂
C.丁一定为生成物 D.参加反应的甲和乙的质量比为 12:19
13.(2022秋·广东东莞·九年级统考期末)在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化如图。下列说法中不正确的是
A.X的数值为3 B.该反应为分解反应
C.丙一定是该反应的催化剂 D.参加反应的乙和丁质量比为3:2
14.(2022秋·广东深圳·九年级统考期末)在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应认识不正确的是
物质 M N Q P
反应前质量(g) 18 1 2 32
反应后质量(g) x 26 2 12
A.该变化的基本反应类型是分解反应
B.反应后物质x的值为13
C.反应中N、P的质量比为5:4
D.物质Q可能是该反应的催化剂
15.(2022秋·广东河源·九年级统考期末)在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如下表所示,下列说法不正确的是
物质 X Y Z W
反应前质量/g 10 3 90 0
反应后质量/g 3.2 3 待测 3.2
A.W可能是单质
B.Y可能是催化剂
C.该反应是分解反应
D.反应后Z物质的质量为86.4g
16.(2022秋·广东河源·九年级统考期末)下列图像能正确反映对应变化关系的是
A.①高温煅烧一定质量的碳酸钙 B.②测定空气中氧气的含量
C.③用两份等质量的氯酸钾固体制取氧气 D.④加热一定质量的高锰酸钾
17.(2022秋·广东东莞·九年级统考期末)看到千奇百怪的钟乳石,大家无不感叹大自然的鬼斧神工,其实里面蕴含了丰富的化学知识。其反应原理为X+CO2+H2O=Ca(HCO3)2(方程式已配平)则X的化学式是
A.CaO B.CaCO3 C.Ca(OH)2 D.CaO2
18.(2022秋·广东韶关·九年级统考期末)将一定质量的a,b,c,d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得各物质的质量如表:下列有关说法正确的是
物质 a b c d
反应前的质量/g 6.0 14.0 3.2 1.0
反应后的质量/g 10.0 7.2 x 1.0
A.x=3.2 B.该反应属于分解反应
C.反应中a与b的质量比为3:7 D.d一定是催化剂
二、选择题组
(2022秋·广东揭阳·九年级统考期末)在每小题给出的四个选项中,有一项或两项符合题目要求。
新鲜大蒜头中含蒜氨酸(C6H11NSO3),蒜氨酸受撞击后,会转化为大蒜素。大蒜素(C6H10S2O)有较强的抗菌作用,易挥发,遇热或碱立即失去抗菌活性,但不受酸的影响。根据以上材料,完成下面小题。
19.下列有关大蒜素和蒜氨酸的说法,正确的是
A.大蒜素和蒜氨酸组成元素相同
B.蒜氨酸中硫、氧元素的质量比为2:1
C.大蒜素完全燃烧时只生成二氧化碳和水
D.与蒜氨酸相比,大蒜素中碳元素的质量分数更高
20.下列有关大蒜性质与变化的说法,不正确的是
A.挥发性是大蒜素的物理性质 B.捣蒜过程中仅发生物理变化
C.大蒜煮熟食用比生食抗菌效果更好 D.捣好的蒜泥可以与醋一起食用
三、多选题
21.(2022秋·广东湛江·九年级统考期末)元素钠(Na)有多种化合价,将4.6gNa在氧气中充分燃烧,得到7.8g钠的氧化物,该氧化物的化学式是
A.Na2O B.NaO C.Na2O2 D.NaO2
四、填空题
22.(2022秋·广东广州·九年级统考期末)化学与生活、生产、科技发展息息相关。
(1)硅酸钠(Na2SiO3)可用作黏合剂和防火材料,其中Si元素的化合价为 。
(2)汽车是重要的交通工具,为了降低污染可以使用电动车,请完成铅酸电池充电反应的方程式:2PbSO4 + 2H2OPb + 2H2SO4 + 。
(3)2020年12月3日,我国“嫦娥五号”成功发射,显示我国科技实力的飞速发展。我国空间站“天宫”内的“空气”与地球上的空气组成基本一致,已知同温同压下,相同体积的气体含有相同数目的分子,“空气”中O2与N2的分子个数比约为 。
(4)Cu能与空气中的 、 (写出其中两种物质的化学式)发生化合反应生成“铜锈”[主要成分为Cu2(OH)2CO3]。
(5)一定条件下,CO2和H2反应生成CH4和H2O,见下图。
①该反应的化学方程式是 。
②从微观角度分析,A图中的物质属于混合物的原因是 。
③请在B图中将该反应的微观粒子补充完整 。
23.(2022秋·广东湛江·九年级统考期末)实验室制取氧气时,某同学取氯酸钾和二氧化锰的固体混合物共 15.0g 进行加热,固体的质量与加热时间的关系如图所示。
(1)解释固体质量不变的原因:t1时间前 ;t4后 ;
(2)t4时,制得氧气的质量是 g。
(3)t5时,固体混合物中 MnO2的质量为多少?
24.(2022秋·广东广州·九年级统考期末)洋溢着绿色与科技元素的2022北京冬奥会以中国式的传奇与浪漫惊艳了世界。
(1)衣:运动服中高科技材料石墨烯的使用,解决了超低温户外环境下运动员的取暖难题。石墨烯是由 元素组成的单质。
(2)住:奥运村实现了5G网络的全覆盖。制造5G芯片的氮化镓(GaN)材料可由氯化镓(GaCl3)制取,氮化镓中氮元素的化合价为 。
(3)行:冬奥会会务用车均使用氢能源汽车,基本实现了碳的零排放。相比于化石燃料,氢气作为燃料的优点是 (只写一点)。
(4)防:日常消杀也是必需的防疫措施。二氧化氯(ClO2)是一种常用消毒剂,其制取的一种原理是:Cl2+2NaClO2═2ClO2+2X,则X的化学式为 。
五、实验题
25.(2022秋·广东湛江·九年级统考期末)为验证质量守恒定律,某兴趣小组做了以下实验进行探究。
实验一:将 10g 水加入 10g 酒精中,一段时间后,称量混合液,质量仍为 20g。
(1)该实验 (填“能”或“不能”)验证质量守恒定律,原因是 。
实验二:如图 1,用细铜丝吊着一根长玻璃棒,两端分别绕上粗铜丝,并使玻璃棒保持水平,然后用酒精灯给 a 端铜丝加热 1~2 分钟。
(2)冷却后,观察到铜丝变黑、玻璃棒 (填“a”或“b”)端下沉。
实验三:称取镁条和石棉网的质量为 m1(如图 2 所示),然后在空气中点燃镁条;反应结束后将所得物质与石棉网一起再次称量,质量为 m2。
(3)写出镁条燃烧的化学方程式 ,该反应属于 反应(填基本反应类型)。
(4)根据质量守恒定律可知:生成氧化镁的质量大于参加反应的镁条的质量;而实验事实是 m2
(5)根据以上实验可知,验证质量守恒定律时,对于有气体参加的反应,应在 容器中进行实验。
【拓展实验】兴趣小组按如图 3 装置改进实验,验证了质量守恒定律,却发现产物白色固体中还有少量黄色固体。查阅资料得知:镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体。
【反思与交流】
(6)空气中 N2的含量远大于 O2的含量,而镁条在空气中燃烧生成的 MgO 却远多于 Mg3N2,原因是 。
(7)图 3 实验中气球的作用除了使装置密闭之外,还可以防止 。
六、科学探究题
26.(2022秋·广东广州·九年级统考期末)2021年12月9日下午,小明观看完“天宫第一课”后,对王亚平老师的泡腾片实验非常感兴趣,想起自己在补充维生素C时也用过泡腾片,于是把一颗维生素C泡腾片药片丢入水中,发现药片表面产生大量的气泡。出于好奇他开展了如下探究:
【查阅资料】维C泡腾片是一种较新的药物剂型,主要成分有:维C(C6H8O6)、碳酸氢钠(NaHCO3)、柠檬酸(C6H8O7)。维C泡腾片利用柠檬酸和碳酸氢钠反应做泡腾崩解剂、置入水中,即刻发生泡腾反应,生成大量的气体,状如沸腾,故名泡腾片。
【提出猜想】假设产生的气体可能是CO2、N2、O2
(1)小明认真思考后认为产生的气体不可能是N2,因为 。
【进行实验】
(2)小明将气体通入 中,观察到 现象,证明该气体是CO2。
【反思评价】
(3)为了验证该反应是否遵循质量守恒定律,小明设计了如图所示的实验,实验前托盘天平的指针指向中间,反应结束后发现天平的指针偏 ,其原因是 。由此他得出凡是有气体参与或生成的化学反应,在验证质量守恒时,反应装置应该在 容器内进行。
小明继续查阅资料,得知:泡腾片在消毒剂上也有广泛的应用,其中二氧化氯泡腾片是其中一种消毒泡腾片。
(4)二氧化氯的化学式为 ,其中氯元素的化合价为 。
(5)我国研制出制取二氧化氯的新方法,其反应的微观过程如下图所示。(其中表示氯原子,表示钠原子,表示氧原子)请在丙方框虚线框内把微粒示意图补充完整 。
参考答案:
1.D
【详解】A、a反应后的质量比反应前的质量小,说明a是反应物;b反应后的质量比反应前的质量小,说明b是反应物;c反应后的质量比反应前的质量多,说明c是生成物;d反应前后质量不变,说明d可能不参加反应,也可能是该反应的催化剂;所以a和b是反应物,d可能是催化剂,此选项正确;
B、根据质量守恒定律反应前后物质的总质量相等,所以待测值=6.4g+3.2g+4.0g+0.5g-2.56g-7.2g-0.5g=3.84g,所以反应后a的质量为3.84g,此选项正确;
C、该反应是,根据质量守恒定律反应前后元素的种类不变,所以c中元素种类一定等于a、b两种物质中元素的种类之和,此选项正确;
D、该反应是,反应物是两种,生成物是一种,符合“多变一”的特点,属于化合反应,此选项错误;
故选D。
2.D
【详解】①该可燃物在足量氧气中燃烧生成二氧化碳和水,根据质量守恒定律,化学反应前后,元素的种类不变,生成物中含C、H、O元素,故该可燃物中一定含有C、H两种元素,则①正确;
②二氧化碳中碳元素的质量为:,水中氢元素的质量为:,3.6g+0.9g=4.5g小于6.9g,根据质量守恒定律,化学反应前后,元素的种类和质量不变,则该可燃物中一定有氧元素,则②错误;
③根据选项②分析可知,可燃物中一定有氧元素,故③错误;
④根据选项②分析可知,可燃物中一定有氧元素,故④正确;
⑤可燃物的分子中C、H的原子个数比为:,则⑤错误;
⑥C、H元素的质量比=3.6g:0.9g=4:1,则⑥正确。
正确的是①④⑥。
故选D。
3.A
【详解】A、根据质量守恒定律,参加反应的物质的总质量等于生成物的总质量,故44+27+R+(-23)=0,R=-48,符合题意;
B、化学反应前后,戊的质量不变,戊可能是催化剂,也可能是不参与反应的杂质,不符合题意;
C、在该反应中,甲、丁为生成物,乙、丙为反应物,戊的质量不变,故反应后容器中一定含甲、丁、戊,可能含乙、丙,不符合题意;
D、该反应中乙、丁的质量比一定为:48:27=16:9,不符合题意。
故选A。
4.B
【详解】A、本选项用的是密闭的容器,反应前后天平平衡,能用于验证质量守恒定律,故选项不符合题意;
B、碳酸钠与稀盐酸反应生成二氧化碳和水和氯化钙,二氧化碳和水都跑到空气中去了,因此不可以验证质量守恒定律,故选项符合题意;
C、铁钉和硫酸铜溶液反应生成铜和硫酸亚铁溶液,反应前后天平平衡,能用于验证质量守恒定律,故选项不符合题意;
D、过氧化氢溶液在二氧化锰催化作用下生成水和氧气,用密闭的容器,反应前后天平平衡,能用于验证质量守恒定律,故选项不符合题意。
故选B。
5.C
【详解】A、过滤液体时发现滤液浑浊,可能的原因是滤纸破损、液面高于滤纸边缘或底部的烧杯不干净,不符合题意;
B、给固体加热时,试管口略向下倾斜,以免冷凝水回流到热的试管底部使其炸裂,不符合题意;
C、 在测定空气里氧气的含量实验中,若弹簧夹没夹紧,红磷燃烧瓶内气压变大,会有大量的气体逸出,导致剩余的气体偏少,会造成所测得的氧气含量偏高,符合题意;
D、在利用红磷燃烧验证质量守恒定律的实验中,只要保证装置密闭并进行了化学反应即可,红磷量的多少不会影响实验结果,不符合题意;
故选C。
6.A
【详解】A、用肥皂水区别硬水和软水,振荡,泡沫多,浮渣少的是软水,泡沫少,浮渣多的是硬水,用肥皂水鉴别井水硬度,产生大量浮渣,说明井水为硬水,选项A正确;
B、镁条在空气中燃烧后固体质量变小,可能是因为产生的白烟逸散到空气中,有新物质生成,属于化学变化,能用质量守恒定律解释,选项B错误;
C、电解水实验,正极产生的气体是氧气,产生气泡少,负极产生的气体是氢气,产生气泡多,氢气由氢元素组成,氧气由氧元素组成,根据质量守恒定律,化学反应前后,元素的种类不变,可证明水是由氢元素和氧元素组成,选项C错误;
D、测定空气中氧气成分实验中,烧杯中的水倒吸进入集气瓶,进入的水的体积约占集气瓶内空气体积的五分之一,进入集气瓶中水的体积等于消耗氧气的体积,说明氧气约占空气体积的五分之一,不是质量分数,选项D错误。
故选A。
7.B
【详解】根据质量守恒定律可知,化学反应前后,原子数目和种类不变。根据图示,该反应中反应前 的个数为4, 的个数为为2,则反应后, 的个数为2, 的个数为1,说明生成物中还需1个 和2个 。
故选B。
8.D
【详解】A、由反应后的微观示意图可知,生成物分子中有由同种原子构成的分子,属于单质,所以反应中有单质生成,故不符合题意;
B、由微观示意图可知,化学变化的实质是分子裂分成原子,原子又重新结合成新分子,所以原子在化学变化中是不可分的,故不符合题意;
C、反应前后都有1个构成相同的化合物的分子,说明该分子在反应后有剩余,所以该分子参与反应的个数为3-1=2个,另一种参与反应的分子的个数为2个,因此,参加反应的两种分子的个数比为2:2,故不符合题意;
D、由反应后的微观示意图可知,有一个分子和反应物分子的构成相同,说明是同种物质,之所以出现在反应后的微观示意图中,是因为该分子在反应中没有完全参与反应,即该分子反应后剩余,不能看做是生成物,所以生成物有两种,故符合题意。
故选D。
9.C
【详解】A、该反应属于化学反应,则该反应符合质量守恒定律,故A正确;
B、该反应为氢气和氧气反应生成水,三者均由分子构成,故B正确;
C、该反应为氢气和氧气反应生成水,符合多变一特点,属于化合反应,故C错误;
D、化学反应中有新物质生成,该反应能获取新物质,故D正确。
故选C。
10.A
【分析】由微观反应示意图可知,该反应是由氨气和氧气在一定条件下反应生成水和一氧化氮,化学方程式为:。
【详解】A.由化学方程式可知,参加反应的甲和乙的分子个数比为5:4,选项A正确;
B.反应前氮元素为-2价,反应后为0价;反应前氧元素为0价,反应后为-2价,反应前后有元素的化合价变化,选项B错误;
C.由化学方程式可知,反应前后分子的种类、数目均发生改变,选项C错误;
D.由物质的构成可知,丙物质的一个分子是由2个氢原子和1个氧原子构成,选项D错误。
故选:A。
11.B
【分析】由表中信息可知,P物质的质量减少为反应物,参加反应的质量是20克;G物质的质量增加为生成物,生成的质量是25克;H物质的质量不变故H物质不参与反应。根据质量守恒定律可知,W是反应物,参加反应的质量是5克。
【详解】A、反应物是两种,生成物是一种,属于化合反应,故错误;
B、反应后物质W的质量为:18g-5g=13g,故正确;
C、P物质的质量减少故为反应物,故错误;
D、物质H的质量在反应前后不变,可能是该反应的催化剂,故错误。
故选B。
12.B
【分析】反应后质量增加的属于生成物,反应后质量减少的属于反应物,反应后质量不变可能属于催化剂。由表中数据分析可知,反应前后甲的质量减少了14g-2g=12g,故是反应物,参加反应的质量为12g;同理可以确定丙的质量不变,可能作该反应的催化剂,也可能没有参加反应;丁是生成物,生成的质量为36g-5g=31g;由质量守恒定律可知,乙是反应物,且参加反应的质量为31g-12g=19g,故x的数值为26-19=7。
【详解】A、x值为7,故选项说法正确;
B、丙可能是该反应的催化剂,故选项说法不正确;
C、丁是生成物,故选项说法正确;
D、参加反应的甲和乙的质量比为12g:19g=12:19,故选项说法正确。
故选B。
13.C
【分析】根据质量守恒定律,反应后丙的质量为:X=4g+10g+3g+4g-(6g+4g+8g)=3g,反应后质量减少的为反应物,质量增加的为生成物,故乙为反应物,甲、丁为生成物,丙质量不变,可能为催化剂,也可能为不参与反应的杂质。
【详解】A、根据分析,反应后丙的质量为:X=4g+10g+3g+4g-(6g+4g+8g)=3g,故A选项叙述正确;
B、乙为反应物,甲、丁为生成物,反应符合一变多的特点,为分解反应,故B选项叙述正确;
C、丙可能为该反应的催化剂,还可能是杂质,故C选项叙述不正确;
D、参加反应的乙、丁质量比为:(10g-4g):(8g-4g)=3:2,故D选项叙述正确;
故选C。
【点睛】化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础。
14.A
【详解】由表中数据分析可知,反应前后N的质量增加了26g-1g=25g,故是生成物,生成的质量为25g;同理可以确定P是反应物,参加反应的质量为32g-12g=20g;Q的质量反应前后不变,可能作该反应的催化剂,也可能没有参加反应;由质量守恒定律,M应是反应物,且参加反应的M的质量为25g-20g=5g,故X的数值为18g-5g=13g。
A、该反应的反应物为M和P,生成物是N,符合“多变一”的形式,属于化合反应,故选项说法错误;
B、参加反应的M的质量为25g-20g=5g,故X的数值为18g-5g=13g,故选项说法正确;
C、反应中N、P的质量比为25g:20g=5:4,故选项说法正确;
D、Q的质量不变,Q可能作该反应的催化剂,也可能没有参加反应,故选项说法正确。
故选:A。
15.D
【分析】由表中的数据可知,X的质量减少是反应物,参加反应的质量为:10g-3.2g=6.8g;W的质量增加是生成物,生成W的质量为3.2g。由于Y的质量不变,6.8g>3.2g,由质量守恒定律可知,Z是生成物,生成Z的质量为:6.8g-3.2g=3.6g。反应后Z的质量为90g+3.6g=93.6g。该反应由一种物质生成了两种物质,属于分解反应。
【详解】由以上分析可知:
A、W是由X分解的产物,可能是单质,故A正确;
B、由于Y的值不变,可能是催化剂,故B正确;
C、该反应是分解反应,故C正确;
D、反应后Z物质的质量93.6g,故D错误。
故选:D。
16.A
【详解】A、高温煅烧碳酸钙生成氧化钙和二氧化碳,固体质量会减少,当反应完固体质量不再改变,故图像正确;
B、因为氧气约占空气体积的五分之一,所以测定空气中氧气的含量时,最终装置内的气体体积剩余五分之四,故图像错误;
C、催化剂只改变化学反应速率,不改变生成物的质量,用两份等质量的氯酸钾固体制取氧气,最终生成氧气质量相等,故图像错误;
D、高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,随着反应进行,二氧化锰质量从零开始逐渐增大到不变,故图像错误。
故选A。
17.B
【详解】根据质量守恒定律可知,化学反应前后元素的种类不变,原子的种类和个数不变,该反应中反应后生成物含有Ca、H、C、O四种元素,且Ca原子个数为1,H原子的个数为2,C原子的个数为2,氧原子的个数为6,;反应前反应物中含C、H、O三种元素,则X中一定含有Ca元素,且Ca原子个数为1,反应前C原子个数为1,H原子个数为2,氧原子个数为3,由此可知X中含有1个Ca原子,1个C原子和3个O原子,则X化学式为CaCO3,故选B。
【点睛】本题主要考查质量守恒定律的应用,难度不大。根据化学反应中元素种类不变,原子的种类和个数不变解题。
18.B
【分析】由表格信息可知反应后a质量增加了10-6.0=4.0g,是生成物;b质量减少了14-7.2=6.8g,是反应物;d质量不变,做催化剂或者是杂质。反应后物质c的质量为6.0+14.0+3.2+1.0-10.0-7.2-1.0=6.0g,所以c是生成物;反应物是b,生成物是a、c,反应符合“一变多”的特点,属于分解反应;
【详解】A、反应后物质c的质量为6.0+14.0+3.2+1.0-10.0-7.2-1.0=6.0g,错误;
B、该反应属于分解反应,正确;
C、反应中a与b的质量比为4.0:6.8=10:17,错误;
D、d质量不变,做催化剂或者是杂质,错误。
故选B。
19.D 20.C
【解析】19.A、大蒜素(C6H10S2O)是由C、H、S、O四种元素组成,蒜氨酸(C6H11NSO3)是由C、H、N、S、O五种元素组成,故A错误;
B、蒜氨酸中硫、氧元素的质量比为:=2:3,故B错误;
C、大蒜素是由C、H、S、O四种元素组成,完全燃烧时生成二氧化碳、水、二氧化硫,故C错误;
D、大蒜素中碳元素的质量分数为:,蒜氨酸中碳元素的质量分数为:,所以大蒜素中碳元素的质量分数更高,故D正确;
故选D;
20.A、物理性质是不通过化学变化就能体现出来的性质,挥发性是大蒜素的物理性质,故A正确;
B、捣蒜过程中没有生成新的物质,发生的是物理变化,故B正确;
C、根据题中信息,大蒜素遇热或碱立即失去抗菌活性,所以大蒜生食抗菌效果更好,故C错误;
D、根据题中信息,大蒜素有较强的抗菌作用,易挥发,遇热或碱立即失去抗菌活性,不受酸的影响,所以捣好的蒜泥可以与醋一起食用,故D正确。
故选C。
21.BC
【详解】将4.6gNa在氧气中充分燃烧,得到7.8g钠的氧化物,所以氧元素质量=7.8g-4.6g=3.2g。
设该氧化物化学式为NaxOy,则23x:16y=4.6g:3.2g,x:y=1:1。
故选BC。
22.(1)+4
(2)PbO2
(3)1︰4
(4) H2O O2、CO2(三个中的任意两个)
(5) A中含有CO2和H2两种分子
【详解】(1)设硅元素化合价是,则:(+1)×2++(-2)×3=0解得=+4;
(2)根据反应的化学方程式,反应物中铅、硫、氧、氢原子个数分别为2、2、10、4,反应后的生成物中铅、硫、氧、氢原子个数分别为1、2、8、4,根据反应前后原子种类、数目不变,则横线上物质的1个分子中含有1个铅原子、2个氧原子,则物质的化学式为PbO2;
(3)已知同温同压下,相同体积的气体含有相同数目的分子,即体积比等于分子个数比,“空气”中O2与N2的体积比约为1:4,故“空气”中O2与N2的分子个数比约为1:4;
(4)根据“铜锈”[主要成分为Cu2(OH)2CO3]和质量守恒定律,Cu能和空气中的CO2、H2O和O2发生反应;
(5)一定条件下,CO2和H2反应生成CH4和H2O,反应的方程式为:;
从微观角度分析,A图中的物质属于混合物的原因是:A中含有CO2和H2两种分子;
根据化学方程式及质量守恒定律,一个二氧化碳分子和四个氢分子反应生成一个甲烷分子和两个水分子,故反应后剩余一个二氧化碳分子和两个氢分子,图示如下:
23.(1) 还未达到氯酸钾分解的温度 氯酸钾已经反应完
(2)4.8
(3)解:设原固体混合物中氯酸钾的质量为。
二氧化锰的质量为
答:固体混合物中的质量为2.75g。
【详解】(1)t1时间前固体质量不变是因为还未达到氯酸钾分解的温度,t4后固体质量不变是因为氯酸钾已经反应完,故填:还未达到氯酸钾分解的温度;氯酸钾已经反应完;
(2)根据质量守恒定律,化学反应前后质量不变,因此氧气质量为,故填:4.8;
(3)见答案。
24.(1)碳/C
(2)-3
(3)以水为原料制取氢气,原料来源广/燃烧的热值高/燃烧产物是水,无污染
(4)NaCl
【详解】(1)石墨烯是由碳元素组成的纯净物,属于单质,故填:碳或C;
(2)GaCl3中Cl元素的化合价是-1价,根据化合物中元素的化合价之和为0可知,Ga元素的化合价为+3价,故GaN中N元素的化合价为-3价;
(3)氢气作为燃料与广泛采用的化石燃料相比的优点:以水为原料制取氢气,原料来源广;燃烧的热值高;燃烧产物是水,无污染;
(4)在中,根据质量守恒定律中化学反应前后原子的种类和数目不变,反应前有4个Cl、2个Na、4个O,反应后有2个Cl、4个O,所以2X中含有2个Cl、2个Na,1个X中含有1个Cl、1个Na,故X的化学式为NaCl。
25.(1) 不能 水和酒精没有发生化学变化(答案合理即可)
(2)a
(3) 化合
(4)一部分镁燃烧产生的白烟逸散到空气中
(5)密闭
(6)相同条件下 O2比 N2活泼
(7)橡皮塞冲出
【详解】(1)质量守恒定律是指化学反应前后物质总质量不变,而水和酒精混合没有发生化学变化,故填:不能;水和酒精没有发生化学变化(答案合理即可);
(2)铜和氧气反应生成氧化铜,则左侧质量偏大,因此玻璃棒a端下沉;
(3)镁和氧气点燃生成氧化镁,化学方程式为:;该反应属于一变多,是化合反应;
(4)由于镁燃烧时,一部分镁燃烧产生的白烟逸散到空气中,而白烟即生成的氧化镁,因此造成反应后固体质量m2
(6)空气中 N2的含量远大于 O2的含量,而镁条在空气中燃烧生成的 MgO 却远多于 Mg3N2,原因是相同条件下 O2比 N2活泼,更容易与镁反应;
(7)图 3 实验中气球的作用除了使装置密闭之外,由于反应放热会使气体膨胀,因此气球还可以防止橡皮塞冲出
26. 根据质量守恒定律,反应前后元素种类不变,反应物没有氮元素 澄清石灰水 澄清石灰水变浑浊 右 反应生成气体逸出,带走了一部分质量 密闭 ClO2 +4
【详解】(1)根据质量守恒定律,化学反应前后元素的质量和种类均不变,维C泡腾片中不含有氮元素,则生成物中不含氮元素,故产生的气体不可能是N2,因为根据质量守恒定律,反应前后元素种类不变,反应物没有氮元素。
(2)二氧化碳能使澄清石灰水变浑浊,则将气体通入澄清石灰水中,观察到澄清石灰水变浑浊现象,证明该气体是CO2。
(3)维C泡腾片利用柠檬酸和碳酸氢钠反应做泡腾崩解剂、置入水中,即刻发生泡腾反应,生成大量的气体,气体逸散进空气中,左边烧杯中质量减少,则反应结束后发现天平的指针偏右,原因是反应生成气体逸出,带走了一部分质量,由此他得出凡是有气体参与或生成的化学反应,在验证质量守恒时,反应装置应该在密闭容器内进行。
(4)1个二氧化氯分子含有2个氧原子,1个氯原子,则二氧化氯的化学式为ClO2,氧元素的化合价为-2价,设氯元素的化合价为x,化合物中各元素的正负化合价代数和为0,,,则氯元素的化合价为+4。
(5)由反应的微观示意图可知,反应前含有4个氯原子,4个氧原子,2个钠原子,反应后有3个氯原子,4个氧原子,1个钠原子,还有1个氯原子,1个钠原子,则丙方框内的微粒示意图为。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
