2023-2024学年高中化学苏教版2019必修第一册 1-2-2物质的化学计量(第2课时) 课件(共21张)
文档属性
| 名称 | 2023-2024学年高中化学苏教版2019必修第一册 1-2-2物质的化学计量(第2课时) 课件(共21张) |

|
|
| 格式 | pptx | ||
| 文件大小 | 949.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-14 00:00:00 | ||
图片预览






文档简介
(共21张PPT)
专题一第二单元
物质的化学计量
02
摩尔质量
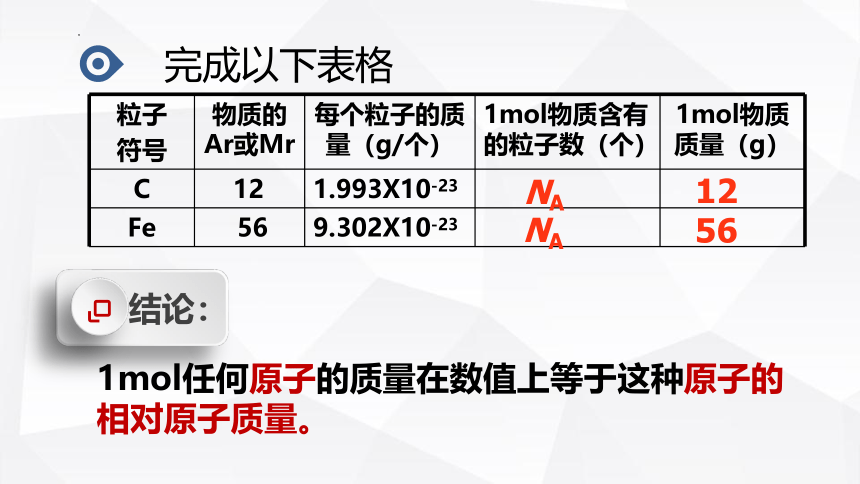
粒子 符号 物质的Ar或Mr 每个粒子的质量(g/个) 1mol物质含有的粒子数(个) 1mol物质质量(g)
C 12 1.993X10-23
Fe 56 9.302X10-23
NA
NA
12
56
结论:
1mol任何原子的质量在数值上等于这种原子的相对原子质量。
完成以下表格
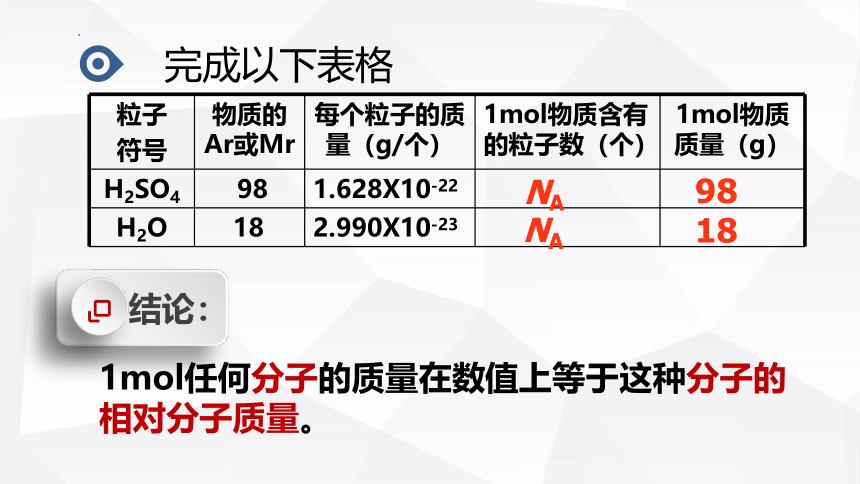
粒子 符号 物质的Ar或Mr 每个粒子的质量(g/个) 1mol物质含有的粒子数(个) 1mol物质质量(g)
H2SO4 98 1.628X10-22
H2O 18 2.990X10-23
NA
NA
98
18
结论:
1mol任何分子的质量在数值上等于这种分子的相对分子质量。
完成以下表格
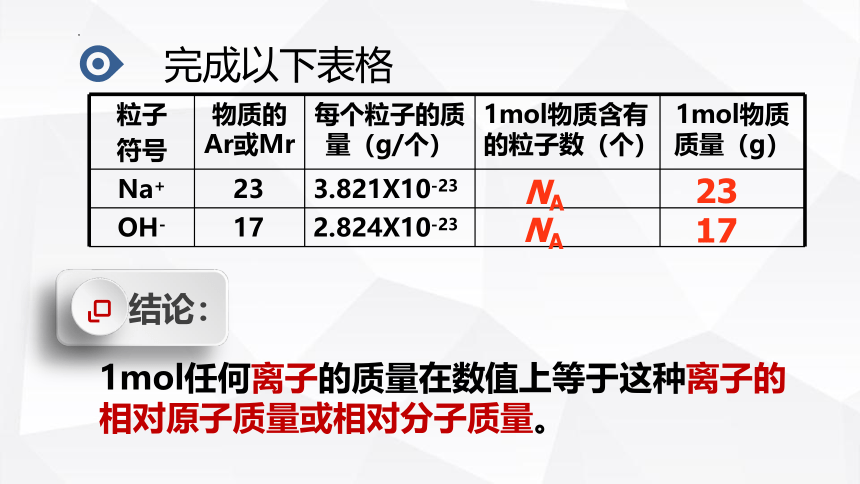
粒子 符号 物质的Ar或Mr 每个粒子的质量(g/个) 1mol物质含有的粒子数(个) 1mol物质质量(g)
Na+ 23 3.821X10-23
OH- 17 2.824X10-23
NA
NA
23
17
结论:
1mol任何离子的质量在数值上等于这种离子的相对原子质量或相对分子质量。
完成以下表格
摩尔质量
1.定义:单位物质的量的物质所具有的质量。即每mol物质具有的质量。
3.符号:g/mol,g·mol-1
2.符号:M 。
当摩尔质量以“g·mol-1”为单位时,与相对原子(分子)质量在数值上相等。
摩尔质量与相对分子质量(或相对原子质量)是否等同?
摩尔质量
不等同。
摩尔质量与相对分子质量(或相对原子质量)是两个不同的概念。
当摩尔质量以“g·mol-1”为单位时,两者在数值上相等,但前者单位是g·mol-1,后者单位是1,故两者不等同。
摩尔质量
①等值性:摩尔质量以g·mol-1作单位时,在数值上与其相对分子质量或相对原子质量相等。
②确定性:对于指定的物质来说,其摩尔质量的值是一个定值,不随物质的物质的量的多少而改变。
特性
摩尔质量
18g·mol-1
n(物质的量)
m(物质质量)
1mol H2O
18g
2mol H2O
36g
……
……
n mol H2O
18ng
=
×
n
M
M(摩尔质量)
3mol H2O
54g
m
摩尔质量
n
=
m
M
物质的量
(单位:mol)
物质质量
(单位:g)
摩尔质量
(单位:g/mol)
M
=
m
n
=
×
n
M
m
摩尔质量
①已知任意状态物质的相对原子质量或分子质量时:
M=Ar或Mr 。
计算方法
例:已知氨气的相对分子质量为17,则氨气的摩尔质量为 。
17 g·mol-1
摩尔质量
计算方法
②已知任意状态物质的质量时: (定义式)。
M
=
m
n
例:(1) 24.5gH2SO4的物质的量是多少?
(2) 1.50molNa2CO3的质量是多少?
nH2SO4= =
mH2SO4
MH2SO4
24.5g
98g.mol-1
=0.25mol
mNa2CO3= =1.5mol×106g.mol-1 =159g
nNa2CO3 MNa2CO3
摩尔质量
计算方法
例:已知一个铁原子的质量为b g,则铁的摩尔质量为 。
③已知一个分子的质量时:M=m(分子)×NA。
17 g·mol-1
摩尔质量
=
N
NA
摩尔质量(M)与微粒总数(N)有什么计算关系?
n
=
m
M
483 g Na2SO4·10H2O中所含Na+和SO42-的物质的量各是多少?所含水分子的数目是多少?
强化巩固
则:n(Na+) = 1.50 mol×2 = 3.00 mol
n(SO42-) = 1.50 mol×1 = 1.50 mol
解:Na2SO4·10H2O的相对分子质量为322,摩尔质量为322 g·mol-1。
483 g Na2SO4·10H2O中所含Na+和SO42-的物质的量各是多少?所含水分子的数目是多少?
强化巩固
n(H2O) = 1.50 mol×10 = 15.0 mol
N(H2O) = n(H2O)×NA = 15.0 mol×6.02×1023 mol-1 = 9.03×1024
答:483 g Na2SO4·10H2O中所含Na+的物质的量为3.00 mol,SO42-的物质的量为1.50 mol,水分子的数目约为9.03×1024。
g·mol-1
强化巩固
1.28 g某气体含有的分子数目为1.204×1022,则该气体的摩尔质量为 。
用NA代表阿伏加德罗常数的值,已知a g某气体中含分子数为b,则该气体的摩尔质量为 。
64 g·mol-1
b
aNA
延时符
课堂小结
01
02
摩尔质量及单位
公式及相关计算
课堂练习
B
1、下列说法正确的是( )A.CO2的摩尔质量是44 gB.CaCO3的摩尔质量是100 g·mol-1C.1 mol O2的质量是32 g·mol-1D.铁的摩尔质量就是铁的相对原子质量
2、5.4 g M和16.0 g N恰好完全反应,生成0.2 mol X和10.2 g Y,则X的摩尔质量为( )A.28 g·mol-1 B.56 g·mol-1C.84 g·mol-1 D.112 g·mol-1
课堂练习
B
2、5.4 g M和16.0 g N恰好完全反应,生成0.2 mol X和10.2 g Y,则X的摩尔质量为( )
A.28 g·mol-1 B.56 g·mol-1C.84 g·mol-1 D.112 g·mol-1
课堂练习
B
课堂练习
1∶1∶3
3、(1)O2、SO2、SO3的质量之比为1∶2∶5,则它们所含的氧原子数之比为 。(2)40.5 g某金属氯化物MCl2中含有0.6 mol Cl-,则MCl2的摩尔质量为 ,M的相对原子质量为 。
135 g·mol-1
64
专题一第二单元
物质的化学计量
02
摩尔质量
粒子 符号 物质的Ar或Mr 每个粒子的质量(g/个) 1mol物质含有的粒子数(个) 1mol物质质量(g)
C 12 1.993X10-23
Fe 56 9.302X10-23
NA
NA
12
56
结论:
1mol任何原子的质量在数值上等于这种原子的相对原子质量。
完成以下表格
粒子 符号 物质的Ar或Mr 每个粒子的质量(g/个) 1mol物质含有的粒子数(个) 1mol物质质量(g)
H2SO4 98 1.628X10-22
H2O 18 2.990X10-23
NA
NA
98
18
结论:
1mol任何分子的质量在数值上等于这种分子的相对分子质量。
完成以下表格
粒子 符号 物质的Ar或Mr 每个粒子的质量(g/个) 1mol物质含有的粒子数(个) 1mol物质质量(g)
Na+ 23 3.821X10-23
OH- 17 2.824X10-23
NA
NA
23
17
结论:
1mol任何离子的质量在数值上等于这种离子的相对原子质量或相对分子质量。
完成以下表格
摩尔质量
1.定义:单位物质的量的物质所具有的质量。即每mol物质具有的质量。
3.符号:g/mol,g·mol-1
2.符号:M 。
当摩尔质量以“g·mol-1”为单位时,与相对原子(分子)质量在数值上相等。
摩尔质量与相对分子质量(或相对原子质量)是否等同?
摩尔质量
不等同。
摩尔质量与相对分子质量(或相对原子质量)是两个不同的概念。
当摩尔质量以“g·mol-1”为单位时,两者在数值上相等,但前者单位是g·mol-1,后者单位是1,故两者不等同。
摩尔质量
①等值性:摩尔质量以g·mol-1作单位时,在数值上与其相对分子质量或相对原子质量相等。
②确定性:对于指定的物质来说,其摩尔质量的值是一个定值,不随物质的物质的量的多少而改变。
特性
摩尔质量
18g·mol-1
n(物质的量)
m(物质质量)
1mol H2O
18g
2mol H2O
36g
……
……
n mol H2O
18ng
=
×
n
M
M(摩尔质量)
3mol H2O
54g
m
摩尔质量
n
=
m
M
物质的量
(单位:mol)
物质质量
(单位:g)
摩尔质量
(单位:g/mol)
M
=
m
n
=
×
n
M
m
摩尔质量
①已知任意状态物质的相对原子质量或分子质量时:
M=Ar或Mr 。
计算方法
例:已知氨气的相对分子质量为17,则氨气的摩尔质量为 。
17 g·mol-1
摩尔质量
计算方法
②已知任意状态物质的质量时: (定义式)。
M
=
m
n
例:(1) 24.5gH2SO4的物质的量是多少?
(2) 1.50molNa2CO3的质量是多少?
nH2SO4= =
mH2SO4
MH2SO4
24.5g
98g.mol-1
=0.25mol
mNa2CO3= =1.5mol×106g.mol-1 =159g
nNa2CO3 MNa2CO3
摩尔质量
计算方法
例:已知一个铁原子的质量为b g,则铁的摩尔质量为 。
③已知一个分子的质量时:M=m(分子)×NA。
17 g·mol-1
摩尔质量
=
N
NA
摩尔质量(M)与微粒总数(N)有什么计算关系?
n
=
m
M
483 g Na2SO4·10H2O中所含Na+和SO42-的物质的量各是多少?所含水分子的数目是多少?
强化巩固
则:n(Na+) = 1.50 mol×2 = 3.00 mol
n(SO42-) = 1.50 mol×1 = 1.50 mol
解:Na2SO4·10H2O的相对分子质量为322,摩尔质量为322 g·mol-1。
483 g Na2SO4·10H2O中所含Na+和SO42-的物质的量各是多少?所含水分子的数目是多少?
强化巩固
n(H2O) = 1.50 mol×10 = 15.0 mol
N(H2O) = n(H2O)×NA = 15.0 mol×6.02×1023 mol-1 = 9.03×1024
答:483 g Na2SO4·10H2O中所含Na+的物质的量为3.00 mol,SO42-的物质的量为1.50 mol,水分子的数目约为9.03×1024。
g·mol-1
强化巩固
1.28 g某气体含有的分子数目为1.204×1022,则该气体的摩尔质量为 。
用NA代表阿伏加德罗常数的值,已知a g某气体中含分子数为b,则该气体的摩尔质量为 。
64 g·mol-1
b
aNA
延时符
课堂小结
01
02
摩尔质量及单位
公式及相关计算
课堂练习
B
1、下列说法正确的是( )A.CO2的摩尔质量是44 gB.CaCO3的摩尔质量是100 g·mol-1C.1 mol O2的质量是32 g·mol-1D.铁的摩尔质量就是铁的相对原子质量
2、5.4 g M和16.0 g N恰好完全反应,生成0.2 mol X和10.2 g Y,则X的摩尔质量为( )A.28 g·mol-1 B.56 g·mol-1C.84 g·mol-1 D.112 g·mol-1
课堂练习
B
2、5.4 g M和16.0 g N恰好完全反应,生成0.2 mol X和10.2 g Y,则X的摩尔质量为( )
A.28 g·mol-1 B.56 g·mol-1C.84 g·mol-1 D.112 g·mol-1
课堂练习
B
课堂练习
1∶1∶3
3、(1)O2、SO2、SO3的质量之比为1∶2∶5,则它们所含的氧原子数之比为 。(2)40.5 g某金属氯化物MCl2中含有0.6 mol Cl-,则MCl2的摩尔质量为 ,M的相对原子质量为 。
135 g·mol-1
64
