2023-2024学年高中化学苏教版2019选择性必修3同步教案 2.1.1有机物中碳原子的成键特点及结构的表示方法
文档属性
| 名称 | 2023-2024学年高中化学苏教版2019选择性必修3同步教案 2.1.1有机物中碳原子的成键特点及结构的表示方法 |

|
|
| 格式 | docx | ||
| 文件大小 | 485.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-14 00:00:00 | ||
图片预览

文档简介
2.1.1有机化合物的结构
(第1课时 有机物中碳原子的成键特点及结构的表示方法)
一、教学目标
1.能从宏观和微观的角度理解有机化合物分子中碳原子的成键特点。
2.学会用结构式、结构简式与键线式等方法表示有机物的结构,能从共价键的角度分析结构特征,能通过有机物分子结构模型建立对有机物分子结构的直观认识。
二、教学重难点
重点:1.会用结构式、结构简式与键线式等方法表示有机物的结构;
2.能利用有机物的结构来解决有机物分子中原子共线、共面问题。
难点:能利用有机物的结构来解决有机物分子中原子共线、共面问题。
三、教学方法
总结归纳法、分组讨论法等
四、教学过程
【导入】思考:为什么碳原子易形成共价键?
【展示】碳原子的电子式
【生】因为碳原子最外层有4个电子,既不易失电子,也不易得电子,所以易与其它原子以共价键相结合。碳原子最外层的4个电子,可以与其它原子分别形成4对共用电子对,达到8电子稳定结构。
【讲解】
碳原子成键方式的多样性,是有机化合物种类繁多的原因之一。
【讲解】比较甲烷、乙烯、乙炔共价键特点及原子的空间位置
有机物 甲烷 乙烯 乙炔
分子式 CH4 C2H4 C2H2
结构式 H—C≡C—H
共价键 C—H 、C—H —C≡C—、C—H
碳原子饱和性 饱和 不饱和 不饱和
原子的成键特点及空间位置 碳原子和4个氢原子形成4个碳碳单键,键角109°28′ 每个碳原子与3个原子成键,形成1个碳碳双键,键角120°,分子中6个原子共平面 每个碳原子与2个原子成键,形成1个碳碳三键,键角180°,分子中4个原子共直线
在烃分子中,仅以单键方式成键的碳原子称为饱和碳原子。
在烃分子中,以双键或三键等方式成键的碳原子称为不饱和碳原子。
【讲解】碳原子的成键方式与分子空间构型的关系
(1)4个单键:碳原子与其他4个原子形成四面体结构,分子中所有原子不可能共面。
(2)双键:形成双键的碳原子与其直接相连的原子处于同一平面上,分子中至少有6个原子共面。
(3)三键:形成三键的碳原子与其直接相连的原子处于同一直线上,分子中至少有4个原子共线。
(4)苯环:有机物分子中含有一个苯环,至少有12个原子共面。
【问】以下表达式在表示有机化合物分子的组成和原子之间的连接情况有哪些优缺点?
【生】表示有机化合物结构的方法中,分子式不能完整表示出有机化合物分子中各原子的成键情况,而结构式可完整表示,但对于结构复杂的分子,结构式太繁琐,采用结构简式既可以删繁就简,又可以展示有机物分子的结构特征。
【讲解】键线式:省略碳、氢元素符号,每个端点、拐点都表示一个碳原子,线表示化学键。
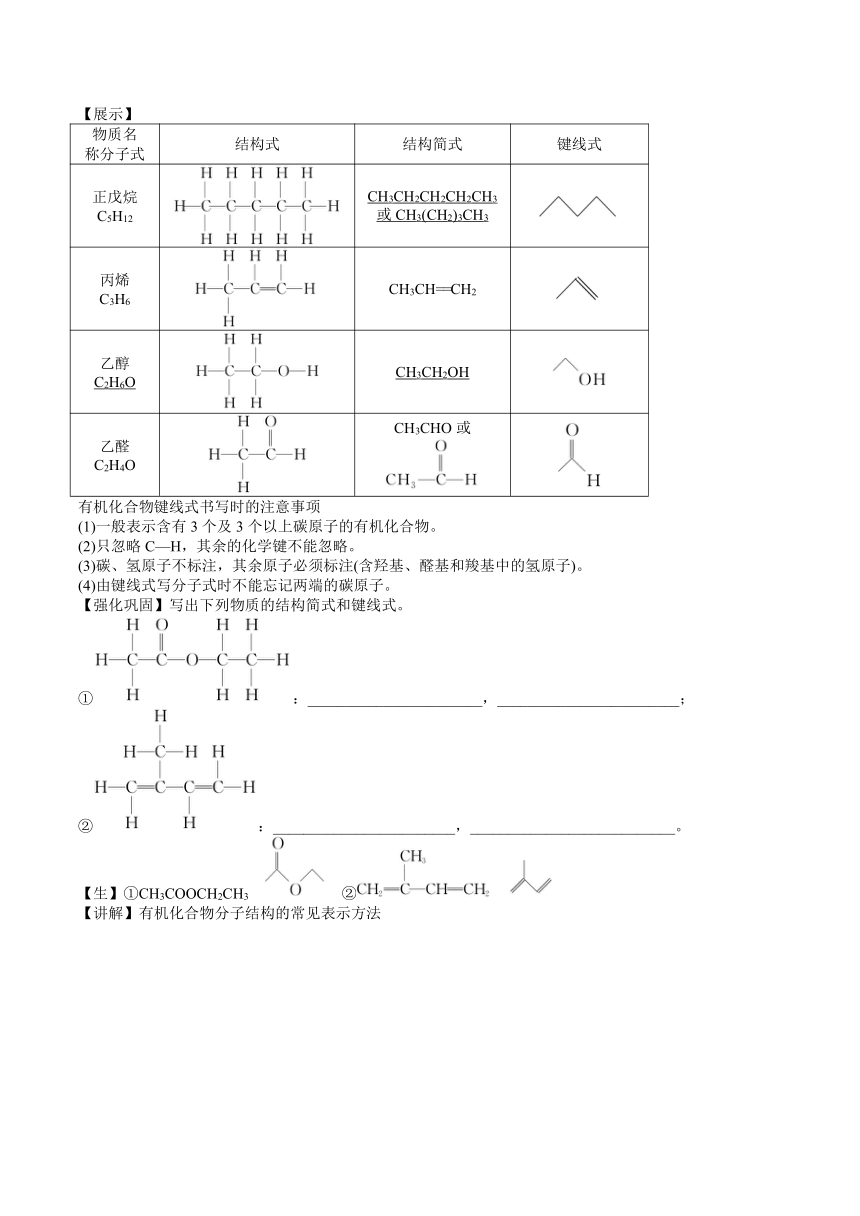
【展示】
物质名 称分子式 结构式 结构简式 键线式
正戊烷 C5H12 CH3CH2CH2CH2CH3 或CH3(CH2)3CH3
丙烯 C3H6 CH3CH==CH2
乙醇 C2H6O CH3CH2OH
乙醛 C2H4O CH3CHO或
有机化合物键线式书写时的注意事项
(1)一般表示含有3个及3个以上碳原子的有机化合物。
(2)只忽略C—H,其余的化学键不能忽略。
(3)碳、氢原子不标注,其余原子必须标注(含羟基、醛基和羧基中的氢原子)。
(4)由键线式写分子式时不能忘记两端的碳原子。
【强化巩固】写出下列物质的结构简式和键线式。
①:_______________________,________________________;
②:________________________,___________________________。
【生】①CH3COOCH2CH3 ②
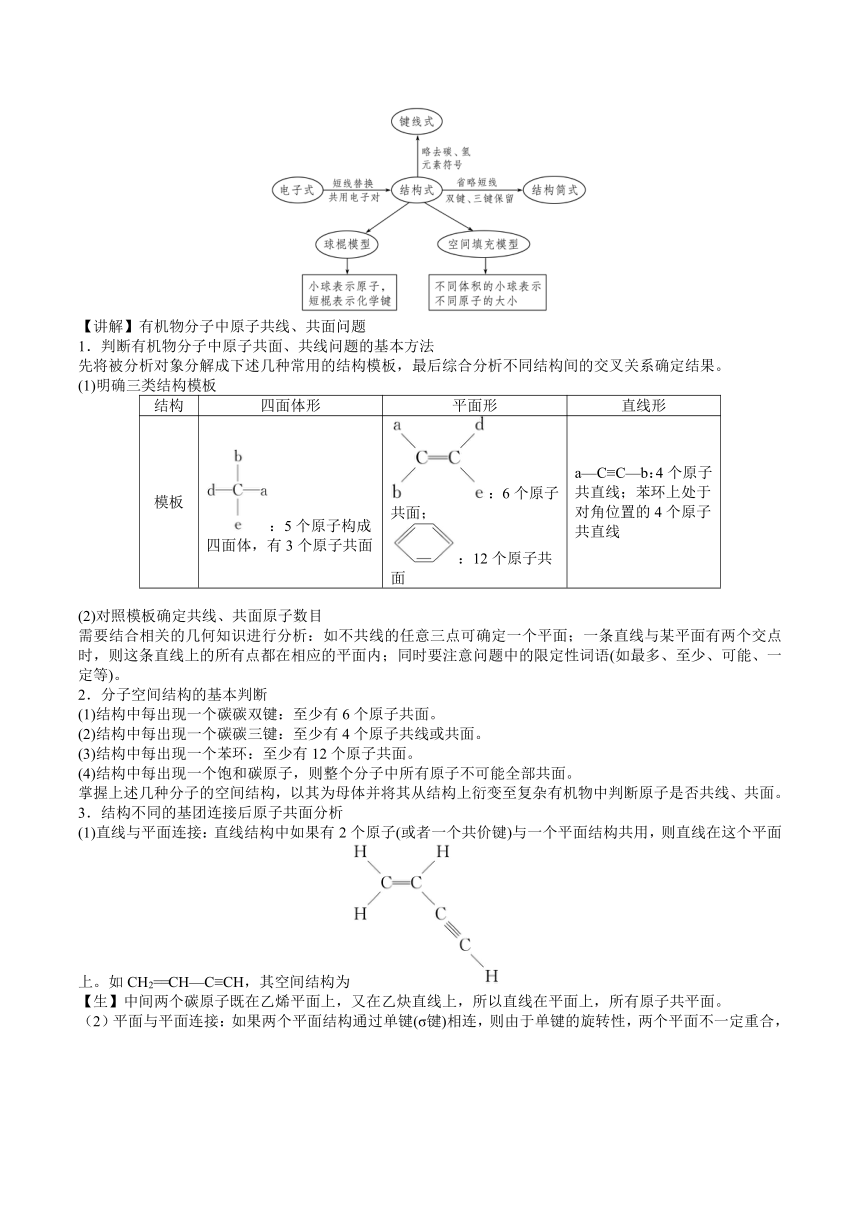
【讲解】有机化合物分子结构的常见表示方法
【讲解】有机物分子中原子共线、共面问题
1.判断有机物分子中原子共面、共线问题的基本方法
先将被分析对象分解成下述几种常用的结构模板,最后综合分析不同结构间的交叉关系确定结果。
(1)明确三类结构模板
结构 四面体形 平面形 直线形
模板 :5个原子构成四面体,有3个原子共面 :6个原子共面; :12个原子共面 a—C≡C—b:4个原子共直线;苯环上处于对角位置的4个原子共直线
(2)对照模板确定共线、共面原子数目
需要结合相关的几何知识进行分析:如不共线的任意三点可确定一个平面;一条直线与某平面有两个交点时,则这条直线上的所有点都在相应的平面内;同时要注意问题中的限定性词语(如最多、至少、可能、一定等)。
2.分子空间结构的基本判断
(1)结构中每出现一个碳碳双键:至少有6个原子共面。
(2)结构中每出现一个碳碳三键:至少有4个原子共线或共面。
(3)结构中每出现一个苯环:至少有12个原子共面。
(4)结构中每出现一个饱和碳原子,则整个分子中所有原子不可能全部共面。
掌握上述几种分子的空间结构,以其为母体并将其从结构上衍变至复杂有机物中判断原子是否共线、共面。
3.结构不同的基团连接后原子共面分析
(1)直线与平面连接:直线结构中如果有2个原子(或者一个共价键)与一个平面结构共用,则直线在这个平面上。如CH2==CH—C≡CH,其空间结构为
【生】中间两个碳原子既在乙烯平面上,又在乙炔直线上,所以直线在平面上,所有原子共平面。
(2)平面与平面连接:如果两个平面结构通过单键(σ键)相连,则由于单键的旋转性,两个平面不一定重合,但可能重合。如苯乙烯分子中
【生】共平面原子最多16个。
(3)平面与立体连接:如果甲基与平面结构通过单键相连,则由于单键的旋转性,甲基的一个氢原子可能暂时处于这个平面上。如丙烯分子中,共平面原子最多7个。
(4)直线、平面与立体连接:如图所示的分子中
【生】共平面原子最多19个。
【讲解】分析时要注意两点:①观察分子结构,先找出甲烷、乙烯、乙炔和苯分子的“影子”,再将甲烷“正四面体”、乙烯“平面形”、乙炔“直线形”和苯“平面形”等分子结构知识迁移过来即可;
②苯环以单键连接在6号不饱和碳原子上,不管单键如何旋转,8号和9号碳原子总是处于乙烯平面上,不要忽视8号碳原子对位上的9号碳原子。
【强化巩固】某烃的结构简式为,分子中处于四面体中心位置的碳原子数为a,一定在同一直线上的碳原子个数为b,一定在同一平面上的碳原子数为c。则a、b、c分别为( )
A.4、4、7 B.4、3、6
C.3、5、4 D.2、6、4
【生】 B
【课堂小结】师生共同完成。
一、有机物中碳原子的成键特点
二、有机物结构的表示方法
三、有机物分子中原子共线、共面问题
【课堂练习】
1、下列化学用语书写正确的是( )
A.甲烷的电子式:
B.丙烯的键线式:
C.乙醇的结构式:
D.丙烯的结构简式:CH3CHCH2
答案 A
2、下列说法正确的是( )
A.丙烷是直链烃,所以分子中3个碳原子也在一条直线上
B.丙烯分子中所有原子均在同一平面上
C.所有碳原子一定在同一平面上
D.至少有16个原子共平面
答案:D
(第1课时 有机物中碳原子的成键特点及结构的表示方法)
一、教学目标
1.能从宏观和微观的角度理解有机化合物分子中碳原子的成键特点。
2.学会用结构式、结构简式与键线式等方法表示有机物的结构,能从共价键的角度分析结构特征,能通过有机物分子结构模型建立对有机物分子结构的直观认识。
二、教学重难点
重点:1.会用结构式、结构简式与键线式等方法表示有机物的结构;
2.能利用有机物的结构来解决有机物分子中原子共线、共面问题。
难点:能利用有机物的结构来解决有机物分子中原子共线、共面问题。
三、教学方法
总结归纳法、分组讨论法等
四、教学过程
【导入】思考:为什么碳原子易形成共价键?
【展示】碳原子的电子式
【生】因为碳原子最外层有4个电子,既不易失电子,也不易得电子,所以易与其它原子以共价键相结合。碳原子最外层的4个电子,可以与其它原子分别形成4对共用电子对,达到8电子稳定结构。
【讲解】
碳原子成键方式的多样性,是有机化合物种类繁多的原因之一。
【讲解】比较甲烷、乙烯、乙炔共价键特点及原子的空间位置
有机物 甲烷 乙烯 乙炔
分子式 CH4 C2H4 C2H2
结构式 H—C≡C—H
共价键 C—H 、C—H —C≡C—、C—H
碳原子饱和性 饱和 不饱和 不饱和
原子的成键特点及空间位置 碳原子和4个氢原子形成4个碳碳单键,键角109°28′ 每个碳原子与3个原子成键,形成1个碳碳双键,键角120°,分子中6个原子共平面 每个碳原子与2个原子成键,形成1个碳碳三键,键角180°,分子中4个原子共直线
在烃分子中,仅以单键方式成键的碳原子称为饱和碳原子。
在烃分子中,以双键或三键等方式成键的碳原子称为不饱和碳原子。
【讲解】碳原子的成键方式与分子空间构型的关系
(1)4个单键:碳原子与其他4个原子形成四面体结构,分子中所有原子不可能共面。
(2)双键:形成双键的碳原子与其直接相连的原子处于同一平面上,分子中至少有6个原子共面。
(3)三键:形成三键的碳原子与其直接相连的原子处于同一直线上,分子中至少有4个原子共线。
(4)苯环:有机物分子中含有一个苯环,至少有12个原子共面。
【问】以下表达式在表示有机化合物分子的组成和原子之间的连接情况有哪些优缺点?
【生】表示有机化合物结构的方法中,分子式不能完整表示出有机化合物分子中各原子的成键情况,而结构式可完整表示,但对于结构复杂的分子,结构式太繁琐,采用结构简式既可以删繁就简,又可以展示有机物分子的结构特征。
【讲解】键线式:省略碳、氢元素符号,每个端点、拐点都表示一个碳原子,线表示化学键。
【展示】
物质名 称分子式 结构式 结构简式 键线式
正戊烷 C5H12 CH3CH2CH2CH2CH3 或CH3(CH2)3CH3
丙烯 C3H6 CH3CH==CH2
乙醇 C2H6O CH3CH2OH
乙醛 C2H4O CH3CHO或
有机化合物键线式书写时的注意事项
(1)一般表示含有3个及3个以上碳原子的有机化合物。
(2)只忽略C—H,其余的化学键不能忽略。
(3)碳、氢原子不标注,其余原子必须标注(含羟基、醛基和羧基中的氢原子)。
(4)由键线式写分子式时不能忘记两端的碳原子。
【强化巩固】写出下列物质的结构简式和键线式。
①:_______________________,________________________;
②:________________________,___________________________。
【生】①CH3COOCH2CH3 ②
【讲解】有机化合物分子结构的常见表示方法
【讲解】有机物分子中原子共线、共面问题
1.判断有机物分子中原子共面、共线问题的基本方法
先将被分析对象分解成下述几种常用的结构模板,最后综合分析不同结构间的交叉关系确定结果。
(1)明确三类结构模板
结构 四面体形 平面形 直线形
模板 :5个原子构成四面体,有3个原子共面 :6个原子共面; :12个原子共面 a—C≡C—b:4个原子共直线;苯环上处于对角位置的4个原子共直线
(2)对照模板确定共线、共面原子数目
需要结合相关的几何知识进行分析:如不共线的任意三点可确定一个平面;一条直线与某平面有两个交点时,则这条直线上的所有点都在相应的平面内;同时要注意问题中的限定性词语(如最多、至少、可能、一定等)。
2.分子空间结构的基本判断
(1)结构中每出现一个碳碳双键:至少有6个原子共面。
(2)结构中每出现一个碳碳三键:至少有4个原子共线或共面。
(3)结构中每出现一个苯环:至少有12个原子共面。
(4)结构中每出现一个饱和碳原子,则整个分子中所有原子不可能全部共面。
掌握上述几种分子的空间结构,以其为母体并将其从结构上衍变至复杂有机物中判断原子是否共线、共面。
3.结构不同的基团连接后原子共面分析
(1)直线与平面连接:直线结构中如果有2个原子(或者一个共价键)与一个平面结构共用,则直线在这个平面上。如CH2==CH—C≡CH,其空间结构为
【生】中间两个碳原子既在乙烯平面上,又在乙炔直线上,所以直线在平面上,所有原子共平面。
(2)平面与平面连接:如果两个平面结构通过单键(σ键)相连,则由于单键的旋转性,两个平面不一定重合,但可能重合。如苯乙烯分子中
【生】共平面原子最多16个。
(3)平面与立体连接:如果甲基与平面结构通过单键相连,则由于单键的旋转性,甲基的一个氢原子可能暂时处于这个平面上。如丙烯分子中,共平面原子最多7个。
(4)直线、平面与立体连接:如图所示的分子中
【生】共平面原子最多19个。
【讲解】分析时要注意两点:①观察分子结构,先找出甲烷、乙烯、乙炔和苯分子的“影子”,再将甲烷“正四面体”、乙烯“平面形”、乙炔“直线形”和苯“平面形”等分子结构知识迁移过来即可;
②苯环以单键连接在6号不饱和碳原子上,不管单键如何旋转,8号和9号碳原子总是处于乙烯平面上,不要忽视8号碳原子对位上的9号碳原子。
【强化巩固】某烃的结构简式为,分子中处于四面体中心位置的碳原子数为a,一定在同一直线上的碳原子个数为b,一定在同一平面上的碳原子数为c。则a、b、c分别为( )
A.4、4、7 B.4、3、6
C.3、5、4 D.2、6、4
【生】 B
【课堂小结】师生共同完成。
一、有机物中碳原子的成键特点
二、有机物结构的表示方法
三、有机物分子中原子共线、共面问题
【课堂练习】
1、下列化学用语书写正确的是( )
A.甲烷的电子式:
B.丙烯的键线式:
C.乙醇的结构式:
D.丙烯的结构简式:CH3CHCH2
答案 A
2、下列说法正确的是( )
A.丙烷是直链烃,所以分子中3个碳原子也在一条直线上
B.丙烯分子中所有原子均在同一平面上
C.所有碳原子一定在同一平面上
D.至少有16个原子共平面
答案:D
